


宫颈癌是一种严重影响女性身心健康的疾病,据世界卫生组织报告发病率占所有癌症的12%,仅次于乳腺癌[1]。估计到2020年,将有1600万新增病例,年龄主要集中在15至44岁之间[2]。报道显示有80%以上宫颈癌是由人类乳头瘤病毒 (HPV)感染引起,HPV可以激活宫颈中原癌基因或抑制抑癌基因,使宫颈肿瘤的病毒DNA整合到染色体DNA中,从而增强细胞增殖能力导致宫颈癌的发生[3, 4]。
ARM重复蛋白家族是指含有多个armadillo repeat结构的蛋白,其成员在肿瘤形成、细胞间通信以及细胞骨架形成等方面发挥着重要作用[5]。Armadillo repeat 结构包含了3个螺旋结构,分别为 H1、H2和H3[5, 6]。ALEX蛋白是一个新的ARM重复蛋白家族成员,主要由ALEX1、ALEX2和ALEX3组成。 其中ALEX1 (arm proteins lost in epithelial cancers on chromosome X1) 蛋白序列含有两个 Armadillo repeat结构,其N端具有一个疏水的跨膜区。目前研究表明,在大多正常组织中均有广泛的表达,在上皮组织来源的肿瘤中低表达或者不表达[7]。有关报道也证明ALEX1参与肿瘤的发生发展[8],过表达ALEX1能抑制直肠癌细胞的克隆形成[9]。但有关ALEX1在宫颈癌中的作用及其机制尚未见报道。为此我们将探讨ALEX1在宫颈癌中的表达情况,并研究其对宫颈癌细胞的相关生物学行为的影响。
1 材料与方法 1.1 材料HeLa细胞由重庆医科大学分子医学与肿瘤研究中心提供。采用含10% 胎牛血清的DMEM培养基,在37℃、5% CO2 培养箱中培养。DMEM培养基、胎牛血清购自Hyclon公司;Opti-MEM购自Gibco公司;Lipofectamine RNAiMAX 购自Invitrogen公司;siRNA由上海吉玛公司合成;BCA试剂购自碧云天公司;CCK-8试剂盒购自Promega公司;DAB底物显色试剂盒购自Beyotime公司; SP9002免疫组化染色试剂购自北京中杉金桥生物技术公司;鼠抗人ALEX1单克隆抗体、兔抗人β-actin多克隆抗体购自Santa Cruz公司;宫颈癌临床组织来源于重庆医科大学第一附属医院。
1.2 方法 1.2.1 免疫组化检测宫颈癌及其癌旁组织中的表达水平收集的临床组织用4%的多聚甲醛固定24 h,体积分数为0.5乙醇90 min、体积分数为0.7乙醇90 min、体积分数为0.85乙醇90 min、体积分数为0.9乙醇90 min、无水乙醇60 min 脱水,石蜡包埋及切片。切片的免疫组化:烘片、脱蜡与水化、封闭、加一抗、加二抗、DAB显色、镜检。根据组织的染色强度和染色阳性细胞比例进行综合性量化评分。染色强度评分标准:阴性(-),0 分;弱阳性(+),1分;中等阳性(++),2分;强阳性(+++),3分。染色阳性细胞比例评分标准:未染色细胞,0 分;染色阳性细胞比例<10%,1分;染色阳性细胞比例10%~50%,2分;染色阳性细胞比例>50%,3分。总分值=染色强度分值+染色阳性细胞比例分值。
1.2.2 siRNA 的合成及转染利用Promega软件系统设计ALEX1 mRNA的3条siRNAs序列片段。序列分别为:RNAi-1,正义链:5′-CCUGGAGCGAACAAAUGAUTT-3′,反义链:5′-AUCAUUUGUUCGCUCCAGGTT-3′;RNAi-2,正义链:5′-GCCUGCUACUGUGUAUACATT-3′,反义链:5′-UGUAUACACAGUAGCAGGCTT-3′;RNAi-3,正义链:5′-GCUGGGCU AAGACUGUUAATT-3′,反义链:5′-UUAACAGUCUUAGCCCAGCTT-3′;control siRNA,正义链:5′-UUCUCCGAACGUGUCACGUTT-3′,反义链:5′-ACGUGACACGUUCGGAGAATT-3′,由上海吉玛公司合成。干粉siRNA用DEPC水溶解稀释成20 μmol·L-1,-20℃保存。HeLa细胞在含10%胎牛血清的DMEM培养基,在37℃、5%CO2培养箱中培养。转染前将细胞制成悬浮液接种于6孔板中在37℃、5%CO2培养箱中培养,当细胞生长到50%~60%时,加入4 μL的Lipofectamine和8 μL的siRNA溶液并补齐2 mL含10%胎牛血清的DMEM培养基培养48 h。实验共4组:RNAi-1组、RNAI-2组、RNA-3组以及control siRNA组。
1.2.3 Western blot检测siRNA对ALEX1的干扰效率收集转染siRNA 48 h后的HeLa细胞,并进行蛋白提取,采用BCA法测定蛋白浓度。按50 μg/孔蛋白量上样,经 8% SDS-PAGE 胶分离后,将目的蛋白转移到PVDF膜上,5%脱脂奶粉封闭2 h,加一抗4℃孵育过夜,TBST洗膜3次,每次15 min,再用二抗室温孵育2 h,ECL化学发光检测结果。
1.2.4 流式细胞技术检测细胞周期SiRNA转染HeLa细胞48 h后,胰酶消化收集各组细胞,1 000 r·min-1离心5 min,弃上清液,PBS重悬清洗,1 000 r · min-1离心5 min,重复1次,再加入1 mL PBS 混匀,转移至1.5 mL EP管中。最后加入5 μL Annexin V-FITC,振荡均匀后4℃孵育15 min,再加入5 μL碘化丙啶(PI),孵育5 min,流式细胞仪检测细胞凋亡的情况,实验重复3次。
1.2.5 流式细胞技术检测细胞凋亡SiRNA转染HeLa细胞48 h后,胰酶消化收集各组细胞,1 000 r·min-1离心5 min,弃上清液,PBS重悬清洗,1 000 r·min-1离心 5 min,弃上清液,重复1次,体积分数为0.7乙醇重悬细胞,放置冰箱4℃,12 h。离心弃去上清,PBS清洗1次,加入含0.01%NaN 3和0.1%BSA 的缓冲液500 μL复溶细胞。加入2.5 μL RNase(100 mg·L-1),37℃孵育15 min,加入25 μL(10 μg·mL-1)PI染液,避光放置15 min。流式细胞仪检测分析各组细胞的DNA含量,计算细胞周期,实验重复3次。
1.2.6 CCK-8测定细胞增殖SiRNA转染HeLa细胞48 h后,胰酶消化重悬细胞,血球计数板计数细胞,以每孔3 000个细胞接种于96孔板中,每组3个复孔,待贴壁后分别测定 0、24、48、72、96 h的细胞生长状况。每孔加入10 μL CCK-8试剂,37℃孵育2 h,酶标仪450 nm测定OD值。
1.2.7 CCK-8 检测细胞对白藜芦醇药物的敏感性SiRNA转染HeLa细胞48 h后胰酶消化重悬细胞,血球计数板计数细胞,以每孔3 000个细胞接种于96孔板中。配制浓度为1 mmol· L-1的白藜芦醇溶液,待贴壁后加入0、5、10、15 μL的白藜芦醇溶液,使其终浓度分别为 0、50、100、150 μmol·L-1,按Promega公司的CCK-8测定细胞生长48 h的抑制率,每组3个复孔。每孔加入10 μL CCK-8试剂,37℃孵育2 h,酶标仪450 nm测定OD值。
1.2.8 统计学分析应用SPSS 17.0统计软件,数据以 ± s表示。两组数据间的比较采用独立样本t检验,多组数据间的比较采用单因素方差分析。
± s表示。两组数据间的比较采用独立样本t检验,多组数据间的比较采用单因素方差分析。
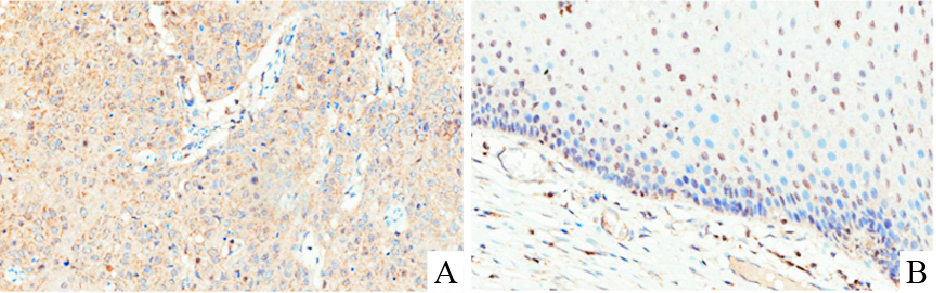
通过免疫组化对比分析显示:与癌旁组织相比,癌组织中ALEX1的表达明显增加。此外,在癌旁组织中ALEX1的表达主要定位在细胞核中,而在癌组织中ALEX1的表达主要定位在细胞质中(Fig1)。表明ALEX1在宫颈中的表达情况与宫颈是否发生癌变有关,推测ALEX1参与宫颈癌的发生和形成。
|
| Fig 1 ALEX1 protein expression in cervical cancer tissues and adjacent non-cancerous tissues A: cervical cancer tissues; B: adjacent non-cancerous tissues |
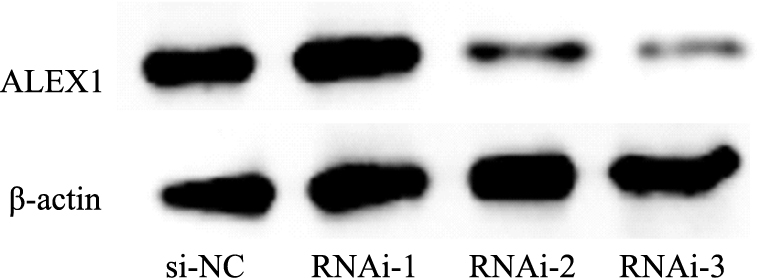
Western blot 结果显示:与对照组相比,实验组RNAi-3中ALEX1的蛋白表达明显下降(Fig2)。说明在3组干扰序列中RNA-3的干扰效率最好,后续实验干扰采用RNA-3序列。
|
| Fig 2 Efficiency of siRNA silencing of ALEX1 gene detected by Western blot |
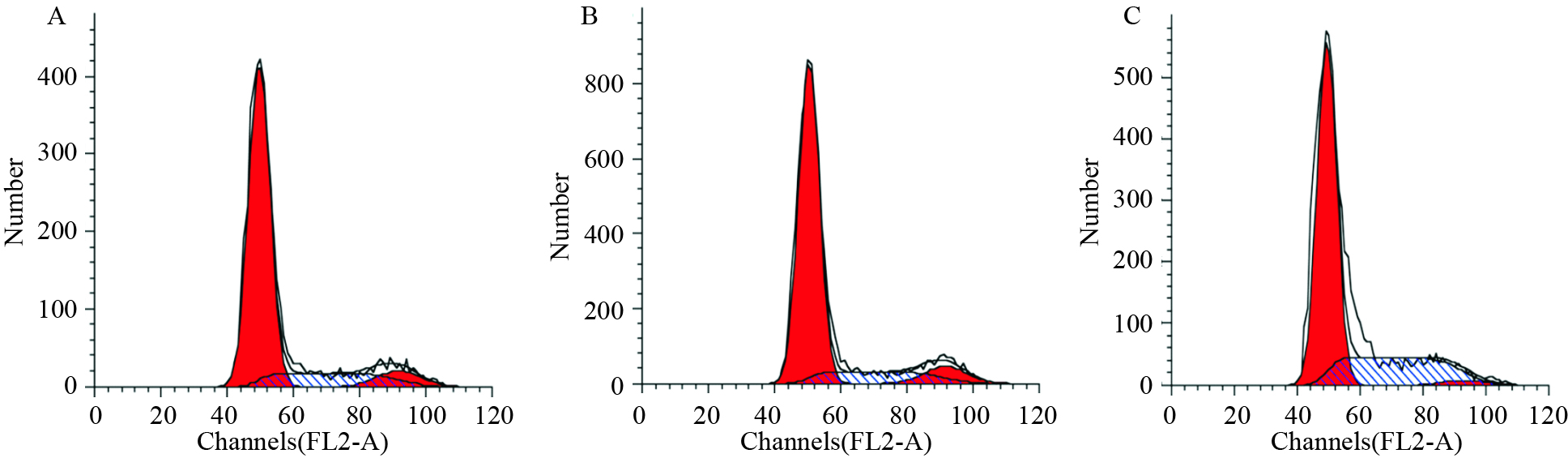
流式细胞检测周期结果显示:空白组和对照组中S期细胞比例分别为16.53%和14.41%,G2 期细胞比例分别为7.38%和8.30%。实验组中S期细胞比例为30.00%,G2期细胞比例为1.72%。空白组与对照组相比,差异无统计学意义;实验组与对照组和空白组相比较,S期细胞明显增多,G2期细胞明显减少,差异有统计学意义(P<0.05),表明沉默ALEX1的表达阻滞HeLa细胞的周期进程(Fig3)。
|
| Fig 3 Cell cycle distribution detected by flow cytometric analysis A:Blank group; B:Control group; C:Experimental group |
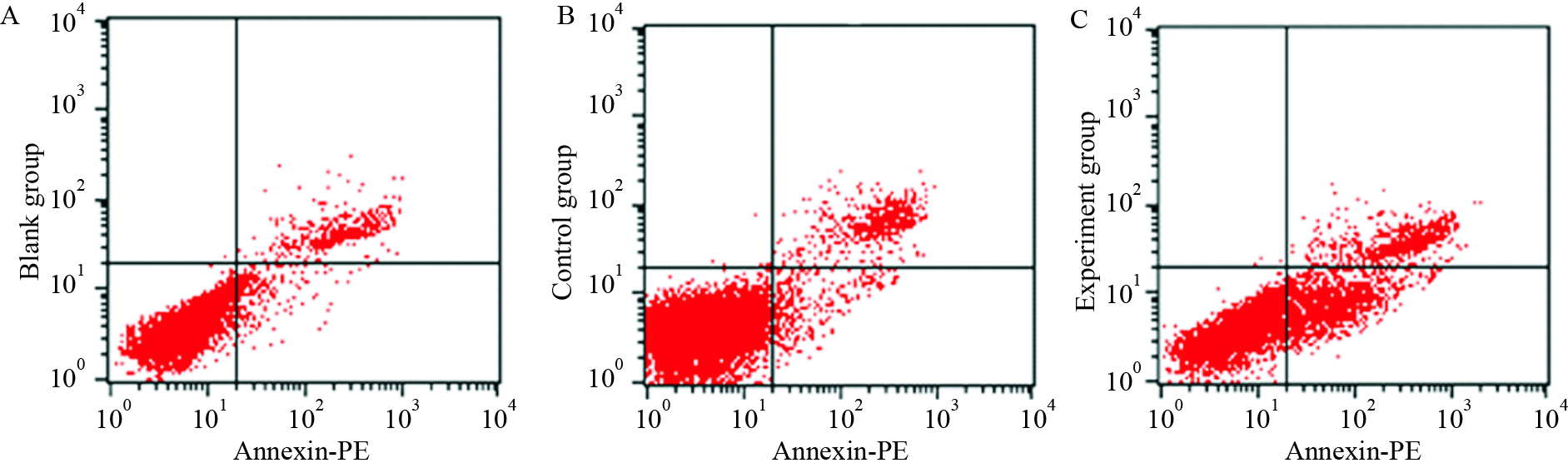
流式细胞检测凋亡结果显示:空白组和对照组中凋亡率分别为2.31%和3.15%,实验组凋亡比例分别为16.41%。空白组与对照组相比,差异无统计学意义;实验组与对照组和空白组相比较,凋亡明显增多,差异有统计学意义(P < 0.05),表明沉默ALEX1的表达促进HeLa细胞的凋亡发生(Fig4)。
|
| Fig 4 Cell apoptosis distribution detected by flow cytometric analysis A:Blank group; B:Control group; C:Experimental group |
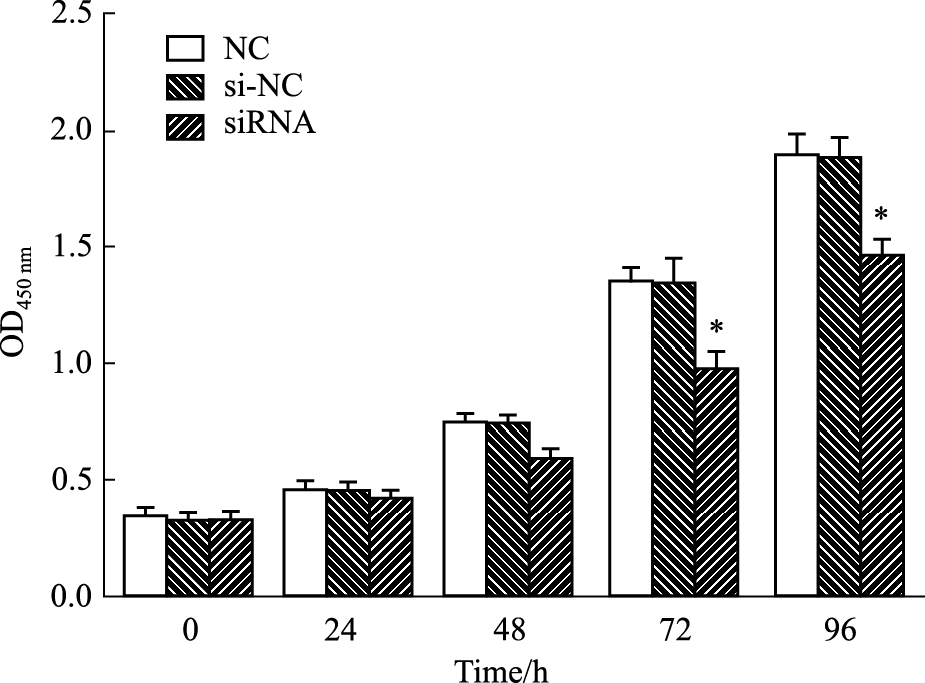
CCK-8结果显示:与对照组和空白组相比较,实验组在72、96 h 细胞生长明显受抑制,差异有统计学意义(P < 0.05),表明沉默ALEX1的表达抑制HeLa细胞的增殖(Fig5)。
|
| Fig 5 Effects of ALEX1 silence on cell growth in HeLa cells analysed by CCK-8 |
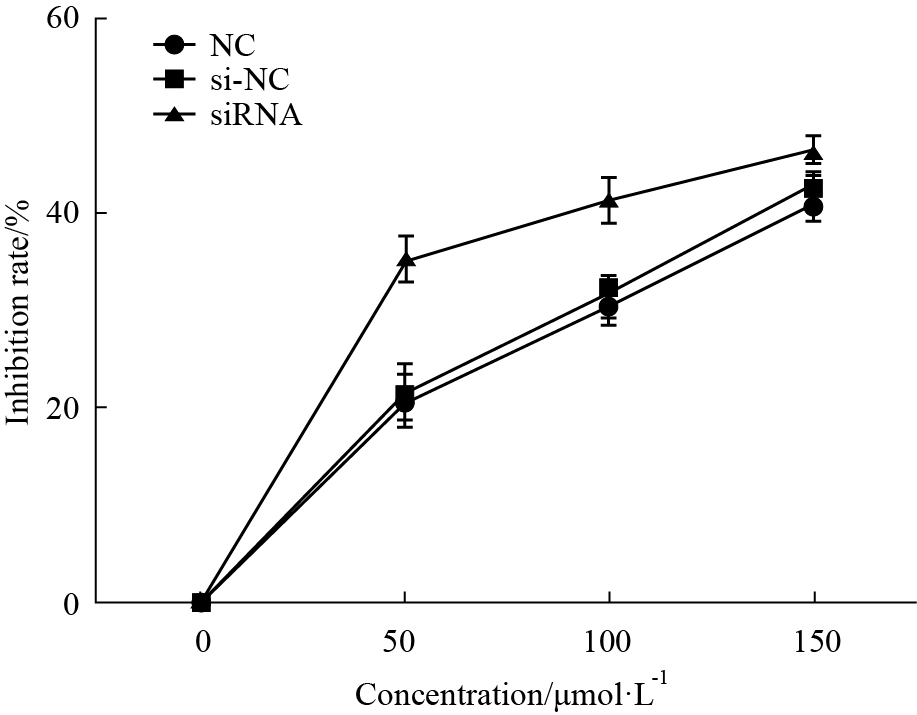
CCK-8结果显示:与对照组和空白组相比较,实验组在细胞生长明显受抑制,特别当浓度为 50、100 μmol·L-1抑制最为明显,表明沉默ALEX1的表达能提高HeLa细胞对白藜芦醇的敏感性,增加白藜芦醇对HeLa细胞的致死能力(Fig6)。
|
| Fig 6 Effects of ALEX1 silence to resveratrol on cell growth in HeLa cells analysed by CCK-8 |
Armadillo repeat结构首次发现于果蝇极性基因 armadillo,该基因在果蝇胚胎形成、维持上皮组织完整性和早期细胞极性形成中起重要作用[10]。Arm repeat 结构的特点是在真核和原核生物中都具有保守的三维结构,其结构是由大约42个氨基酸形成3个α-螺旋,再由前后2个Arm repeat 结构相互折叠,形成1个右手超螺旋结构[11]。Arm repeat 蛋白家族是指含有多个Armadillo repeat结构的蛋白家族,其家族蛋白在肿瘤形成、发展、细胞间通讯,维持组织完整性等多方面发挥着重要作用[12]。
ALEX1蛋白是Kurochin在用酵母双杂交技术寻找与pp110蛋白相互作用时发现的,属于Arm repeat蛋白家族新成员。ALEX1在Xq21.33-q22.2上,其基因全长为4.2 kb,含有4个外显子,编码着453个氨基酸,蛋白质分子质量为49 ku,含有两个arm repeat结构 ,包括8个潜在的蛋白激酶C和5个酪蛋白激酶Ⅱ 结合位点[7, 8]。近年来研究表明,ALEX1能够抑制人直肠癌细胞的克隆形[9] ,ALEX1 mRNA 在心脏、脑、睾丸、前列腺、卵巢、结肠等大多正常组织组织中高表达,在人肿瘤组织中没有表达或低于其正常组织的表达。在细胞系中,ALEX1 mRNA在胶质瘤细胞系和骨肉瘤细胞系中有表达,在永生上皮细胞系、肺癌细胞系和乳腺癌细胞系中不表达,而在正常的乳腺上皮细胞系中有表达[7, 13]。这些研究表明 ALEX1基因有可能参与了肿瘤的发生发展。
2010年日本学者Iseki等[9]在直肠癌中研究ALEX1基因时发现:在直肠癌和胰腺癌中环腺苷反应元件和 E-box 基因定点突变会削弱ALEX1基因启动子的活性,过表达反应元件结合蛋白和过表达β-catenin 能促进 ALEX1基因的表达。表明环腺苷反应元件和E-box是调控ALEX1基因启动子的重要元件,ALEX1基因本身是被反应元件结合蛋白和β-catenin 蛋白调节的。除此之外ALEX1也受Wnt β-catenin信号通路的调控[8]。
为了探讨ALEX1基因在宫颈癌中的表达情况以及对宫颈癌细胞生物学作用的影响。本研究采用免疫组化检测ALEX1在宫颈癌及其癌旁组织中的表达情况,应用siRNA干扰技术研究ALEX1对宫颈癌HeLa细胞的生物学形态影响。研究结果发现,ALEX1在宫颈癌组织中的表达高于其对应癌旁组织,沉默ALEX1表达后,HeLa细胞的周期、增殖受到抑制、促进HeLa细胞凋亡的发生,同时增强了白藜芦醇对HeLa 细胞的抑制作用,说明ALEX1与宫颈癌的发生发展有着密切联系。Wnt /β-catenin信号通路异常活化是肿瘤重要发病原因之一,Wnt/ β-catenin通路可以通过调控核内β-catenin的累积,激活Wnt 相关靶基因[14]。ALEX1基因在宫颈癌中的激活,也有可能是Wnt /β-catenin异常活化所导致的。此外,本研究还发现,沉默ALEX1后能增强白藜芦醇对HeLa细胞增殖的抑制作用,这可能是因白藜芦醇降低了细胞内的β-catenin蛋白水平,从而抑制了Wnt/ β-catenin通路的活性[15],导致ALEX1的表达受抑制,促进了细胞的凋亡。
本研究首次证明,ALEX1在宫颈癌组织中高表达于其癌旁组织,沉默ALEX1能够抑制宫颈癌细胞的增殖能力,这些结果为进一步研究ALEX1在肿瘤的发生发展中的作用及其机制奠定了理论基础。同时,ALEX1有望能作为一个新的宫颈癌标志物,用于临床诊断和基因药物的开发。
(致谢:本实验完成于重庆医科大学分子医学与肿瘤研究中心,在此感谢本实验室的老师及实验管理人员,同时也感谢我的指导老师宋方洲教授在实验过程的指导及帮助。)
| [1] | Barnett K B, McRee A L, Reiter P L, et al. Cervical cancer prevention services at college health centers:historically black colleges and universities (HBCUs) compared to predominantly white institutions (PWIs)[J].Cancer Epidemiol Biomarkers Prev,2015,24:758-72. |
| [2] | Bhatt A N, Mathur R, Farooque A, et al. Cancer biomarkers-current perspectives[J]. Indian J Med Res, 2010,132:129-49. |
| [3] | Senapathy J G, Umadevi P, Kannika P S. The present scenario of cervical cancer control and HPV epidemiology in India:an outline[J]. Asian Pac J Cancer Prev,2011,12(5):1107-15. |
| [4] | Sun Z Q, Wang H J, Zhao Z L, et al. Significance of HPV infection and genic mutation of APC and K-ras in patients with rectal cancer[J]. Asian Pac J Cancer Prev,2013,14(1):121-6. |
| [5] | Striegl H, Andrade-Navarro M A, Heinemann U. Armadillo motifs involved in vesicular transport[J]. PLoS One,2010, 5(2):e8991. |
| [6] | Choi H J,Weis W I. Structure of the armadillo repeat domain of plakophilin 1[J]. J Mol Biol,2005,346(1):367-76. |
| [7] | Kurochkin I V, Yonemitsu N, Funahashi S I, et al. ALEX1, a novel human armadillo repeat protein that is expressed differentially in normal tissues and carcinomas[J]. Biochem Biophys Res Commun,2001,280(1):340-7. |
| [8] | Iseki H, Takeda A, Andoh T, et al. Human Arm protein lost in epithelial cancers, on chromosome X 1 (ALEX1) gene is transcriptionally regulated by CREB and Wnt/beta-catenin signaling[J]. Cancer Sci,2010,101(6):1361-6. |
| [9] | Iseki H, Takeda A, Andoh T, et al. ALEX1 suppresses colony formation ability of human colorectal carcinoma cell lines[J].Cancer Sci,2012,103(7):1267-71. |
| [10] | Riggleman B, Wieschaus E, Schedl P. Molecular analysis of the armadillo locus:uniformly distributed transcripts and a protein with novel internal repeats are associated with a Drosophila segment polarity gene[J]. Genes Dev,1989,3(1):96-113. |
| [11] | Ketal M. Importin alpha nuclear localization signal binding sites for STAT1,STAT2,and influenza A virus nucleoprotein[J]. J Biol Chem,2003, 278(30):28193-200. |
| [12] | Hatzfeld M. The armadillo family of structural proteins[J]. Int Rev Cytol,1999,186:179-224. |
| [13] | Zender L, Xue W, Zuber J, et al. An oncogenomics-based in vivo RNAi screen identifies tumor suppressors in liver cancer[J]. Cell,2008,135(5):852-69. |
| [14] | 朱智杰,阮君山,李 尧,等.Wnt信号通路诱导肿瘤细胞上皮间质转化的研究进展[J].中国药理学通报,2012,28(7):904-7.Zhu Z J,Ruan J S, li R, et al.Research progress of Wnt signaling pathway induced EMT in tumor cells[J]. Chin Pharmacol Bull,2012, 28(7):904-7. |
| [15] | 袁霜雪,王东旭,伍秋香,等.白藜芦醇抑制HCT116结肠癌细胞增殖与Wnt/β-catenin 的关系研究[J].中国药理学通报,2015,31(4):537-41.Yuan X X, Wang D X, Wu Q X, et al. Study on the relationship between anti-proliferation effect of resveratrol on HCT116 colon cancer cells and Wnt/β-catenin[J].Chin Pharmacol Bull,2015,31(4):537-41. |

