


2. 贵州省中国科学院天然产物化学重点实验室, 贵州 贵阳 550002
2. The Key Laboratory of Chemistry for Natural Products, Guizhou Province and Chinese Academy of Sciences, Guiyang 550002, China
内皮细胞作为血管内壁的屏障,与炎症、心血管疾病、糖尿病、静脉血栓形成和病毒感染性疾病的发生发展直接相关[1]。其中多种疾病的发生都伴随有补体旁路的激活,激活的补体能够导致内皮细胞活化,引起一系列结构和功能的改变,在诸如血管扩张、血管通透性增加、炎症细胞黏附、迁移及趋化等过程中均发挥重要的作用[2],并能影响纤溶和凝血功能[3, 4]。其中黏附分子的表达是炎症反应启动和发展的一个重要环节。本文研究了Res、PDTC和AG490三种化学小分子对补体旁路激活致内皮细胞黏附分子表达的干预作用和可能的作用机制。
1 材料与方法 1.1 材料RPMI 1640培养基为美国Gibco公司产品,胎牛血清为天津灏洋生物产品;人ICAM-1、E-selectin、VCAM-1 ELISA检测试剂盒购自武汉博士德生物工程有限公司;吡咯烷二硫氨基甲酸(pyrrolidine dithiocarbamate,PDTC)、白藜芦醇(resveratrol,Res)购自美国Sigma公司;AG490、兔抗人NF-κB p65单克隆抗体(93H1)、MDA检测试剂盒为碧云天生物研究所产品;兔抗人β-actin单克隆抗体(13E5)购自美国CST公司;眼镜蛇毒因子(cobra venom factor,CVF)由本实验室制备提供,其分离纯化和检测方法参照文献[5]进行;正常人血清(normal human serum,NHS)由本实验室健康志愿者献血制备,灭活人血清(inactive normal human serum,INHS)由正常人血清56 ℃灭活30 min制备。
1.2 主要仪器Forma 3111 CO2培养箱和Revco超低温冰箱(美国Thermo公司);Nikon TS100倒置相差显微镜(日本Nikon公司);Spectra MAX-190连续波长酶标仪(美国MD公司);5810R冷冻离心机(德国Eppendorf公司);Elix 纯水系统和Milli-Q超纯水系统(美国Millipore公司);DYCZ-24D型和DYCZ-4013型电泳槽(北京市六一仪器厂)。
1.3 实验方法 1.3.1 细胞培养人微血管内皮细胞株(HMEC)由本实验室传代培养,用含胎牛血清体积分数为0.2的RPMI 1640培养基于37 ℃培养箱进行培养,收集对数生长期的细胞进行实验。
1.3.2 补体旁路激活产物的制备参照文献[6]方 法,将CVF(6.5×104 U·L-1)与NHS等比例进行混合,37 ℃水浴30 min,CVF激活产物(CVF-activated complement,CAC)根据需要于临用时提前制备。实验中以CVF与INHS混合制备的孵育物作对照。
1.3.3 CAC对MDA浓度的影响HMEC以1×105 cells每孔接种24孔培养板,培养24 h后去除细胞培养液,以温育的无血清RPMI 1640培养基清洗1次,加入140 μL无血清RPMI 1640培养基和60 μL CAC孵育产物,分别于不同时间点取细胞培养上清,按试剂盒说明书检测MDA。
1.3.4 CAC对HMEC黏附分子表达的影响HMEC以1×104 cells每孔接种96孔培养板,培养24 h后去除细胞培养液,加入140 μL温育的无血清RPMI 1640培养基和60 μL CAC孵育产物,分别于不同时间点取细胞培养上清,按试剂盒说明书检测E-selectin、ICAM-1和VCAM-1。
1.3.5 Western blot检测CAC对NF-κB p65磷酸化的HMEC以5×105 cells接种75 mL培养瓶,48 h后弃去培养基,加入CAC并以无血清RPMI 1640培养基补足至2 mL,于37 ℃培养箱中分别作用5 min、30 min和1 h。弃上清,在冰水浴中刮取细胞,提取细胞质蛋白,经BCA蛋白定量后以SDS-PAGE分离,转至PVDF膜上,经一抗4℃孵育过夜,二抗室温孵育1 h后,以DAB显色试剂显色后晾干拍照。照片以Image J作图软件进行灰度分析。
1.3.6 Res对MDA的干预作用HMEC以1×105 cells每孔接种24孔培养板,培养24 h后去除细胞培养液,以温育的无血清RPMI 1640培养基清洗1次,加入140 μL以无血清RPMI 1640培养基配制的Res,37 ℃预处理1 h后加入60 μl CAC,轻轻混匀后培养24 h,收集细胞培养液按试剂盒说明书检测MDA。
1.3.7 Res、PDTC和AG490对黏附分子表达的干预作用HMEC以1×104 cells每孔接种96孔培养板,培养24 h后去除细胞培养液,以温育的无血清RPMI 1640培养基清洗1次,加入140 μL以无血清RPMI 1640培养基配制的Res、PDTC、AG490,37 ℃预处理1 h后加入60 μL CAC,轻轻混匀后分别作用不同时间,收集细胞培养液,按试剂盒说明书检测E-selectin、ICAM-1和VCAM-1。
1.3.8 Res、PDTC和AG490对NF-κB p65磷酸化的干预作用HMEC以5×105 cells接种75 mL培养瓶,48 h后弃去培养基,以温育的无血清RPMI 1640培养基清洗1次,加入1 400 μL以无血清RPMI 1640培养基配制的的Res(20 μmol·L-1)、PDTC(100 μmol·L-1)和AG490(100 μmol·L-1),37 ℃预处理1 h后,加入600 μL CAC,轻轻混匀后37 ℃作用30 min,于冰水浴中刮取细胞提取胞质蛋白,按前述方法进行Western blot检测和灰度分析。
1.3.9 统计学分析 实验检测数据以 ± s 表示,以SPSS 19.0进行单因素方差分析。
± s 表示,以SPSS 19.0进行单因素方差分析。
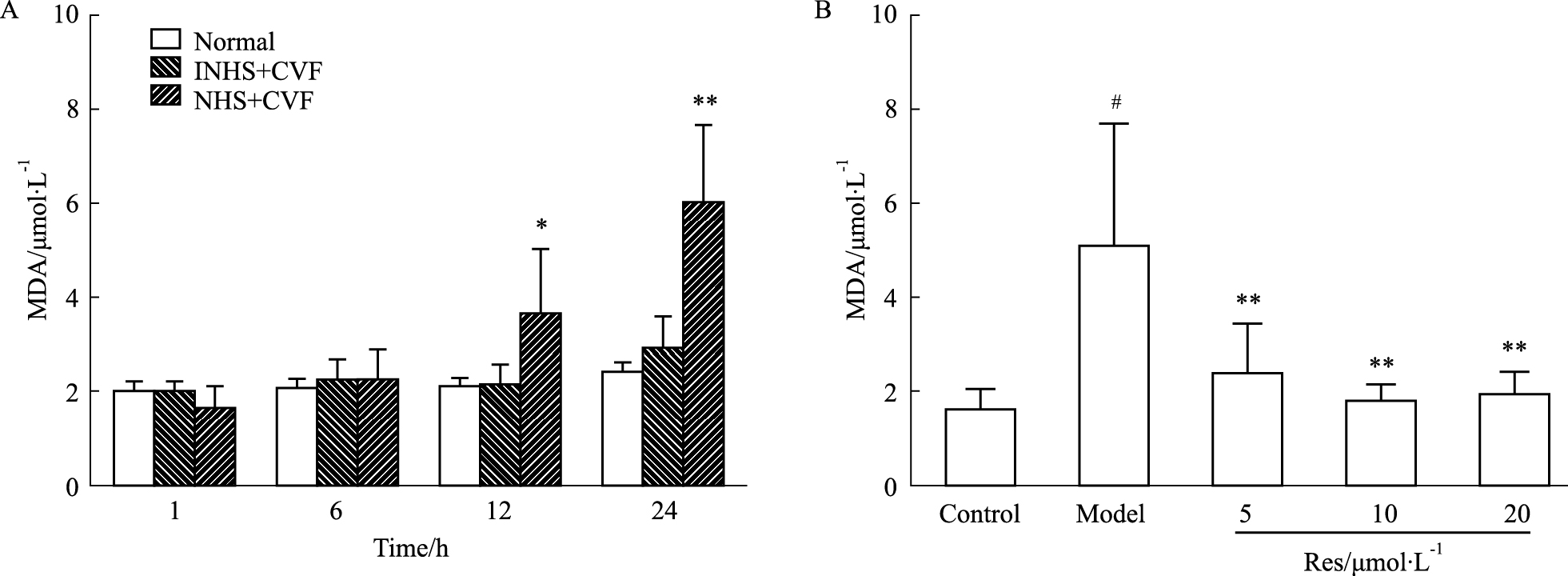
CAC作用于内皮细胞,其细胞培养液中MDA浓度随作用时间延长含量逐渐升高,在12 h时检测到MDA浓度的升高(P < 0.05),24 h时差异更明显(P < 0.01)。5 μmol·L-1的Res即可明显降低MDA的浓度,与模型组相比差异具有显著性(P < 0.01)(Fig1)。
|
| Fig 1 Effect of CAC on MDA concentration (n=4) A:Effect of CAC on MDA level with different stimulation time. *P<0.05,**P<0.01 vs 1 h (NHS+CVF) group; B:Effect of Res on MDA level induced by CAC for 24 h.**P<0.01 vs model;#P<0.05 vs control |
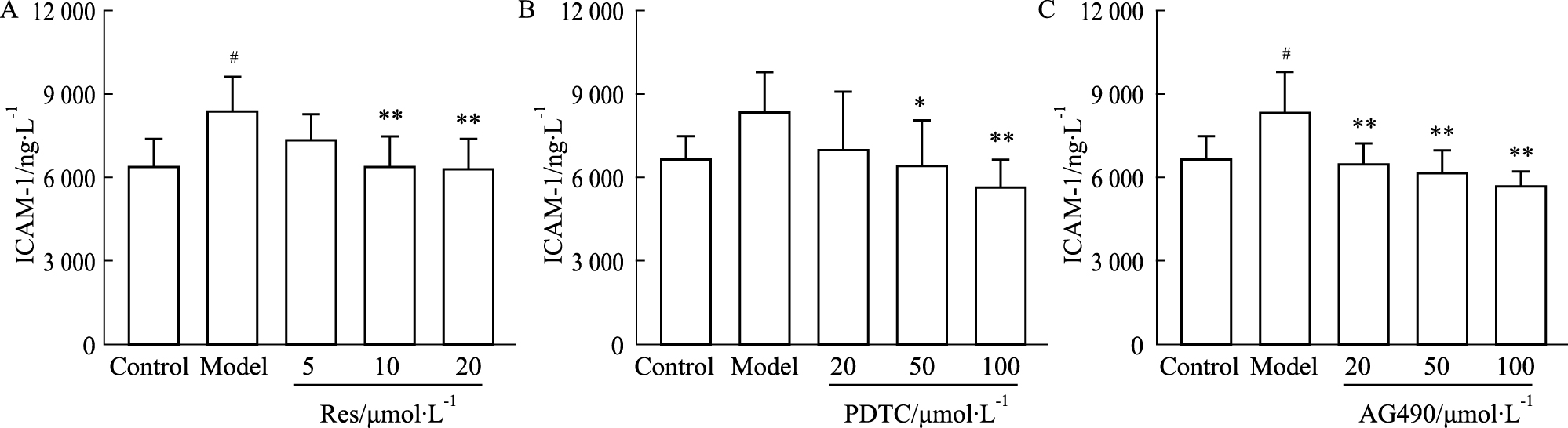
CAC作用于内皮细胞导致ICAM-1的表达上调,在6 h时检测到表达的高峰,与之前的结果类似[6]。不同浓度的Res、PDTC和AG490都能抑制ICAM-1的表达,其中10和20 μmol·L-1的Res、50和100 μmol·L-1的PDTC和20、50、100 μmol·L-1的AG490与模型组相比差异有显著性(P < 0.01或P < 0.05)(Fig2)。
|
| Fig 2 Effect of Res, PDTC and AG490 on ICAM-1 expression induced by CAC for 6 h (n=4) A:Res;B:PDTC;C:AG490. #P<0.05 vs control; *P<0.05,**P<0.01 vs model |
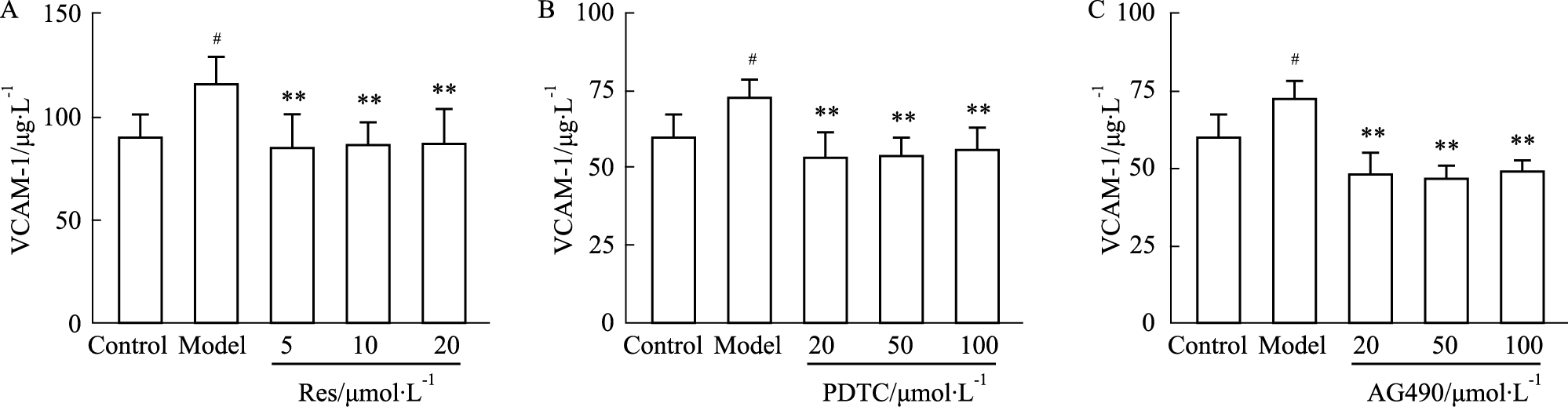
CAC作用于内皮细胞导致VCAM-1的表达上调,在6 h时检测到表达的高峰(数据未列)。测试的不同浓度的Res PDTC和AG490都能明显抑制VCAM-1的表达(P < 0.01)(Fig3)。
|
| Fig 3 Effect of Res, PDTC and AG490 on VCAM-1 expression induced by CAC for 6 h (n=4) A:Res;B:PDTC;C:AG490. #P<0.05 vs control;**P<0.01 vs model |
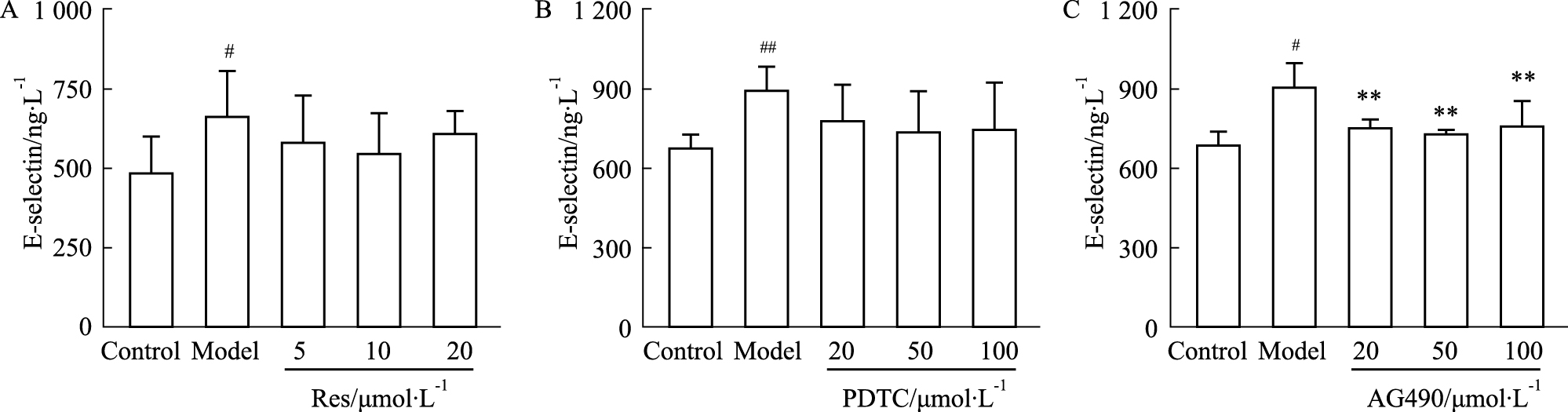
CAC作用于内皮细胞导致E-selectin的表达上调,并在12 h时检测到表达的高峰,与之前的结果类似[6]。Res和PDTC能在一定程度上抑制E-selectin的表达,而AG490能明显抑制E-selectin的表达(P < 0.01)(Fig4)。
|
| Fig 4 Effect of Res, PDTC and AG490 on E-selectin expression induced by CAC for 12 h (n=4) A:Res;B:PDTC;C:AG490. #P<0.05,##P<0.01 vs control; **P<0.01 vs model |
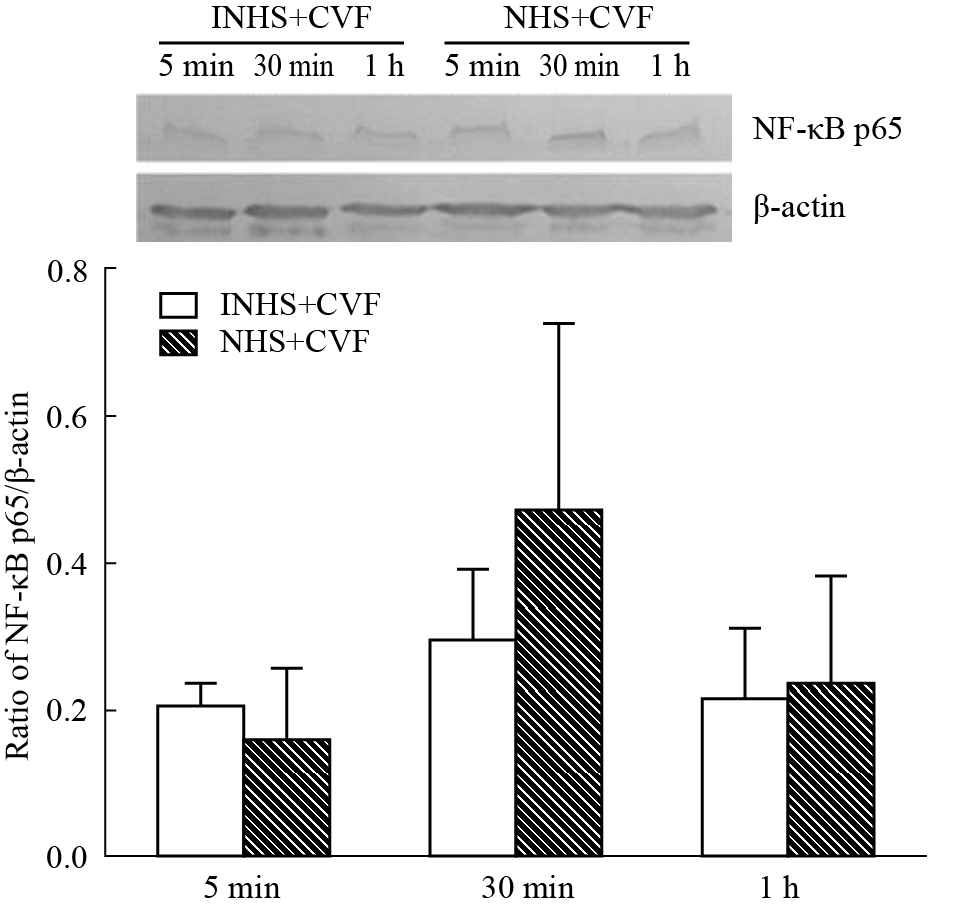
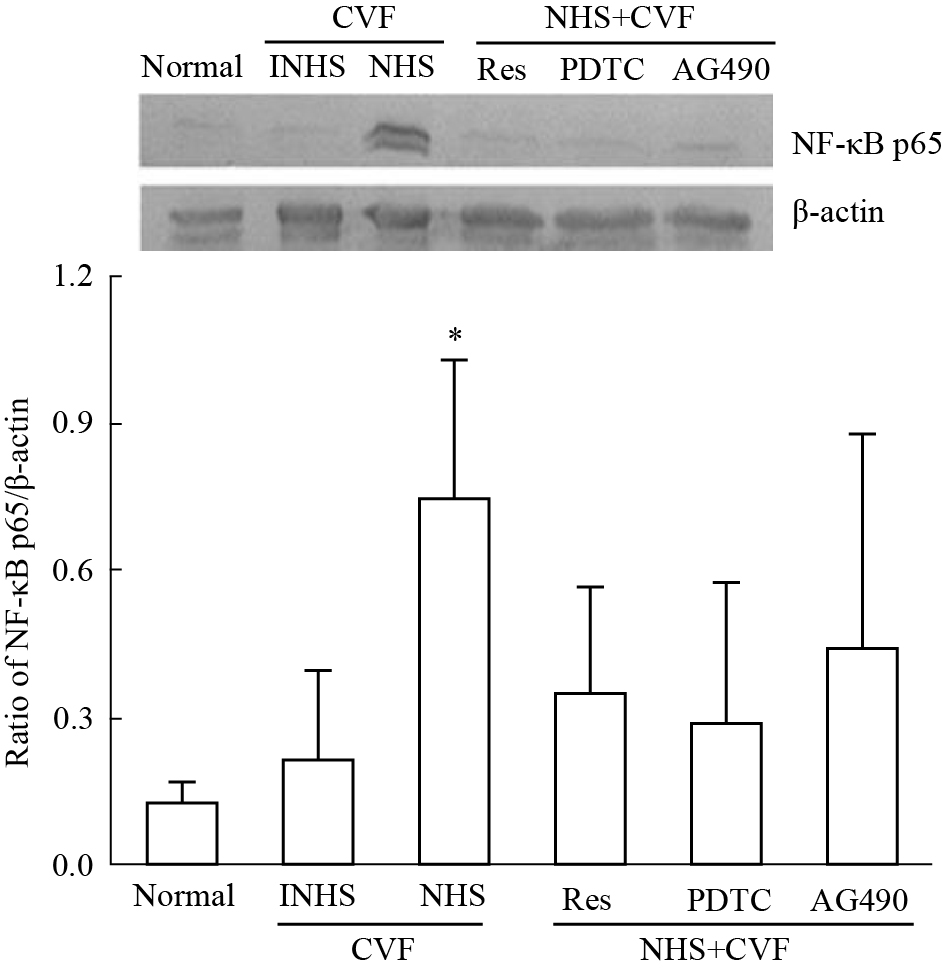
CAC分别刺激HMEC 5、30和60 min,检测到30 min组的NF-κB p65的磷酸化作用最明显(Fig5)。Res、PDTC和AG490对补体旁路激活产物引起的NF-κB p65磷酸化都表现出一定的抑制作用(Fig6)。
|
| Fig 5 NF-κB p65 phosphorylation in HMECS after exposure to CAC for different stimulation time (n=3) |
|
| Fig 6 Effect of different inhibitors on inhibiting NF-κB p65 phosphorylation in HMECS after exposure to CAC for 30 min (n=3) *P<0.05 vs (INHS+CVF) group |
补体旁路激活在多种疾病的发生发展中扮演着重要角色,补体激活产物会导致内皮细胞形态和功能改变,引起多种细胞因子的表达变化。本研究在课题组前期工作的基础上,采用CVF这一高度特异的补体替代途径激活蛋白来激活补体旁路。CVF在血清环境中可与补体B因子特异性结合,形成CVF·B复合物,它能被补体D因子特异性地识别和酶切,进而形成CVF·Bb复合物。该复合物具有C3/C5转化酶的活性,可以持续激活补体旁路途径,产生C3a、C3b、C5a及攻膜复合物等一系列活化产物。这种补体旁路途径的激活方式与体内病理生理条件下补体旁路途径的过度激活高度一致[6]。
研究结果显示,内皮细胞受到CAC刺激后会引起MDA浓度的持续升高,5 μmol·L-1的Res即能明显抑制补体旁路激活产物引起的MDA水平增高。这表明,补体旁路激活产物刺激内皮细胞存在氧化应激的作用,而Res能有效抑制氧化应激,与文献[7]报道的Res的抗氧化作用相吻合。
之前的研究表明,补体旁路激活会引起内皮细胞NF-κB、JAK2和p38 MAPK信号通路的活化[8],导致黏附分子P-selectin、ICAM-1和E-selectin的表达上调[6]。本实验采用能够抑制NF-κB信号通路和氧化应激的Res、NF-κB信号通路特异性抑制剂PDTC和JAK2信号通路特异性抑制剂AG490对黏附分子ICAM-1、VCAM-1和E-selectin的表达进行干预。结果显示,补体旁路激活产物刺激内皮细胞,引起NF-κB p65的磷酸化和内皮细胞可溶性黏附分子ICAM-1、VCAM-1、E-selectin的蛋白表达上调。Res、PDTC和AG490都能抑制NF-κB p65的磷酸化,但对黏附分子ICAM-1、VCAM-1和E-selectin表达的作用结果不同。Res与PDTC的作用结果相似,都能抑制ICAM-1和VCAM-1的表达,但对E-selectin表达的抑制作用不明显。这提示,NF-κB信号通路是补体旁路激活致黏附分子ICAM-1和VCAM-1表达的重要调控路径,但E-selectin的表达与NF-κB的关联度不高。AG490能明显抑制上述三种黏附分子的表达上调,提示了JAK2在补体旁路激活致黏附分子表达中可能是一个更重要的干预靶点。
目前的研究表明,与炎症相关的NF-κB、JAK2和MAPK信号通路之间存在网络交互性,同时氧化应激在炎症相关黏附分子的表达中也扮演着重要角色,其中VCAM-1的表达与NADPH氧化酶的活化和ROS的增高密切相关[9, 10, 11]。之前的研究表明,补体旁路激活引起的黏附分子表达变化至少涉及NF-κB和JAK2通路的活化,PDTC和AG490合用时能更明显抑制ICAM-1的表达[8]。目前对Res的研究表明,Res能抑制NF-κB信号通路的活化和氧化应激,而氧化应激主要与NADPH氧化酶活性相关,对NADPH氧化酶活性的抑制能减少ROS的生成[7],同时ROS又能刺激NF-κB的活化,这两种作用在Res抑制补体旁路激活致内皮细胞黏附分子的表达过程中是否同步存在尚需进一步验证。而Western blot的检测结果提示,AG490对JAK2的抑制也导致了对NF-κB p65磷酸化的抑制,JAK2可能是补体旁路激活致内皮细胞炎症反应中NF-κB和JAK2所组成的调控网络中的一个上游调控位点。
本研究表明,Res、PDTC和AG490三种化学小分子对补体旁路激活致内皮细胞黏附分子表达上调有不同程度的抑制作用,其作用机制与NF-κB信号通路的活化有关,而JAK2可能是一个更重要的调控位点。本研究为进一步阐明补体旁路激活致内皮细胞炎症反应相关信号通路的调控机制和潜在的作用靶点提供线索,同时也为Res的开发应用提供参考依据。
(致谢:本文实验是在贵州省中国科学院天然产物化学重点实验室药理与活性筛选中心孙黔云研究员课题组的实验室完成。)
| [1] | Rajendran P,Rengarajan T,Thangavel J,et al. The vascular endothelium and human diseases[J]. Int J Biol Sci,2013,9(10):1057-69. |
| [2] | Kerr H,Richards A. Complement-mediated injury and protection of endothelium:lessons from atypical haemolytic uraemic syndrome[J]. Immunobiology,2012,217(2):195-203. |
| [3] | 蒿雨露,孙黔云,李 敏. 补体旁路激活对内皮细胞纤溶功能的影响[J]. 中国药理学通报,2012,28(12):1772-3.Hao Y L,Sun Q Y,Li M. Effect of complement alternative activation on the fibrinolytic activity of endothelial cells[J].Chin Pharmacol Bull,2012,28(12):1772-3. |
| [4] | 李 敏,孙黔云,赵 琼,等. 补体旁路过度激活影响体内凝血功能[J]. 中国药理学通报,2014,30(1):39-44.Li M,Sun Q Y,Zhao Q,et al. Abnormality of blood coagulation induced by excessive activation of the alternative complement pathway[J]. Chin Pharmacol Bull,2014,30(1):39-44. |
| [5] | 孙黔云,王婉瑜,熊郁良. 眼镜蛇毒高活性抗补体因子的体外溶血活性研究[J]. 中国药理学通报,2003,19(8):909-13.Sun Q Y,Wang W Y,Xiong Y L. In vitro hemolyzation of a highly active anticomplement factor from the venom of Naja kaouthia[J]. Chin Pharmacol Bull,2003,19(8):909-13. |
| [6] | 孙黔云,李 敏,叶巧玲,李红玲. 补体旁路激活导致内皮细胞活化和损伤[J]. 中国药理学通报,2012,28(7):925-9. Sun Q Y,Li M,Ye Q L,Li H L. Endothelial cell activation and injury induced by complement alternative pathway[J]. Chin Pharmacol Bull,2012,28(7):925-9. |
| [7] | Chen F,Qian L H,Deng B,et al. Resveratrol protects vascular endothelial cells from high glucose-induced apoptosis through inhibition of NADPH oxidase activation-driven oxidative stress[J]. CNS Neurosci Ther,2013,19(9):675-81. |
| [8] | 李红玲,孙黔云,李 敏,石京山. 补体旁路激活产物刺激内皮细胞NF-κB、p38MAPK、JAK2通路活化及抑制剂的干预研究[J].中国细胞生物学学报,2013,35(6):836-41. Li H L,Sun Q Y,Li M,Shi J S. Activation of NF-κB, p38MAPK, and JAK2 in endothelial cells induced by activated complement alternative pathway and intervention by inhibitors[J]. Chin J Cell Biol,2013,35(6):836-41. |
| [9] | Wung B S,Hsu M C,Wu C C,Hsieh C W. Resveratrol suppresses IL-6-induced ICAM-1 gene expression in endothelial cells:effects on the inhibition of STAT3 phosphorylation[J]. Life Sci,2005,78(4):389-97. |
| [10] | Cook-Mills J M. VCAM-1 signals during lymphocyte migration:role of reactive oxygen species[J]. Mol Immunol,2002,39(9):499-508. |
| [11] | Carluccio M A,Ancora M A,Massaro M,et al. Homocysteine induces VCAM-1 gene expression through NF-kappaB and NAD(P)H oxidase activation:protective role of Mediterranean diet polyphenolic antioxidants[J]. Am J Physiol Heart Circ Physiol,2007,293(4):H2344-54. |

