2. 南通大学附属医院心胸外科实验室, 江苏 南通 226001
2. Dept of Cardiothoracic Surgery, Affiliated Hospital of Nantong University, Nantong Jiangsu 226001, China
心肌纤维化是指在心肌的正常组织结构中胶原纤维过量积聚,胶原浓度明显升高,各型胶原比例失调以及排列紊乱等[1]。它是多种心脏疾病发展到一定阶段的共同病理改变,是心肌重构的主要表现之一。基于心肌纤维化已成为慢性心功能不全难以逆转的原因之一,常导致严重的后果,因此研究切实有效的防治措施具有十分重要的意义。
2,3,5,4′-四羟基二苯乙烯-2-O-β-D葡糖苷(2,3,5,4′-tetrahydroxystilbene-2-O-β-D-glucoside,TSG)简称二苯乙烯苷,是何首乌的主要药效成分,已被证实对心血管系统有一系列有效作用,如:TSG能降低血脂[2]、抑制动脉粥样硬化进程[3]、修复血管内皮[4]、抑制血管平滑肌细胞增殖及内膜增生[5, 6]、对心肌细胞具有保护作用[7]。但TSG对心肌纤维化作用尚在进一步探讨中。本实验首次研究TSG对异丙肾上腺诱导的小鼠心肌纤维化的作用及其相关机制,为TSG的开发和临床应用提供理论和实验依据。
1 材料与方法 1.1 材料 1.1.1 动物昆明种小鼠,♂,体质量(20±2)g,SPF级,由南通大学实验动物中心提供,许可证号:SYXK9 (苏)2002-0022。
1.1.2 药品及试剂二苯乙烯苷口服液由南通大学医学院中药研究室提取提供,含量>95% (HPLC法),批号20130702;异丙肾上腺素购于上海禾丰制药有限公司,批号130701;卡托普利购于上海衡山药业有限公司,批号120308;羟脯氨酸(hydroxyproline,HYP)、超氧化物歧化酶(superoxide dismutase,SOD)、谷胱甘肽过氧化物酶(glutathione peroxidase-Px,GSH-Px)检测试剂盒购于南京建成生物公司;胶原Ⅰ型 (CollagenⅠ)和胶原Ⅲ型(Collagen Ⅲ)一抗购于Proteintech Group公司;转化生长因子-β1(transforming growth factor-β1,TGF-β1)一抗购于巴傲得生物科技有限公司公司;内参GAPDH购于康成生物;鼠抗、兔抗等二抗均购自 Odessey 公司;山羊血清封闭液购于EATAR公司;Cy3标记山羊抗兔IgG、BCA蛋白定量试剂盒、细胞裂解液均购于碧云天公司。其它试剂均为国产分析纯。
1.1.3 仪器PowerWave340酶标仪(美国Bio-TEK公司)、红外双色激光成像系统扫描仪(美国Odessey 公司)、电泳及转印装置(美国BIO-RAD公司)、冰冻切片机(LEICA CM1900)。
1.2 方法 1.2.1 动物模型制备小鼠背部皮下注射异丙肾上腺素(isoproterenol,ISO),首次剂量为40 mg·kg-1,d 2剂量为20 mg·kg-1,d 3剂量为10 mg·kg-1,d 4剂量为5 mg·kg-1,并以此剂量再维持10 d,自由进食、给水,对照组小鼠皮下注射相同体积的生理盐水[8]。
1.2.2 给药和分组小鼠随机分为6组,即正常对照组、模型组、二苯乙烯苷高、中、低剂量组(120,60,30 mg·kg-1)、卡托普利组(40 mg·kg-1)。每组10只。给药组小鼠连续灌胃14 d,对照组和模型组给予相同体积的生理盐水。实验期间,未见被观察动物死亡。
1.2.3 心肌组织病理学检查末次给药12 h后,颈椎脱臼处死小鼠,用冷生理盐水清洗小鼠心脏组织,滤纸吸干,取左室心肌组织,4%多聚甲醛固定,HE和Masson染色制片,镜下观察心肌细胞变性、炎症浸润、胶原纤维增生程度等组织形态学变化,用Image Pro Plus 6.0软件对图像进行分析,计算心肌胶原容积分数(collagen volume fraction,CVF) 。CVF 为胶原的面积占总面积的比值。
1.2.4 Weston blot检测取各组新鲜大鼠左室心肌组织,提取蛋白,采用BCA比色法进行蛋白定量。加上样缓冲液,100℃变性5 min。每孔50 μg蛋白上样,10% SDS-聚丙烯酰胺凝胶电泳,转膜,封闭,加入一抗稀释液,4℃过夜,TBST洗膜,加入二抗(1 ∶ 5 000稀释),室温孵育2 h,显影。以GAPDH为内参照,测定各组蛋白表达量与内参表达量的比。
1.2.5 免疫荧光检测小鼠心肌组织中TGF-β1的表达取各组心肌组织包埋后行冰冻切片,每片5 μm厚,室温风干。将切片放入已沸腾的柠檬酸缓冲液中,中档微波处理10 min,取出微波盒,流水冷却,取出玻片,用蒸馏水冲洗2次,再用PBS冲洗2次。每张切片加10 ~20 μL山羊血清,37℃封闭20 min。除去多余血清,加入TGF-β1一抗,37℃孵育1 h。PBS洗涤3次。空白对照组中用PBS代替一抗。每张切片加入Cy3标记山羊抗兔IgG,37℃避光孵育1h。PBS洗涤3次。蒸馏水浸洗1 min。用50%甘油封片,荧光显微镜观察。Image Pro Plus 6.0软件测量每张切片阳性表达颗粒的积分光密度(integral optical density,IOD)值。
1.2.6 心肌组织HYP、SOD及GSH-Px测定取适量的组织样品,然后准确称重。按照重量体积比1 ∶ 9加入9倍体积生理盐水,剪碎组织,冰浴中用玻璃匀浆器制备10%组织匀浆,3 000 r·min-1,离心10 min,取上清即待用。心肌组织HYP、SOD及GSH-PX测定分别按照相关检测试剂盒的说明书操作。
1.2.7 数据统计分析实验数据以  ± s表示,采用单因素方差分析方法进行分析,组间比较用Student-Newman-Keuls检验。
± s表示,采用单因素方差分析方法进行分析,组间比较用Student-Newman-Keuls检验。
HE 和 Masson 染色结果 HE染色结果显示,正常组心肌纤维均匀致密,排列整齐,无心肌纤维破坏,横纹清晰,核居中,间质未见明显血管扩张及炎细胞浸润。模型组心肌细胞灶状变性、坏死,坏死灶内及周围心肌间质可见大量炎细胞浸润,心肌细胞横径稍大,心肌纤维断裂,心肌细胞间隙明显增宽,间质水肿,血管周围和心肌细胞间可见明显纤维结缔组织增生。给药组均能不同程度地减轻心肌细胞损伤,即心肌细胞变性、坏死及纤维化程度减轻,炎细胞浸润程度降低,间质水肿减轻。与低剂量组相比,二苯乙烯苷高剂量组改善的更为明显(Fig1)。

|
| Fig 1 HE staining of myocardial tissues (200×) 1: Control group; 2: Model group; 3: Captopril (40 mg·kg-1) group; 4: 120 mg·kg-1 TSG group; 5: 60 mg·kg-1TSG group; 6: 30 mg·kg-1 TSG group. |
经Masson特殊染色后,光镜下可见心肌被染成红色,心肌间质胶原纤维被染成蓝色。与正常对照组相比,模型组心肌细胞间胶原纤维增生明显,CVF值明显增加(P < 0.01);与模型组相比,二苯乙烯苷能抑制心肌细胞间胶原纤维增生,尤其是高剂量组CVF值明显降低(P < 0.01)(Fig2)。

|
| Fig 2 Masson specific staining of myocardial tissues (200×) A: Masson staining, 1: Control group; 2: Model group; 3: Captopril (40 mg·kg-1·d-1) group; 4: 120 mg·kg-1 TSG group; 5: 60 mg·kg-1TSG group; 6: 30 mg·kg-1 TSG group. B: CVF (x±s, n=6). TSG 120:TSG, 120 mg·kg-1; TSG 60:TSG, 60 mg·kg-1; TSG 30:TSG, 30 mg·kg-1. **P < 0.01 vs control; #P < 0.05,##P < 0.01 vs model. |
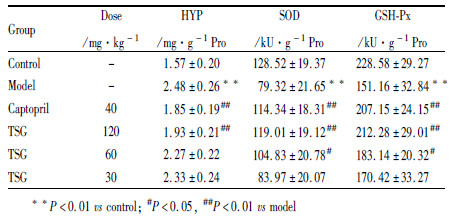
小鼠心肌组织内羟脯氨酸检测结果显示,与正常对照相比,模型组羟脯氨酸含量明显升高 (P < 0.01);相较于模型组,二苯乙烯苷120 mg·kg-1剂量组羟脯氨酸含量明显降低(P < 0.01)(Tab1)。
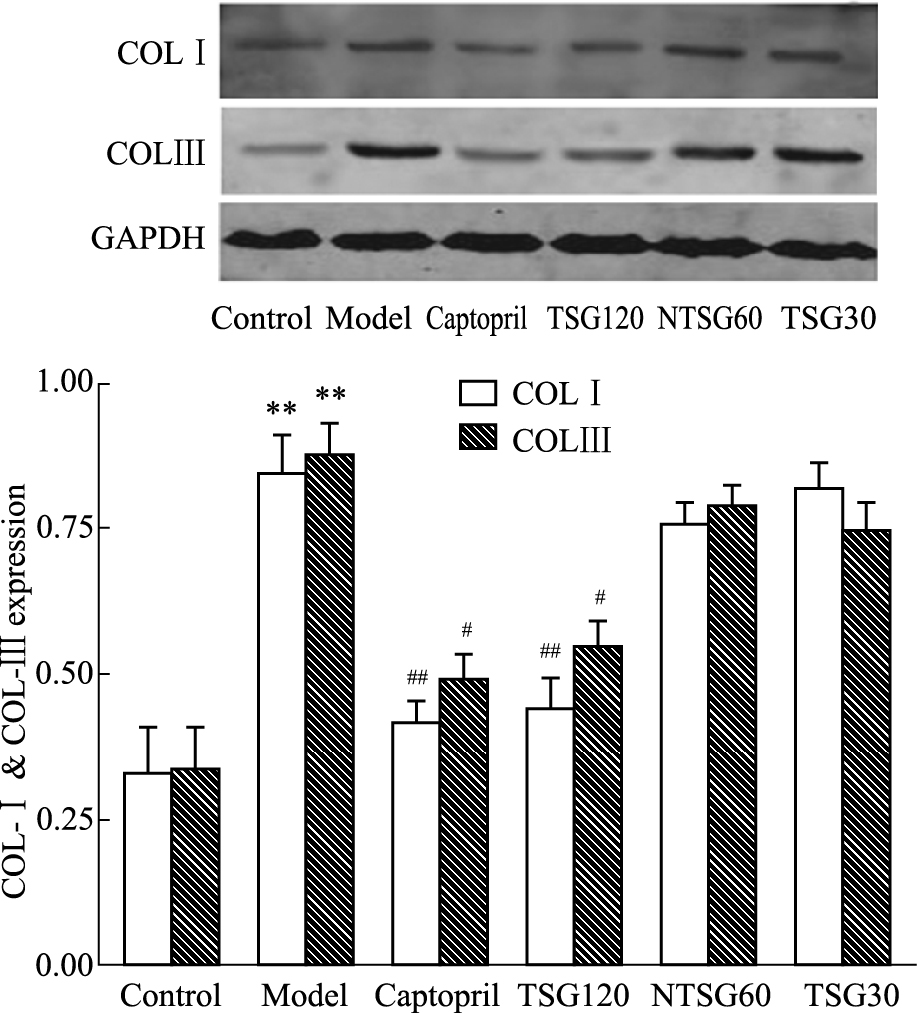
Western blot检测结果显示,模型组小鼠心脏组织中Ⅰ、Ⅲ型胶原表达较正常对照组明显提高(P < 0.01);与模型组相比,二苯乙烯苷120 mg·kg-1剂量组的Ⅰ、Ⅲ型胶原表达均明显下降(分别P < 0.01,P < 0.05) (Fig3)。
|
Fig 3
Effect of TSG on protein levels of collagenⅠ(COL-Ⅰ) and collagen Ⅲ (COL-Ⅲ) (  ± s, n=8)
TSG 120:TSG, 120 mg·kg-1; TSG 60:TSG, 60 mg·kg-1; TSG 30:TSG, 30 mg·kg-1. **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model. ± s, n=8)
TSG 120:TSG, 120 mg·kg-1; TSG 60:TSG, 60 mg·kg-1; TSG 30:TSG, 30 mg·kg-1. **P < 0.01 vs control; #P < 0.05, ##P < 0.01 vs model.
|
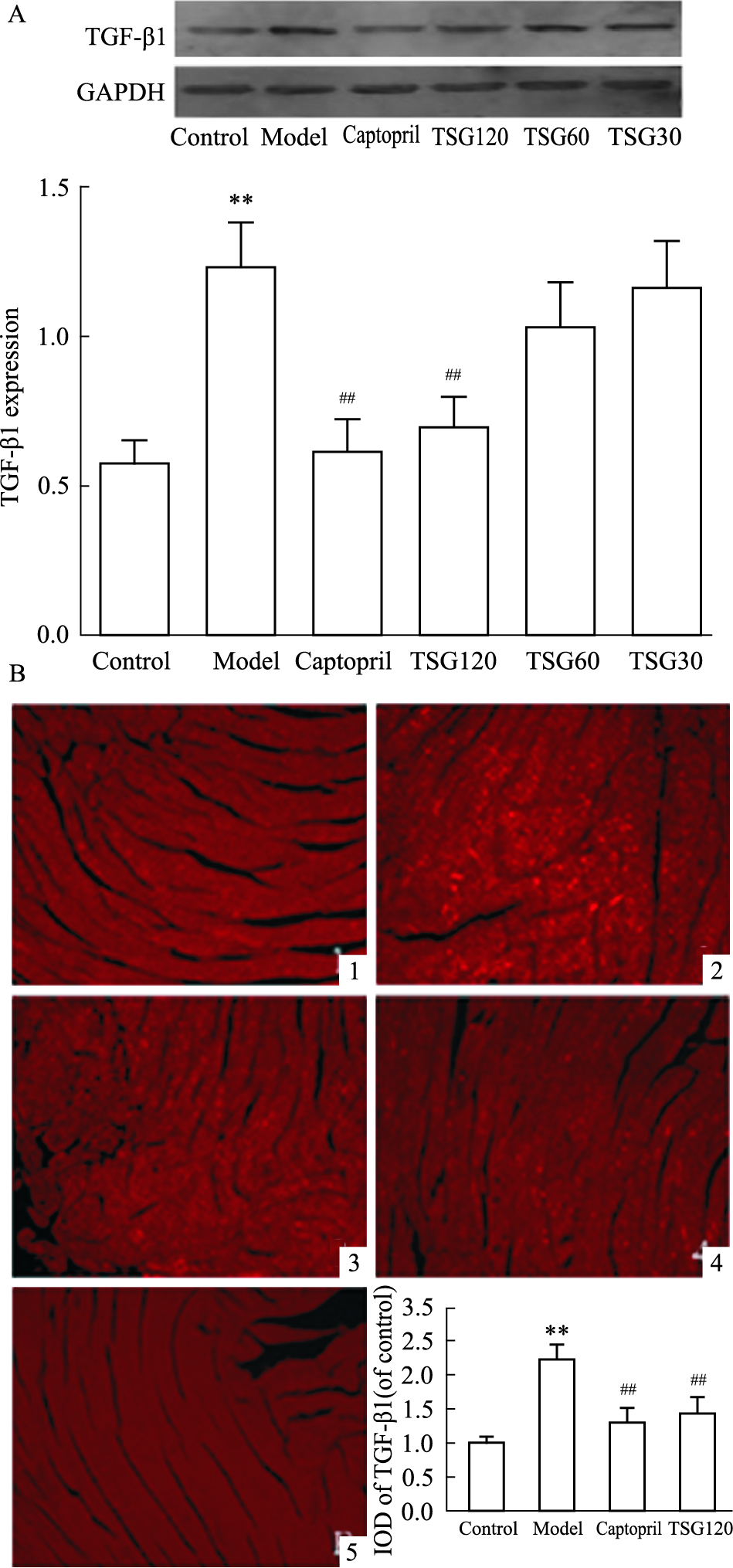
Western blot和小鼠心肌组织免疫荧光检测结果显示,模型组TGF-β1的表达明显高于正常对照组(P < 0.01);与模型组相比,卡托普利和二苯乙烯苷120 mg·kg-1剂量组明显下调TGF-β1的表达水平(P < 0.01)(Fig4)。
|
Fig 4
Effect of TSG on TGF-β1 protein expression (  ± s)
A: Western blot analysis of TGF-β1 protein expression. B: Representative immunofluorescence images of TGF-β1 (100×). 1: control group; 2: model group; 3: Captopril (40 mg·kg-1) group; 4: 120 mg·kg-1 TSG group. 5: Blank control. IOD of TGF-β1 normalized to the control group. TSG 120:TSG, 120 mg·kg-1; TSG 60:TSG, 60 mg·kg-1; TSG 30:TSG, 30 mg·kg-1. **P < 0.01 vs control; ## P < 0.01 vs model. ± s)
A: Western blot analysis of TGF-β1 protein expression. B: Representative immunofluorescence images of TGF-β1 (100×). 1: control group; 2: model group; 3: Captopril (40 mg·kg-1) group; 4: 120 mg·kg-1 TSG group. 5: Blank control. IOD of TGF-β1 normalized to the control group. TSG 120:TSG, 120 mg·kg-1; TSG 60:TSG, 60 mg·kg-1; TSG 30:TSG, 30 mg·kg-1. **P < 0.01 vs control; ## P < 0.01 vs model.
|
与正常对照组相比,模型组小鼠心肌组织中SOD的酶活力明显下降(P < 0.01);与模型组相比,TSG 120 mg·kg-1和 60 mg·kg-1剂量组均能明显升高小鼠心肌组织中SOD的酶活力(P < 0.01或P < 0.05);与SOD酶活力相似,TSG 120 mg·kg-1和60 mg·kg-1剂量组能抑制异丙肾上腺素引起的小鼠心肌组织中GSH-Px活力的下降(P < 0.01或P < 0.05)(Tab1)。
3 讨论心肌纤维化可分反应性纤维化和修复性纤维化。反应性纤维化是压力超负荷心脏所致,引起心脏收缩及舒张功能不全,最终导致心衰;修复性纤维化主要表现为心肌细胞凋亡坏死、纤维化灶(疤痕)形成并可有心脏功能的异常[9]。我们以往的研究已表明二苯乙烯苷能明显抑制大鼠腹主动脉结扎致 心脏压力超负荷所复制的反应性心肌纤维化模型[10]。为了全面了解二苯乙烯苷对心肌纤维化的作用,本实验采用注射异丙肾上腺素建立修复性心肌纤维化模型,观察二苯乙烯苷对修复性心肌纤维化的作用。
大剂量异丙肾上腺素引起心肌细胞变性与坏死、心肌细胞肥大、胶原纤维增生等超微结构改变类似缺血性心肌坏死,连续用能引起动物心肌肥厚和心肌纤维化,其机制为激活β受体、肾素血管紧张素醛固酮系统,并可能通过多种细胞信号转导途径影响纤维化过程[11]。该模型具有心肌纤维化改变出现早、效果稳定持久、简单易行,为研究心肌修复性纤维化的常用模型。本实验中,我们给小鼠连续皮下注射异丙肾上腺素2周,病理学检查显示,模型组有明显的胶原纤维增生、断裂,大量的心肌细胞坏死,心肌纤维化程度重要指标羟脯氨酸含量明显增加,与文献的报道相一致[8, 12],证实了异丙肾上腺素能造成明显的心肌损伤和纤维化。正常心肌细胞外基质中的胶原主要为 I 型及Ⅲ型。异常增多且比例失调的胶原纤维使心室壁的顺应性下降,如果心肌纤维化进一步加重,势必损害心肌的收缩功能[1]。连续注射异丙肾上腺素后,心肌组织I 、Ⅲ型胶原蛋白表达明显增高。以上实验结果显示该注射方案成功复制了修复性心肌纤维化。而二苯乙烯苷干预组可有效减轻心肌纤维化损伤,降低心肌羟脯氨酸含量及I 、Ⅲ型胶原蛋白表达。二苯乙烯苷高剂量组改善的更为明显。
TGF-β1是导致心肌纤维化诸多因素最后的共同中介之一,在心肌中对于细胞增殖、分化、迁移和细胞外基质的沉积均有重要的作用。一方面,TGF-β1可刺激心肌成纤维细胞大量增生及分化,促进细胞中Ⅰ、Ⅲ型胶原蛋白的表达;另一方面,TGF-β1可以诱导心肌成纤维细胞表型转变,心肌成纤维细胞转变成肌成纤维细胞,进一步促进以Ⅰ、Ⅲ型胶原为主的间质蛋白质的合成;同时TGF-β1能抑制蛋白分解酶,最终加速细胞外基质的沉积并导致心肌纤维化发生[13]。Western blot和心肌组织免疫荧光检测显示,与模型组相比二苯乙烯苷能明显下调TGF-β1蛋白表达。结合体外细胞实验表明,TSG能抑制TGF-β1诱导的心肌成纤维细胞增殖和Ⅰ、Ⅲ型胶原合成[14],推测二苯乙烯苷对修复性心肌纤维化抑制作用可能与调节TGF-β1蛋白表达有关。
心肌纤维化的发展与大量氧自由基生成及脂质过氧化反应密切相关[15]。正常情况下,细胞所具有的抗氧化机制可清除活性氧(reactive oxygen species,ROS),维持细胞氧化还原自稳态。当某些因素作用于细胞使这一稳态失调,活性氧产生的速率大于清除的速率时,就会造成ROS的蓄积。ROS扮演着类似第二信使的角色,通过激活包括蛋白激酶在内的多种下游受控子,刺激许多转录因子和信号级联,包括活化TGF-β1 信号通路,促进胶原的合成[16]。二苯乙烯苷属多酚类化合物,具有强大的抗氧化作用[5]。在本实验中,我们发现心肌纤维化小鼠心肌组织中的抗氧化酶SOD和GSH-Px活性明显降低,中、高剂量的二苯乙烯苷可以明显增强SOD和GSH-Px的酶活性。因此结合氧化应激与心肌纤维化关系密切的理论基础,我们推测二苯乙烯苷的抗氧化作用为其抗心肌纤维化作用的机制之一。
综上所述,氧化应激和TGF-β1过度表达参与修复性心肌纤维化的过程,二苯乙烯苷对异丙肾上腺素引起的心肌纤维化具有良好的改善作用,其可能的作用机制包括抗氧化和抑制TGF-β1表达等。
(致谢:本实验在南通大学药学院药理学教研室和江苏省炎症与分子药靶重点实验室完成。)
| [1] | Kong P, Christia P, Frangogiannis N G. The pathogenesis of cardiac fibrosis[J]. Cell Mol Life Sci, 2014, 71(4):549-74. |
| [2] | Zhang W, Wang C H, Li F, Zhu W Z. 2,3,4',5-Tetrahydroxystilbene-2-O-beta-D-glucoside suppresses matrix metalloproteinase expression and inflammation in atherosclerotic rats[J]. Clin Exp Pharmacol Physiol, 2008; 35(3):310-316. |
| [3] | 崔慧辉,田 英,龙石银.二苯乙烯苷抗动脉粥样硬化的作用和机制[J]. 现代生物医学进展,2009, 9(20):3968-71. Cui H H, Tian Y, Long S Y. The effective mechanism of 2,3,5,'4-tetrahydroxystilbene-2-O-β-D-glucoside in anti-atherosclerosis[J]. Prog Mod Biomed, 2009, 9(20):3968-71. |
| [4] | Zhang W, Xu X L, Wang Y Q, et al. Effects of 2,3,4',5-tetrahydroxystilbene 2-O-beta-D-glucoside on vascular endothelial dysfunction in atherogenic-diet rats[J]. Planta Med, 2009, 75(11):1209-14. 许晓乐,张 伟,黄燕娟,王玉琴. 二苯乙烯苷对平滑肌细胞增殖及其抗氧化作用的影响[J]. 中国药理学通报, 2010, 26(7):934-9. |
| [5] | Xu X L, Zhang W, Huang Y J, Wang Y Q. Effect of 2,3,4',5-tetrahydroxystilbene-2-O-β-D glucoside on proliferation and antioxidation of vascular smooth muscle cells[J]. Chin Pharmacol Bull, 2010, 26(7):934-9. |
| [6] | Xu X L, Ling D Y, Zhu Q Y, et al. The effect of 2,3,4',5-tetrahydroxystilbene-2-O-β-D glucoside on neointima formation in a rat artery balloon injury model and its possible mechanisms[J]. Eur J Pharmacol, 2013, 698(1-3):370-8. |
| [7] | Zhang S H, Wang W Q, Wang J L. Protective effect of tetrahydroxystilbene glucoside on cardiotoxicity induced by doxorubicin in vitro and in vivo[J]. Acta Pharmacol Sin, 2009, 30(11):1479-87. |
| [8] | 李 明,张 军,陈 燕,等. 丹参抑制异丙肾上腺素引起的小鼠心肌肥厚和纤维化及其作用机制[J]. 中国药科大学学报, 2003, 34(6):565-8. Li M,Zhang J, Chen Y, et al. Danshen inhibiting isoproterenol induced cardiac hypertrophy and fibrosis in mice and its mechanisms[J]. J China Pharm Univ, 2003, 34(6):565-8. |
| [9] | 张 运,徐 瑞.心肌纤维化-心力衰竭治疗的新靶标[J].中华医学杂志, 2006, 86(17):1155-7. Zhang Y, Xu R. Myocardial fibrosis-A new target for the treatment of heart failure[J]. Nat Med J Chin, 2006, 86(17):1155-7. |
| [10] | Xu X L, Zhu Q Y, Zhao C, et al. The effect of 2,3,4',5-tetrahydroxystilbene-2-O-β-D-glucoside on pressure overload-induced cardiac remodeling in rats and its possible mechanism[J]. Planta Med, 2014, 80(2-3):130-8. |
| [11] | Grimm D, Elsner D, Schunkert H, et al. Development of heart failure following isoproterenol administration in the rat:role of the renin-angiotensin system[J]. Cardiovasc Res, 1998, 37:91-100. |
| [12] | 陈 蓉, 谢梅林. 异丙肾上腺素致小鼠心肌纤维化模型的制备及评价[J]. 中国药理学通报, 2014, 30(9):1325-8. Chen R, Xie M L. Establishment and evaluation of isoprenaline-induced myocardial fibrosis mouse model[J]. Chin Pharmacol Bull, 2014, 30(9):1325-8. |
| [13] | Khan R, Sheppard R. Fibrosis in heart disease:understanding the role of transforming growth factor-beta in cardiomyopathy, valvular disease and arrhythmia[J]. Immunology, 2006, 118(1):10-24. |
| [14] | 曾 翼,赵 诚,王 霏,等.二苯乙烯苷对 TGF-β1 诱导新生大鼠心肌成纤维细胞增殖和胶原合成的影响及其机制[J]. 中国药科大学学报, 2014,45(3):362-7. Zeng Y, Zhao C, Wang F, et al. Effects and mechanisms of stilbene glucoside on the proliferation and collagen synthesis of cardiac fibroblasts stimulated by TGF-β1[J]. J China Pharm Univ, 2014,45(3):362-7. |
| [15] | Tanaka R, Shimizu M. The relationship between reactive oxygen species and cardiac fibrosis in the dahl salt-sensitive rat under ACEI administration[J]. Vet Med Int, 2012, 2012:105316. |
| [16] | Purnomo Y, Piccart Y, Coenen T, et al. Oxidative stress and transforming growth factor-β1-induced cardiac fibrosis[J]. Cardiovasc Hematol Disord Drug Targets, 2013, 13(2):165-72. |