


2. 娄底市卫生学校, 湖南 娄底 417000
2. Loudi Health School, Loudi Hunan 417000, China
氧化应激诱导机体产生大量的活性氧(ROS)。ROS是诱发心血管疾病的潜在危险因素。ROS可降解一氧化氮合酶(nitric oxide synthase,NOS),并直接灭活NO;ROS还能通过与底物的相互作用,引起内皮细胞损伤,启动炎症反应;通过激活核因子- κB(NF-κB)及转录活化因子(AP-1)而引发细胞凋亡,并进一步促进损伤的血管内皮处的炎性反应;同时ROS还能诱导血管平滑肌细胞的增殖。所有这些都可能导致血管内皮功能障碍。
体内有多种酶参与了 ROS的生成,目前研究表明[1],NADPH氧化酶在多种因素刺激内皮细胞生成 ROS的过程中起主要作用。NADPH氧化酶在体内主要分布于吞噬细胞,另外也分布于血管内皮细胞、平滑肌细胞、心肌细胞、成纤维细胞等非吞噬细胞。近来的研究表明,NADPH氧化酶由6种亚基构成,内皮细胞上有其主要功能亚基 Nox4及 p22phox亚基的表达。研究发现,异位表达的 Nox4可与 p22phox结合形成复合物,增加 Nox4的稳定性;同时 Nox4也能促进 p22phox的表达,促进依赖 Nox4的ROS产生[2, 3]。
对氧磷(paraoxon,PO)是有机磷酸酯类在体内的活性代谢形式。PO可引起机体产生大量过氧化物及氧自由基,抑制对氧磷酶-1(PON1)的过氧化物酶样作用,抑制 SOD活性,诱发机体氧化应激,导致血管内皮细胞损伤。我们早期通过离体血管环实验也证实了 PO可导致大鼠胸主动脉内皮依赖性舒张功能(EDR)损伤,引起血管舒缩功能异常[4]。
染料木素(genistein,GST)为一种植物雌激素,广泛存在于豆科植物中。很多研究都证实,GST具有抗氧化活性,可对抗 DNA氧化损伤[5, 6]。GST具有多羟基酚结构,可直接与超氧阴离子等自由基结合,抑制氧自由基反应及脂质的过氧化反应;GST可升高 SOD的活性、谷胱甘肽(glutathione,GSH)水平,并上调谷胱甘肽过氧化物酶(GSH-Px)的水平和活性,加快氧自由基的清除[7, 8];抑制 NADPH氧化酶 p22phox亚基的表达,抑制 ROS的产生[9]。GST的抗氧化作用可避免或减轻血管内皮细胞的氧化损伤,维持血管内皮的正常功能。本实验室早期研究发现,GST可明显改善 PO诱导的大鼠胸主动脉内皮依赖性舒张功能异常,维持血管正常舒缩功能[4]。
综上所述,PO引起机体氧化应激,造成血管内皮细胞氧化损伤,血管正常结构和功能受损。GST则具有抗氧化作用,减低氧化应激对血管内皮造成的损伤。结合本实验室早期大鼠胸主动脉内皮依赖性舒张功能的实验结果,笔者推测 GST通过其抗氧化作用对抗 PO对血管功能的损伤。本实验旨在于探讨PO氧化损伤血管内皮,导致血管内皮功能失调及GST抗氧化、保护血管内皮功能,是否均与 NADPH氧化酶分布在血管内皮上的 p22phox与 Nox4亚基的表达水平相关。本课题的研究将为有机磷酸酯类农药诱发心血管疾病的发生机制及GST对此类疾病可能的防治提供理论参考及实验依据。
1 材料与方法 1.1 材料 1.1.1 动物与试剂♂ SD大鼠20 只,体质量220~280 g,南华大学实验动物中心提供。对氧磷(Dr. Ehrenstorfer GmbH);染料木素(杭州浙大泛科化工有限公司);Nox4、p22phox引物[生工生物工程(上海)有限公司];β-actin(235bp)引物[英潍捷基(上海)贸易有限公司];β-actin(394bp)引物(上海捷倍思基因技术有限公司);抗 p22phox鼠单克隆抗体(Santa Cruz Biotechnology);抗 Nox4兔单克隆抗体(Abcam);抗 β-actin鼠单克隆抗体(北京康为世纪生物技术有限公司);其余试剂均为进口或国产生物试剂。对氧磷、染料木素均用0.1%的 DMSO溶解后,再用去离子水稀释至所需浓度。
1.1.2 仪器pH计(MP220型,METTLER TOLEDO);高速低温离心机(5810R型,Eppendorf);紫外-可见分光光度计(UV2450型,SHIMADZU);PCR仪、Mini-Protean垂直板电泳槽、湿转仪(Bio-Rad);凝胶成像系统(Tanon);琼脂糖水平电泳槽(北京六一仪器厂);酶标仪(ELX 800,Bio-TEK INSTRUMENTS. INC)。
1.2 方法 1.2.1 模型建立♂ SD大鼠,颈椎脱臼处死,取出胸主动脉,置于实验当天配制的充氧(95% O2/5% CO2)的冰 Kreb’s液中[4℃,Kerb′s液用高压处理后的0.1%焦碳酸二乙酯(DEPC)水配制,调pH 7.2~7.4,于超净工作台滤过除菌],剥离周围结缔组织,将胸主动脉移置含10 mL Kerb′s液的安瓿瓶内,37℃恒温,同时通入95% O2/5% CO2混合气体。实验设4组:① 溶媒对照组:加入终浓度0.1% DMSO;② GST处理组:加入终浓度100 μmol·L-1的 GST;③ PO处理组:加入终浓度40.5 μmol·L-1的 PO;④ PO+GST处理组:加入终浓度40.5 μmol·L-1的 PO+终浓度100 μmol·L-1的 GST。各组均于37℃下孵育血管30 min,取出,用冰 PBS冲洗(0.1% DEPC水配制并高压),置于-80℃冰箱保存备用。
1.2.2 RT-PCR检测大鼠胸主动脉p22phox和 Nox4 mRNA的表达各组标本分置于各研钵中,加入液氮,于冰上研磨匀浆后,按照RNA提取试剂盒说明提取组织总 RNA。取适量总 RNA与 6×loading buffer按 5 ∶ 1的比例混匀后,于 110 V恒压下在2.0%的琼脂糖凝胶中电泳,于凝胶成像系统中观察电泳结果,若可见 28S、18S、5S(此条带也有可能降解)条带,且 28S条带亮度是 18S条带亮度2倍左右,提取的总 RNA合格,可以用于后续实验。将提取的总 RNA稀释,分别于 260 nm、280 nm处测定其吸光度(A),计算A260/A280,比值在2左右时,说明提取的总 RNA质量合格;根据 A260计算各组 RNA浓度。根据计算所得各组 RNA浓度,取等质量 1.5 μg RNA按逆转录试剂盒说明的实验程序完成各组 RNA逆转录,合成互补脱氧核糖核酸(cDNA),并以其作为模板进行 PCR扩增。各引物序列及 PCR反应条件见 Tab1,各组扩增目的基因的同时扩增内参照 β-actin。 PCR产物在2.0%的琼脂糖凝胶中电泳,恒压 110 V,上样量为 10 μL,于凝胶成像系统中扫描分析产物条带。将各组目的基因(p22phox、Nox4)与其内参照(β-actin)扩增条带的吸光度比值作为目的基因 mRNA表达水平的相对指标。
| Gene | Sequence(5′~3′) | Product length/bp | T/℃ | Cycles |
| p22phox | Forward TATTGTTGCAGGAGTGCTCATC | 455 | 58 | 30 |
| Reverse GTCACACGACCTCATCTGTCAC | ||||
| β-actin | Forward CTGGGTATGGAATCCTGTGG | 235 | 56 | 30 |
| Reverse TAGAGCCACCAATCCACACA | ||||
| Nox4 | Forward GGAAGTCCATTTGAGGAGTCAC | 245 | 56 | 35 |
| Reverse TGGATGTTCACAAAGTCAGGTC | ||||
| β-actin | Forward GAGACCTTCAACACCCCAGCC | 394 | 63 | 30 |
| Reverse TCGGGGCATCGGAACCGCTCA |
各组标本分置于各研钵中,加入液氮,研磨匀浆后,按照总蛋白提取试剂盒说明提取组织总蛋白。
1.2.3.1 蛋白浓度测定按照BCA蛋白浓度测定试剂盒说明的实验步骤,使用酶标仪于570 nm处测定并计算各组蛋白浓度。
1.2.3.2 SDS-PAGE凝胶电泳根据相关抗体说明书,目的基因 p22phox蛋白条带位于 26 ku位置处,Nox4蛋白条带位于 63 ku位置处,β-actin蛋白条带位于 43 ku位置处,10%分离胶可较好分离 20~80 ku大小的蛋白质,满足上述3种蛋白质分离要求。照凝胶配制试剂盒规定步骤制备10%分离胶,37℃恒温放置30 min,制备浓缩胶,并于37℃恒温放置40 min,待胶凝固,即可上样。根据蛋白定量结果,将各组不同浓度蛋白均稀释至同一浓度,取等质量等体积蛋白(70 μg,22 μL)按4 ∶ 1比例与 5×蛋白上样缓冲液(溴酚蓝染料预染)混匀(总体积约 27.5 μL),100℃煮沸 5 min,即可上样、电泳。浓缩胶的电泳条件为 80 V恒压,观察蛋白条带进入分离胶后即调节电压至 120 V,待蛋白 Marker各条带跑开,蛋白条带接近凝胶底部时,即可停止电泳。
1.2.3.3 蛋白质转膜剪下比胶略小的 PVDF膜,置甲醇中活化 2 min。盘内倒入适量转膜液,按转膜装置从阴极到阳极的顺序,依次放上滤纸、凝胶、PVDF膜、滤纸,每一步均需去除气泡。接通电源,恒流 350 mA,3 h。
1.2.3.4 免疫杂交剪下 p22phox、Nox4、β-actin所处位置 PVDF膜,用 TBST洗涤2次,5%封闭液封闭,置摇床上振摇1 h,TBST洗涤,分别加入用1%脱脂奶粉稀释的1 ∶ 100 p22phox一抗,1 ∶ 200 Nox4一抗,1 ∶ 500 β-actin一抗,密封,与膜共振摇1 h,置 4℃冰箱过夜。取出 PVDF膜,TBST洗涤3次,每次 10 min,加入1 ∶ 1 500的辣根过氧化物酶标记的相应二抗,密封,于 37℃放置 30 min,室温振摇 1 h,TBST 洗涤3次,每次 15 min。按照超敏 ECL化学发光试剂盒说明滴加化学发光底物到 PVDF膜上,观察荧光现象,压片、显影、定影。定影后的 X胶片扫描至计算机,图像分析系统 AlphaImager 2200计算目的条带的灰度值与内参照 β-actin条带灰度值的比值,作为目的蛋白表达水平的相对指标。
1.3 统计学分析采用统计软件 SPSS 16.0进行统计分析,数据均以 ± s表示,组间差异比较采用 ANOVA及 Dunnett-t、S-N-K多重比较。
± s表示,组间差异比较采用 ANOVA及 Dunnett-t、S-N-K多重比较。
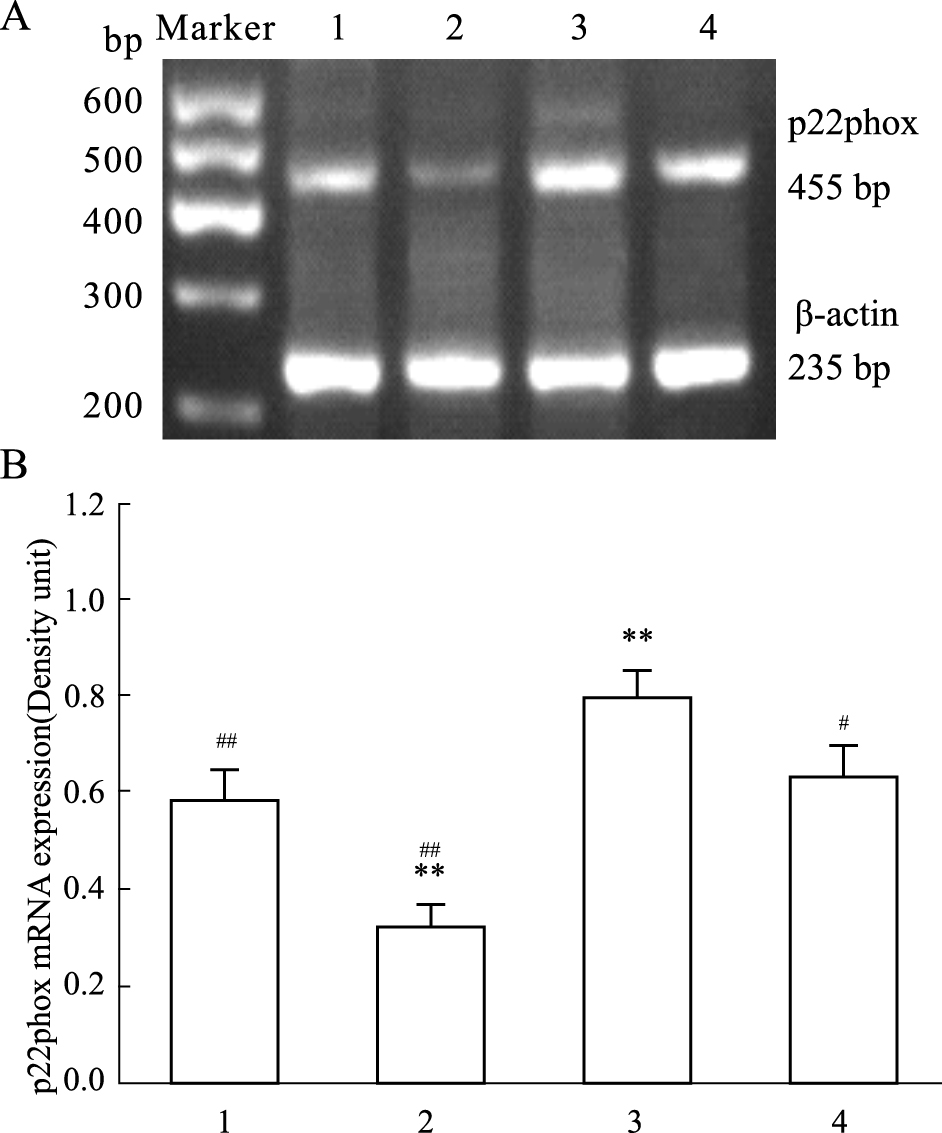
RT-PCR结果显示(Fig1),较之溶媒对照组,PO 处理引起 p22phox mRNA表达明显上调(P < 0.01);GST处理导致 p22phox mRNA表达下调(P < 0.01);PO+GST共同处理对 p22phox mRNA表达的影响不大,差异无显著性。但相对于 PO处理组,PO+GST共同处理可下调 p22phox mRNA的表达(P < 0.05)。
|
| Fig 1 RT-PCR results show the effects of genistein and paraoxon on the expression of p22phox mRNA in rat thoracic aorta tissues(n=3) 1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: RT-PCR results; B: Statistic analysis of band relative intensity. **P < 0.01 vs control group; #P < 0.05,##P < 0.01 vs paraoxon group. |
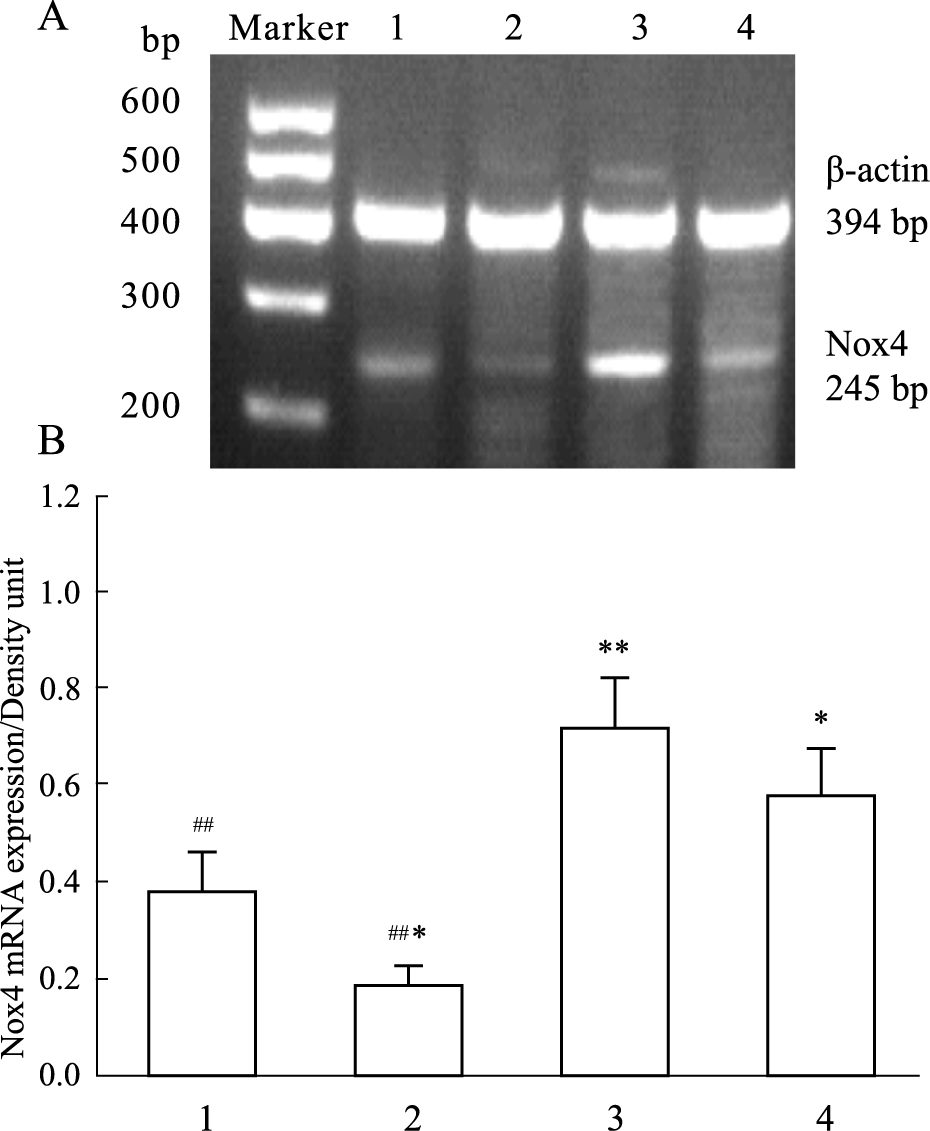
RT-PCR结果显示(Fig2),相对于溶媒对照组,PO处理引起 Nox4 mRNA表达明显上调(P < 0.01);GST处理导致 Nox4 mRNA表达下调(P < 0.05);PO+GST共同处理导致 Nox4 mRNA 表达上调(P < 0.05)。但相对于 PO处理组,PO+GST共同处理对 Nox4 mRNA表达的影响不大,差异无显著性。
|
Fig 2
RT-PCR results show the effects of genistein and paraoxon on the expression of Nox4 mRNA in rat thoracic aorta tissues ( ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: RT-PCR results; B: Statistic analysis of band relative intensity. *P < 0.05,**P < 0.01 vs control group; ##P < 0.01 vs paraoxon group. ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: RT-PCR results; B: Statistic analysis of band relative intensity. *P < 0.05,**P < 0.01 vs control group; ##P < 0.01 vs paraoxon group.
|
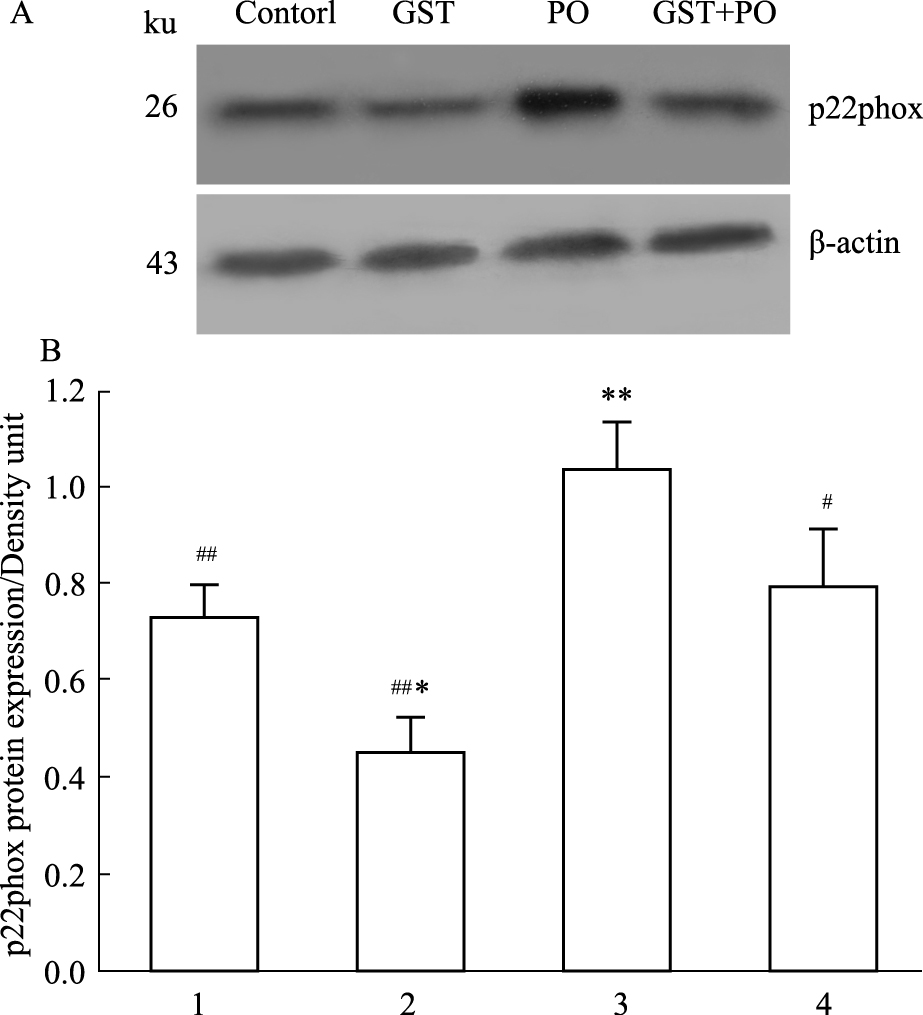
Western blot结果显示(Fig3),较之溶媒对照组,PO处理引起p22phox蛋白表达明显上调(P < 0.01);GST处理导致 p22phox蛋白表达下调(P < 0.05);PO+GST共同处理后,较溶媒对照组,p22phox蛋白表达有所增加,但差异无显著性。但相对于 PO处理组,PO+GST共同处理使 p22phox蛋白表达减少(P < 0.05)。
|
Fig 3
Western blot results show the effects of genistein and paraoxon on the expression of p22phox protein in rat thoracic aorta rings ( ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: Western blot results; B:Statistic analysis of band relative intensity. *P < 0.05,**P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs paraoxon group. ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: Western blot results; B:Statistic analysis of band relative intensity. *P < 0.05,**P < 0.01 vs control group; #P < 0.05, ##P < 0.01 vs paraoxon group.
|
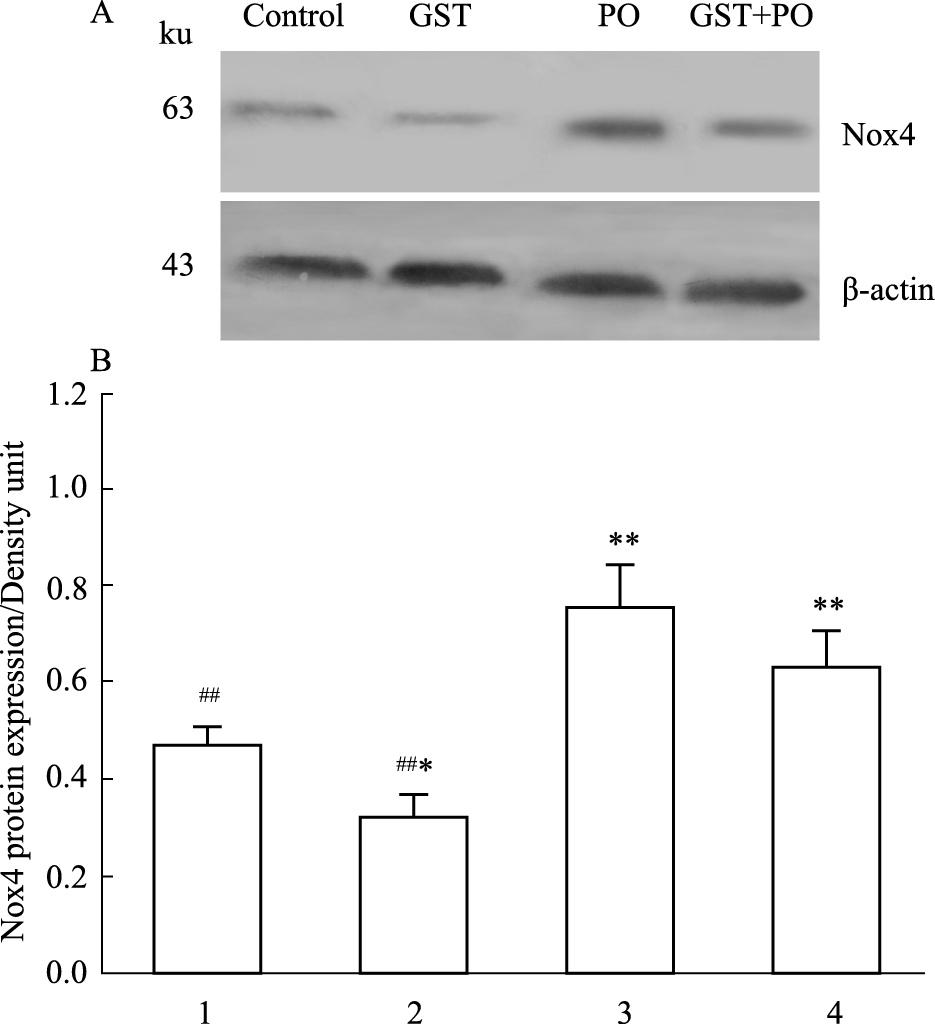
Western blot结果显示(Fig4),与溶媒对照组比较,PO处理引起 Nox4蛋白表达明显上调(P < 0.01);GST处理导致 Nox4蛋白表达下调(P < 0.05);PO+GST共同处理导致 Nox4蛋白表达上调(P < 0.01);相对于 PO处理组,PO+GST共同处理组 Nox4蛋白表达有所降低,但差异无显著性。
|
Fig 4
Western blot results show the effects of genistein and paraoxon on the expression of Nox4 protein in rat thoracic aorta rings ( ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: Western blot results; B: Statistic analysis of band relative intensity. *P < 0.05; **P < 0.01 vs control group; ##P < 0.01 vs paraoxon group. ± s,n=3)
1: Control; 2:GST(100 μmol·L-1); 3:PO(40.5 μmol·L-1); 4:GST+PO. A: Western blot results; B: Statistic analysis of band relative intensity. *P < 0.05; **P < 0.01 vs control group; ##P < 0.01 vs paraoxon group.
|
心血管疾病目前已成为影响人类健康的头号疾病,其发病机制和病理过程各异,已经证实血管内皮损伤与心血管疾病的发展密切相关。血管内皮细胞可合成、分泌多种生物活性物质,参与调节血管紧张度、维持血管正常的舒缩功能。血管内皮细胞损伤导致细胞功能障碍、血管正常舒缩功能受损,诱发一系列病理性应激反应的产生。很多心血管疾病的早期诱因均牵涉到血管内皮损伤、血管舒缩功能异常。
有机磷酸酯类(OPs)化合物是目前广泛使用的一类农药,OPs侵入机体后,在体内经肝脏 P450系统代谢为具有生物活性的 PO。少量的 PO可进一步被PON1水解失活,随尿液排出体外。但长期或大量接触 OPs,可导致机体 PON1浓度及活性降低[10],PO水解排出减少。PON1具有抗氧化作用,可抑制血浆氧化物形成并清除血浆氧化物。体内PO的蓄积可诱发氧化应激,损伤血管内皮,诱发心血管疾病。已有研究表明[11],给兔长期灌胃敌百虫,可降低兔血清及肝 PON1的活性,加速兔动脉粥样硬化的形成;Prozorovskiǐ 等[12]研究也发现 OPs可导致内皮细胞变形,并损伤内皮细胞功能;李鹏等[13]实验表明,对氧磷(0.036 3~36.3 μmol·L-1)与人脐静脉内皮细胞(HUVEC)及血管组织共孵30 min,浓度和时间依赖性地增加了单层内皮细胞的通透性,内皮细胞活力下降,细胞萎缩;大鼠血管组织及细胞培养液中丙二醛(MDA)的含量增高、SOD活性降低、一氧化氮(NO)含量减少,血管内皮细胞损伤;且 PO可浓度依赖性及时间依赖性抑制血管内皮依赖性舒张功能。
本实验室前期实验证实了PO可浓度依赖性(0.004 05~40.5 μmol·L-1)抑制大鼠胸主动脉 EDR功能[4]。但 PO损伤内皮细胞导致心血管疾病的发生除了与其直接毒性刺激作用及抑制机体抗氧化酶活性有关外,是否还涉及到内皮细胞ROS生成的主要酶体——NADPH氧化酶,目前尚未见报道。本实验通过建立大鼠胸主动脉 PO损伤模型,检测 NADPH氧化酶在血管组织中的2个主要亚基 p22phox、Nox4的表达情况,发现 PO能够上调 p22phox、Nox4 mRNA及蛋白的表达。从机体ROS的产生途径初步探讨了 PO造成血管内皮损伤的另一可能机制。
目前,实验室研究、临床试验、流行病学统计均表明摄入GST可降低心血管疾病发病率。大量研究资料表明GST具有确切的抗炎、抗氧化、保护血管内皮、维持血管正常的舒缩功能的作用[14]。GST可直接作用于血管平滑肌,浓度依赖性地降低氯化钾(KCl)诱导的血管收缩[15, 16]。文献报道[17],连续给予♂糖尿病大鼠 GST 31 d,发现在内皮完整的血管环,GST组对 KCl、PE诱导的收缩反应明显低于糖尿病组;对 ACh诱导的舒张反应明显高于糖尿病组。本实验室早期的实验也发现GST可明显抑制PO导致的血管EDR功能损伤[4]。所有这些证据均表明GST调节血管紧张度,保护血管内皮,进而改善血管内皮依赖性舒张功能。
关于GST保护心血管系统的相关机制众多。GST可降低鼠血浆中 TC、LDL-C、TC/HDL-C[10, 18],减轻血管结构与功能的损伤;同时,GST也可抑制TNF-α的下游因子 NF-κB表达[19],快速激活 p38β丝裂原蛋白激酶[20],进而对抗 TNF-α诱导的内皮细胞损伤及编程性细胞死亡。然而,GST的抗氧化作用是其保护心血管系统的主要作用机制之一。研究发现,GST可升高机体 SOD的活性、GSH水平,并上调 GSH-Px的水平和活性,增强机体抗氧化水平[8];Vera等[21]发现,长期给予自发性高血压大鼠 GST,可抑制 NADPH氧化酶活性,降低ROS的产生,改善血管内皮功能紊乱;Xu 等[9]也发现 GST可下调大鼠p22phox亚基的表达,抑制 ROS的产生。但 GST对内皮细胞上NADPH氧化酶另一重要的亚基 Nox4表达的影响,目前尚未见报道。本研究通过用100 μmol·L-1 GST处理大鼠胸主动脉后,观察血管组织中p22phox、Nox4表达的情况,发现 GST可下调 p22phox、Nox4的表达。
本实验室前期实验已发现,GST与 PO共同预处理血管环后,血管环 EDR功能较 PO单独处理血管环有了明显改善[4],GST与PO对 p22phox、Nox4表达的相反的调节作用是否可以解释这一现象?GST是否可通过下调内皮细胞上 NADPH氧化酶相关亚基p22phox、Nox4的表达这一途径来拮抗 PO诱导的内皮细胞氧化损伤?本课题从离体组织器官水平就这些问题展开实验,发现 GST可拮抗 PO诱导的大鼠胸主动脉组织 p22phox表达上调。对于 PO诱导的 Nox4表达的上调,GST具有一定拮抗效应,但该效应并不明显。这可能涉及p22phox、Nox4亚基对 PO、GST的敏感性不同,Nox4对PO更为敏感;也可能涉及离体模型(大鼠胸主动脉)的建模时间及建模条件等多方面的原因。
综上所述,通过对PO与 GST对血管内皮的作用及其可能机制的初探性研究,为有机磷酸酯类农药诱发心血管疾病发生的机制及GST对此类疾病可能的防治提供理论参考及实验依据。
(致谢:本文实验部分在南华大学药物药理研究所完成。在此衷心感谢导师黄红林教授及药物药理研究所全体老师、同学对本实验工作的关心、支持和帮助!)
| [1] | Garrido-Urbani S, Jaquet V, Imhof B A. ROS and NADPH oxidase: key regulators of tumor vascularisation [J]. Med Sci (Paris), 2014, 30(4):415-21. |
| [2] | Martyn K D, Frederick L M, von Loehneysen K, et al. Functional analysis of Nox4 reveals unique characteristics compared to other NADPH oxidases[J]. Cell Signal, 2006,18(1): 69-82. |
| [3] | Laurindo F R, Araujo T L, Abrahão T B. Nox NADPH oxidases and the endoplasmic reticulum [J]. Antioxid Redox Signal, 2014, 20(17):2755-75. |
| [4] | 刘玉玲,饶志威,李 震,等. 染料木素对对氧磷损伤大鼠胸主动脉内皮依赖性舒张功能的保护作用[J]. 国际病理科学与临床杂志,2011,31(6):471-5.Liu Y L, Rao Z W, Li Z, et al. Protective effect of genistein on damages of paraoxon-induced endothelium-dependent relaxation in the rat thoracicaorta[J]. Int J Pathol Clin Med,2011,31(6):471-5. |
| [5] | Erba D, Casiraghi M C, Martinez-Conesa C, et al. Isoflavone supplementation reduces DNA oxidative damage and increases O-β-N-acetyl-D-glucosaminidase activity in healthy women [J]. Nutr Res, 2012, 32(4):233-40. |
| [6] | Wu H J, Chan W H. Genistein protects methylglyoxal-induced oxidative DNA damage and cell injury in human mononuclear cells [J]. Toxicol In Vitro, 2007, 21(3):335-42. |
| [7] | Liu H, Zhang C, Zeng W. Estrogenic and antioxidant effects of a phytoestrogen daidzein on ovarian germ cells in embryonic chickens[J]. Domest Anim Endocrin, 2006, 31(3):258-68. |
| [8] | 季莉莉,周 虹,李贤标,张玉梅. 大豆异黄酮对动脉硬化大鼠的抗氧化作用研究[J].中国预防医学杂志, 2006,7(1):1-4.Ji L L, Zhou H, Li X B, Zhang Y M. Effect of soy isoflavones on anti-oxidative enzyme and lipid peroxide in rat[J]. China Prev Med, 2006,7(1):1-4. |
| [9] | Xu J W, Ikeda K, Yamori Y. Genistein inhibits expressions of NADPH oxidase p22phox and angiotensin II type 1 receptor in aortic endothelial cells from stroke-prone spontaneously hypertensive rats[J]. Hypertens Res,2004,27(9): 675-83. |
| [10] | 赵绿英,刘玉玲,李金兰,等.染料木素对大鼠食饵性高脂血症PON1及CRP的影响[J]. 中国药理学通报,2012,28(4):567-72.Zhao L Y, Liu Y L, Li J L, et al. Effect of genistein on paraoxonase and C-reactive protein of the rats with food-induced hyperlipidemia[J]. Chin Pharmacol Bull, 2012,28(4):567-72. |
| [11] | 熊小明,周寿红,胡 敏,刘立英. 敌百虫加重高脂饮食致兔动脉粥样硬化作用与降低对氧磷酶活性有关[J]. 中国动脉硬化杂志,2009,17(3):172-6.Xiong X M, Zhou S H, Hu M, Liu L Y. Effect of organophosphorus insecticide to aggravate hyperlipidemic diet inducing atherosclerosis ralated to decrease of paraoxonase activity in rabbits[J]. Chin J Arterioscler, 2009,17(3):172-6. |
| [12] | Prozorovskiǐ V B, Skopichev V G. Finding cholinesterase in endotheliocytes: cholinesterase inhibition by organophosphorus compounds leads to endotheliocyte deformation[J]. Eksp Klin Farmakol, 2005,68(3):64-7. |
| [13] | 李 鹏,刘立英,周寿红,吴树金.对氧磷对血管内皮细胞的损伤作用及机制探讨[J]. 中国动脉硬化杂志,2007,15(9): 666-70.Li P, Liu L Y, Zhou S H, Wu S J. Paraoxon-induced injuries of vascular endothelial cell and exploration of potential mechanisms[J]. Chin J Arterioscler, 2007,15(9):666-70. |
| [14] | Zhou X, Yuan L, Zhao X, et al. Genistein antagonizes inflammatory damage induced by β-amyloid peptide in microglia through TLR4 and NF-κB[J]. Nutrition, 2014, 30(1):90-5. |
| [15] | Je H D, Sohn U D. Inhibitory effect of genistein on agonist-induced modulation of vascular contractility[J]. Mol Cells, 2009, 27(2):191-8. |
| [16] | Seok Y M, Baek I, Kim Y H, et al. Isoflavone attenuates vascular contraction through inhibition of the RhoA/Rho-Kinase signaling pathway[J]. J Pharmacol Exp Ther, 2008,326(3):991-8. |
| [17] | Baluchnejadmojarad T, Roghani M. Chronic administration of genistein improves aortic reactivity of streptozotocin-diabetic rats:mode of action [J]. Vascul Pharmacol, 2008, 49(1):1-5. |
| [18] | Ae Park S, Choi M S, Cho S Y, et al. Genistein and daidzein modulate hepatic glucose and lipid regulating enzyme activities in C57BL/KsJ-db/db mice[J]. Life Sci, 2006,79(12):1207-13. |
| [19] | Li H Q, Luo Y, Qiao C H. The mechanisms of anticancer agents by genistein and synthetic derivatives of isoflavone[J]. Mini Rev Med Chem, 2012,12(4):350-62. |
| [20] | Si H, Liu D. Isoflavone genistein protects human vascular endothelial cell against tumor necrosis factor-alpha-induced apoptosis through the p38beta mitogen-activated protein kinase[J]. Apoptosis,2009,14(1):66-76. |
| [21] | Vera R, Sánchez M, Galisteo M, et al. Chronic administration of genistein improves endothelial dysfunction in spontaneously hypertensive rats: involvement of eNOS, caveolin and calmodulin expression and NADPH oxidase activity[J]. Clin Sci, 2007,112(3):183-91. |

