


维甲酸类化合物在脊椎动物发育、细胞分化和维持机体平衡中发挥着非常广泛的效应,在体内生理活性代谢产物包括全反式维甲酸、13-顺式维甲酸、9-顺式维甲酸,它们可以通过和细胞核内维甲酸受体(RARs)和维甲类受体(RXRs) 结合于DNA的应答元件,进而调节靶基因的表达,发挥抑制细胞增殖和诱导分化作用。全反式维甲酸 (all trans retinoic acid,ATRA) 作为诱导分化剂的代表目前广泛用于急性早幼粒白血病的临床治疗[1],但同时存在维甲酸综合征耐药性等不足限制其进一步临床使用[2, 3, 4]。本实验室以ATRA为先导化合物,通过对其碳链末端极性基团进行结构修饰,合成了一系列新的维甲酸衍生物,经过体外药效学筛选发现4-氨基-2-三氟甲基苯基维甲酸酯具有较强的抗肿瘤增殖和诱导分化活性,有望成为一种新型抗肿瘤药。课题组前期研究发现4-氨基-2-三氟甲基苯基维甲酸酯(4-anino-2-trifluoromethyl-phenyl retimate,ATPR)对多种肿瘤细胞具有诱导分化作用[5, 6, 7, 8],本实验观察ATPR对人乳腺癌细胞株MDA-MB-231是否具有诱导分化作用,并探究ATPR对维甲酸受体RARs及维甲类受体RXRs表达的影响。
1 材料与方法 1.1 材料新型维甲酸衍生物由安徽医科大学药学院合成 (Fig1),纯度为99.66 %,溶于无水乙醇,配制成1×10-2 mol·L-1浓度,-20℃储存备用。高糖DMEM培养液为Hyclone公司产品;胎牛血清购自杭州四季青生物工程材料有限公司;瑞氏-吉姆萨染料购自南京建成生物工程研究所;MUC-1试剂盒为美国R&D公司产品;逆转录试剂盒和PCR试剂盒均为Promage公司产品;q-PCR引物由上海生工生物工程技术服务有限公司合成;实时荧光定量PCR仪,立陶宛Fermentas公司产品;抗RARα、RARβ、RARγ、RXRα、RXRβ、RXRγ 抗体购自Santa Cruz公司;β-actin抗体购自北京中杉金桥生物技术有限公司。
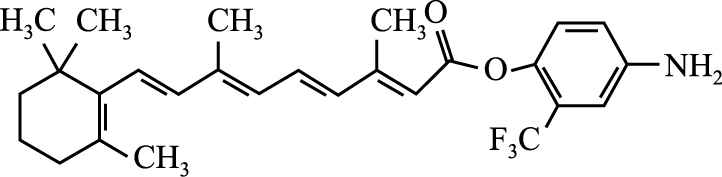
|
| Fig 1 Chemical structure of 4-Amino-2-Trifluoromethyl Phenyl Retinate (ATPR) |
MDA MB 231细胞株购自中科院上海细胞所,采用含10 %胎牛血清(FCS)的DMEM培养液,并加入青霉素105 IU·L-1和链霉素100 mg·L-1的培养体系培养。培养环境为37℃,5 % CO2培养箱,每2天换1次液,取对数生长期细胞进行实验。
1.3 MTT法检测细胞增殖将MDA MB 231细胞以3×104个/孔的浓度接种于96孔培养板,每孔接种量为100 μL。待细胞贴壁后,分为空白对照组 (加入DMEM培养液100 μL)、溶剂对照组 (含0.05 %无水乙醇)、阳性对照组ATRA (10-5mol·L-1)及ATPR (10-4、10-5、10-6、10-7、10-8、10-9mol·L-1)组,每组设6个复孔,每孔的总体积为200 μL。分别于24、48、72、96 h后更换为无血清培养液,并加入MTT (浓度为5 g·L-1) 20 μL,继续培养4 h后,弃上清,每孔加入150 μL的DMSO,震荡摇匀,使甲瓒颗粒充分溶解。于酶联免疫检测仪上,以波长490nm,试剂对照组调零,测吸光度(A490)值,重复3次,取其平均值,并用SPSS计算IC50值。
1.4 细胞生长曲线绘制将MDA MB 231细胞以1×104个/孔的浓度接种于24孔培养板,每孔接种量为1 mL。待细胞贴壁后,实验分组同“1.3”,将其置于37℃含5 % CO2培养箱中,培养1~7 d。每天进行细胞计数,每个时间点设3个复孔,取其均值,以培养时间为横轴,细胞计数为纵轴,绘制细胞生长曲线。
1.5 细胞形态学观察以1×106个/孔的浓度接种于6孔板,每孔加入盖玻片,将细胞悬液滴于盖玻片上,实验分组同1.3,作用72 h收集盖玻片,用PBS冲洗盖玻片,甲醇固定10 min,自然干燥,在盖玻片上依次滴加瑞氏-吉姆萨染料A液和B液,流水冲洗细胞,干燥后在显微镜下观察细胞形态并拍照。
1.6 分化标志物MUC-1检测取对数生长期细胞,以1×104个/孔的浓度接种于24孔板,待细胞贴壁后,实验分组同1.3,作用72 h后,收集细胞上清,3 000 r·min-1离心10 min后,参照试剂盒方法检测MUC-1。
1.7 细胞周期和DNA倍体分析取对数生长期细胞,以1×106个/孔的浓度接种于6孔板,实验分组同1.3,作用72h后,收集细胞,用PBS洗涤2次,70%冷乙醇-20℃冰箱固定过夜。固定后的细胞离心,弃上清,加入碘化丙啶(PI,终浓度为100 mg·L-1)和RNase(终浓度为50 mg·L-1),4℃避光染色30 min后,在EPICS XL MCL型流式细胞仪上分析,检测3×104以上细胞,并用ModfitLT软件进行DNA倍体及细胞周期分析。
1.8 实时定量荧光逆转录聚合酶链反应(q RT PCR)检测RARα、RARβ、RARγ、RXRα、RXRβ、RXRγmRNA的表达
1.8.1 RNA提取和逆转录将1×109·L-1细胞接种于培养瓶,实验分为空白对照组 (加入DMEM培养液)、溶剂对照组 (含0.05%无水乙醇)、阳性对照组ATRA (10-5mol·L-1) 及ATPR (10-5mol·L-1) 组,作用72 h后,按TRIzol一步法提取细胞中总RNA,以紫外分光光度计测RNA含量和纯度 (RNA在260和280 nm的光密度比值为1.8~2.0),以1.5%琼脂糖凝胶电泳鉴定其完整性(28S和18SRNA条带比值I>2.0),用5 μg总RNA为模板,逆转录成cDNA。
| Gene | Sequences | Product size/bp |
| RARα | F:5′-ACAACAGCTCAGAACAACGTGTCTC-3′ R:5′-CTTGGCGAACTCCACAGTCTTAAT-3′ | 101 |
| RARβ | F:5′-ATGCCATTTGCCTCCACACCTA-3′ R:5′-CCCAGGACTCACTGACAGAACATC-3′ | 102 |
| RARγ | F:5′-TCGAGATGCTGAGCCCTAGCTT-3′ R:5′-CAGAGGACTTGTCATTGCACACG-3′ | 180 |
| RXRα | F:5′-AAAGACCCAACGCCAACACCT-3′ R:5′-AGCGCCGGAAACGACAAAGT-3′ | 161 |
| RXRβ | F:5′-CGGTCCATTGGCCTTAAGTGTCT-3′ R:5′-GGATGTGTGCTCCTCCAGTGTGA-3′ | 161 |
| RXRγ | F:5′-GCCTACACCAAGCAGAAGTATCCG-3′ R:5′-AGAGGTGCTCCAGGCATTTCAA-3′ | 106 |
| GAPDH | F:5′-CGCTGAGTACGTCGTGGAGTC-3′ R:5′-GCTGATGATCTTGAGGCTGTTGTC-3′ | 111 |
将cDNA用无酶水稀释10倍,上、下游引物各稀释10倍后,按以下体系将反应物加至q-RT-PCR反应板中,每组至少3个复孔,冰上操作:Syber green I:5 μL;cDNA:0.5 μL;P1:0.3 μL;P2:0.3 μL;无酶水:3.9 μL共10 μL体系。反应条件1:预变性95℃,10 min;变性95℃ 15 s;反应条件2:退火95℃ 15 s;60℃ 30 s;延伸72℃ 30 s,45个循环后,延伸7℃ 230 s。扩增反应结束后取出96孔反应板,关闭仪器,分析数据,若观察到各基因熔解曲线为锐利的单一峰,说明扩增序列特异性强,定量准确。
1.9 Western blot检测RARα、RARβ、RARγ、RXRα、RXRβ、RXRγ蛋白的表达将1×109·L-1细胞接种于培养瓶中,实验分组同“1.8.1”,作用72 h后,弃培养液,用预冷的PBS洗3遍,每瓶加入400 μL RIPA裂解液(含10 % PMSF)裂解30 min,用细胞刮快速将细胞转入1.5 mL EP管中,离心取上清,用BCA蛋白定量试剂盒进行定量。将上清与上样缓冲液按4 ∶ 1进行分装,100℃煮10 min变性,-80℃保存待用。等量的蛋白样品进行SDS-PAGE,将电泳分离的蛋白转移到PVDF膜上。TBST洗膜10 min,室温下用含5 %的脱脂奶粉(TBST溶解)封闭3 h,随后加入一抗(1 ∶ 300)4℃孵育过夜,TBST洗脱4次,加入相应的二抗孵育1 h,用TBST漂洗4次,将PVDF膜用化学发光剂染色1 min。
1.10 统计学分析实验数据均用 ± s表示,采用SPSS 16.0软件分析结果,组间数据比较采用单因素方差分析。
± s表示,采用SPSS 16.0软件分析结果,组间数据比较采用单因素方差分析。
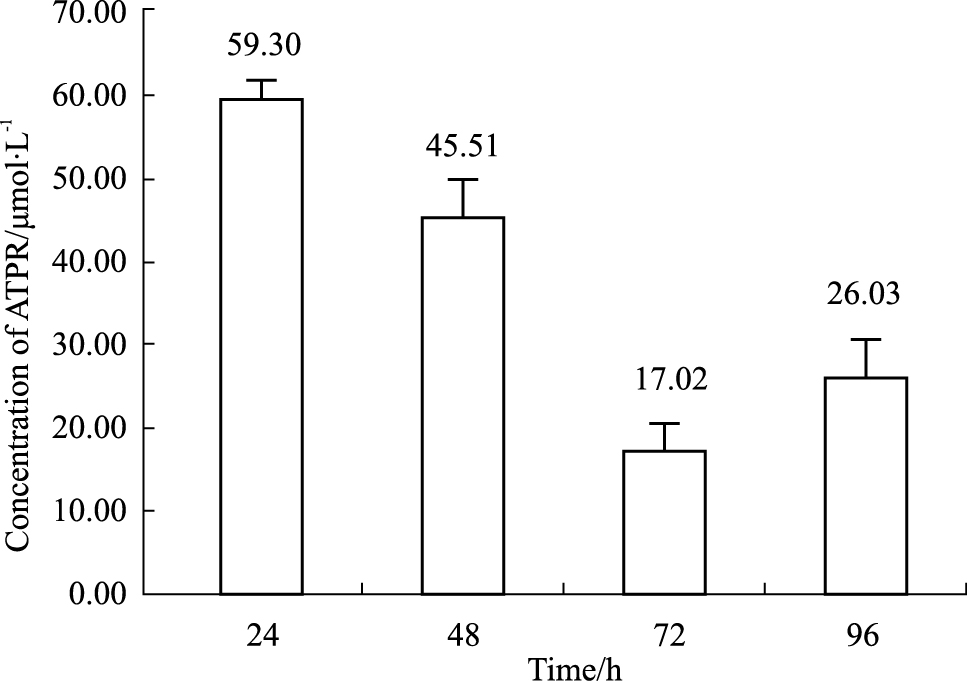
如Tab2所示,与空白对照组相比,溶剂对照组A490变化不明显,表明无水乙醇 (0.05 %)作为溶剂对细胞增殖无影响,因此可排除无水乙醇对本实验的影响。显微镜下观察各组细胞发现,与溶剂对照组比较,ATPR(10-4 mol·L-1) 体外给药24 h时即对MDA-MB-231细胞的增殖产生明显影响,细胞形态皱缩,细胞凋亡;ATPR(10-5、10-6、10-7、10-8、10-9 mol·L-1) 体外给药24 h时对MDA-MB-231细胞增殖并无明显影响,但作用48、72和96 h后,ATPR (10-5、10-6、10-7、10-8、10-9mol·L-1)对细胞增殖均具有不同程度的抑制作用。如Fig2所示,72 h时ATPR对MDA-MB-231细胞抑制作用的IC50值最低。
|
Fig 2
ATPR inhibits the half inhibition concentration (IC50) in MDA-MB-231 cells( ± s,n=3) ± s,n=3)
|
 ± s,n=3)
± s,n=3)
| Group | Concentration/ mol·L-1 | A490 | ||||
| 24 h | 48 h | 72 h | 96 h | |||
| *P<0.05, **P<0.01 vs the solvent group. | ||||||
| Control | 0.303±0.02 | 0.537±0.055 | 0.867±0.069 | 0.942±0.043 | ||
| Solvent | 0.329±0.04 | 0.535±0.041 | 0.972±0.023 | 0.951±0.040 | ||
| ATPR | 10-4 | 0.081±0.016** | 0.079±0.018** | 0.088±0.009** | 0.070±0.06** | |
| 10-5 | 0.325±0.038 | 0.477±0.036* | 0.584±0.068** | 0.668±0.104* | ||
| 10-6 | 0.349±0.050 | 0.489±0.055* | 0.606±0.018** | 0.735±0.074* | ||
| 10-7 | 0.362±0.030 | 0.552±0.049 | 0.604±0.084* | 0.772±0.112 | ||
| 10-8 | 0.359±0.047 | 0.563±0.067 | 0.764±0.044 | 0.851±0.091 | ||
| 10-9 | 0.363±0.034 | 0.597±0.068 | 0.789±0.104 | 0.914±0.103 | ||
| ATRA | 10-5 | 0.331±0.038 | 0.463±0.03** | 0.578±0.074** | 0.642±0.073* | |
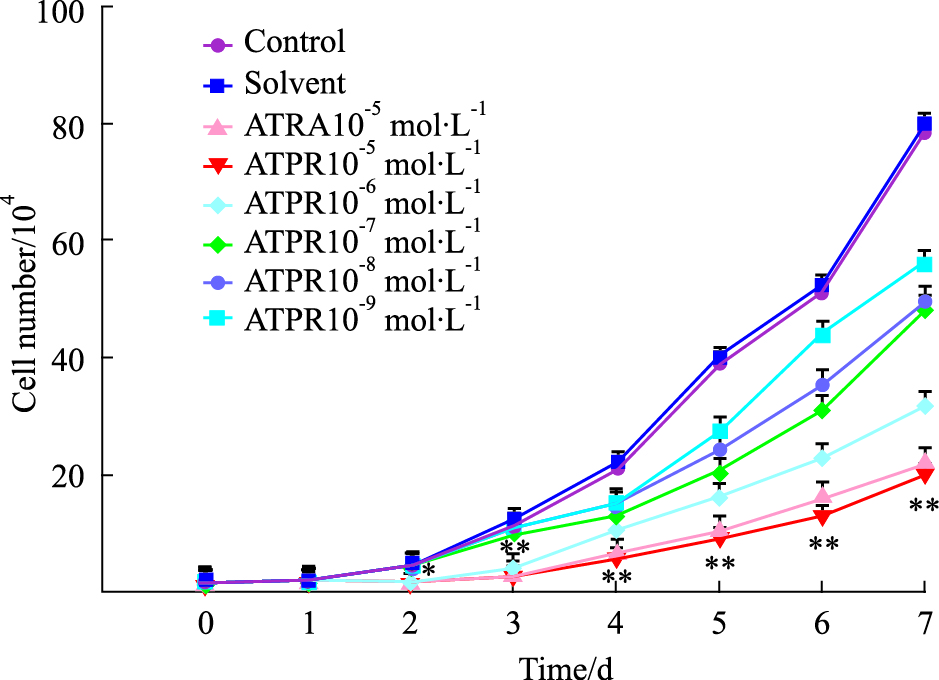
台盼蓝染色后绘制细胞生长曲线,结果如Fig3所示,与溶剂对照组比较,ATPR浓度越大,细胞生长曲线越低平,其中10-5mol·L-1ATPR对MDA-MB-231细胞 增殖的抑制作用最强,用药后24 h开始出现抑制作用,并且在72 h抑制作用最明显,说明ATPR对MDA-MB-231细胞的抑制作用具有浓度-时间依赖性。
|
Fig 3
Growth curves of MDA-MB-231 cells treated with ATPR( ± s, n=3)
**P<0.01 vs the solvent group. ± s, n=3)
**P<0.01 vs the solvent group.
|
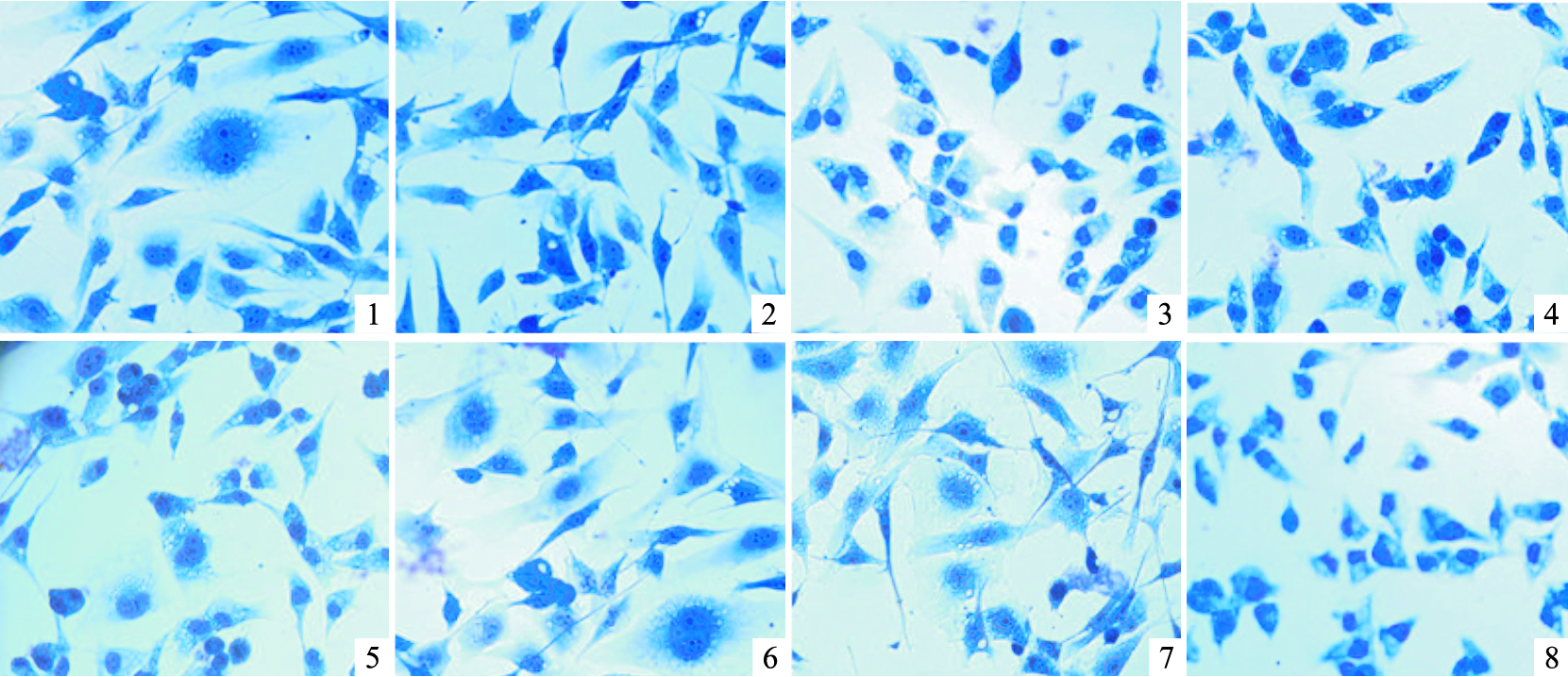
不同浓度ATPR作用后,MDA-MB-231细胞形态学变化如Fig4所示,正常组细胞生长密度大,细胞形态不规则,ATPR用药后细胞生长密度降低,核质比降低,细胞形态规则,细胞形态随药物浓度增加改变越明显。
|
| Fig 4 Effect of ATPR on the morphological changes of MDA-MB-231 cells after 72h (400×) 1:Control;2:Solvent;3:ATPR(10-5mol·L-1);4:ATPR(10-6 mol·L-1);5:ATPR(10-7 mol·L-1);6:ATPR(10-8 mol·L-1);7:ATPR(10-9 mol·L-1);8:ATRA(10-5mol·L-1). |
ATPR作用后观察MDA-MB-231细胞上清中MUC-1的变化,结果如Tab3所示,与溶剂对照组相比,MUC-1含量随ATPR浓度的升高而下降,ATPR浓度为10-5 mol·L-1时MUC-1含量下降最明显,差异具有统计学意义。
 ± s,n=3)
± s,n=3)
| Group | Concentration/mol·L-1 | MUC-1/kU·L-1 |
| *P<0.05, **P<0.01 vs the solvent group. | ||
| Control | - | 61.49±1.66 |
| Solvent | - | 61.00±1.28 |
| ATPR | 10-5 | 43.87±1.37** |
| 10-6 | 51.31±2.22* | |
| 10-7 | 54.08±3.39 | |
| 10-8 | 57.55±3.59 | |
| 10-9 | 59.47±1.48 | |
| ATRA | 10-5 | 44.08±2.25** |
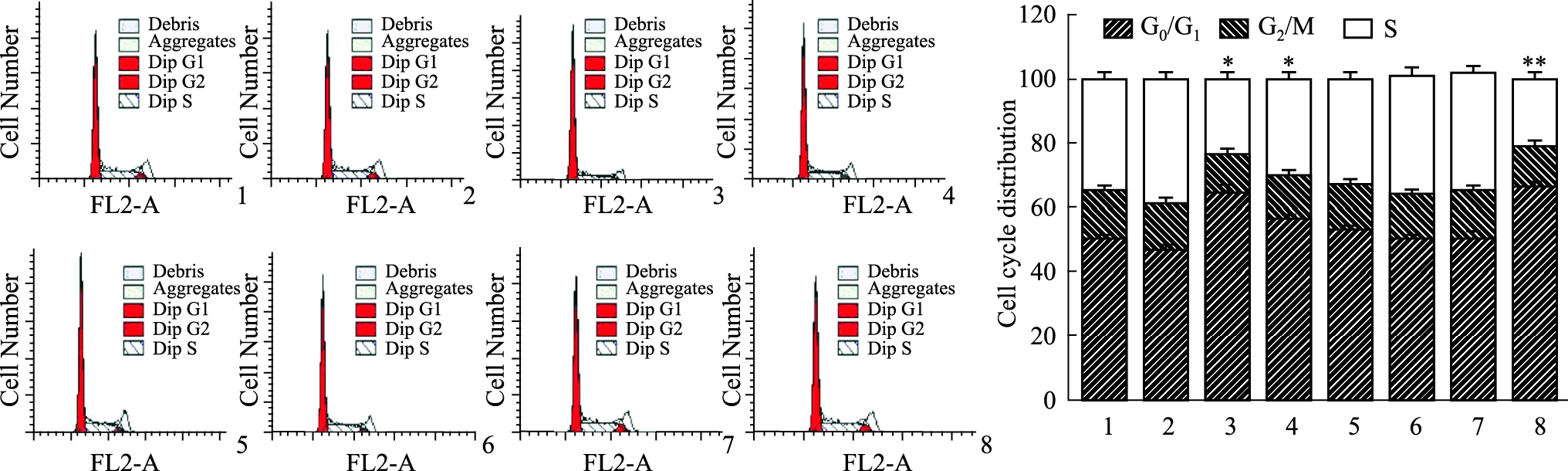
如Fig5所示,FCM检测细胞周期显示,与溶剂对照组相比,ATRA(10-5mol·L-1)和ATPR(10-5、10-6 mol·L-1)用药后,G0/G1期细胞百分比上升,S期细胞百分比下降,差异有统计学意义(P<0.05);G2/M期细胞改变不明显。结果表明ATPR影响MDA-MB-231细胞周期,将细胞阻滞在G0/G1期。
|
Fig 5
Change of cell cycle distribution of MDA-MB-231 cells treated with ATPR(n=3,  ± s)
1:Control;2:Solvent;3:ATPR(10-5mol·L-1);4:ATPR(10-6 mol·L-1);5:ATPR(10-7 mol/L);6:ATPR(10-8 mol·L-1);7:ATPR(10-9 mol·L-1);8:ATRA(10-5mol·L-1),*P<0.05, **P<0.01 vs the solvent group. ± s)
1:Control;2:Solvent;3:ATPR(10-5mol·L-1);4:ATPR(10-6 mol·L-1);5:ATPR(10-7 mol/L);6:ATPR(10-8 mol·L-1);7:ATPR(10-9 mol·L-1);8:ATRA(10-5mol·L-1),*P<0.05, **P<0.01 vs the solvent group.
|
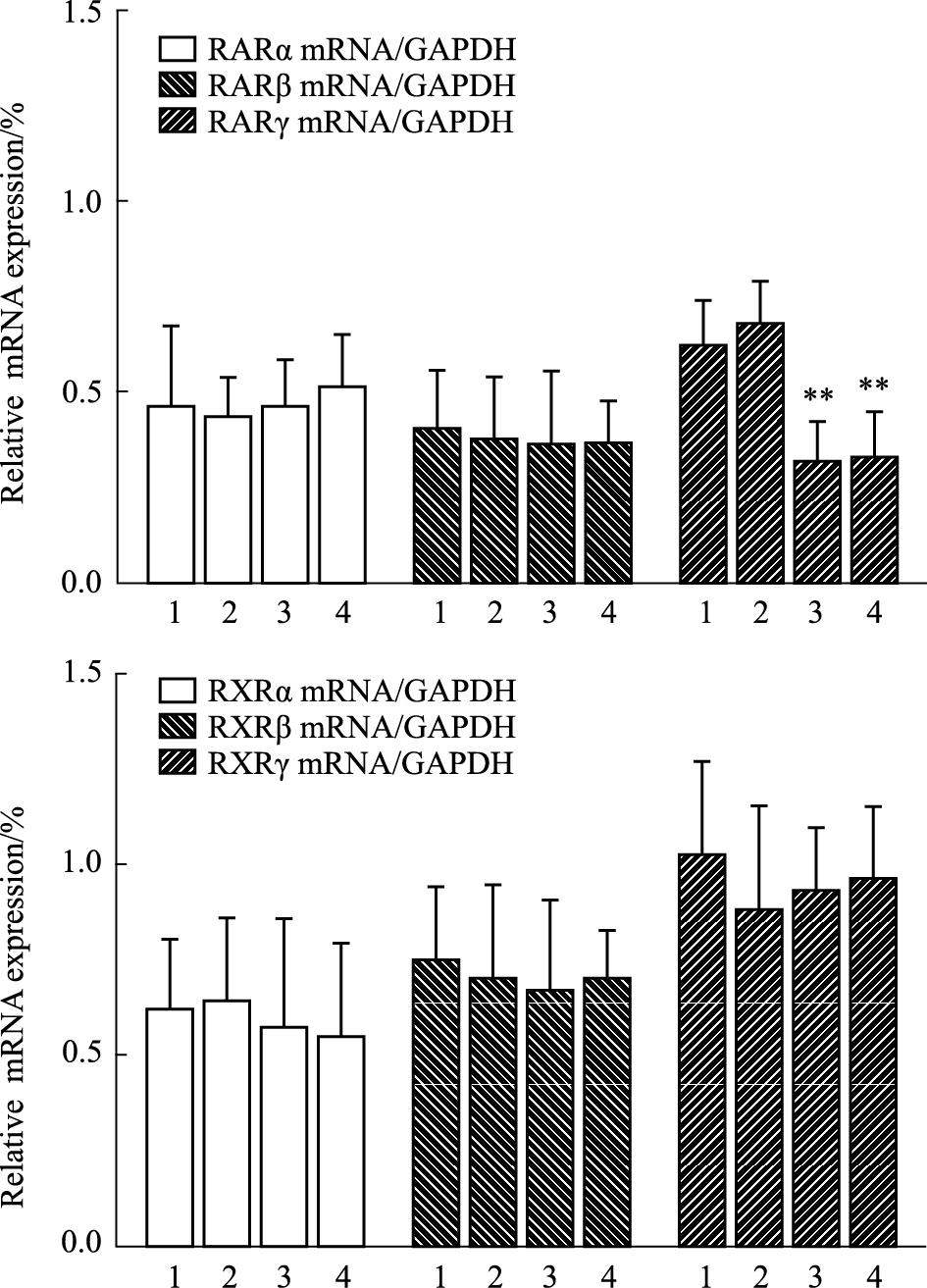
结果如Fig6所示,与溶剂对照组相比,ATPR(10-5mol·L-1)作用后,RARα、RARβ mRNA表达无明显变化,RARγ mRNA表达下降,RXRα、RXRβ、RXRγ mRNA表达无明显变化。提示ATPR用药后MDA-MB-231细胞RARγ mRNA表达下降。
|
Fig 6
Effect of ATPR on the mRNA expression of retinoic acid receptors (RARs) and Retinoid X acid receptor (RXRs) in MDA-MB-231 cells (n=3,  ± s)
1:Control;2:Solvent;3:ATRA(10-5 mol·L-1);4:ATPR(10-5mol·L-1). **P<0.01 vs the solvent group. ± s)
1:Control;2:Solvent;3:ATRA(10-5 mol·L-1);4:ATPR(10-5mol·L-1). **P<0.01 vs the solvent group.
|
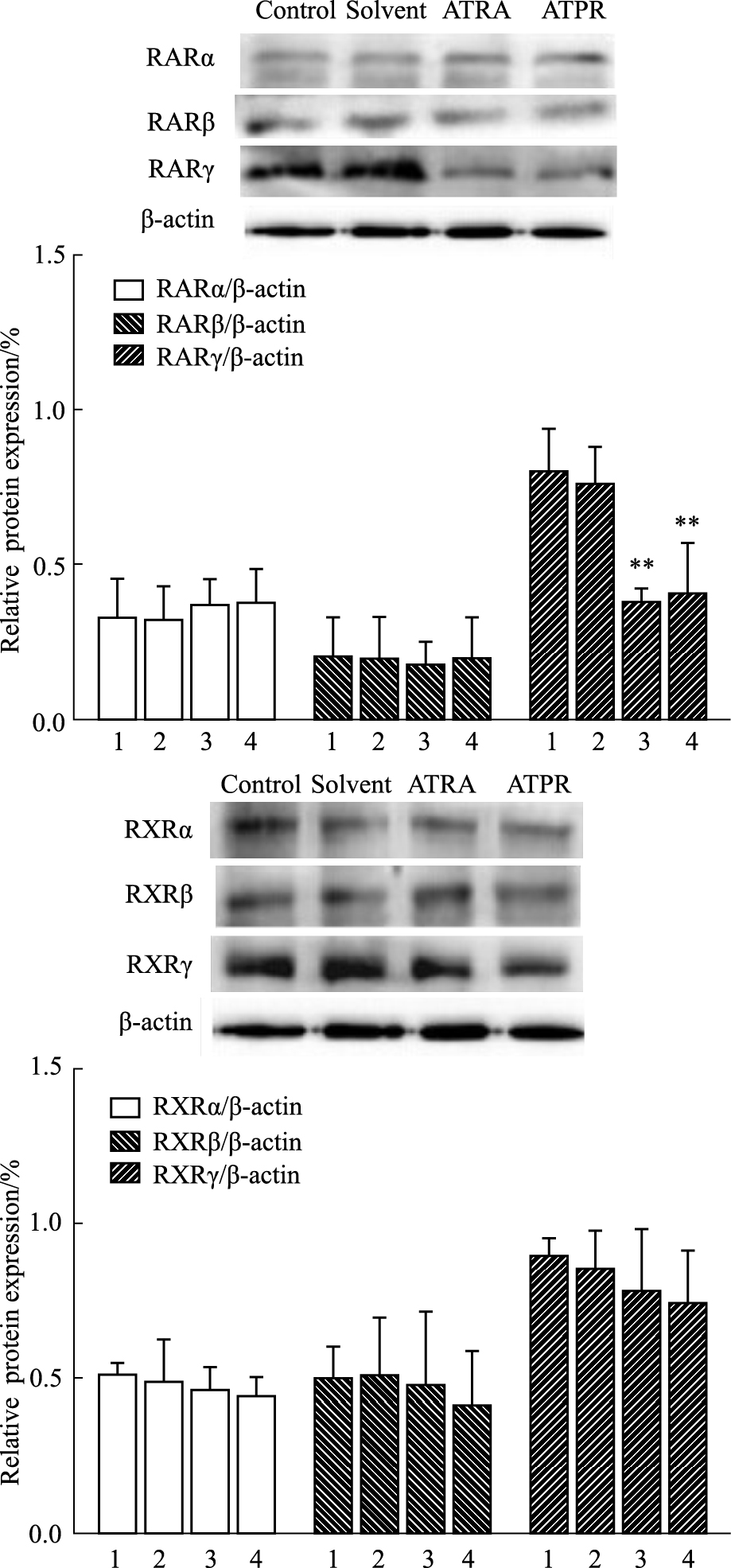
结果如Fig7所示,与溶剂对照组相比,ATPR(10-5mol·L-1)作用后,RARα、RARβ蛋白表达无明显变化,RARγ蛋白表达下降,RXRα、RXRβ、RXRγ蛋白表达无明显变化。提示ATPR用药后MDA-MB-231细胞 RARγ蛋白表达下降。
|
Fig 7
Effect of ATPR on the proteins expression of retinoic acid receptors (RARs) and retinoid X receptors (RXRs) in MDA-MB-231 cells (n=3,  ± s)
1:Control;2:Solvent;3:ATRA(10-5mol·L-1);4:ATPR(10-5mol·L-1). **P<0.01 vs the solvent group. ± s)
1:Control;2:Solvent;3:ATRA(10-5mol·L-1);4:ATPR(10-5mol·L-1). **P<0.01 vs the solvent group.
|
乳腺癌是女性最常见的恶性肿瘤,目前对乳腺癌的治疗手段包括手术治疗、全身化疗、放射治疗及内分泌治疗等[9]。放化疗通常不具有选择性,既能杀死肿瘤细胞,又杀死了大量的正常细胞。20世纪80年代Sachs[10]发现在一些抑制增殖和诱导分化的物质作用下,小鼠白血病细胞系的异常分化是可逆的,由此提出了诱导分化治疗的概念。诱导分化 治疗的基本特点是不直接杀伤肿瘤细胞,而是诱导 其分化为正常或接近正常的细胞,减慢肿瘤细胞增殖速度,最终使恶性肿瘤缓解,从而避免常规放、化疗所引起的骨髓抑制、免疫抑制等毒副作用[11]。全反式维甲酸作为经典的诱导分化剂,已广泛应用于急性早幼粒白血病的临床治疗,但ATRA存在一系列的问题,如维甲酸综合征耐药等影响其疗效,本课题组以ATRA为先导化合物,合成的维甲酸衍生物ATPR对多种肿瘤细胞株具有抑制增殖诱导分化作用,前期研究发现,ATPR对雌激素受体阳性人乳腺癌细胞株MCF-7具有诱导分化作用,本实验探讨在雌激素受体阴性人乳腺癌细胞株MDA-MB-231上,ATPR对其是否具有诱导分化作用? 实验结果表明,ATPR抑制MDA-MB-231细胞的增殖存在浓度-时间依赖性行为。
细胞分化主要表现在形态和功能两个方面,形态分化是细胞分化的基本特征。瑞氏-吉姆萨染色结果显示,MDA-MB-231细胞经ATPR处理后形态发生改变,细胞生长密度下降,核质比降低。MUC-1是一种在上皮性肿瘤高度或异常表达的膜糖蛋白,常作为乳腺癌细胞分化程度的一个重要指标[12]。研究发现,ATPR作用后,MDA-MB-231细胞分泌MUC-1含量为(43.87±1.37) kU·L-1,较溶剂对照组(61.00±1.28) kU·L-1差异有显著性。细胞形态学的改变和分化标志物MUC-1含量的变化都说明ATPR对MDA-MB-231细胞具有诱导分化作用。
肿瘤细胞的周期学特点是细胞群体主要分布于DNA合成活跃S期,而分化细胞群体主要分布于DNA合成静止的G1/G0 期。因此细胞周期不可逆的阻滞于G0/G1期是细胞分化的重要特征。本研究结果显示,MDA-MB-231细胞周期发生明显改变,G0/G1期的细胞比例增多,S期细胞比例下降,呈明显的G0/G1期阻滞。说明ATPR可以调控MDA-MB-231细胞周期,将其阻滞在G0/G1期比例升高,具有诱导分化效果。
维甲酸受体属于核受体超家族中的一个子家族,在这个超家族中还包括甾体类、维生素D和甲状腺激素受体及过氧化物酶体增殖物激活受体、昆虫脱皮类固醇受体和许多尚未知其配体的孤儿受体。Ayaori等[13]研究表明,维甲酸类化合物如ATRA、9cis RA首先通过与细胞质的维甲酸结合蛋白Ⅰ、Ⅱ(CRABPⅠ、CRABPⅡ)结合,转运至细胞核,与核受体RARs和RXRs形成的同/异二聚体结合,从而发挥抑制细胞生长、分化以及凋亡等调节作用。维甲酸受体子家族包括:RARs和RXRs,分别有α、β、γ 3种亚型。有文献指出在激素依赖性和非激素依赖性乳腺癌中,维甲酸作用后,维甲酸受体表达各不相同,在MDA-MB-231细胞中RARα、RXRα的表达非常低[14]。本课题组前 期研究发现ATPR抑制MCF-7细胞增殖过程中,维甲酸受体RARs、雌激素受体ERs的表达发生变化。根据这一现象我们探讨维甲酸受体在ATPR对MDA-MB-231细胞诱导分化过程发挥怎样的变化?q-PCR和Western blot结果表明与溶剂对照组相比,ATPR用药后,RARγ的表达降低,RARα、RARβ、RXRα、RXRβ和RXRγ表达无明显变化。上述结果提示,ATPR对MDA-MB-231细胞中不同的维甲酸受体表达的影响是不同的,与文献的研究结果一致[14]。
(本实验在安徽省天然药物活性研究重点实验室完成,衷心感谢导师陈飞虎教授对我的课题悉心指导,感谢葛金芳老师在我实验遇到困难时耐心解答,感谢实验室的同学们在实验期间对我实验技术的帮助,最后感谢母校安徽医科大学给我提供良好的学习环境。)
| [1] | Sanz M A, Martin G, Diaz-Mediavilla J. All-trans-retinoic acid in acute promyelocytic leukemia [J]. N Engl J Med,1998, 338 (6):393-4. |
| [2] | De la Serna J, Montesinos P, Vellenqa E,et al. Causes and prognostic factors of remission induction failure in patients with acute promyelocytic leukemia treated with all-trans retinoic acid and idarubicin [J]. Blood, 2008, 111(7):3395-402. |
| [3] | Montesinos P, Díaz-Mediavilla D J, Debén G, et al. Central nervous system involvement at first relapse in patients with acute promyelocytic leukemia treated with all-trans retinoic acid and anthracycline monochemotherapy without intrathecal Prophylaxis[J]. Haematologica,2009, 94(9):1242-9. |
| [4] | Yarali N,Tavil B, Kara A, et al. Acute renal failure during ATRA treatment [J].Pediatr Hematol Oncol,2008,25(2):115-8. |
| [5] | 阮晶晶,陈飞虎,徐 佼,等. 4-氨基-2-三氟甲基苯基维甲酸酯对K562细胞分化和细胞周期的影响[J]. 中国药理学通报,2009,25(9):1238-43. Ruan J J,Chen F H,Xu J,et al.4-amino-2-trifluoromethyl-phenyl retinate induced K562 cell differentiation and cell cycle influence[J]. Chin Pharmacol Bull,2009, 25(9):1238-43. |
| [6] | 彭晓清,陈飞虎,雷 静,等.4-氨基-2-三氟甲基苯基维甲酸酯通过PTEN/PI3K/AKT抑制YAC-1细胞增殖和诱导其分化[J]. 中国药理学通报,2014,30(1):60-5. Peng X Q, Chen F H, Lei J, et al. Differentiation induction effect of 4-amino-2-trifluoromethyl-phenyl retinate on lymphoma cancer cell and its possible mechanisms[J]. Chin Pharmacol Bull, 2014, 30(1):60-5. |
| [7] | 汪 楠,陈飞虎,葛金芳,等.4-氨基-2-三氟甲基苯基维甲酸酯对MCF-7细胞增殖分化的影响极其机制研究[J].中国药理学通报, 2013, 29(6):767-72. Wang N, Chen F H, Ge J F, et al. Differentiation induction effect of 4-amino-2-trifluoromethyl-phenyl retinate on human breast cancer MCF-7 cell and its possible mechanisms[J]. Chin Pharmacol Bull, 2013, 29(6):767-72. |
| [8] | Hu K W, Pan X H,Chen F H, et al. A novel retinoic acid analog, 4-amino-2-trifluoromethyl-phenyl Retinate, inhibits gastric cancer cell Growth[J]. Int J Mol Med, 2014, 33(2):415-22. |
| [9] | DeSantis C E, Lin C C,Mariotto A B, et al. Cancer treatment and survivorship statistics, 2014[J]. CA Cancer J Clin, 2014, 64(4):252-71.doi:10.3322 |
| [10] | Sachs L. Growth, differentiation and the reveral of malignancy[J]. Sci Am, 1986,254(1):40-7. |
| [11] | Machner B, Neppert B, Paulsen M, et al. Pseudotumor cerebri as a reversible side effect of all-trans retinoic acid treatment in acute promyelocytic leukaemia[J]. European J Neurol,2008, 15:e68-e69. |
| [12] | Yu F, Yao H, Zhu P, et al. Let-7 regulates self renewal and tumorigenicity of breast cancer cells[J]. Cell,2007, 14(11):1109-23. |
| [13] | Ayaori M, Yakushiji E, Ogura M, et al. Retinoic acid receptor agonists regulate expression of ATRA-binding cassette transporter G1 in macrophages [J]. Biochim Biophys Acta,2012, 1821(4):561-72. |
| [14] | Conzen S. Minireview:nuclear receptors and breast cancer[J]. Mol Endocrinol, 2008, 22(10):2215-28. |

