2. 沈阳医学院 科学实验中心, 辽宁 沈阳 110034
 , WANG Li1, LI Zhu1, LIU Zhao-yang1, LIU Chang1, GUO Li2, FU Jia2, QI Rong2, WANG Jun-ping1
, WANG Li1, LI Zhu1, LIU Zhao-yang1, LIU Chang1, GUO Li2, FU Jia2, QI Rong2, WANG Jun-ping1

2. Central Laboratory, Shenyang Medical College, Shenyang 110034, China
胃癌作为当今世界范围内常见的恶性肿瘤,其发病率占消化道肿瘤的40%~50%,在我国胃癌死亡率为各种癌症之首,多数患者在就诊时己经处于进展期,预后较差,5年生存率不足10%[1]。转移作为胃癌进展期重要特点之一,是胃癌治疗所面临最大障碍,因此迫切需要研究防治胃癌转移的药物和方法,改善患者的预后。
棉酚是从锦葵科植物成熟种子、根皮中提取的一种黄色多元酚类物质,作为口服男用避孕药及治疗妇科疾病应用于临床。自上世纪80年代起诸多研究表明,棉酚及其衍生物具有明显的抗肿瘤作用,并具有多重机制、不良反应小等优点,故有很大的研究价值[2]。目前研究多为观察其影响肿瘤细胞增殖和诱导凋亡作用,关于其对肿瘤细胞迁移能力影响的报道较少见[3, 4]。
本研究拟采用Transwell 小室法检测棉酚对胃癌细胞迁移能力的抑制作用,同时检测胞内Akt/β-catenin信号通路活性及相关蛋白cyclin D1、MMP-2、E-cadherin和vimentin表达的变化,从分子水平探讨其抑制人胃癌细胞迁移能力的机制。
1 材料与方法 1.1 材料棉酚和溴化四氮唑蓝(MTT)(Sigma公司); RPMI 1640培养基及胰酶(Gibco公司);新生牛血清(FBS)(杭州四季青公司);化学发光检测试剂盒(Pierce公司) ; Transwell小室(Costar公司);cyclin D1、MMP-2、β-actin抗体(Santa Cruz公司);p-Akt、β-catenin、E-cadherin和vimentin抗体(CST公司);NC膜(Millipore公司);多聚甲醛、结晶紫均为国产分析级产品。
1.2 细胞培养人胃癌MGC-803和MKN1细胞株由中国科学院上海细胞生物学研究所细胞库提供。将细胞于37℃、5% CO2培养箱中,用RPMI 1640培养基+10% FBS培养,1~2 d更换培养液1次,每2~3天传代1次,实验时选用对数生长期细胞。
1.3 MTT 比色法检测细胞增殖取对数生长期细胞,制备成单细胞悬液,调整细胞浓度为每毫升5×104个细胞,体积为100 μL,接种于96 孔板内,于37 ℃、5% CO2条件下培养。加入含棉酚培养液(终浓度分别为50、25、12.5、6.25 μmol·L-1),同时设立正常对照组,空白组不加细胞,只加RPMI 1640培养基。体外培养48 h后,每孔加入20 μL MTT (终浓度5 g·L-1),37℃继续孵育4 h,弃上清,每孔加入150 μL DMSO 振荡10 min,于490 nm 测定吸光度值(A),实验重复3次。依下列公式计算细胞存活率/%=(A实验组-A空白组)/(A对照组-A空白组)×100%。实验重复3次。
1.4 Transwell 小室实验用0.25% 的胰蛋白酶消化细胞,用无血清的RPMI 1640培养液制成细胞浓度为每毫升5×104个的细胞悬液。取细胞悬液200 μL,培养基中分别加入终浓度0、2.5、5、10 μmol·L-1的棉酚,加入上室中,并在下室中加入600 μl含10% FBS的RPMI 1640培养基,每组设3个复孔。培养24 h后,取出小室用无菌棉签擦去上室内的细胞,多聚甲醛固定10 min;0.1%结晶紫染色液室温染色20 min,清水漂洗3遍;Transwell小室翻过来,底面朝上置镜下观察小室穿膜细胞数,每个小室取5个视野。细胞迁移抑制率/%=(对照组迁移细胞数-棉酚组迁移细胞数)/对照组迁移细胞数×100%。实验重复3次。
1.5 Western blot法检测相关蛋白表达变化提取经0、2.5、5、10 μmol·L-1的棉酚处理24 h后细胞总蛋白,离心后取上清经Lowry法蛋白定量后电泳,完毕后将样品转移至NC膜上,封闭1 h,分别加入p-Akt抗体 (1 ∶ 500)、β-catenin抗体 (1 ∶ 500)、cyclin D1抗体 (1 ∶ 500)、E-cadherin抗体(1 ∶ 500)、vimentin抗体 (1 ∶ 500)、MMP-2抗体 (1 ∶ 200)、β-actin抗体(1 ∶ 1 000),4℃过夜。漂洗后加入辣根过氧化物酶(HRP)标记的二抗(1 ∶ 1000)室温孵育0.5 h,TBST洗膜4次,用化学发光法(ECL)显色,凝胶图像分析系统照像,并利用Image J 软件对目的条带进行灰度值检测,以β-actin为内参照分析蛋白相对表达量。所有结果都被至少重复3次。
1.6 统计学分析 数据以 表示。应用SPSS 19.0软件进行数据统计分析,组间差异比较采用双尾student′s t-test 检验。
表示。应用SPSS 19.0软件进行数据统计分析,组间差异比较采用双尾student′s t-test 检验。
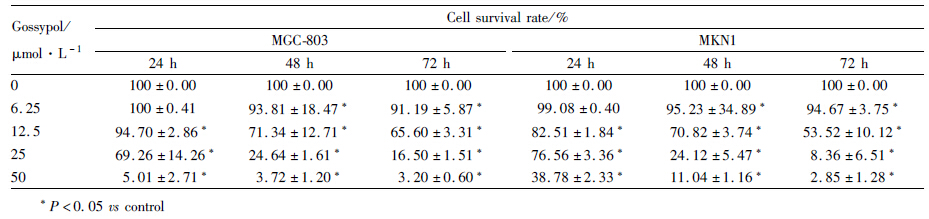
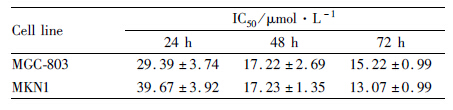
以0、6.25、12.5、25、50 μmol·L-1棉酚分别处理细胞24、48、72 h后,采用MTT法检测各组吸光度,计算棉酚对MGC-803细胞和MKN1细胞的增殖抑制率。与对照组比较,棉酚对两种胃癌细胞均有抑制作用。在一定范围内,随着棉酚浓度的增加和作用时间的延长,抑制作用增强 (Tab1)。 棉酚作用24、48、72 h抑制胃癌细胞增殖50%的药物浓度(IC50)见Tab2。
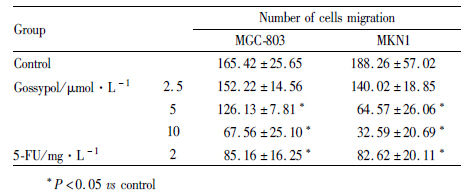
采用Transwell小室法检测以小于72 h的IC50浓度的棉酚(0、2.5、5、10 μmol·L-1)分别处理MGC-803细胞和MKN1细胞24 h后对细胞迁移能力的影响,以5-氟尿嘧啶(2 mg·L-1)做为阳性对照组。由MTT实验结果可知,以上浓度的棉酚作用24 h对MGC-803细胞和MKN1细胞增殖影响极小,故在判断此浓度药物对细胞迁移能力影响时可排除药物对细胞增殖的影响。结果显示,与对照组相比,5-氟尿嘧啶组、5和10 μmol·L-1棉酚组穿膜细胞数明显减少,差异有统计学意义(P<0.05)(Tab3、Fig1)。

|
| Fig 1 Inhibition of migration of gastric carcinoma cells by gossypol 5-FU was regarded as a positive control.MGC-803 and MKN1 cells were treated with gossypol for 24 h.Inhibition of cell migration was assessed by the transwell assay(×100) |
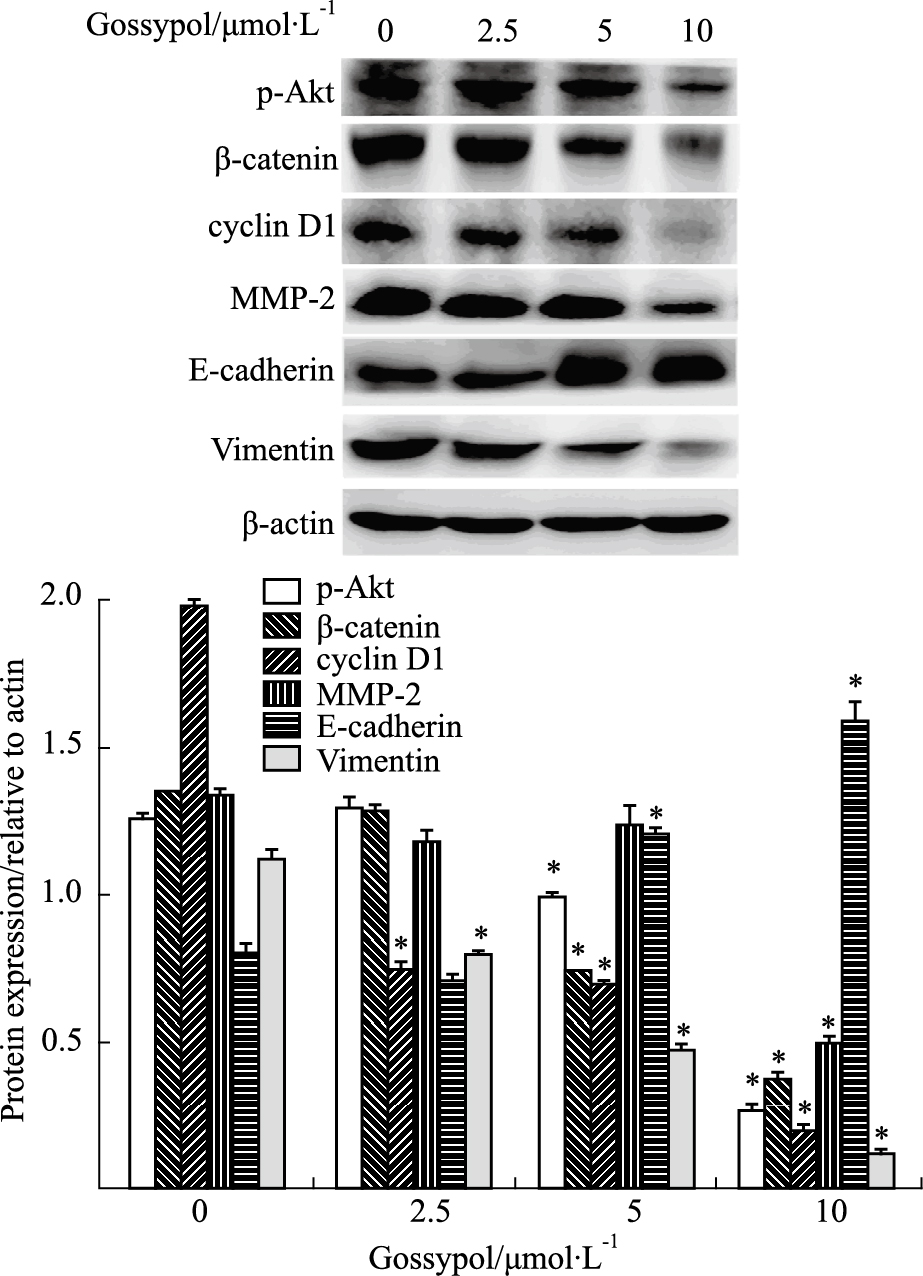
分别以0、2.5、5、10 μmol·L-1棉酚处理胃癌MKN1细胞24 h后,提取细胞总蛋白,Western blot法检测发现随着棉酚浓度的增加,细胞总蛋白的p-Akt、β-catenin、cyclin Dl、MMP-2和vimentin的蛋白表达下降,而E-cadherin蛋白表达明显升高,差异有统计学意义(P<0.05)(Fig2)。
|
| Fig 2 Effects of activation of Akt/β-catenin pathway and expression of related proteins in MKN1 cells after treated by gossypol The expressions of p-Akt,β-catenin,cyclin D1,MMP-2,E-cadherin and vimentin were detected by Western blot,β-actin was used as a loading control. *P<0.05 vs control |
本研究显示棉酚具有抑制胃癌细胞增殖、迁移的作用,且对胃癌细胞迁移能力的抑制率高于增殖抑制率,说明大量细胞在死亡之前就已经丧失迁移能力,此结果提示棉酚在胃癌恶性转移方面可能发挥有效的治疗作用。
Akt是多个信号转导通路中的关键中枢效应蛋白。磷酸化的Akt激活其下游分子,与肿瘤的运动、侵袭与转移关系密切,抑制Akt的活化可以降低多种肿瘤细胞的侵袭转移能力[5]。β-catenin是一种分子量为90 ku多功能蛋白质,在细胞内可存在于细胞膜、细胞质及细胞核中。β-catenin能与多种蛋白相互作用,如E-cadherin、淋巴增强因子/T细胞因子(LEF/TCF)、α-连环链蛋白等,参与Wnt信号通路和细胞间黏附、肿瘤转移等过程[6]。Akt活性增加能够增加β-catenin 在肿瘤细胞中的浓度,促进β- catenin蛋白入核及转录活性,从而加快肿瘤细胞的迁移和侵袭[7]。故为了进一步探讨棉酚抑制胃癌细胞迁移作用的分子机制,本研究选择Akt/β-catenin为研究的切入点。结果显示,棉酚明显降低了胃癌细胞中p-Akt和β-catenin蛋白表达,说明棉酚抑制胃癌细胞迁移作用可能与其抑制Akt/β-catenin信号通路活性有关。
为进一步明确棉酚对胃癌细胞Akt/β-catenin信号通路抑制作用与其抑制胃癌细胞迁移作用的相关性,本研究检测了棉酚对几种Akt/β-catenin信号通路下游和肿瘤细胞迁移能力相关蛋白(E-cadherin、vimentin、cyclin D和MMP-2)表达的影响。
E-cadherin是上皮细胞中的一类依赖Ca2+的细胞黏着跨膜糖蛋白,位于细胞胞质内β-catenin大部分与胞膜上E-cadherin的胞质端相连构成E-cadherin/β-catenin复合物,与细胞骨架相连,介导细胞间黏附连接,以维持上皮细胞的极性、完整性和细胞间黏附的稳定性[8]。Akt能够抑制E-cadherin基因的转录,而E-cadherin表达水平的下降可使β-catenin在胞质内积聚,并促进其入核,进一步激活下游基因的转录[9]。
MMP-2为基质金属蛋白酶类中的重要一员,具有很强的降解基底膜成份能力,被认为是与肿瘤的恶性进程、侵袭和转移密切相关的一类明胶酶,是细胞迁移能力增加的标志蛋白,体外研究显示抑制MMP-2的活性可以阻滞肿瘤细胞迁移[10, 11]。已有多项研究表明,Wnt/β-catenin信号通路活化可提高MMP-2的表达[12]。cyclin D1是Wnt/β-catenin信号通路下游蛋白,Wnt/β-catenin信号通路能够促进cyclin D1的表达[13]。有多项研究都表明,cyclin D1的表达与肿瘤的浸润和转移密切相关,抑制cyclin D1表达后能够明显抑制肿瘤细胞的浸润、迁移。
Vimentin为细胞结构蛋白中间丝蛋白的Ⅲ型,现在越来越多的资料表明,vimentin参与肿瘤细胞的黏附、迁移、侵袭等过程,在肿瘤转移过程中起重要作用。Vimentin可以介导细胞移动相关骨架蛋白的重组,高表达vimentin的细胞具有高侵袭能力,抑制vimentin的表达可以降低癌细胞的迁移、侵袭能力,vimentin基因敲除鼠创伤愈合速度非常缓慢[14]。这些资料均表明vimentin参与上皮细胞的迁移过程。Vimentin的表达水平受β-catenin表达水平的调控,β-catenin/T细胞因子(β-catenin /TCF)复合物能激活vimentin启动子,敲低β-catenin表达能引起vimentin的表达下降[15, 16]。
本研究结果显示,棉酚能够明显降低胃癌MGC-803细胞和MKN1细胞MMP-2、vimetin和cyclin D1蛋白表达,而上调E-cadherin表达水平,这与其下调Akt/β-catenin通路活性而抑制胃癌细胞迁移能力一致。
有研究显示,E-cadherin和vimentin均可通过不同作用机制影响细胞凋亡进程。Vimentin通过与p53蛋白结合,减少p53入核数量,减少促凋亡因子(如Bad、caspase等)的释放等作用而促进细胞凋亡[17, 18]。而E-cadherin通过上调Bcl-2或其他抗凋亡蛋白的表达而产生抗细胞凋亡作用[19, 20]。本研究结果显示,当以对细胞增殖无明显影响的较低浓度的棉酚处理胃癌细胞表现为vimentin蛋白表达明显下调,而E-cadherin蛋白表达上调,说明此时E-cadherin和vimentin可产生抑制胃癌细胞凋亡、促进胃癌细胞迁移的作用,这可能与较低浓度的棉酚表现出对胃癌细胞迁移能力的抑制率高于增殖抑制率有关。
综上,本研究表明棉酚可抑制胃癌细胞迁移能力,其作用机制与抑制Akt/β-catenin信号传导通路活性,进而影响其下游肿瘤细胞迁移相关的关键调节因子MMP-2、vimetin、cyclin D1和E-cadherin的蛋白表达相关。
(致谢:本文实验在沈阳医学院科学实验中心完成。)
| [1] | 李鸿梅,李雪岩,蔡德富,等.齐墩果酸对顺铂耐药胃癌SGC-7901细胞增殖的影响及其机制研究[J].中国药理学通报,2010,26(5):657-60. Li H M,Li X Y,Cai D F,etal.Effectsofoleanolicacidon proliferationofSGC-7901/CDDP in vitro and its potential mechanisms[J].Chin Pharmacol Bull,2010,26(5):657-60. |
| [2] | 付帅,吴勇.棉酚及其衍生物抗肿瘤机制的研究进展[J].医学综述,2011,17(4):524-6. Fu S,Wu Y.Research progress in anti-neoplastic mechanisms of gossypol and derivative[J].Med Rev,2011,17(4):524-6. |
| [3] | Li H,Piao L,Xu P,et al.Liposomes containing (-)-gossypol-enriched cottonseed oil suppress Bcl-2 and Bcl-xL expression in breast cancer cells[J].Pharm Res,2011,28(12):3256-64. |
| [4] | Chien C C,Ko C H,Shen S C,et al.The role of COX-2/PGE2 in gossypol-induced apoptosis of colorectal carcinoma cells[J].J Cell Physiol,2012,227(8):3128-37. |
| [5] | Qiao M, Iglehart J D, Pardee A B.Metastatic potential of 21T human breast cancer cells depends on Akt/protein kinase B activation[J].Cancer Res,2007,67(11):5293-9. |
| [6] | Pronobis M I, Peifer M. Wnt Signaling:the many interfaces of β-catenin[J].Curr Biol,2012,22(4):R137-9. |
| [7] | Zhang X,Chen T,Zhang J,et al. Notch1 promotes glioma cell migration and invasion by stimulating β-catenin and NF-κB signaling via Akt activation[J].Cancer Sci, 2012,103(2):181-90. |
| [8] | Jeanes A,Gottardi C J,Yap A S.Cadherin and cancer:how does cadherin dysfunction promote tumor progression[J].Oneogene,2008,27(55):6920-9. |
| [9] | Behrens J, von Kries J P, Kühl M, et al. Functional interaction of beta-catenin with the transcription factor LEF-1[J].Nature,1996,382(6592):638-42. |
| [10] | Ryu B J,Lee H,Kim S H,et al.PF-3758309,p21-activated kinase 4 inhibitor, suppresses migration and invasion of A549 human lung cancer cells via regulation of CREB, NF-κB, and β-catenin signalings[J].Mol Cell Biochem,2014,389(1-2):69-77. |
| [11] | 王秀峰,周钱梅,苏式兵.黄芩素抑制人乳腺癌细胞侵袭和迁移的实验研究[J].中国药理学通报,2010,26(6):745-50. Wang X F,Zhou Q M,Su S B.Experimental study on baicalein inhibiting the invasion and migration of breast cancer cells[J].Chin Pharmacol Bull,2010,26(6):745-50. |
| [12] | Hsieh C H,Cheng L H,Hsu H H,et al.Apicidin-resistant HA22T hepatocellular carcinoma cells strongly activated the Wnt/β-catenin signaling pathway and MMP-2 expression via the IGF-IR/PI3K/Akt signaling pathway enhancing cell metastatic effect[J].Biosci Biotechnol Biochem, 2013,77(12):2397-404. |
| [13] | 李尊岭,邵淑红,焦飞,等. Cyclin D1调控肺癌细胞的浸润和转移[J].生理学报,2012,64(1):55-61. Li Z L,Shao S H,Jiao F,et al. Cyclin D1 regulates lung cancer invasion and metastasis[J].Acta Physiol Sin,2012,64(1):55-61. |
| [14] | McInroy L, Määttä A.Down-regulation of vimentin expression inhibits carcinoma cell migration and adhesion[J].Biochem Biophys Res Commun, 2007,360(1):109-14. |
| [15] | 鞠吉雨,于文静,高志芹,等.PLK1稳定β-catenin促进食管鳞癌细胞上皮间质转化[J].中国药理学通报,2014,30(12):1948-51. Ju J Y,Yu W J,Gao Z Q,et al.PLK1 promotes epithelial-mesenchymal transition of esophageal squamous cell carcinoma cells by stabilizing β-catenin[J].Chin Pharmacol Bull,2014,30(12):1948-51. |
| [16] | Hu TH,Yao Y,Yu S,et al.SDF-1/CXCR4 promotes epithelial-mesenchymal transition and progression of colorectal cancer by activation of the Wnt/β-catenin signaling pathway[J]. Cancer Lett,2014,354(2):417-26. |
| [17] | Yang X,Wang J,Liu C,et al.Cleavage of p53-vimentin complex enhances tumor necrosis factor-related apoptosis-inducing ligand-mediated apoptosis of rheumatoid arthritis synovial fibroblasts[J].Am J Pathol,2005,167(3):705-19. |
| [18] | Byun Y,Chen F,Chang R,et al.Caspase cleavage of vimentin disrupts intermediate filaments and promotes apoptosis[J].Cell Death Differ, 2001,8(5):443-50. |
| [19] | Tran N L,Adams D G,Vaillancourt R R,et al.Signal transduction from N-cadherin increases Bcl-2.Regulation of the phosphatidylinositol 3-kinase/Akt pathway by homophilic adhesion and actin cytoskeletal organization[J].J Biol Chem,2002,277(36):32905-14. |
| [20] | Ferreira A C,Suriano G,Mendes N,et al.E-cadherin impairment increases cell survival through Notch-dependent upregulation of Bcl-2[J].Hum Mol Genet,2012,21(2):334-43. |