


2. 汕头大学医学院药理学教研室, 广东 汕头 515041
2. Dept of Pharmacology, Shantou University Medical College, Shantou Guangdong 515041, China
氯米帕明是临床治疗重度抑郁常用的三环类药物之一,并用于强迫症、焦虑症治疗。其机制主要是抑制五羟色胺再摄取,同时也是组胺H1受体、乙酰胆碱毒蕈碱受体和肾上腺素α1受体的拮抗剂/反向激动剂,后三者效应与其不良反应直接有关[1]。众所周知,氯米帕明在临床有好的治疗效果,但明显的副作用也影响它应用的安全性,如:增加癫痫发作、心脏毒性、认知损害、抗胆碱能不良反应、药物相互作用以及过量致死性等[2],在临床需个体化治疗,监测患者血药浓度是个体化用药的重要保证。
地西泮、奥沙西泮、氯硝西泮和阿普唑仑等苯二氮 类药物是临床广泛应用镇静催眠抗焦虑药,主要通过与苯二氮 受体结合发挥中枢神经系统抑制作用[3],奥沙西泮同时还是地西泮的活性代谢产物[4]。这类药物与其它中枢药物联用已成为治疗神经系统疾病的常见手段,抑郁症、强迫症、焦虑症患者往往需要氯米帕明与这类药物合用,因患者的个体差异及其它因素,在增强疗效的同时,耐受性、依赖性及毒性可能有所增加[5]。所以就更必要同时对它们进行监测。目前,有用高效液相色谱法[6]、液质联用[7]测定苯二氮 类药物及其代谢物,气质联用测安眠药[8, 9],液质联用测三环类抗抑郁药[10, 11],但用高效液相色谱法同时测定这几种药物国内报道罕见,且方法复杂[12]。在测定方法中,目前国内对于血浆样品前处理方法有着明显的缺陷,大家采用的固相萃取多用C18固相萃取柱预处理血样[13, 14],这样对极性、非极性混合物同时萃取回收率偏低,降低测试灵敏度。本研究针对以上的需要与不足,建立用HPLC同时测定血浆中氯米帕明和4种苯二氮 类药物浓度的方法,并改进前处理萃取方法,以获得更高的回收率,提高灵敏度。
1 材料与仪器 1.1 药品试剂甲醇(北京百灵威科技有限公司)和乙腈(瑞典Oceanpak公司)为色谱纯,其它试剂为分析纯; 去离子水为Milli-Q50超纯水;地西泮、奥沙西泮、氯硝西泮、阿普唑仑, 氯米帕明和盐酸苯海拉明(内标)对照品(中国药品生物制品检定所),空白血浆(汕头大学医学院第一附属医院血库)。
1.2 仪器设备Agilent 1100高效液相色谱系统(包括四元泵、真空脱气泵、自动进样器、柱温箱、二极管阵列检测器DAD、数据分析软件Chem Station for LC 3D Rev.A.10.01[1635],美国Agileng公司);AL204电子天平(瑞士Mettle Toledo公司);PHS-3CA精密酸度计(上海大浦仪器有限公司);Anke TGL-16G高速低温冷冻离心机(上海安亭科学仪器厂);MS3涡旋仪(德国IKA 公司);Milli-Q50超纯水仪(美国Millipore公司)。
2 方法 2.1 标准溶液配制分别精密称量地西泮、奥沙西泮、氯硝西泮、阿普唑仑、氯米帕明和内标对照品10 mg,用甲醇定容至10 mL,配制浓度为1 g·L-1的标准品储备液,-20 ℃保存。浓度0.05 g·L-1的工作液当天用流动相新鲜配制。所有溶液避光保存。
2.2 标准曲线和质控样品配制精密量取对照品地西泮、奥沙西泮、氯硝西泮、阿普唑仑和氯米帕明工作液(0.05 g·L-1),加入空白血浆,配制如下终浓度的标准曲线样品:氯硝西泮和阿普唑仑:5.0~200.0 μg·L-1(5、12.5、25、50、100、200 μg·L-1);地西泮:10.0~500.0 μg·L-1(10.0、31.25、62.5、125、250、500 μg·L-1);氯米帕明:20.0~500.0 μg·L-1(20.0、31.25、62.5、125、250、500 μg·L-1);奥沙西泮:7.5~2000 μg·L-1(7.5、50、125、250、500、1000、2000 μg·L-1)。并配制各低中高浓度质控样品(QC)。
2.3 血浆样品预处理取固相萃取柱Bond Elut-C1(100 mg,1 mL) (美国Agilent公司),依次用5 mL甲醇、超纯水活化;取500 μL 血浆,加入1 000 μL磷酸盐缓冲液(pH 7.0),加入内标工作液50 μL,涡旋1 min混匀后上样至上述C1柱;分别用1 mL去离子水、1 mL水/甲醇混合液(80 ∶ 20,V/V)淋洗1次弃去;用2 mL甲醇洗脱,收集洗脱液,45 ℃氮气吹干,复溶于125 μL流动相,离心后取上清液进样。
2.4 色谱条件色谱柱Waters XTerra C8 RP(4.6 mm×150 mm,5 μm),保护柱Agilent Zobax-Extend C18 (4.6 mm×10 mm,5 μm);流动相50 mmol·L-1 磷酸盐缓冲液(pH3.0):乙腈(73.2:26.8,V/V);检测波长 220 nm,柱温45 ℃,流速1.2 mL·min-1,进样量50 μL。
2.5 临床应用患者服用恒定日剂量药物2周后,于末次服药后12 h取血约1.2 ml,置于枸橼酸钠抗凝管,2 h内离心(1 400 r·min-1,15 min),取血浆存于-20 ℃待测。
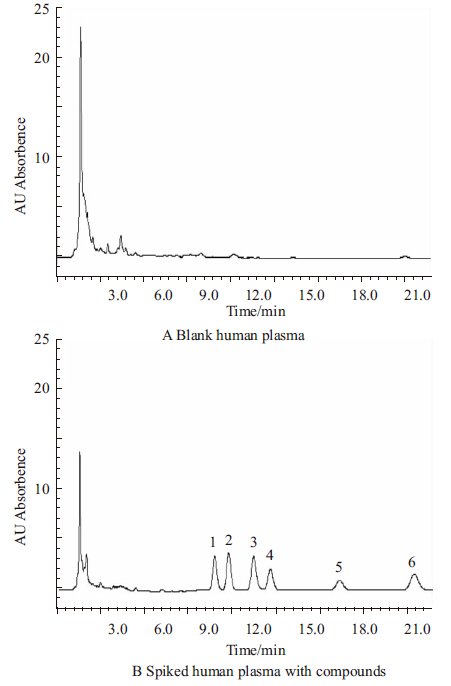
3 结果 3.1 方法选择性取6份不同来源空白血浆500 μL,除不加内标外,其余按“2.3 血浆样品预处理”项下操作,获空白血浆色谱图A;将标准溶液和内标溶液加入空白血浆,依同法操作,获含药血浆色谱图B;由Fig 1 可以看出,成分间分离良好,未见血浆中杂质干扰。
|
| Fig 1 Chromatograms obtained from (A) blank human plasma, (B) spiked human plasma with compounds (all in 100 μg·L-1). Peaks: 1: Oxazepam, 2: Alprazolam, 3: Clonazepam, 4: Clomipramine, 5: IS, 6: Diazepam. |
将标准曲线样品按“2.3 血浆样品预处理”项下操作。以被测药物峰面积与内标峰面积之比为纵坐标Y,被测药物浓度为横坐标X,用最小二乘法进行线性回归,计算回归方程。LOD定义为信噪比≥3。从Tab 1可以看出,各药物在其线性范围内均呈现良好线性关系,相关系数均在0.9994及以上,LOD在1.4~5.5 μg·L-1之间。
| Compound | Linearity range/ μg·L-1 | Regression
equation | Correlation
coefficient/r | LOD/
μg·L-1 | LOQ/
μg·L-1 |
| Y represents the peak area ratio of each drug to the IS,X represents the concentration of compound (μg·L-1) | |||||
| Alprazolam | 5.0-200.0 | 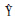 =0.0381X+0.0106 =0.0381X+0.0106 | 0.9999 | 1.5 | 5.0 |
| Clonazepam | 5.0-200.0 | 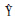 =0.0465X+0.0664 =0.0465X+0.0664 | 0.9994 | 1.4 | 4.8 |
| Diazepam | 10.0-500.0 | 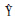 =0.0153X+0.0141 =0.0153X+0.0141 | 0.9999 | 3.0 | 10.0 |
| Clomipramine | 20.0-500.0 |  =0.0291X+0.069 =0.0291X+0.069 | 0.9995 | 5.5 | 18.5 |
| Oxazepam | 7.5-2000 |  =0.0496X-0.1334 =0.0496X-0.1334 | 0.9995 | 2.2 | 7.4 |
将“2.2”项下配制的QC样品,每个浓度进行5 样本分析,连续测定5 d,与标准曲线同时进行。根据当日标准曲线计算QC浓度,与配制浓度对比,求得本方法的精密度与准确度。结果表明(Tab 2),被测化合物的日内误差(CV%) 为2.2%~12.6%,日间误差(CV%) 为2.1%~13.2%,偏差为-10.6%~14.6%。
3.4 提取回收率取低中高浓度质控样品,重复测定5次,记录峰面积,与未经处理相应浓度药物标准溶液直接进样峰面积比较,计算提取回收率。被测药物及内标的提取回收率为81.1%~100.9%,见Tab 2。
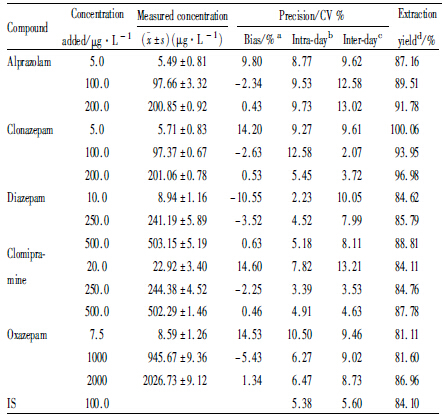 |
| a:Bias (%)=100×[(mean measured concentration)-(theoretical concentration)]/(theoretical concentration). b: Intra-day (n=5). c: Inter-day (n=5×5). d: Extraction yield (%)=analyte peak area compared to those obtained by injecting standard solutions at the same theoretical concentrations and the extraction yield values were calculated. |
标准品贮备液-20 ℃冻存2个月稳定,含药血浆-20 ℃冻存2个月稳定,含药血浆冻融3次稳定,样品处理后4 ℃放置0、12、24 h稳定,未处理样品室温放置0、2、4 h稳定。
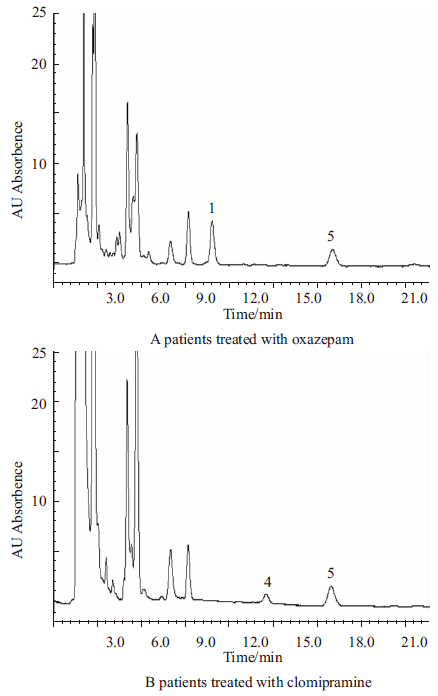
3.6 临床应用目前已对临床服用奥沙西泮、氯米帕明的患者进行了血药浓度检测,色谱图见Fig 2。
|
| Fig 2 Chromatograms obtained from plasma samples in patients treated with (A) oxazepam; (B) clomipramine 1 :Oxazepam;4:Clomipramine;5:IS |
本工作建立了在临床单用HPLC同时测定血浆中氯米[CM(25*2]帕明和4 种苯二氮〖XC卓.eps,JZ;P〗类药物浓度的方法,这对于科研实验 中采用液质联用或气质联用测定相比花费低、且操作简便,并可做到同时迅速、准确地一次性分别进行定性定量分析,可满足临床对血浆样品中此类药物含量测定要求。该方法在临床尤其实用,可在国内推广使用。
实验中观察了2种色谱柱:ODS2(4.6 mm×250 mm,5 μm) 和 C8 (4.6 mm×150 mm,5 μm)。结果显示,前者C18柱不能完全分离5种被测物,且分析时间长,可能源于药物极性较小,在C18柱上保留时间长;而C8柱则能较好分离各组分,并缩短分析时间。流动相pH 值对色谱行为影响非常明显。在流动相摸索中,首先采用流动相水相pH 2.5、pH 4.3,发现峰展宽、拖尾、且分离不完全。我们又考察了不同的pH值,结果显示,pH 3.0效果最好,改善分离度及峰形,且具适当保留时间。
本工作的难点是样品的前处理,在血浆中,同时、高效提取氯米帕明和苯二氮 这两类药物并去除干扰是非常困难,但又是必须的。文献报道[12]采用弱阳离子交换(WCX) 固相萃取柱进行血浆预处理,但洗脱时需分酸性和碱性洗脱层分别收集被测物,再分别进样,方法耗时、复杂,不适于临床应用。孙红雷等[9]结果显示C18柱提取苯二氮 等安眠药效果最差,C2柱提取效果不均匀,而且去除杂质效果较差。乔静等[15]测试了几种固相萃取柱对氯硝西泮的提取效率,结果显示Silica柱、C18柱及HLB柱的回收率均较低,为36%~73.5%。Shinozuka等[11]结果显示,HLB柱对氯米帕明提取回收率仅为72.4%。我们根据以上报道,改进了萃取方法,采用了极性较大的C1柱,提高了极性及非极性化合物,即苯二氮 类及其活性代谢产物的回收率。改进的方法国内未见报道。
本实验中的另一难点是氯米帕明的回收率偏低。苯二氮 类药物pKa 1.5~3.5,为中性偏碱性药物。氯米帕明pKa 9.38,为弱碱性药物。两类药物pKa值相差较大,缓冲溶液pH值对提取回收率、降低杂质干扰有大的影响。当我们用去离子水(pH 5~6) 稀释血浆样品时,苯二氮 类药物均有90%左右的回收率,但氯米帕明的回收率始终仅略高于50%。为提高氯米帕明的回收率,实验中观察了pH 6.0、7.0和8.0磷酸盐缓冲液对提取回收率的影响,结果显示,用pH 7.0磷酸盐缓冲液稀释血浆样品,提取回收率达84%以上,且明显降低杂质干扰。但却对苯二氮 类药物回收率影响不大。经过以上方法的改进,处理后药物浓度富集为原来的4倍,大大地提高了方法的灵敏度。
| [1] | Baldessarini R J. Drug therapy of depression and anxiety disorders[M]//Brunton L L,Lazo J S,Parker K L,Eds. Goodman & Gilman's The Pharmacological Basis of Therapeutics.11th Edition. McGraw-Hill,New York,2006:429-60. |
| [2] | 尉秀峰,徐作国,隋忠庆. 氯米帕明的不良反应/事件分析[J]. 中国药物警戒,2013,10(2):101-3. |
| [2] | Wei X F,Xu Z G,Sui Z Q. Analysis of clomipramine adverse reaction/event[J]. Chin J Pharmacov,2013,10(2):101-3. |
| [3] | 李瑞芝,郭建友,李昌煜,石晋丽. 焦虑症γ-氨基丁酸受体机制与药物干预研究进展[J]. 中国药理学通报,2010,26(9):1135-8. |
| [3] | Li R Z,Guo J Y,Li C Y,Shi J L. Progress of the research in GABA receptors and anxiety disorder:mechanism and pharmaceutical intervention[J]. Chin Pharmacol Bull,2010,26(9):1135-8. |
| [4] | George M B,Craig W S. Pharmacology[M]. 4th Edition. Elsevier Inc. Saunders,2013:186-97. |
| [5] | 张亭亭,薛 瑞,李云峰,等. 单胺转运蛋白与单胺重摄取抑制剂研究进展[J]. 中国药理学通报,2013,29(6):741-4. |
| [5] | Zhang T T,Xue R,Li Y F,et al. Research progress in monoamine transporters and monoamine transmitter reuptake inhibitors[J]. Chin Pharmacol Bull,2013,29(6):741-4. |
| [6] | Mercolini L,Mandrioli R,Iannello C,et al. Simultaneous analysis of diazepam and its metabolites in rat plasma and brain tissue by HPLC-UV and SPE[J]. Talanta,2009,80:279-85. |
| [7] | Smink B E,Brandsma J E,Dijkhuizen A,et al. Quantitative analysis of 33 benzo-diazepines, metabolites and benzodiazepine-like substances in whole blood by liquid chromatography-(tandem) mass spectrometry[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2004,811:13-20. |
| [8] | Gunnar T,Ariniemi K,Lillsunde P. Determination of 14 benzodiazepines and hydroxy metabolites,zaleplon and zolpidem as tert-butyldimethylsilyl derivatives compared with other common silylating reagents in whole blood by gas chromatography-mass spectrometry[J]. J Chromatogr B Analyt Technol Biomed Life Sci,2005,818:175-89. |
| [9] | 孙红雷,李文海. 血中安眠药物的固相萃取 GC/MS 分析方法研究[J]. 分析测试技术与仪器,2008,14(4):209-13. |
| [9] | Sun H L,Li W H. The research on the analysis of common hypnotic sedative drugs in blood by GC/MS with SPE[J]. Analysis and Testing Technol Instruments,2008,14(4):209-13. |
| [10] | 贾晶莹,张梦琪,桂雨舟,等. 液相色谱-串联质谱法同时测定7 种抗抑郁类和5 种抗精神病类药物的血药浓度[J]. 中国药物应用与监测,2010,7(5):272-5. |
| [10] | Jia J Y,Zhang M Q,Gui Y Z,et al. Quantitative determination of seven antidepressants and five antipsychotics in human serum by HPLC-MS/MS[J]. Chin J Drug Appl Monit,2010,7(5):272-5. |
| [11] | Shinozuka T,Terada M,Tanaka E. Solid-phase extraction and analysis of 20 antidepressant drugs in human plasma by LC/MS with SSI method[J]. Forensic Sci Int,2006,162:108-12. |
| [12] | 张 吟,陈一农,陈崇宏. 固相萃取-高效液相色谱法分析血浆中的13种药物[J]. 中国药学杂志,2010,45(21):1648-51. |
| [12] | Zhang Y,Chen Y N,Chen C H. Determination of 13 drugs in plasma by high performance liquid chromatography with solid phase extraction[J]. Chin Pharm J,2010,45(21):1648-51. |
| [13] | Uddin M N,Samanidou V F,Papadoyannis I N. Validation of SPE-HPLC determination of 1,4-benzodiazepines and metabolites in blood plasma,urine,and saliva[J]. J Sep Sci,2008,31:3704-17. |
| [14] | Badawi N,Simonsen K W,Steentoft A,et al. Simultaneous screening and quantification of 29 drugs of abuse in oral fluid by solid-phase extraction and ultraperformance LC-MS/MS[J]. Clin Chem,2009,55:2004-18. |
| [15] | 乔 静,刘宪平,辛国斌. 固相萃取HPLC/MS法测定血中氯硝安定[J]. 中国法医学杂志,2007,22(3):149-50. |
| [15] | Qiao J,Liu X P,Xin G B. Determination of clonazepam in blood sample by SPE-HPLC-MS[J]. Chin J Forensic Med,2007,22(3):149-50. |

