


2. 延边大学附属医院呼吸内科, 吉林 延吉 133000
2. Dept of Respiratory Medicine, Yanbian University, Yanji Jilin 133000, China
支气管哮喘是由嗜酸性粒细胞、肥大细胞等多种炎症细胞参与的慢性气道炎症性疾病[1]。糖皮质激素是治疗哮喘的一线药物,但长期使用可引起耐药性和严重的副反应。因此,有必要研究哮喘的发病机制,寻求新的治疗哮喘的靶点。芝麻素从芝麻中提取,在体内表现出较强的生物学活性,其药物作用近年逐渐被人们所重视。研究表明,芝麻素通过抑制p38磷酸化和NF-κB激活,抑制IL-6释放[2],通过p38和JNK信号途径降低MMP-1,3和13的表达[3],也可以通过降低VCAM-1表达抑制白细胞迁移,改善器官炎症[4],对血管内皮有明显的保护作用[5],表明芝麻素有明显的抗炎作用,但芝麻素抗哮喘作用研究却未见报道。本研究利用哮喘动物模型观察芝麻素抗哮喘作用,探讨其作用机制。
1 材料与方法 1.1 药品与试剂卵清蛋白 (OVA)、氢氧化铝购自美国Sigma公司;细胞因子 IL-4、IL-5、IL-13 和 IFN-γ 检测试剂盒购自美国Invitrogen公司;IL-4、IL-5、IL-13 和IFN-γ多克隆抗体购自美国Santa Cruz公司;IκBα、NF-κB p65 和β-actin购自美国Cell Signaling公司。雾化器(上海四菱医疗器械厂402型超声雾化器);酶联免疫检测仪 (RT-2100C,美国);电泳仪及电泳槽 (E-C Apparatus Corporation,美国);Western blot转膜仪和Gel Doc凝胶成像仪(BioRad公司)。
1.2 哮喘模型的建立和动物分组♂ BALB/c 小鼠 40只,体质量(18±5)g,由延边大学实验动物中心提供,合格证号:SCXK(吉)2003-000。小鼠随机分成5组,每组 8 只。正常组(Normal)、哮喘组(OVA)、芝麻素低、高剂量组(Sesamin 50、100 mg·kg-1)、阳性对照地塞米松组(DXM)。除正常组外,其余各组分别于d 1、d 14给小鼠腹腔注射2% OVA和氢氧化铝混合溶液 0.2 mL致敏。d 21将致敏小鼠置于玻璃罩内,以1% 生理盐水 OVA 溶液15 mL雾化激发 30 min,每天1次,共 5 d。芝麻素低、高剂量组分别在激发前灌服芝麻素50、100 mg·kg-1,地塞米松组按0.5 mg·kg-1灌服地塞米松。共计6 d。
1.3 实验样本获取与处理末次激发 24 h 后处死小鼠,以磷酸盐缓冲液1 mL行支气管肺泡灌洗,收集支气管肺泡灌洗液(BALF)。用细胞计数板计数细胞总数。然后4℃、3 000 r·min-1离心 10 min,取上清液,-80℃ 低温保存,待测细胞因子。沉淀涂片,Diff-Quik染色,高倍镜下进行细胞分类计数。取右肺下叶,10%甲醛溶液固定,石蜡包埋后切片,进行HE染色。其余各肺叶放入液氮中速冻,-80℃保存。
1.4 BALF中细胞因子IL-4、IL-5、IL-13和IFN-γ含量的检测采用酶联免疫吸附法(ELISA)测定,具体操作按试剂盒说明书进行,结果单位以pg·L-1表示。
1.5 免疫印迹参照延光海等[6]方法,取 200 mg 肺组织置入裂解液 0.5 mL匀浆,4℃ 12 000×g离心 2 min,取上清液,BCA法测定蛋白浓度,取30 μg蛋白,经12%SDS-PAGE电泳,120 V,90 min,然后电转移至PVDF膜上,在5%脱脂奶粉TBS-T缓冲液(25 mmol·L-1 Tris,150 mmol·L-1 NaCl,1% Tween 20,pH 7.5)室温下封闭2 h,分别加入一抗4℃过夜,洗膜后再用 HRP标记的二抗杂交,37℃ 1 h。洗膜后,在暗室中加ECL发光试剂,显影及定影。杂交信号在图像分析系统中进行光密度扫描。以β-actin 作为内参对照。
1.6 统计学处理 数值用 表示,用SPSS 13.0统计软件,各组计量数据采用单因素方差分析(ANOVA),组间两两比较采用LSD法。
表示,用SPSS 13.0统计软件,各组计量数据采用单因素方差分析(ANOVA),组间两两比较采用LSD法。
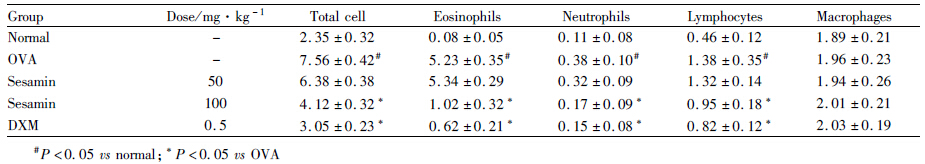
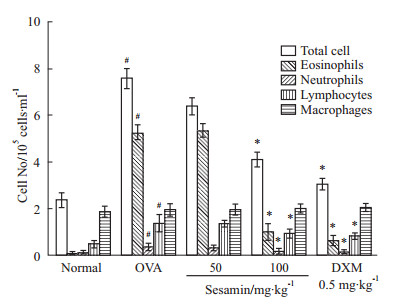
与正常组比较,哮喘组BALF中炎症细胞总数、中性粒细胞、嗜酸性粒细胞、淋巴细胞计数明显升高,差异有统计学意义(P<0.05);芝麻素高剂量组和地塞米松组明显降低哮喘小鼠BALF中上述细胞数量,与模型组比较差异有统计学意义(P<0.05),单核细胞在各组无明显变化(Tab1、Fig1)。
 , n=8,×105 ·ml-1)
, n=8,×105 ·ml-1)
 |
|
Fig 1
Effect of sesamin on total and differential cellular components count in BALF of asthma model mice ( ,n=8)
#P<0.05 vs normal; *P<0.05 vs OVA ,n=8)
#P<0.05 vs normal; *P<0.05 vs OVA
|
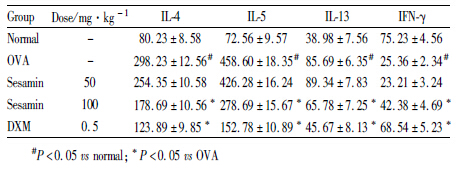
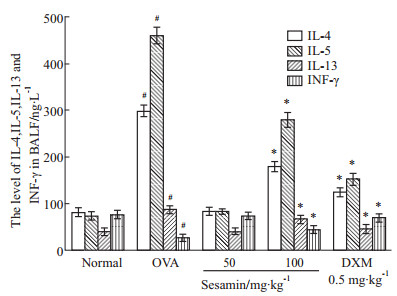
哮喘组BALF中IL-4、IL-5、IL-13水平升高,而IFN-γ水平降低,与正常组比较,差异均有统计学意义(P<0.05);芝麻素高剂量组和地塞米松组能明显降低哮喘小鼠BALF中细胞因子IL-4、IL-5、IL-13水平,并提高IFN-γ水平,差异均有统计学意义(P<0.05)(Tab2、Fig2)。
 , n=8,pg·L-1)
, n=8,pg·L-1)
 |
|
Fig 2
Effect of sesamin on levels of IL-4,IL-5,IL-13 and IFN-γ in BALF of asthma model mice (n=8, )
#P<0.05 vs normal;*P<0.05 vs OVA )
#P<0.05 vs normal;*P<0.05 vs OVA
|
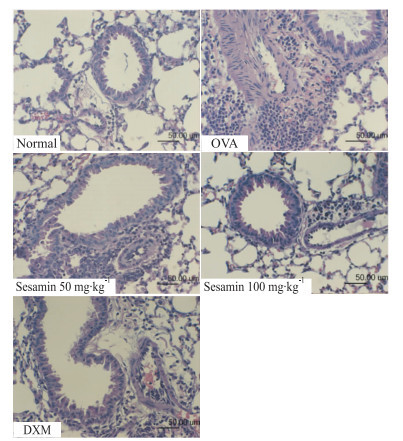
HE染色结果显示,正常组气道无明显改变; 模型组气[CM(22]道壁变粗,气道平滑肌增厚,炎症细胞浸润比较明显,多层的炎症细胞围绕在气管和血管周围,黏膜下层增生;芝麻素高剂量组和地塞米松组能明显减轻哮喘病理改变(Fig3)。
|
| Fig 3 Effect of sesamin on pathologic changes in lung tissues of asthma model mice (HE staining, bar=50 μm) |
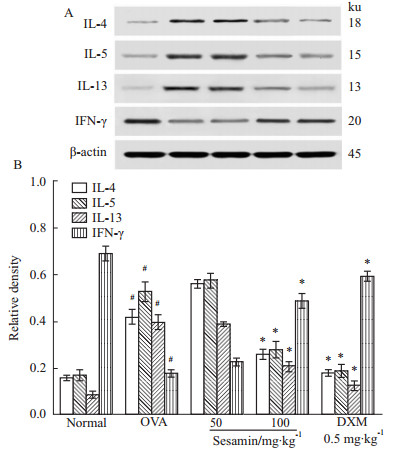
哮喘组肺组织IL-4、IL-5和IL-13蛋白表达明显增高,但IFN-γ蛋白表达明显降低,与正常组比较差异有统计学意义(P<0.05);芝麻素高剂量组和地塞米松组IL-4、IL-5和IL-13蛋白表达明显降低,但IFN-γ蛋白表达明显升高,与哮喘组比较差异有统计学意义(P<0.05),见Fig4。
|
Fig 4
Effect of sesamin on protein production of cytokines (IL-4,IL-5,IL-13 and IFN-γ) in lung tissue of asthma model mice ( ,n=8)
A:Western blot;B:Relative density. #P<0.05 vs normal;*P<0.05 vs OVA. ,n=8)
A:Western blot;B:Relative density. #P<0.05 vs normal;*P<0.05 vs OVA.
|
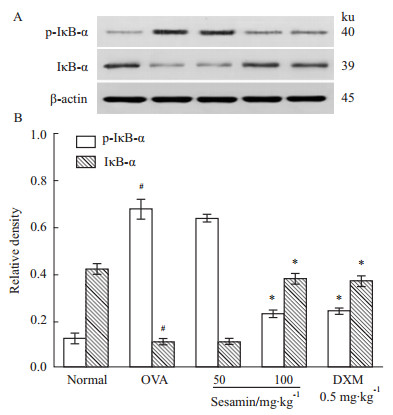
哮喘组肺组织的磷酸化IκBα蛋白表达高于正常组,差异有统计学意义(P<0.05);与哮喘组比较,芝麻素高剂量组和地塞米松组磷酸化IκBα蛋白明显减少,差异有统计学意义(P<0.05),总IκBα蛋白变化与磷酸化刚好相反(Fig5)。表明芝麻素能明显抑制哮喘小鼠IκBα磷酸化和IκBα的降解。
|
Fig 5
Effect of sesamin on IκBα phosphorylation in lung tissue of asthma model mice ( ,n=8)
A:Western blot,B:Relative density.#P<0.05 vs normal;*P<0.05 vs OVA. ,n=8)
A:Western blot,B:Relative density.#P<0.05 vs normal;*P<0.05 vs OVA.
|
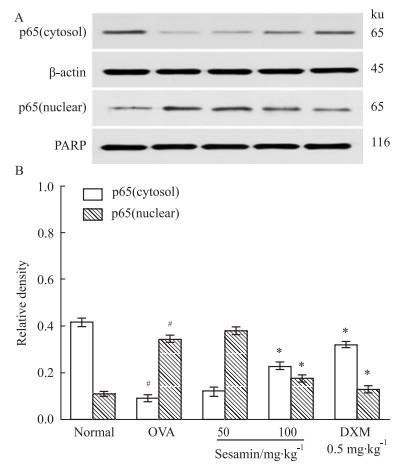
哮喘组细胞核内NF-κB p65明显增加,但胞质中NF-κB p65明显减少,与正常组比较有统计学意义(P<0.05)。芝麻素高剂量组和地塞米松组细胞核内NF-κB p65减少,而胞质中NF-κB p65明显增加,与模型组比较有统计学意义(P<0.05)。说明芝麻素有效减少NF-κB核转位,抑制NF-κB活化(Fig6)。
|
Fig 6
Effect of sesamin on NF-κB activation in lung tissue of asthma model mice ( ,n=8)
A:Western blot;B:Relative density. #P<0.05 vs normal;*P<0.05 vs OVA. ,n=8)
A:Western blot;B:Relative density. #P<0.05 vs normal;*P<0.05 vs OVA.
|
支气管哮喘是一种气道和肺部慢性炎症性疾病,浸润的炎症细胞主要以嗜酸性粒细胞为主,也包括肥大细胞、中性粒细胞和淋巴细胞等。这些细胞释放多种细胞因子,如Th1细胞因子IFN-γ和Th2细胞因子IL-4、IL-5 和IL-13等,Th1和Th2细胞因子表达的变化直接影响哮喘的发病。研究表明,芝麻素有明显的抗炎作用。芝麻素通过抑制Δ5脂肪酸去饱和酶活性,降低炎症介质前列腺素E2和TNF-α。在LPS诱导的炎症休克小鼠中,芝麻素能明显降低IL-1β、前列腺素E2和血栓素B2水平,提高IL-6和IL-10的表达,从而提高小鼠的存活率[8]。本实验研究显示,芝麻素能明显降低哮喘小鼠BALF中细胞总数和包括嗜酸性粒细胞、淋巴细胞和中性粒细胞数量;减少哮喘小鼠BALF和肺组织中 IL-4 、IL-5 和IL-13水平,提高IFN-γ的表达;HE染色也显示芝麻素减轻哮喘小鼠肺部炎症细胞浸 润。芝麻素能明显降低Th2代表细胞因子水平,提高Th1代表细胞因子的水平,并能明显抑制哮喘小鼠肺部炎症,提示芝麻素有明显的抗哮喘炎症作用。
哮喘炎症与复杂信号网络转导有关,有关哮喘的发病机制仍然不清楚。NF-κB是一个核转录因子,与包括哮喘等免疫和炎症反应密切相关[9, 10]。正常NF-κB与NF-κB抑制蛋白IκBα结合并稳定的存在于细胞质中,当细胞激活后,IκBα发生磷酸化并降解,NF-κB和IκBα复合体解离,暴露NF-κB核定位序列,NF-κB进入细胞核内与目的基因特异性结合位点结合,促进包括IL-4、IL-5 和IL-13等目的基因的转录。Jeng等[2]研究发现,芝麻素通过抑制p38和NF-κB活化减低BV-2细胞IL-6 mRNA和蛋白的表达。Harikumar等[11]也发现芝麻素通过NF-κB调节KBM-5等多种肿瘤细胞存活、增殖和侵袭。Cui等[12]通过体内和体外实验证明了芝麻素通过ERK1/2和NF-κB信号途径抑制细菌趋化肽诱导的炎症反应,提示NF-κB可能是芝麻素潜在的作用靶点。本实验显示,哮喘小鼠IκBα磷酸化明显增加,总IκBα明显减少,同时细胞质NF-κB p65减少,细胞核内NF-κB p65增多,引起NF-κB核转位。芝麻素能明显抑制IκBα磷酸化,增加总IκBα的表达,同时增加细胞质NF-κB p65,减少细胞核内NF-κB p65,表明芝麻素能够抑制IκBα磷酸化并减少其降解,阻止NF-κB p65与IκBα解离,抑制NF-κB核转位。综上所述,芝麻素有明显的抗哮喘作用,其作用机制部分是通过调节NF-κB激活。
| [1] | Kay A B.Asthma and inflammation[J].J Allergy Clin Immunol, 1991, 87(5):893-910. |
| [2] | Jeng K C, Hou R C, Wang J C, Ping L I.Sesamin inhibits lipopolysaccharide-induced cytokine production by suppression of p38 mitogen-activated protein kinase and nuclear factor-kappaB[J].Immunol Lett, 2005, 97(1):101-6. |
| [3] | Phitak T, Pothacharoen P, Settakorn J, et al.Chondroprotective and anti-inflammatory effects of sesamin[J].Phytochemistry, 2012, 80(1):77-88. |
| [4] | 周勇, 杨解人.芝麻素对代谢综合征大鼠血糖、血脂及主动脉血管细胞黏附分子-1蛋白表达的影响[J].中国临床药理学与治疗学, 2008, 13(2):195-200. Zhou Y, Yang J R.Effects of sesamin on blood glucose, blood lipids and vascular cell adhesion molecule-1 protein expression of aorta in rats with metabolic syndrome[J].Chin J Clin Pharmacol Ther, 2008, 13(2):195-200. |
| [5] | 郭莉群, 杨解人, 孔祥.芝麻素对2型糖尿病大鼠主动脉内皮功能的保护作用[J].中国药理学通报, 2012, 28(3):392-6. Guo L Q, Yang J R, Kong X.Protective effect of sesamin on endothelial function of type-2 diabetic rats[J].Chin Pharmacol Bull, 2012, 28(3):392-6. |
| [6] | 延光海, 崔云浩, 李光昭, 等.姜黄素抗过敏性作用的实验研究[J].中国药理学通报, 2010, 26(3):416-7. Yan G H, Cui Y H, Li G Z, et al.Anti-allergic effects of curcumin[J].Chin Pharmacol Bull, 2010, 26(3):416-7. |
| [7] | Chavali S R, Zhong W W, Forse R A.Dietary alpha-linolenic acid increases TNF-alpha, and decreases IL-6, IL-10 in response to LPS:effects of sesamin on the delta-5 desaturation of omega6 and omega3 fatty acids in mice[J].Prostaglandins Leukot Essent Fatty Acids, 1998, 58(3):185-91. |
| [8] | Chavali S R, Zhong W W, Utsunomiya T, Forse R A.Decreased production of interleukin-1-beta, prostaglandin-E2 and thromboxane-B2, and elevated levels of interleukin-6 and-10 are associated with increased survival during endotoxic shock in mice consuming diets enriched with sesame seed oil supplemented with Quil-A saponin[J].Int Arch Allergy Immunol, 1997, 114(2):153-60. |
| [9] | Imanifooladi A A, Yazdani S, Nourani M R.The role of nuclear factor-kappa B in inflammatory lung disease[J].Inflamm Allergy Drug Targets, 2010, 9(3):197-205. |
| [10] | Janssen-Heininger Y M, Poynter M E, Aesif S W, et al.Nuclear factor kappa B, airway epithelium, and asthma:avenues for redox control[J].Proc Am Thorac Soc, 2009, 6(3):249-55. |
| [11] | Harikumar K B, Sung B, Tharakan S T, Pandey M K.Sesamin manifests chemopreventive effects through the suppression of NF-kappa B-regulated cell survival, proliferation, invasion, and angiogenic gene products[J].Mol Cancer Res, 2010, 8(5):751-61. |
| [12] | Cui Y, Hou X, Chen J, et al.Sesamin inhibits bacterial formylpeptide-induced inflammatory responses in a murine air-pouch model and in THP-1 human monocytes[J].J Nutr, 2010, 140(2):377-81. |

