顺铂是临床上最常用的化疗药物之一,主要用于治疗多种实体瘤,但它的肾毒性和治疗效果均与剂量呈正相关,因此其肾毒性严重限制其在临床上的使用。目前有关顺铂肾毒性的分子机制尚未完全阐明,有研究发现顺铂可积聚在线粒体内引起线粒体受损,从而诱导肾小管上皮细胞凋亡[1, 2]。另外,有报道三七总皂苷(panax nonstaining saponins,PNS)可通过抑制细胞凋亡而对缺血性脑病和糖尿病肾病发挥保护作用[3, 4]。近来,有研究发现PNS对顺铂肾损伤具有保护作用[5],但尚未见报道PNS是否可通过抑制细胞凋亡而对顺铂肾损害发挥保护作用。本实验从线粒体途径探讨PNS对顺铂诱导的肾细胞凋亡的影响,为进一步研究顺铂肾毒性和PNS的防治作用提供理论依据。
1 材料与方法 1.1 实验动物健康♂ Sprague-Dawley(SD)大鼠36只,体重(200±20) g,SPF级,由广西医科大学实验动物中心提供。实验动物批号:SCXK(桂)2003-0030。
1.2 药品与试剂三七总皂苷粉针剂为广西梧州制药(集团)股份有限公司产品,批号20120305;注射用顺铂(冻干型)齐鲁制药有限公司产品,批号3040101DBDB;Bcl-2抗体和Bax抗体购于美国Cell Signaling公司;caspase-9抗体购于英国Abcam公司;内参β-actin抗体购于广州晶欣生物科技有限公司;荧光二抗羊抗兔抗体购于美国Licor公司;肌酐(serum creatinine,Cr)试剂盒、尿素氮(blood urea nitrogen,BUN)试剂盒、β-N-乙酰胺基葡萄糖苷酶(N-acetyl-β-D-Glucosaminidase,NAG)试剂盒均购于南京建成生物工程研究所,批号分别为C011-1、C013-2、A031;TUNEL试剂盒购于德国Roche公司。
1.3 仪器透射电子显微镜(日立H7650,日本);蛋白质电泳仪、蛋白质转膜仪(Bio-Rad,美国);Odyssey红外荧光扫描成像系统(LICOR,美国)。
1.4 动物分组及给药36只健康♂ SD大鼠,在代谢笼中适应性喂养1周,随机分为以下3组(n=12):(A) 空白对照组(Control组):d 1~8,大鼠每天接受相同容积的生理盐水。(B) 顺铂模型组(Cisplatin组):实验d 1,大鼠接受单剂量顺铂 (5 mg·kg-1)和相同容积的生理盐水;d 2~8,每天1次接受同体积生理盐水。(C) 顺铂+PNS 组(Cisplatin+PNS组):实验d 1,大鼠接受单剂量的顺铂 (5 mg·kg-1)和PNS(31.35 mg·kg-1);d 2~8,每天1次PNS(31.35 mg·kg-1)。B组和C组大鼠给予顺铂来诱导肾损害。顺铂和PNS的剂量是根据本课题组的前期研究结果,课题组的前期研究中,曾以价格昂贵的有一定临床效果的氨磷汀作为阳性对照药物,发现PNS中剂量组降低BUN、Cr的作用与氨磷汀组没有明显差异,表明PNS对顺铂肾损害有保护作用[5]。所有药物均采用腹腔注射给药。
1.5 样本采集和指标测定 1.5.1 血清Cr、BUN和尿NAG测定在实验d 8,利用代谢笼收集尿液测NAG含量,腹主动脉取血,离心,取血清测Cr、BUN含量;血清BUN水平采用二乙酰一肟法测定,Cr含量采用苦味酸法测定,尿液NAG测定采用对硝基苯酚比色法,均严格按照试剂盒说明书进行操作。
1.5.2 肾组织病理形态学检查采用HE染色法肾组织经10% 福尔马林固定、常规石蜡包埋切片后进行HE染色,采用光学显微镜进行病理组织学检查。
1.5.3 肾小管上皮细胞线粒体的检查大鼠肾组织用3%戊二醛固定、PBS漂洗、1%锇酸后固定1 h,再经过酒精、丙酮逐级脱水,环氧树脂618包埋,甲苯胺蓝染色后定位、切片,最后经醋酸铀、柠檬酸铅分别染色后,利用透射电镜观察肾小管上皮细胞的线粒体形态。
1.5.4 TUNEL染色法测定肾组织细胞凋亡率肾组织经10%福尔马林固定后,采用石蜡包埋切片。按照TUNEL试剂盒说明操作,切片采用荧光素标记,使用POD试剂与荧光素结合,底物用DAB显色。切片最后经过脱水、透明和封片后,用高倍光学显微镜观察肾组织凋亡细胞。根据凋亡细胞的位置,每张切片随机取10个视野,计数高倍视野下凋亡细胞数,计算每组肾组织凋亡率,细胞核呈棕色的为阳性细胞。凋亡率/%=凋亡细胞数/细胞总数×100%,取其平均值为凋亡指标。
1.5.5 SP法免疫组化检测肾组织Bax与caspase-9的表达肾组织Bax与caspase-9的表达水平采用SP法免疫组化技术检测。肾组织切片经脱蜡、水化、枸橼酸修复、山羊血清封闭后,与单克隆一抗(1 ∶ 500)4℃孵育过夜。次日,切片与相应的生物素标记二抗(1 ∶ 100)孵育,最后经DAB显色、质染。胞核蓝色,胞质棕黄色为阳性细胞。每组10张切片,每张切片随机选5个不重叠视野,在400倍光镜下观察,并用Image Pro-plus 6.0图像分析软件分别对免疫组化及原位杂交染色切片所采集图像进行测量其阳性面积、光密度和IOD值。
1.5.6 Western blot检测Bcl-2蛋白表达提取肾组织蛋白,100 mg组织加1 mL裂解液,冰上匀浆,充分裂解后离心取上清,使用BCA法检测组织蛋白浓度,使上样蛋白浓度为40~60 g·L-1,上样量为10 μL。取样品与蛋白上样缓冲液按4 ∶ 1混合,煮沸5 min,经10%SDS-PAGE凝胶电泳分离后,使用PVDF膜湿转50 min,封闭液封闭1 h。然后PVDF膜与Bcl-2一抗抗体(1 ∶ 1 000)和内参β-actin(1 ∶ 1 000),4℃孵育过夜。次日,3次PBST洗膜后,用荧光二抗(1 ∶ 15 000)孵育1 h,再经3次PBST洗膜后,采用Odyssey红外荧光扫描成像系统分析。
1.6 统计学分析 所有数据均采用 表示,采用SPSS 16.0统计软件,多组间进行方差分析(ANOVA),组间比较采用t检验。
表示,采用SPSS 16.0统计软件,多组间进行方差分析(ANOVA),组间比较采用t检验。
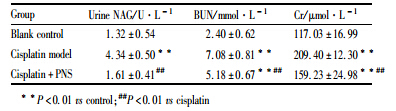
如Tab1所示,顺铂模型组大鼠的血清Cr、BUN和尿NAG水平均明显高于空白对照组(P<0.01);而顺铂+PNS组大鼠的血清Cr、BUN 和尿NAG水平均明显低于顺铂模型组(P<0.01)。
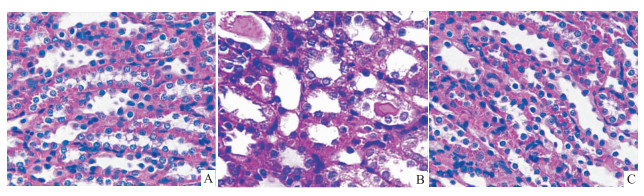
空白对照组的大鼠肾组织结构未见异常(Fig1A)。顺铂模型组的肾小管上皮细胞明显水肿、脱落,肾小管管腔狭窄,可见蛋白质或红细胞管型(Fig1B)。顺铂+PNS组的肾组织病理损害较顺铂模型组明显改善(Fig1C)。
|
| Fig 1 HE-staining of rat renal tissues in each group A:Control ;B:Cisplatin;C:Cisplatin+PNS. |
空白对照组肾小管上皮细胞的结构和形态未见异常,线粒体形态正常,结构完整(Fig2A)。顺铂模型组肾小管上皮细胞的溶酶体增多;线粒体明显肿胀,是细胞内损伤最严重的细胞器,线粒体嵴模糊、断裂或溶解,可见凋亡小体(Fig2B)。与顺铂模型组比较,顺铂+PNS组线粒体损伤明显改善,可见凋亡小体(Fig2C)。

|
| Fig 2 Renal cells of each group observed by electron microscopy A:Control;B:Cisplatin;C:Cisplatin+PNS. |
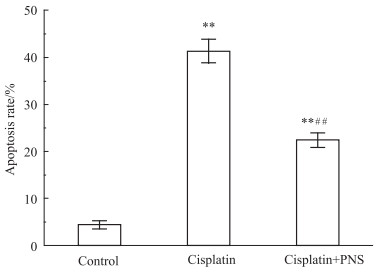
采用TUNEL染色法检测肾组织凋亡率。结果显示,空白对照组大鼠肾组织中少见凋亡细胞(Fig3A),而在顺铂模型组大鼠肾组织中凋亡细胞明显增多,主要集中在 肾小管(Fig3B)。与顺铂模型组比较,顺铂+PNS组大鼠肾组织的凋亡细胞明显减少(Fig3C)。由Fig4可知,顺铂模型组大鼠的肾组织细胞凋亡率明显高于空白对照组(P<0.01),而顺铂+PNS组大鼠的肾组织细胞凋亡率明显低于顺铂模型组(P<0.01)。
|
| Fig 3 TUNEL-staining of rat renal tissues in each group A:Control;B:Cisplatin;C:Cisplatin+PNS. |
|
| Fig 4 Apoptosis rate of rat renal tissues in each group **P<0.01 vs control; ##P<0.01 vs cisplatin |
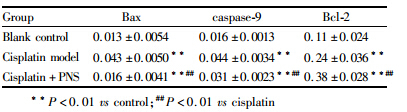
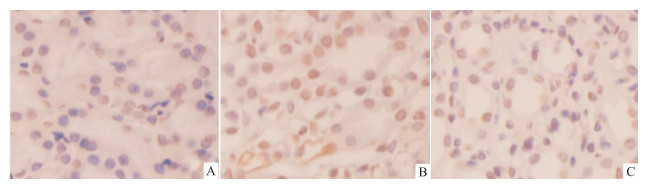
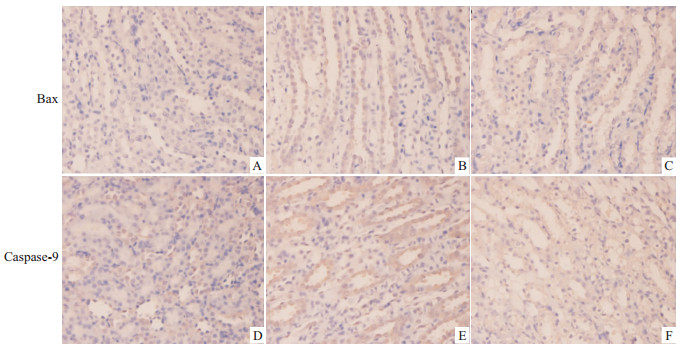
SP法免疫组化检测结果显示,Bax和caspase-9蛋白主要表达在肾小管上皮细胞(Fig5)。由Tab2可知,顺铂模型组的Bax、caspase-9表达水平均明显高于空白对照组(P<0.01),分别升高5.38、1.75倍;与顺铂模型组比较,顺铂+PNS组的Bax和caspase-9表达水平均明显降低(P<0.01),分别下降50.9%和30.2%。
|
| Fig 5 Expression of Bax and caspase-9 detected by immunohistochemistry A-C:Bax expression,D-F:caspase-9 expression. A,D:Control;B,E:Cisplatin;C,F:Cisplatin+PNS. |
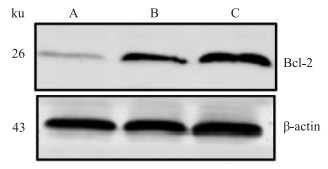
Western blot检测结果显示,顺铂模型组大鼠的肾组织Bcl-2蛋白的表达高于空白组,而在顺铂+PNS组中Bcl-2蛋白表达高于顺铂模型组(Fig6)。由Tab2可知,顺铂模型组的Bcl-2的表达水平明显高于空白对照组(P<0.01),升高3.47倍,Bcl-2/Bax比值明显降低(P<0.01);与顺铂模型组比较,顺铂+PNS组的Bcl-2蛋白表达水平明显升高(P<0.01),升高58.3%,Bcl-2/Bax比值明显升高(P<0.01)。
|
| Fig 6 Expression of Bcl-2 protein detected by Western blot A:Control;B:Cisplatin;C:Cisplatin+PNS. |
众所周知,顺铂可减少肾小球滤过率,升高血清Cr、BUN和尿NAG水平[1, 6],顺铂肾毒性的病理改变主要在肾小管,可表现为肾小管狭窄、蛋白管型,肾小管上皮细胞水肿、坏死,电镜下可见线粒体嵴断裂,出现空泡等[7],这主要与顺铂易在肾小管上皮细胞及其线粒体内积聚有密切关系[2]。本实验中,顺铂模型组大鼠在暴露于顺铂8 d后,血清Cr、BUN与尿NAG水平均明显高于空白对照组(P<0.01);肾组织HE染色可见肾小管上皮细胞水肿,胞质疏松,肾小管管腔狭窄;透射电镜下见肾小管上皮细胞线粒体明显肿胀,线粒体嵴模糊不清、断裂或溶解,说明本实验的顺铂诱导大鼠肾损伤模型制备成功。
细胞凋亡又称为细胞程序化死亡,是细胞死亡的一种形式,也是脏器损伤的一个重要指标。研究表明,诱导肾小管上皮细胞凋亡是顺铂肾损伤的重要机制之一[8]。其中,线粒体凋亡途径是顺铂诱导肾小管上皮细胞凋亡的主要途径[9]。caspase-9是线粒体凋亡途径中的关键蛋白及启动子[10]。当线粒体凋亡通路被顺铂激活时,线粒体中的细胞色素C释放到细胞质,参与形成凋亡体。caspase-9与凋亡体结合能有效激活下游caspase酶,包括caspase-3/6/7,最终导致细胞凋亡[7]。本实验中,顺铂模型组大鼠肾细胞凋亡率明显高于空白对照组,提示顺铂肾毒性与其诱导肾组织细胞凋亡有关,这与文献报道一致[10]。同时,顺铂模型组大鼠肾组织caspase-9的表达水平明显高于空白对照组,这与线粒体损伤以及肾细胞凋亡率的变化相符合,提示顺铂诱导肾组织的细胞凋亡与caspase-9依赖的线粒体通路密切相关。
顺铂诱导细胞线粒体凋亡的信号传导主要受Bcl-2家族基因的调控,其中包括促凋亡基因Bax与抗凋亡基因Bcl-2。研究发现,当细胞受到顺铂刺激时,Bax基因被激活而使Bax蛋白表达增多,并发生构象改变,通过其疏水性的C端结合到线粒体膜上,导致线粒体渗透性转换孔(mitochondrial permeability transition pore,MPTP)形成,引起细胞色素C释放,从而促进凋亡[11]。而另一种细胞凋亡相关蛋白Bcl-2的作用恰恰与Bax相反,Bcl-2可通过多种途径来稳定线粒体膜电位,抑制细胞色素C的释放,从而抑制线粒体途径的细胞凋亡[12]。凋亡基因Bax与Bcl-2的比值是调节细胞凋亡的关键,当Bcl-2高表达时,可以与Bax形成异源二聚体,抑制凋亡;而Bax高表达时,则形成Bax/Bax同源二聚体,促进细胞凋亡。本实验中,顺铂模型组肾组织Bax的表达水平明显高于空白对照组,提示细胞受顺铂刺激后应激性地增强Bax蛋白的表达,从而促进线粒体途径的细胞凋亡。
PNS是从中国传统中药三七中提取的有效部位,主要有三七皂苷Rl,以及人参皂苷Rgl、Rbl、Re、Rd等多种成分,具有抗氧化、抗增殖、抗凋亡等活性[13],并且可降低顺铂诱导的肾损伤[6]。在本实验中,PNS可明显降低大鼠血清Cr、BUN和尿NAG水平,明显改善肾小管坏死程度以及肾小管上皮细胞线粒体的损伤程度,说明PNS对顺铂诱导的大鼠肾损伤有保护作用,这与报道相符[5, 6]。本实验还发现,PNS可明显降低肾组织的细胞凋亡率,提示PNS可通过抑制肾组织的细胞凋亡而发挥保护肾脏细胞的作用。另外,本实验结果显示,PNS可使肾组织的Bax蛋白、caspase-9表达水平明显降低,而Bcl-2蛋白表达则明显增强(P<0.01),所以,Bax/Bcl-2比值明显降低。结合电镜下PNS能改善顺铂引起的线粒体损害的病理结果,提示PNS可能通过下调促凋亡蛋白Bax和上调抑凋亡蛋白Bcl-2的表达,从而抑制顺铂诱导的caspase依赖性线粒体通路的肾细胞凋亡,达到保护肾组织细胞的作用。这是首次有关PNS通过抑制肾细胞凋亡而保护顺铂肾损害的报道。
| [1] | Pabla N, Dong Z. Cisplatin nephrotoxicity:mechanisms and renoprotective strategies[J]. Kidney Int, 2008, 73(9):994-1007. |
| [2] | dos Santos N A, Carvalho Rodrigues M A, Martins N M, et al. Cisplatin-induced nephrotoxicity and targets of nephroprotection:an update[J].Arch Toxicol, 2012, 86(8):1233-50. |
| [3] | 李 花, 邓常清, 陈北阳, 等. 三七总皂苷对大鼠脑缺血再灌注后caspase表达的影响[J].中国药理学通报, 2006, 22(2):189-93. Li H, Deng C Q, Chen B Y, et al. Effects of panax notoginseng saponins on expression of caspase after focal cerebral ischemia-reperfusion in rats[J]. Chin Pharmacol Bull, 2006, 22(2):189-93. |
| [4] | Uzayisenga R, Ayeka P A, Wang Y. Anti-diabetic potential of panax notoginseng saponins (PNS):a review[J]. Phytother Res, 2014, 28(4):510-6. |
| [5] | 席加喜, 杨玉芳, 刘华钢, 等. 血栓通对顺铂肾损伤大鼠的肾功能和氧化指标的影响[J].中国实验方剂学杂志, 2012, 18(10):263-6. Xi J X, Yang Y F, Liu H G, el al. Effect of xueshuantong on renal function and oxidation indexes in cisplatin-induced nephroxicity rats[J]. Chin J Exp Tradit Med Form, 2012, 18(10):263-6. |
| [6] | Liu S J, Zhou S W. Panax notoginseng saponins attenuated cisplatin-induced nephrotoxicity[J]. Acta Pharmacol Sin, 2000, 21(3):257-60. |
| [7] | Hengartner M O. The biochemistry of apoptosis[J]. Nature, 2000, 407(6805):770-6. |
| [8] | Jeong J J, Park N, Kwon Y J, et al. Role of Annexin A5 in cisplatin-induced toxicity in renal cells:molecular mechanism of apoptosis[J]. J Biol Chem, 2014, 289(4):2469-81. |
| [9] | Wang X. The expanding role of mitochondria in apoptosis[J]. Genes Dev, 2001, 15(22):2922-33. |
| [10] | Cain K, Bratton S B, Langlais C, et al. Apaf-1 oligomerizes into biologically active approximately 700-kDa and inactive approximately 1.4-MDa apoptosome complexes[J]. J Biol Chem, 2000, 275(9):6067-70. |
| [11] | Wei Q, Dong G, Franklin J, et al. The pathological role of Bax in cisplatin nephrotoxicity[J]. Kidney Int, 2007, 72(1):53-62. |
| [12] | Breckenridge D G, Germain M, Mathai J P, et al. Regulation of apoptosis by endoplasmic reticulum pathways[J]. Oncogene, 2003, 22(53):8608-18. |
| [13] | Ng T B. Pharmacological activity of sanchi ginseng (Panax notoginseng)[J]. J Pharm Pharmacol, 2006, 58(8):1007-19. |