2.南昌大学药学院江西省基础药理学重点实验室,江西 南昌 330006
何 明(1956-),男,博士,教授,研究方向:心肌急性损伤与保护;通讯作者,E-mail:jxhm56@163.com
2.Jiangxi Provincial Key Laboratory of Basic Pharmacology,Nanchang University,Nanchang 330006,China
Fliss等[1]指出心肌缺血/再灌注(ischemia/reperfusion,I/R)损伤细胞死亡本质上可能是细胞凋亡。后者由许多调控基因直接控制,其中Bcl-2家族是已知细胞凋亡中最重要的调控因子[2, 3, 4]。因此,可望通过适度干预Bcl-2基因表达以阻断细胞凋亡过程,实现抗心肌I/R损伤。
芹菜素(apigenin,Api),化学名为4′,5,7-三羟基黄酮,分子式为C15H10O5。近年来研究发现Api能抑制心肌I/R损伤引起的细胞凋亡[5]、明显缩小心肌I/R梗死面积[6]、抗心律失常[7];尚具有减轻脑缺血性损伤[8]等心血管药理活性,但其对心肌I/R损伤保护作用的具体机制还不很清楚。
本文选用大鼠H9c2心肌样细胞,行缺氧/复氧(anoxia/reoxygenation,A/R)损伤,经Api预处理产生心肌保护作用后,用Western blot检测细胞内Bcl-2蛋白表达水平;加用Bcl-2特异性抑制剂ABT-737[9],探讨Api预处理抗心肌A/R损伤作用与其对Bcl-2蛋白表达水平上调之间的关系及其细胞线粒体功能的影响。
1 材料与方法 1.1 受试药品与试剂芹菜素(Api):中国药品生物制品检定所;ABT-737:Selleck公司;Bcl-2抗体、β-actin抗体及相应二抗:Santa Cruz;蛋白提取试剂盒:北京普利来公司;MEM培养基:Gibco BRL公司产品;胎牛血清:杭州四季青生物工程材料有限公司;增强化学发光印迹试剂、硝酸纤维素膜(Amersham,UK)、MTT、HEPES、PMSF、亮肽素、丙烯酰胺、SDS、亚甲基双丙烯酰胺、过硫酸铵、TEMED、EDTA和DTT:Sigma公司;其它试剂均为分析纯。
1.2 细胞系大鼠H9c2心肌样细胞购自中国科学院细胞库。
1.3 H9c2心肌细胞培养与A/R模型建立[10]H9c2细胞培养于含10% FBS的高糖DMEM培养基中,置于CO2培养箱(37℃)培养。细胞生长接近融合状态时,对培养的H9c2心肌细胞换用模拟缺氧缺糖溶液(NaH2PO4 0.9 mmol·L-1,NaHCO3 6.0 mmol·L-1,CaCl2 1.8 mmol·L-1,MgSO4 1.2 mmol·L-1,Sodium Lactate 40 mmol·L-1,HEPES 20 mmol·L-1,NaCl 98.5 mmol·L-1,KCl 10.0 mmol·L-1,pH 6.8),置于持续95% N2-5% CO2平衡的A/R装置(37℃)中缺氧孵育3 h后,再换用模拟再灌注溶液(NaCl 129.5 mmol·L-1,KCl 5.0 mmol·L-1,NaH2PO4 0.9 mmol·L-1,NaHCO3 20 mmol·L-1,CaCl2 1.8 mmol·L-1,MgSO4 1.2 mmol·L-1,glucose 5.5 mmol·L-1,HEPES 20 mmol·L-1,pH 7.4)于95% O2-5% CO2环境中复氧孵育2 h,建立A/R损伤模型。
1.4 实验分组①正常对照(Cont)组:取正常培养H9c2细胞,弃去原培养液,换用复氧液置于培养箱(5% CO2-95%空气,37℃)3 h,再换上复氧液孵育2 h;②A/R组:按上述方法建立A/R损伤模型;③Api预处理组:取正常培养H9c2细胞,加入终浓度分别为10、20、40、80 μmol·L-1 Api,孵育25 h,换正常培养液,再进行A/R处理;④Api+ABT-737组:取正常培养H9c2细胞,加入终浓度为40 μmol ·L-1 Api,孵育24 h后,加入终浓度为1μmol ·L-1 ABT-737孵育1 h,换正常培养液,再进行A/R处理;每组复孔处理,重复4次。
1.5 细胞存活率采用MTT比色法检测。胰酶消化后收集细胞,每组细胞以104 cells·well-1浓度接种于96孔培养板中。细胞覆盖率达70%~80%后吸出培养基。每孔加入MTT溶液(5 g·L-1溶于PBS)20 μL,37℃孵育4 h。小心地吸弃孔内培养上清液,再每孔加DMSO 150 μL振荡10 min,使蓝色结晶充分溶解。酶联免疫检测仪在490 nm波长处测定其光吸收值即OD值。细胞存活率/%=(试验组光吸收值/对照组光吸收值)×100%。
1.6 Western印迹检测实验结束后,按蛋白提取试剂盒的方法提取细胞总蛋白,BCA法蛋白定量后进行聚丙烯酰胺凝胶电泳(SDS-PAGE,12%分离胶),湿转至PVDF膜,5%脱脂奶粉封闭,Bcl-2抗体(1:500)或β-actin抗体(1:500)孵育,4℃过夜。洗膜后以辣根过氧化物酶标记的二抗(1:2 000)孵育1 h后洗膜,ECL化学发光法检测。将X线片扫描后,在Quantity One图形分析软件上进行分析。以各组β-actin条带的密度标化相应组Bcl-2的蛋白条带密度。
1.7 生化检测实验结束后各组分别取孵育液200 μL,美国Beckman生化自动分析仪测定LDH活性;消化收集心肌细胞,反复冻融破碎细胞,离心后取上清液,按试剂盒说明书测定细胞内丙二醛(MDA)含量、SOD及GSH-Px活性。
1.8 检测细胞内ROS含量[11]实验结束后,用4℃预冷的PBS洗涤细胞2~3次,加入0.25%胰蛋白酶(含0.02% EDTA)消化细胞后收集,将配制好的10 μmol DCFH-DA溶液500 μL重悬细胞,37℃孵育30 min,800×g、5 min离心,弃上清,预冷的PBS洗涤细胞2~3次,制成108 cells ·L-1的悬液,立即进行流式细胞仪检测以488 nm为激发波长,以530 nm为发射波长。以不加DCFH-DA的一管为阴性对照。
1.9 检测细胞线粒体膜电位[12]实验结束后,用4℃预冷的PBS洗涤细胞2~3次,加入0.25%胰蛋白酶(含0.02% EDTA)消化细胞后收集,将配制好的10 μmol JC-1溶液200 μL重悬细胞,37℃孵育20 min,800×g、5 min离心,弃上清,预冷的PBS洗涤细胞2~3次,制成109 cells ·L-1的悬液,立即进行流式细胞仪检测,分别以488 nm为激发光波长,527 nm和590 nm为发射光波长测绿色和红色荧光强度,以各组红/绿荧光强度的比值反映线粒体膜电位水平。
1.10 细胞凋亡检测细胞凋亡的检测采用Annexin V-PI凋亡检测试剂盒。用4℃预冷的PBS洗涤细胞2~3次,不含EDTA的胰蛋白酶消化后收集各组细胞。用预冷的PBS洗两次后,用1×Binding buffer重悬细胞,使细胞密度为约5×109 cells ·L-1。先后加入5 μL Annexin V-FITC和5 μL PI,重悬后,室温避光孵育15 min,加入500 μL Binding buffer,立即进行流式细胞仪检测(激发光488 nm,发射光578 nm),各组阳性细胞百分率用于表示细胞凋亡水平。
1.11 数据处理应用SPSS11.5统计软件行组间方差分析,各实验组数据均以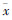 ± s表示。
± s表示。
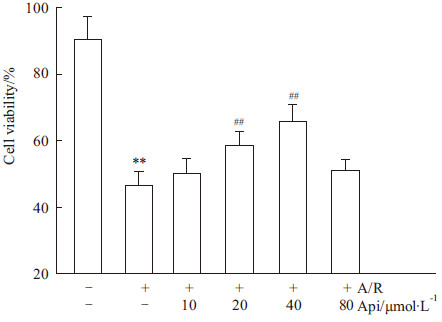
MTT结果显示(Fig1),A/R处理后,细胞存活率降低(P<0.01),表明A/R损伤模型构建成功;Api预处理细胞存活率在10~40 μmol·L-1区间呈剂量依赖性升高(P<0.01),表现出较好的细胞保护作用;而80 μmol·L-1 Api细胞存活率反而降低,提示该剂量对心肌细胞可能已产生毒性损伤。
|
Fig 1
Effects of apigenin on cell viability of H9c2 cardiomyocytes suffering A/R (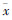 ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group
|
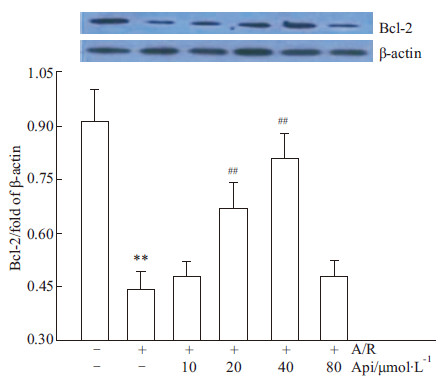
Western blot结果所示(Fig2),与Cont组和A/R相比,在10~40 μmol·L-1Api预处理区间Bcl-2蛋白表达呈剂量依赖性上调,其中40 μmol·L-1Api预处理组Bcl-2蛋白表达上调最为明显(P<0.01);而80μmol·L-1Api Bcl-2蛋白表达反而下调,与上述细胞存活率实验结果类似。根据上述结果,本文后续实验中凡涉及Api预处理之终浓度均为40 μmol·L-1。
|
Fig 2
Apigenin pretreatment upregulates Bcl-2 expression in H9c2 cardiomyocytes suffering A/R(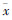 ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group
|
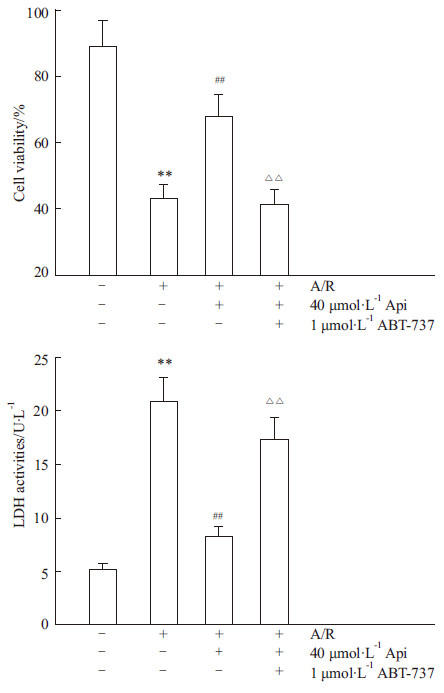
如Fig3所示:40 μmol·L-1Api预处理可使得心肌细胞存活率明显升高(P<0.01)、培养液中LDH活性明显降低(P<0.01),表现出良好的抗A/R损伤作用;而Api+ABT-737组细胞存活率降低(P<0.01)、培养液中LDH活性增加(P<0.01),表明Bcl-2特异性抑制剂ABT-737可基本取消Api预处理的保护作用。
|
Fig 3
Effects of apigenin on cell viability and LDH activity in H9c2 cells subjected to A/R (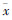 ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group;ΔΔP<0.01 vs Api ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group;ΔΔP<0.01 vs Api
|
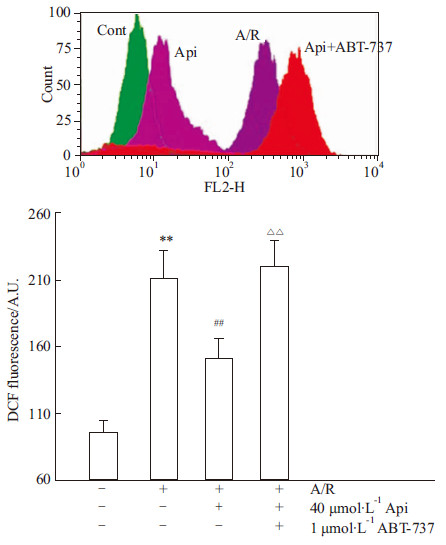
如Fig4所示:H9c2心肌细胞经A/R处理后,ROS含量峰右移,表明与Cont组比较ROS生成明显增加(P<0.01);40 μmol·L-1Api预处理后,ROS含量峰左移,表明与A/R组相比ROS生成明显降低(P<0.01),提示Api预处理后能减少A/R损伤所致的ROS爆发;而Bcl-2特异性抑制剂ABT-737可取消Api预处理的这一作用(P<0.01)。
|
Fig 4
Effects of apigenin on ROS generation in H9c2 cardiomyocytes suffering A/R (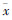 ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group;ΔΔP<0.01 vs Api group ± s,n=8)
**P<0.01 vs control group; ## P<0.01 vs A/R group;ΔΔP<0.01 vs Api group
|
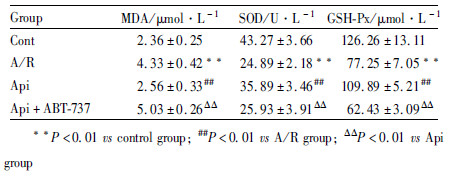
Tab1结果显示,A/R组心肌细胞MDA含量升高,SOD、GSH-Px活性明显下降(P<0.01),提示细胞经A/R损伤后发生明显的氧化应激;40 μmol·L-1Api预处理后心肌细胞MDA含量明显降低,同时SOD和GSH-Px活性升高(P<0.01);而Api+ABT-737组则MDA含量升高、SOD和GSH-Px活性降低(P<0.01),表明Api预处理可以减轻A/R引起的细胞损伤,而Bcl-2特异性抑制剂ABT-737的加入则可取消此作用。
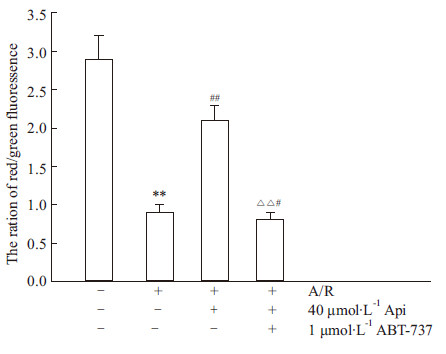
如Fig5所示,40 μmol·L-1Api预处理后,红色/绿色荧光比值明显高于A/R组(P<0.01);而Api+ABT-737组则红色/绿色荧光比值的明显降低(P<0.01),表明Api预处理可以稳定线体粒膜电位,而Bcl-2特异性抑制剂ABT-737可取消这一保护作用。
|
Fig 5
Effects of apigenin on mitochondria membrane potential of H9c2 cardiomyocytes suffering A/R (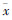 ± s,n=8)
**P<0.01 vs control group;#P<0.05,##P<0.01 vs A/R group;ΔΔP<0.01 ± s,n=8)
**P<0.01 vs control group;#P<0.05,##P<0.01 vs A/R group;ΔΔP<0.01 |
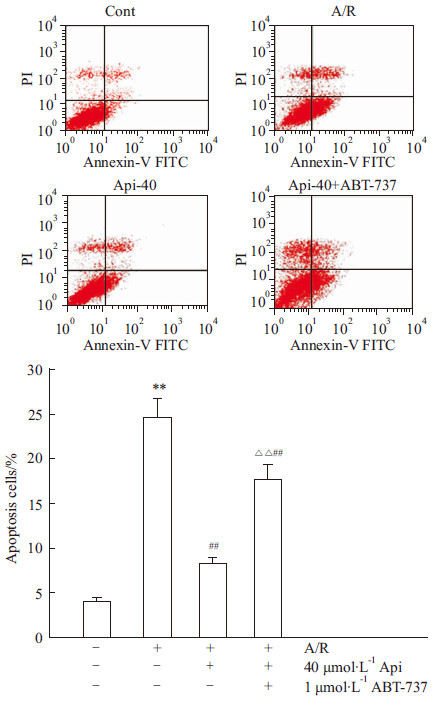
如Fig6所示,A/R组阳性细胞百分率明显高于Cont组(P<0.01);与之相比,40 μmol·L-1Api预处理后细胞凋亡水平明显降低(P<0.01),说明Api预处理可以对抗A/R引起的心肌细胞凋亡;而Api+ABT-737组凋亡水平明显高于Api处理组(P<0.01),说明Bcl-2特异性抑制剂ABT-737可明显削弱Api的抗凋亡作用。
|
Fig 6
Effects of apigenin on apoptosis of H9c2 cardiomyocytes suffering A/R (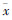 ± s,n=8)
**P<0.01 vs control group; ##P<0.01 vs A/R group; △△P<0.01 vs Api group ± s,n=8)
**P<0.01 vs control group; ##P<0.01 vs A/R group; △△P<0.01 vs Api group
|
Api属于黄酮类化合物,广泛存在于多种水果和蔬菜中,以常吃的芹菜中含量最高,被称为"植物雌激素"。其药理作用广泛,研究发现:Api具有多种药理作用,保护心、肝、脑等重要脏器免遭I/R损伤[5~8]。
我们在确认Api预处理对H9c2心肌样细胞产生保护作用后,检测发现细胞内Bcl-2表达水平明显上调,这一结果与史婷婷等[5]报道一致;但本文进一步首次证实:Bcl-2特异性抑制剂ABT-737可取消或是明显减弱Api对心肌细胞的相关保护作用,表明其作用机制依赖于上调Bcl-2表达。
Bcl-2蛋白家族分为抗凋亡蛋白和促凋亡蛋白两大类。前者包括Bcl-2、Bcl-xL和Bcl-w等,后者包括Bak、Bad、Bax等。其主要定位于线粒体膜和内质网膜等上,在细胞凋亡中起着非常关键性作用[2, 3]。抗凋亡蛋白和促凋亡蛋白二者之间会形成二聚体,其比值可决定细胞的生存或死亡。Bax的BH-3区域是其活性中心,Bcl-2通过疏水区与其BH-3活性中心结合发挥作用[4]。Bcl-2特异性抑制剂ABT-737等类似Bax BH-3区域的小分子物质,能与Bcl-2的疏水区结合,抑制其抗凋亡活性[9]。
研究资料表明:线粒体功能衰竭是心肌I/R损伤过程中的重要事件。I/R发生时,线粒体膜上的mPTP (mitochondrial permeability transition pore)开放可诱发线粒体膜电位的崩塌;随之基质肿胀,外膜破裂,细胞色素C等凋亡信号分子释放,导致心肌细胞凋亡[2, 3, 11]。其中,Bcl-2与促凋亡蛋白Bax二者相互作用,通过影响线粒体结构和功能的稳定性,发挥着细胞凋亡"主开关"的作用[4]。
本研究证实,40 μmol·L-1 Api预处理明显上调Bcl-2表达水平后,细胞存活率增加,细胞内SOD和GSH-Px活性升高,ROS生成及MDA含量降低,线粒体膜电位稳定,细胞凋亡减少;而Bcl-2抑制剂ABT-737可取消或是明显减弱Api上述保护作用。
综上所述,Api预处理可以上调A/R损伤的H9c2心肌样细胞Bcl-2表达,而Api的心肌保护作用涉及Bcl-2信号通路,至少部分依赖于其对Bcl-2表达的上调,这为我们深入探讨Api作为心血管保护药物的作用机制提供了新的思路。
| [1] | Fliss H,Gattinger D.Apoptosis in isc,hemic and reperfused rat myocardium[J].Circ Res,1996,79(5):949-56. |
| [2] |
Hajnoczky G,Csordas G,Das S,et al.Mitochondrial calcium signaling and cell death:approaches for assessing the role of mitochondrial Ca |
| [3] | Xie Z,Koyama T,Suzuki J,et al.Coronary reperfusion following ischemia:different expressionof Bcl-2 and bax proteins,and cardiomyocyte apopotosis[J].Jpn Heart J,2001,42(6):759-70. |
| [4] | Cao Y,Shibata T,Rainov N G.Liposome-mediated transfer of the Bcl-2 gene results in neuroprotection after in vivo transient focal cerebral ischemia in an animal mode[J].Gene Ther,2002,9(6):415-9. |
| [5] | 史婷婷,白建平,梁月琴,等.芹菜素对大鼠缺血/再灌注心肌细胞凋亡及相关蛋白Bcl-2、bax、caspase-3表达的影响[J].中国药理学通报,2011,27(5):666-71.Shi T T,Bai J P,Liang Y Q,et al.Efect of apigenin on the cardiomyocyte apoptosis in rats with ischemia and reperfusion and the expression of Bcl-2,Bax,Caspase-3[J].Chin Pharmacol Bull,2011,27(5):666-71. |
| [6] | 程细桃,白建平,张慧芝,于肯明.芹菜素对大鼠心肌缺血/再灌注损伤保护作用[J].中药药理与临床,2011,27(2):48-51. Cheng X T,Bai J P,Zhang H Z,Yu K M.The protective effects of apigenin in myocardium of rats with ischemia-reperfusion injury[J].Pharmacol Clin Chin Mat Med,2011,27(2):48-51. |
| [7] | 林丽文,辛勤.芹菜素药理作用的研究进展[J].中国热带医学,2012,12(8):1023-6.Lin L W,Xin Q.New progress in the pharmacology of apigenin[J].China Tropical Meb,2012,12(8):1023-6. |
| [8] | 牛文泽,李雪梅,王果,等.芹菜素对局灶性脑缺血/再灌注大鼠脑内caveolin-1表达的影响[J].中草药,2010,41(10):1658-62.Niu W Z,Li X M,Wang G,et al.Effects of apigenin on caveolin-1 expression of focal cerebral ischem ia-reperfusion in rats[J].Chin Tradit Herbal Drug,2010,41(10):1658-62. |
| [9] | Richardson A,Kaye S B.Pharmacological inhibition of the Bcl-2 family of apoptosis regulators as cancer therapy[J].Curr Mol Pharmacol,2008,1(3):244-54. |
| [10] | 刘丹,钟斌,万青,等.pFLAG-AMPKα2真核表达质粒构建及对心肌缺氧/复氧损伤的作用[J].中国临床药理学与治疗学,2012,17(12):1333-8.Liu D,Zhong B,Wang Q,et al.Construction of eukaryotic plasmid of pFLAG-AMPKα2 and the effect on cardiomyocytes subjected to anoxia-reoxygenation injury[J].Chin J Clin Pharmacol Ther,2012,17(12):1333-8. |
| [11] | Tang L,Peng Y,Xu T,et al.The effects of quercetin protect cardiomyocytes from A/R injury is related to its capability to increasing expression and activity of PKCε protein[J].Mol Cell Biochem,2013,382(1-2):145-52. |
| [12] | 汤蕾,胥甜甜,易小清,等.PKCε信号通路介导的葛根素抗心肌细胞缺氧/复氧损伤作用[J].中国药理学通报,2014,30(1):77-81.Tang L,Xu T T,Yi X Q,et al.Role of PKCε signal pathway in puerarin preconditioning against cardiomyocytes anoxia/reoxygenation injury[J].Chin Pharmacol Bull,2014,30(1):77-81. |