


2.济南大学、山东省医学科学院医学与生命科学学院,山东 济南 250200
 , GUO Yu-qi1, LI Xia1, WANG Li1, ZHOU Xian-bin1, ZHENG Xiao-dan1, 2, LAI Nan-nan1, 2, YAO Cheng-fang1
, GUO Yu-qi1, LI Xia1, WANG Li1, ZHOU Xian-bin1, ZHENG Xiao-dan1, 2, LAI Nan-nan1, 2, YAO Cheng-fang1 

2.Academy of Medical and Life Science,Jinan University,Jinan 250200,China
骨重建依赖于成骨细胞(osteoblast,OB)骨形成和破骨细胞(osteoclast,OC)骨吸收之间的动态平衡。糖皮质激素通过促进破骨细胞介导的骨吸收增强,可导致骨代谢性疾病,如骨质疏松症及炎症性骨丢失等[1],目前国内外关于骨代谢疾病的治疗也多靶向OC。桂皮醛(cinnamic aldehyde,CA)是中药肉桂挥发油的主要成分,已有研究证实[2],低浓度的CA能促进成骨细胞的成骨功能,但关于CA对激素诱导的OC骨吸收功能增强的抑制作用及其分子机制研究较少。本实验以目前公认的唯一成系的破骨细胞前体细胞--RAW264.7细胞为研究对象[3],体外观察了CA对激素诱导的OC细胞增殖分化及骨吸收功能增强的抑制作用,并探讨其分子机制,为CA有效防治骨代谢疾病提供的实验依据。
1 材料与方法 1.1 主要材料、仪器小鼠破骨细胞前体细胞-RAW264.7(中科院上海细胞库),桂皮醛标准品(CA,国家食品药品检验所),新生胎牛血清(比利时BI公司),改良型α-MEM、RPMI 1640培养基(美国Gibco公司),sRANKL、M-CSF (美国Peprotech),TRAP试剂盒(美国Sigma公司),MTT检测试剂盒(碧云天公司),TRACP5b ELISA Kit (武汉华美,CSB-E08492m),TRIzol (美国Invitrogen公司),M-MLV逆转录酶(北京Promega公司)、2×Taq MasterMix (北京康为世纪公司);酶标仪(美国Thermo公司),ND-1000分光光度计(Gene Company,美国)。
1.2 方法 1.2.1 破骨细胞诱导培养RAW264.7细胞以5×104个/孔的密度接种于放有玻璃片的6孔板中,在37℃、5% CO2、饱和湿度条件下,用含有10% FBS、100 kU·L-1青霉素、100 kU·L-1链霉素的改良型α-MEM培养基培养,每孔加入RANKL (50 μg·L-1)和M-CSF (10 μg·L-1),隔2 d换液1次,持续诱导培养5 d。
1.2.2 TRAP染色法鉴定成熟破骨细胞诱导培养5 d后取出玻璃片,按照TRAP染色试剂盒说明,用PBS缓冲液洗1次,浸入固定液(25 mL柠檬酸盐溶液,65 mL丙酮,8 mL体积分数0.37甲醛)固定30 s,用双蒸水轻轻的冲洗后,放入预热的TRAP染液中,37℃避光孵育1 h,双蒸水洗1 min,然后用苏木精复染2 min,碱性自来水冲洗,直至能看到部分显蓝色为止。倒置显微镜下观察,以TRAP染色阳性,细胞核≥3个为破骨细胞。
1.2.3 MTT法检测药物对破骨细胞增殖分化的影响RAW264.7细胞以1×108个·L-1的密度接种于96孔板上,每孔100 μL细胞悬液,分为对照组、地塞米松组和地塞米松+不同浓度的桂皮醛干预组。各处理组(对照组除外)在细胞培养过程中分别加入100 μL含地塞米松(1×10-6 mol·L-1)和不同浓度桂皮醛(11.6、23.2、46.4 μg·L-1)的培养液,共培养96 h,每组设5个平行孔,于终止前4 h每孔加入MTT (5 g·L-1)10 μL,继续培养4 h。弃上清液,加入150 μl/孔DMSO,在振荡器上振荡10 min,待结晶溶解后在波长为490 nm的酶标仪上测其光密度值。计算细胞生长抑制率,同时进行台盼蓝染色观察细胞活力并计数。生长抑制率计算公式:生长抑制率/%=(对照组OD值-实验组OD值)/对照组OD值×100%。(对照组:不加药组;实验组:加药组)
1.2.4 ELISA法检测药物对破骨细胞骨吸收功能的影响RAW264.7细胞以5×104个cell/孔接种于24孔板上,分为对照组、地塞米松组和地塞米松+不同浓度的CA干预组。分别加入地塞米松(1×10-6 mol·L-1)和不同浓度的CA (对照组除外),细胞每3天换液1次,共培养7 d。
收集细胞培养液,ELISA法检测培养液中骨吸收功能标志物--抗酒石酸酸性磷酸酶TRACP5b的含量。按说明书要求,终止反应后立即采用酶标仪450 nm读取数据,记录分析检测结果。
1.2.5 引物的设计与合成GAPDH、RANK、NFATc1引物由上海博尚生物技术有限公司合成。引物序列见Tab1。
RNA提取与分析:破骨细胞药物作用7 d后,采用TRIzol一步法提取细胞总RNA,紫外分光光度仪检测A260/A280比值,验证RNA纯度和浓度。
RT反应体系为:采用oligo dT为RT反应引物,总反应体系为60 μL,包括4 μg的总RNA,5×RT buffer 12 μL、RNA酶抑制剂120 U,10 mmol·L-1 dNTP 6 μL,M-MLV 600 U,DEPC水调总体积至60 μL,70℃ 5 min,37℃ 5 min,42℃,1 h,70℃,10 min。
PCR扩增:PCR总反应体积25 μL,包括2× Taq MasterMix 12.5 μL,cDNA 4 μL,目的基因引物(Sense+Antisense)(10 μmol·L-1)2 μL,补DEPC水至25 μL,进行PCR扩增。循环参数:94℃预变性5 min,94℃ 1 min,58℃~60℃ 1 min,72℃ 1 min,26个循环后,70℃延长10 min。
目的基因表达水平分析方法:PCR产物经体积分数0.015琼脂糖凝胶电泳,Alpha凝胶成像分析系统分析图像:以GAPDH为内参照,计算各基因与同步GAPDH灰度值的比值(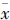 ± s)作为相对表达量,比值越大,表达水平越高,反之则越低。
± s)作为相对表达量,比值越大,表达水平越高,反之则越低。
实验数据采用SPSS 17.0统计软件做统计学处理,数据以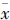 ± s表示。多组间比较采用One Way-ANOVA方差分析,差异有显著性时,采用LSD法进行两两比较。
± s表示。多组间比较采用One Way-ANOVA方差分析,差异有显著性时,采用LSD法进行两两比较。
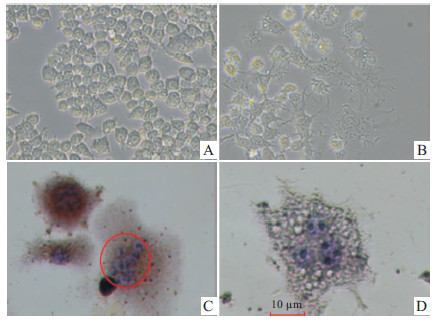
刚接种的RAW264.7细胞悬液中,细胞呈圆形,贴壁后细胞呈类圆形、椭圆形,少许为梭形,多为单核。RANKL和M-CSF联合诱导5 d后,培养瓶中细胞多为融合的多核细胞,体积较大,有皱褶(Fig1A、B)。TRAP染色后,倒置显微镜下观察,出现大量多核细胞(核≥3个),胞核蓝染,细胞大,染成淡红,胞膜边界不整,周边可见伪足伸展(Fig1C、D)。
|
| Fig 1 Morphological identification of mature osteoclasts A:Raw 264.7 cells;B:Raw 264.7 cells were treated for 5 days;C:TRAP staining (×200);D:TRAP staining (×400) |
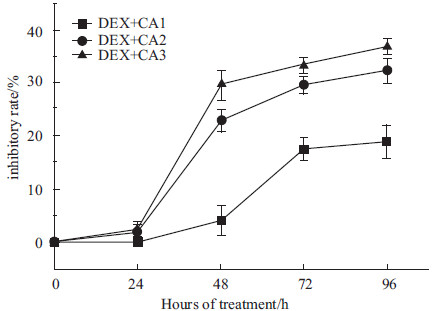
经台盼蓝染色,药物处理组及对照组细胞活力均在0.90以上,不伴有死细胞比例增高。MTT结果显示,与对照组相比,地塞米松能够明显促进细胞的增殖(结果未显示),这一结果与文献报道一致[4];而经不同浓度的桂皮醛(11.6、23.2、46.4 μg·L-1)干预24 h后,与地塞米松组相比,破骨细胞的增殖抑制无明显变化;48 h后,抑制率明显增强,分别为:0.039±0.028、0.228±0.023、0.295±0.025;72 h后,抑制率分别为0.175±0.021、0.296±0.014、0.332±0.013;96 h后,抑制率达到0.182±0.033、0.331±0.021、0.381±0.017,差异有显著性(P<0.05)。可见11.6~46.4 μg·L-1的CA能够不同程度的抑制破骨细胞的增殖活性,其效应呈明显的时间、剂量依赖性(Fig2)。
|
| Fig 2 Inhibitory effect of CA on osteoclasts proliferation treated with DEX CA1:11.6 μg·L-1;CA2:23.2 μg·L-1;CA3:46.4 μg·L-1 |
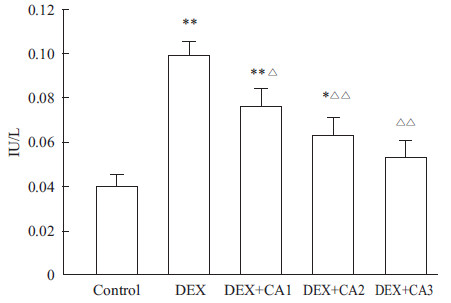
ELISA结果显示,与对照组相比,地塞米松能够明显增加上清中TRACP5b的活性表达(P<0.05);而不同浓度CA干预后,与地塞米松组相比,TRACP5b的表达受到明显的抑制(P<0.05),其抑制效应具有明显的剂量依赖性(Fig3)。
|
|
Fig 3
Reverse effects of CA on DEX-induced enhanced expression of TRAP5b
CA1:11.6 μg·L-1;CA2:23.2 μg·L-1;CA3:46.4 μg·L-1. *P<0.05,**P<0.01 vs control group;ΔP<0.05,ΔΔP<0.01 vs DEX group |
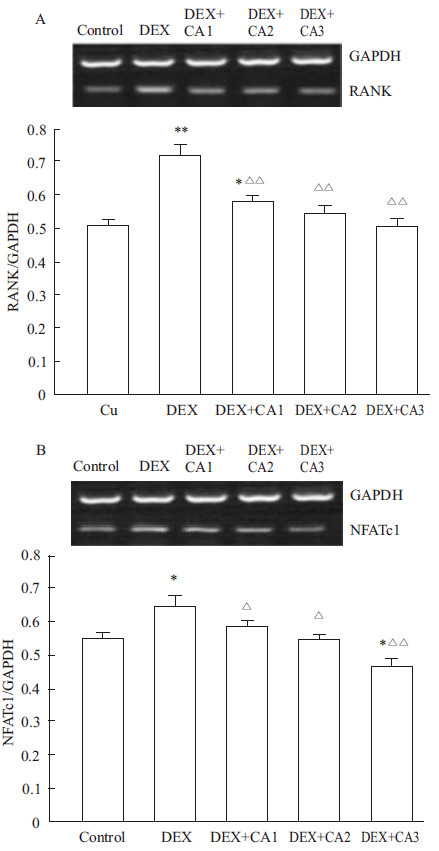
RT-PCR结果表明,经地塞米松诱导后,RANK、NFATc1 mRNA的表达均明显升高(P<0.05),而CA干预后,与地塞米松组相比,RANK、NFATc1 mRNA的表达均出现不同程度降低,且随药物浓度的升高抑制作用越明显(Fig4)。
|
| Fig 4 Down-regulatory effect of CA on DEX-induced overexpressions of RANK,NFATc1 mRNA A:The expression of RANK mRNA;B:The expression of NFATc1mRNA,CA1:11.6 μg·L-1;CA2:23.2 μg·L-1;CA3:46.4 μg·L-1,*P<0.05,**P<0.01 vs control group;ΔP<0.05,ΔΔP<0.01 vs DEX group |
近年来,激素类药物在重大感染性疾病和器官移植中的应用所引发的医源性骨代谢病呈整体上升之势,而目前国内外关于骨代谢疾病的治疗多靶向OC,本研究中用RANKL和M-CSF来诱导小鼠破骨样前体细胞--RAW264.7细胞[4],使其分化成为成熟的破骨细胞作为研究对象。MTT结果证实,地塞米松能够促进OC细胞增殖分化,并具有明显的时间依赖性,这一结果亦与文献报道一致[5];TRAP5b是破骨细胞特异性来源的骨吸收标志物,本研究用ELISA方法检测其活性,结果显示,与正常对照组相比,地塞米松诱导后TRAP5b的活性明显增强。而随着CA浓度的增加,OC的增殖和TRAP5b的活性受到抑制,并具有明显的剂量依赖性。
OC分化因子RANKL与其配体(RANK)及诱骗配体-骨保护素(osteoprotegerin,OPG)是近年来骨代谢研究领域中影响OC分化和功能、调节骨重建的核心调节因素,RANKL/RANK/OPG信号通路在生理和病理性骨重建中起决定性作用[6]。RANKL可与OC前体细胞和OC膜上的RANK结合,引起级联反应,从而促进OC分化、成熟,增强骨吸收功能,而RANK减少可以使RANKL结合不足,细胞信息通路不能顺利传导给细胞内,从而使OC分化、成熟受限,骨吸收功能下降[7]。本研究发现,地塞米松诱导后,RANK mRNA表达明显增强,而11.6~46.4 μg·L-1的桂皮醛能够使RANK mRNA表达下降,故我们推测RANK mRNA的表达下降导致RANK蛋白翻译的减少,封闭RANKL/RANK的信息传递,使OC前体细胞不能分化融合形成OC,抑制OC生成和骨吸收活性。同时,本研究还观察了NFATc1 mRNA的表达变化。NFATc1(nuclear factor of activated T cells cytoplasmic 1)是破骨细胞成熟过程中最主要的调节子,体内外研究已证实NFATc1基因在破骨细胞生成中的必要及充分的作用[8]。NFATc1在调节破骨细胞特异基因表达的方面具有重要作用[9],并且是RANKL/RANK通路下游信号分子[10]。近年来,NFATc1已作为抗破骨细胞疗法的一个首要靶向目标[11, 12]。RT-PCR结果表明,伴随着CA浓度的升高,NFATc1的mRNA表达明显降低,进一步证实了CA能够抑制破骨细胞的分化成熟,其机制可能是通过降低RANKL/RANK信号通路中RANK、NFATc1 mRNA的表达。
本研究结果揭示:在体外培养的情况下,CA通过降低RANK、NFATc1mRNA的高表达,从而有效降低激素诱导的破骨细胞增殖分化以及骨吸收功能的增强。目前在防治骨相关疾病当中,中药所占份额极低,这主要是由于目前中药对防治骨相关疾病的细胞选择性、疗效稳定性和作用针对性的研究基础较弱,科研依据不够充分,我们的实验结果可能是CA临床有效防治医源性骨代谢疾病的药理机制和物质基础,为CA用于骨代谢病的早期防治提供了科学的实验依据。但毕竟骨组织是多种细胞生活在一起的整体,药物对体内骨环境的影响是不能仅仅通过体外培养的实验结果来推断的,所以建立成骨细胞和破骨细胞共存的细胞系以及小鼠体内实验是我们下一步的重点。
| [1] | 陈艳,黄连芳,刘衍志,等.不同剂量地塞米松对大鼠松质骨代谢的影响[J].中国药理学通报,2012,28(9):1311-4. Chen Y,Huang L F,Liu Y Z,et al.Rats cancellous bone metabolism in different doses of dexamethasone[J].Chin Pharmacol Bull,2012,28(9):1311-4. |
| [2] | 邵培,曹桂芬,赵美林,等.中药桂皮醛对成骨细胞增殖及成骨功能的影响[J].中国口腔种植学杂志,2009,14(4):111-4. Shao P,Cao G F,Zhao M L,et al.Effects of cinnamaldehyde on osteoblast proliferation and differentiation[J].Chin J Oral Implantol,2009,14(4):111-4. |
| [3] | Yamamoto A,Miyazaki T,Kadono Y,et al.Possible involvement of IkappaB kinase 2 and MKK7 in osteoclastogenesis induced by receptor activator of nuclear factor kappa B ligand[J].J Bone Miner Res,2002,17(4):612-21. |
| [4] | Takahashi N,Udagawa N,Kobayashi Y,Suda T.Generation of osteoclasts in vitro,and assay of osteoclast activity[J].Methods Mol Med,2007,135:285-301. |
| [5] | Kaji H,Sugimoto T,Kanatani M,et al.Dexamethasone stimulates osteoclast-like cell formation by directly acting on hemopoietic blast cells and enhances osteoclast-like cell formation stimulated by parathyroid hormone and prostaglandin E2[J].J Bone Miner Res,1997,12:734-41. |
| [6] | Sundaram K,Nishimura R,Senn J,et al.RANK ligand signaling modulates the matrix metalloproteinase-9 gene expression during osteoclast differentiation[J].Exp Cell Res,2007,313(1):168-78. |
| [7] | Kong Y Y,Yoshida H,Sarosi I.OPGL is a key regulator of osteoclastogenesis,lymphocyte development and lymphnode organogenesis[J].Nature,1999,397:315-23. |
| [8] | Asagiri M,Sato K,Usami T,et al.Autoamplification of NFATc1 expression determines its essential role in bone homeostasis[J].J Exp Med,2005,202(9):1261-9. |
| [9] | Kim Y,Sato K,Asagiri M,et al.Contribution of nuclear factor of activated T cells c1 to the transcriptional control of immunoreceptor osteoclast-associated receptor but not triggering receptor expressed by myeloid cells-2 during osteoclastogenesis[J].J Biol Chem,2005,280:32905-13. |
| [10] | Han K Y,Yang D,Chang E J,et al.Inhibition of osteoclast differentiation and bone resorption by sauchinone[J].Biochem Pharmacol,2007,74(6):911-23. |
| [11] | Takayanagi H,Kim S,Koga T,et al.Induction and activation of the transcription factor NFATc1(NFAT2) integrate RANKL signaling in terminal differentiation of osteoclasts[J].Dev Cell,2002,3(6):889-901. |
| [12] | Takayanagi H.Osteoimmunology:shared mechanisms and crosstalk between the immune and bone systems[J].Nat Rev Immunol,2007,7(4):292-304. |
