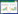文章信息
- 苏晓港, 马晶茹
- SU Xiaogang, MA Jingru
- 恶性肿瘤靶向治疗后发生急性ST段抬高型心肌梗死1例报道
- ST-segment elevation myocardial infarction after targeted therapy for malignancy: a case report
- 中国医科大学学报, 2026, 55(4): 377-380
- Journal of China Medical University, 2026, 55(4): 377-380
-
文章历史
- 收稿日期:2026-01-16
- 网络出版时间:2026-04-15 13:41:56
近年来,恶性肿瘤患者中急性ST段抬高型心肌梗死(acute ST-elevation myocardial infarction,STEMI)的发生率有所上升[1]。恶性肿瘤患者因病理状态、肿瘤相关慢性炎症及促凝状态,心血管事件(尤其是冠状动脉病变)风险显著升高。在接受包括血管内皮生长因子受体酪氨酸激酶抑制剂(vascular endothelial growth factor receptor tyrosine kinase inhibitor,VEGF-TKI)在内的靶向药物治疗患者中,动脉血栓事件与心血管不良事件发生率均有所增加,提示在关注VEGF-TKI抗肿瘤疗效的同时,需额外警惕其可能带来的心血管毒性[2]。此外,一项在新诊断且未接受抗癌治疗的癌症患者的研究[3]中发现,炎症水平高者冠状动脉病变严重程度更大,炎症是恶性肿瘤与冠状动脉粥样硬化性心脏病之间的关键中介因素。在此类患者中,如何平衡抗肿瘤治疗与经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术后抗栓、降低出血风险,一直是临床关注的热点。本文报道了1例肾癌肺转移患者在靶向治疗过程中发生STEMI后行PCI的临床诊治过程,并结合文献探讨其病变特征、抗栓方案与应对策略。
1 临床资料 1.1 病史及临床表现患者,女,65岁。2015年确诊右肾透明细胞癌并接受手术治疗,2020年发现肺部转移后,开始接受多靶点VEGF-TKI靶向药物治疗。2025年6月15日于劳累后出现心前区疼痛,伴胸闷、气短、大汗,服用速效救心丸6粒,症状持续约10 min后缓解,未就诊,次日患者胸痛症状加重伴大汗,持续不缓解,呼叫120送至我院,绿色通道送至导管室行介入治疗。既往无高血压、糖尿病等病史,无吸烟、饮酒史。入院查体:血压172/110 mmHg,心率103次/min,心律齐,面色苍白,双肺呼吸音清,腹部无压痛,双下肢无浮肿。
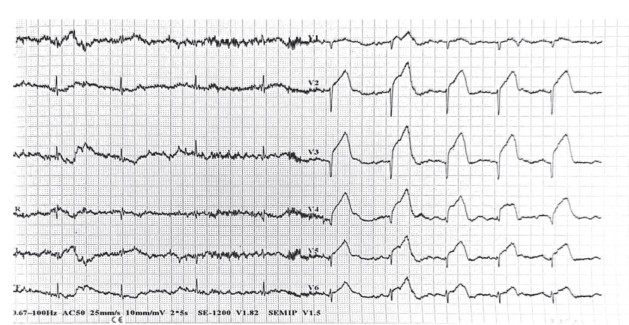
1.2 辅助检查心电图(图 1)V1~V6导联ST段弓背抬高0.1~0.6 mV,提示广泛前壁心肌梗死。白细胞计数7.48×109/L,血红蛋白80 g/L,血小板计数222×109/L,白蛋白30 g/L,丙氨酸氨基转移酶45.4 U/L,天门冬氨酸氨基转移酶189.4 U/L,肌酐83.3 μmol/L,血钾4.08 mmol/L,N末端脑钠肽前体(N-terminal pro-B-type natriuretic peptide,NT-proBNP)202 pg/mL,肌钙蛋白T < 0.01 ng/mL,国际标准化比值(international normalized ratio,INR)0.95,低密度脂蛋白胆固醇2.85 mmol/L。超声心动图(图 2)显示,左心房内径27.0 mm,左心室舒张末内径43.0 mm,右心室内径20.0 mm,左心室壁节段性运动异常,左心室舒张功能正常,静息状态下左心室整体收缩功能减低,左室射血分数(left ventricular ejection fractions,LVEF)为51%。
|
| 图 1 心电图检查结果 |
|
| 图 2 超声心动图检查结果 |
1.3 治疗经过
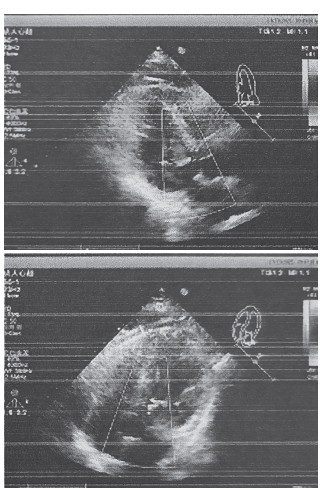
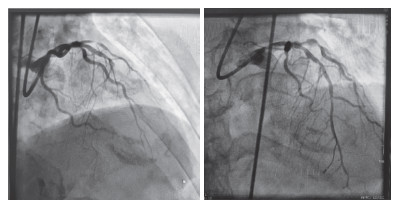
患者入院后予以阿司匹林300 mg、替格瑞洛180 mg嚼服。向患者及家属交代病情,绿色通道送至导管室,立即予以心电、血压监护,建立输液通路。予以1%利多卡因局麻,穿刺右股动脉入路,以直导丝导入6F动脉鞘,鞘内注入肝素6 500 U及硝酸甘油200 μg,行多体位冠状动脉数字减影血管造影(digital subtraction angiography,DSA),结果显示,冠状动脉血管内膜光滑,左主干未见明显狭窄,前降支近段40%狭窄,中段100%闭塞,回旋支中段95%狭窄,第1钝缘支95%狭窄,第2钝缘支80%狭窄,右冠状动脉中段30%狭窄,后降支60%狭窄,右冠优势型冠状动脉,立即行PCI,EBU3.5/6F指引导管至左冠状动脉口,导丝顺利开通前降支闭塞病变,并于前降支植入1枚药物涂层支架,造影见支架扩张满意,无血栓形成及内膜撕裂,血流TIMI3级,退出支架球囊及导丝,拔出指引导管,见图 3。术中血流开通时出现一过性血压下降,对症给予间羟胺1 mg静脉推注后血压恢复。患者术中躁动,对症给予安定5 mg静脉推注镇静。术中无恶性心律失常发生,离开导管室时,血压141/70 mmHg,心率72次/min。胸痛明显减轻,复查心电图提示室性逸搏心律,心率71次/min,V1~V6导联可见病理性Q波,ST段抬高0.1~0.3 mV,予以胺碘酮0.3 g+5%葡萄糖注射液50 mL,以6 mL/h静脉泵入调整节律;硝酸甘油5 mg+0.9%氯化钠注射液50 mL,以4~6 mL/h静脉泵入扩张冠状动脉;法莫替丁20 mg+0.9%氯化钠注射液100 mL静脉滴注预防消化道出血;磷酸肌酸钠1 g+0.9%氯化钠注射液100 mL静脉滴注营养心肌;阿司匹林(100 mg,1次/d)及替格瑞洛(90 mg,2次/d)口服双联抗血小板;阿托伐他汀(20 mg,1次/d)口服并联合英克司兰(284 mg,1次)皮下注射降脂及稳定斑块。次日复查肌钙蛋白T 4.94 ng/mL,NT-proBNP1 230.9 pg/mL,肌酐77.2 μmol/L。6月22日(PCI术后6 d)患者偶有心前区不适,伴气短,复查NT-proBNP 3 972.2 pg/mL,予以呋塞米(20 mg,1次/d)静脉注射及螺内酯(40 mg,1次/d)口服,减轻心脏负荷,并加用沙库巴曲缬沙坦(50 mg,2次/d)口服改善心室重构,6月23日复查肌钙蛋白T 0.589 ng/mL,较前明显减低,出院。院外继续口服用药。出院后10 d(2025年7月4日)再次心绞痛加重,入院行介入治疗,钝缘支病变较上次加重,紧急植入1枚支架,回旋支及中间支行球囊扩张术,见图 4。在原治疗药物的基础上,加用磺达甘癸钠注射液2.5 mg皮下注射抗凝3 d。术后随访6个月,患者一般情况良好,规律服药。随访期间未发生缺血及出血事件,亦未发生不良心血管事件,预后良好。
|
| 图 3 术前(左)和术后(右)左冠状动脉影像 |
|
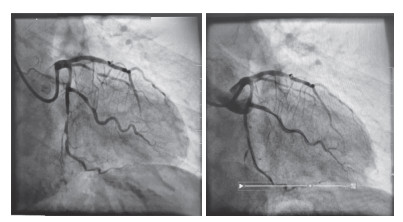
| 图 4 术前(左)和术后(右)回旋支影像 |
本研究获得我院医学伦理委员会批准(2025-沈医二院伦理-061)。
2 讨论恶性肿瘤患者发生STEMI的机制与普通人群显著不同。肿瘤可诱导持续高凝状态,由于肿瘤细胞释放组织因子,后者携带微颗粒,激活外源性凝血途径,加速冠状动脉血栓形成;部分肿瘤可直接侵犯或压迫冠状动脉,甚至由转移灶导致机械性闭塞[4]。此外,肿瘤治疗本身亦增加心肌梗死风险。VEGF-TKI可抑制VEGF-一氧化氮(nitric oxide,NO)信号,减少NO与前列环素,导致血管舒张受损、内皮屏障破坏,从而诱发冠状动脉痉挛、微循环障碍及促凝状态;同时促进黏附分子上调与动脉粥样硬化加速,使斑块更易破裂[5-7]。肿瘤患者常伴慢性炎症、贫血及低蛋白血症,进一步降低心肌供氧能力。炎性细胞因子可增强内皮激活及凝血反应,贫血及由此引发的低氧状态影响尤为关键:贫血会直接减少血液携氧能力,导致心肌供氧不足;低氧状态则会进一步加重心肌细胞代谢紊乱,降低心肌对缺血的耐受阈值[8]。在此基础上,即便患者冠状动脉内仅存在轻度斑块或微小血栓(此前因病情较轻未引发明显症状),贫血与低氧也会通过这2个核心机制诱发急性闭塞。上述多因素共同作用使肿瘤患者更易发生STEMI,且起病急骤,临床表现隐匿,病程不稳定。
对肿瘤合并STEMI患者的抗栓策略是平衡血栓与出血风险,需在标准急性心肌梗死抗栓基础上,结合肿瘤类型、分期、治疗方案及患者个体情况动态调整[9]。本例患者入院冠状动脉DSA显示多支重度病变,基于极高缺血风险(GRACE 159分)、斑块负荷及肿瘤背景导致的促凝状态,急性期采用阿司匹林联合替格瑞洛强化双联抗血小板治疗,符合高危STEMI患者的循证策略。然而,患者于首次出院后10 d再次发生急性胸痛,提示冠状动脉斑块高度不稳定及短期复发性缺血趋势,这在肿瘤合并急性冠状动脉综合征患者中较常见,可能与肿瘤相关炎症激活、凝血因子上调及VEGF-TKI引起的内皮功能障碍持续存在密切相关。第2次PCI后,对患者加强了抗栓治疗方案,在原有药物的基础上,短期联合磺达肝癸钠抗凝,结合症状、心肌标志物、血小板及凝血功能的动态监测,实现了抗栓强度与安全性的实时平衡。随着患者心功能改善[7月23日(第2次PCI术后19 d)]复查超声心动图LVEF 57%,NT-proBNP 806.6 pg/mL],症状逐渐稳定,出院1个月后,抗栓策略逐步向兼顾出血风险的方案过渡。将双联抗血小板治疗方案由“阿司匹林联合替格瑞洛”调整为“阿司匹林联合氯吡格雷”,主要基于两方面考量:从病情管理角度,患者PCI术后病情已趋稳定,需通过抗栓方案“降阶”以平衡抗栓疗效与长期出血风险;从药物相互作用角度,因后续可能还要使用VEGF-TKI,而替格瑞洛与VEGF-TKI的核心代谢途径均依赖CYP3A4酶系,二者联用易竞争同一代谢酶导致血药浓度异常,增加毒性反应或出血风险;换用氯吡格雷后,其核心代谢酶为CYP2C19(辅助酶为CYP3A4),与VEGF-TKI的代谢酶依赖重叠度显著降低,可减少药物间相互作用风险[10],并计划于PCI术后6个月改为单药维持,以降低大出血事件发生。目前对该患者已随访6个月,未出现缺血或出血事件,支持动态调整抗栓强度在复杂患者中的可行性。肿瘤患者抗栓治疗期间的严密监测尤为关键,除症状和心肌标志物外,应重点观察血小板、凝血功能及消化道出血风险,并结合肿瘤治疗节奏留出必要的停药窗口,以减少药物相互作用。
结合本例患者的治疗经验,对具有心血管危险因素的肿瘤患者管理,需贯穿“救治—随访—预防”全程。靶向治疗前应进行基线评估,包括冠状动脉计算机断层扫描血管造影、超声心动图及心肌酶谱,以评估潜在冠状动脉病变与心功能储备。高危患者(高血压、糖尿病或既往冠状动脉粥样硬化性心脏病)需提前制定个体化心血管预防策略,如强化血压和血脂管理,或必要时预防性抗血小板治疗。在治疗过程中,通过心血管内科与肿瘤科多学科诊疗管理模式,每3~6个月动态监测心电图、心肌标志物及超声心动图,以便及早发现亚临床心肌损伤,避免进展为急性心肌梗死[11]。急性期后长期随访应关注肿瘤复发、转移及冠状动脉病变进展,定期评估冠状动脉造影、心脏负荷试验或冠状动脉CT血流储备分数,以动态优化抗栓策略、靶向治疗及心血管保护,实现肿瘤控制与心血管安全的双重目标。
综上所述,接受VEGF-TKI等靶向治疗的肿瘤患者若出现胸痛,应高度警惕急性冠状动脉综合征,需即刻启动急症评估与多学科协作,同时将“救治—随访—预防”全程心血管风险管理贯穿始终,通过基线筛查、动态监测与个体化方案调整,实现肿瘤治疗与心血管安全的双重保障。作为单例观察,本研究无法验证策略普适性,亦缺乏长期随访数据,未来仍需多中心、大样本研究,以明确肿瘤患者STEMI的最佳抗栓策略与随访管理路径。
| [1] |
BIMA P, LOPEZ-AYALA P, KOECHLIN L, et al. Chest pain in cancer patients: prevalence of myocardial infarction and performance of high-sensitivity cardiac troponins[J]. JACC CardioOncol, 2023, 5(5): 591-609. DOI:10.1016/j.jaccao.2023.08.001 |
| [2] |
CHEN YC, CHEN JH, HSIEH FI. Major adverse cardiovascular events of vascular endothelial growth factor tyrosine kinase inhibitors among patients with different malignancy: a systemic review and network meta-analysis[J]. J Chin Med Assoc, 2024, 87(1): 48-57. DOI:10.1097/JCMA.0000000000001026 |
| [3] |
SUN MZ, ZHU SN, WANG YH, et al. Effect of inflammation on association between cancer and coronary artery disease[J]. BMC Cardiovasc Disord, 2024, 24(1): 72. DOI:10.1186/s12872-023-03613-0 |
| [4] |
CHOU SC, CHANG SL, YU CY, et al. Tissue factor, factor Ⅷ and Ⅸ in microvesicle-induced thrombosis and tumor growth of pancreatic cancer[J]. Thromb J, 2025, 23(1): 32. DOI:10.1186/s12959-025-00715-x |
| [5] |
BUTEL-SIMOES LE, ALBAYATI A, YU J, et al. Tyrosine kinase inhibitors-balancing the haemostatic scales: a review of associated thrombosis and bleeding[J]. J Thromb Thrombolysis, 2025, 59(2): 393-410. DOI:10.1007/s11239-025-03151-w |
| [6] |
LI J, ZHANG LS, GE T, et al. Understanding sorafenib-induced cardiovascular toxicity: mechanisms and treatment implications[J]. Drug Des Devel Ther, 2024, 18: 829-843. DOI:10.2147/DDDT.S443107 |
| [7] |
张卫芳, 谢珊珊, 苏海. 血管内皮生长因子抑制剂相关高血压的治疗和管理[J]. 中华高血压杂志, 2023, 31(1): 27-33. DOI:10.16439/j.issn.1673-7245.2023.01.009 |
| [8] |
NIE JL, ZHOU L, TIAN WW, et al. Deep insight into cytokine storm: from pathogenesis to treatment[J]. Signal Transduct Target Ther, 2025, 10(1): 112. DOI:10.1038/s41392-025-02178-y |
| [9] |
VAN LINTHOUT S. Shared mechanisms in cancer and cardiovascular disease: S100A8/9 and the NLRP3 inflammasome: JACC: cardiooncology state-of-the-art review[J]. JACC CardioOncol, 2025, 7(5): 501-513. DOI:10.1016/j.jaccao.2024.10.010 |
| [10] |
VAVROVÁ K, INDRA R, POMPACH P, et al. The impact of individual human cytochrome P450 enzymes on oxidative metabolism of anticancer drug lenvatinib[J]. Biomed Pharmacother, 2022, 145: 112391. DOI:10.1016/j.biopha.2021.112391 |
| [11] |
LYON AR, LOPEZ-FERNANDEZ T, COUCH LS, et al. 2022 ESC guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ESTRO) and the International Cardio-Oncology Society (IC-OS)[J]. Eur Heart J Cardiovasc Ima-ging, 2022, 23(10): e333-e465. DOI:10.1093/ehjci/jeac106 |
 2026, Vol. 55
2026, Vol. 55