文章信息
- 赵樊, 郭庭维, 戴宗伯, 戴显通, 李越, 周子燚, 柏涵, 张佳林
- ZHAO Fan, GUO Tingwei, DAI Zongbo, DAI Xiantong, LI Yue, ZHOU Ziyi, BAI Han, ZHANG Jialin
- 长期高脂饮食对小鼠胰岛形态和功能的影响
- Effects of long-term high-fat diet on morphology and function of pancreatic islets in mice
- 中国医科大学学报, 2026, 55(4): 366-371
- Journal of China Medical University, 2026, 55(4): 366-371
-
文章历史
- 收稿日期:2024-08-05
- 网络出版时间:2026-04-15 13:28:44
糖尿病是导致全球死亡和残疾的重要病因之一,其中约96%为2型糖尿病患者[1-2]。糖尿病前期是发展成为2型糖尿病前的高危状态[3],此时胰岛功能进行性减退,每年约有5%~10%的糖尿病前期患者会发展为糖尿病。如果在此阶段采取有效的干预措施,可以阻止和减缓病情的进展。
研究[4]表明,糖尿病前期与高热量饮食密切相关,高热量饮食可诱导产生大量炎性细胞因子,介导氧化应激形成慢性炎症以及代谢压力,对机体各系统造成进行性损害。同时,高热量饮食可使动脉微血管内皮细胞损伤,显著减少毛细血管内皮囊泡数量,损害跨内皮细胞的胰岛素转运,加重胰岛素抵抗[5]。高热量饮食还会导致胰岛巨噬细胞浸润,产生促炎性细胞因子,进一步诱发糖耐量异常,但关于其具体机制的研究仍较少。Toll样受体(Toll-like receptor,TLR)为先天免疫系统的一部分,其中TLR2和TLR4位于巨噬细胞表面,被激活后可通过下游级联信号通路增加促炎性细胞因子生成。糖尿病肾病患者外周血中TLR2和TLR4 mRNA表达水平显著升高,表明其可能参与糖尿病发病过程[6]。本研究采用高脂饲料喂养C57BL/6J雄性小鼠12个月,模拟高热量饮食状态,构建糖耐量受损小鼠模型,观察小鼠体重、随机血糖、糖耐量的变化,通过血管内皮生长因子A(vascular endothelial growth factor A,VEGFA)和CD31染色观察胰岛血管密度变化,并观察胰岛组织中CD11c+细胞浸润数量和TLR2、TLR4表达水平的变化,以探讨长期高脂饮食对小鼠胰岛形态和功能的影响。
1 材料与方法 1.1 实验动物和分组20只6~8周龄、体重16~20 g的SPF级雄性C57BL/6J小鼠,购自辽宁长生生物技术股份有限公司,于SPF级环境中饲养。将小鼠随机分为高脂饮食组(HFD组)和正常饮食组(ND组),每组10只。HFD组小鼠喂养高脂饲料(北京华阜康生物科技股份有限公司),ND组小鼠喂养标准饲料。实验周期12个月,每个月测量小鼠体重,尾静脉血采血,检测随机血糖,每4个月进行腹腔葡萄糖耐量试验(intraperitoneal glucose tolerance test,IPGTT)。喂养12个月后,乙醚麻醉小鼠,眼球取血测定胰岛素浓度,取胰腺组织置于10%中性甲醛固定液中固定,用于后续组织学分析,之后颈椎脱臼处死小鼠。本研究获得中国医科大学附属第一医院医学科学伦理委员会审核批准(科伦审[2023]397号)。
1.2 方法 1.2.1 IPGTT在4、8、12个月时分别进行IPGTT。小鼠禁食12 h后,腹腔注射50%葡萄糖溶液(2 g/kg)。在注射前和注射后15、30、60、90、120 min尾静脉采血,检测小鼠血糖。应用GraphPad Prism软件绘制IPGTT曲线,计算曲线下面积。
1.2.2 组织病理学观察将固定好的胰腺组织进行乙醇梯度脱水,二甲苯透明,石蜡包埋,将蜡块切成5 μm的切片进HE染色。测量每张切片同一视野下最大胰岛的截面面积和细胞计数。应用ImageJ软件对小鼠胰岛面积和胰岛细胞数量进行分析。
1.2.3 免疫组织化学染色取小鼠胰岛组织,制备石蜡切片,选取兔抗鼠CD31抗体(美国Proteintech公司)和兔抗鼠Insulin抗体(美国Proteintech公司)进行免疫组织化学染色,同一视野下选取最大胰岛拍照,计算阳性面积。用光密度(optical density,OD)值衡量胰岛细胞胰岛素强度。计算胰岛血管密度,胰岛血管密度=CD31+血管内皮细胞标示的血管数量/胰岛面积。
1.2.4 免疫荧光染色取小鼠胰岛组织,制备石蜡切片,常规脱蜡水化,抗原修复,样品固定通透化。封闭后,一抗孵育过夜,室温下孵育二抗。洗涤后,荧光显微镜下观察并采集图像,同一视野下选取最大胰岛拍照。
1.2.5 酶联免疫吸附试验将全血标本在室温下放置2 h后,4 ℃、3 000 r/min离心15 min,取上清液进行检测。使用胰岛素抗体孵育,洗涤后加入显色底物,终止反应,空白对照孔调零后,采用酶标仪检测450 nm处各孔OD值。根据标准品的浓度和OD值做标准曲线,根据标准曲线方程计算样本浓度。
1.3 统计学分析应用GraphPad Prism 8软件进行统计分析和作图。计量资料用x±s表示,2组间比较采用Student’s t检验。采用Pearson相关分析对胰岛面积、单位面积胰岛细胞数量、胰岛血管密度与IPGTT曲线下面积的相关性进行分析。P < 0.05为差异有统计学意义。
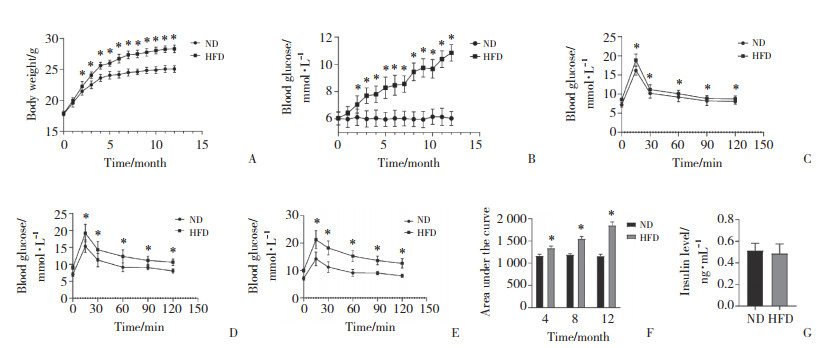
2 结果 2.1 高脂饮食对小鼠体重、随机血糖、糖耐量曲线和外周血清胰岛素水平的影响HFD组小鼠体重在整个实验周期内均呈增长趋势,前4个月增长尤为迅速;ND组小鼠体重在前2个月增张较快,之后增长速度减缓。2~12个月,HFD组小鼠体重均显著大于ND组(P < 0.05);12个月时,2组小鼠体重差值最大(P < 0.001)。见图 1A。
|
| A, line chart showing changes in body weight over the feeding period; B, line chart showing changes in random blood glucose levels over the feeding period; C, IPGTT curve at 4 months; D, IPGTT curve at 8 months; E, IPGTT curve at 12 months; F, area under the curve (AUC) of IPGTT; G, quantitative analysis of peripheral serum insulin at 12 months. * P < 0.05 vs. ND group. 图 1 高脂饮食对小鼠体重、随机血糖、糖耐量和外周血清胰岛素水平的影响 Fig.1 Effects of high-fat diet on body weight, random blood glucose, glucose tolerance, and serum insulin level of mice |
HFD组小鼠随机血糖在整个实验周期内呈明显升高趋势,而ND组小鼠无明显变化。2~12个月,HFD组小鼠随机血糖均显著高于ND组(P < 0.05);12个月时,2组小鼠随机血糖差值最大(P < 0.001)。见图 1B。
4、8和12个月时的IPGTT曲线显示,2组小鼠血糖均在15 min时最高,且HFD组小鼠血糖在15、30、60、90、120 min各时间点均显著高于ND组(P < 0.05),IPGTT曲线下面积也显著大于ND组(P < 0.01)。见图 1C~1F。
ELISA结果显示,12个月时,2组小鼠外周血清胰岛素浓度无统计学差异(P = 0.46)。见图 1G。
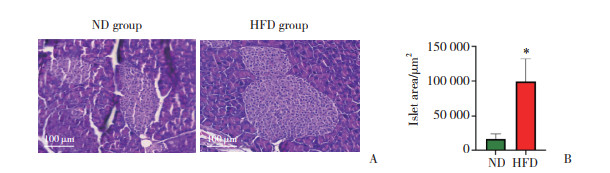
2.2 高脂饮食对小鼠胰岛面积的影响12个月时,HFD组小鼠的胰岛面积显著大于ND组(P < 0.01),约为ND组的5.77倍。见图 2。Pearson相关分析结果显示,IPGTT曲线下面积与胰岛面积呈正相关(r = 0.740 1,P < 0.01)。
|
| A, HE staining of pancreatic tissues; B, quantitative analysis of the pancreatic islet area. * P < 0.05 vs. ND group. 图 2 2组小鼠的胰岛面积 Fig.2 Pancreatic islet areas of mice in the two groups |
2.3 高脂饮食对小鼠胰岛细胞密度的影响
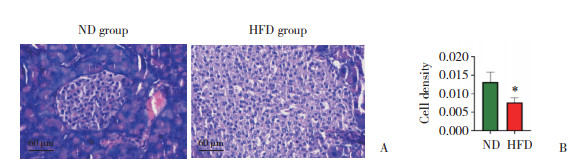
小鼠胰腺组织HE染色结果显示,与ND组相比,HFD组小鼠胰岛显著增大,胰岛细胞核大淡染。计算胰岛内细胞数量与胰岛面积的比值,作为细胞密度。结果显示,HFD组小鼠胰岛的细胞密度显著低于ND组(P < 0.01)。见图 3。Pearson相关分析结果显示,IPGTT曲线下面积与胰岛的细胞密度呈负相关(r = -0.624 7,P < 0.01)。
|
| A, HE staining of pancreatic islets; B, quantitative analysis of cell density in the pancreatic islets. * P < 0.05 vs. ND group. 图 3 2组小鼠胰岛的细胞密度 Fig.3 Cell density in the pancreatic islets of mice in the two groups |
2.4 高脂饮食对小鼠胰岛血管分布的影响
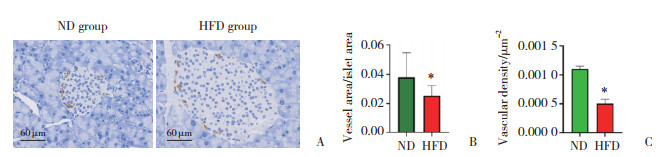
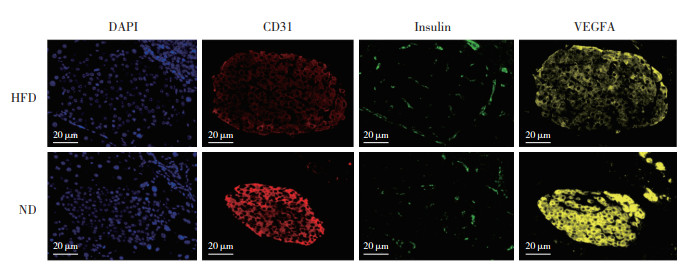
免疫组织化学染色结果显示,胰岛的供血血管主要分布于胰岛边缘,HFD组小鼠胰岛血管面积与胰岛面积的比值显著低于ND组(P < 0.05)。计算胰岛血管密度,结果显示,HFD组小鼠胰岛血管密度显著低于ND组。见图 4。免疫荧光染色结果显示,HFD组小鼠胰岛内胰岛素、VEGFA荧光强度显著低于ND组。见图 5。Pearson相关分析结果显示,IPGTT曲线下面积与胰岛血管密度呈负相关(r = -0.419 0,P < 0.01)。
|
| A, immunohistochemical staining for CD31;B, quantitative analysis of vascular area; C, quantitative analysis of vascular density. * P < 0.05 vs. ND group. 图 4 2组小鼠胰岛中血管分布 Fig.4 Distribution of blood vessels in the pancreatic islets of mice in the two groups |
|
| 图 5 2组小鼠胰岛中胰岛素、CD31、VEGFA的免疫荧光染色 Fig.5 Immunofluorescence staining of insulin, CD31, and VEGFA in the pancreatic islets of mice in the two groups |
2.5 高脂饮食对小鼠胰岛中胰岛素含量的影响
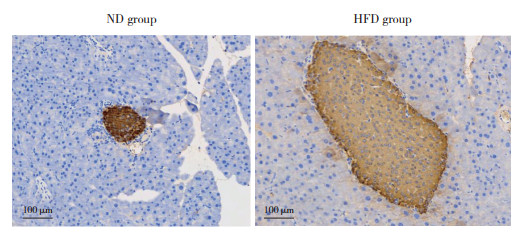
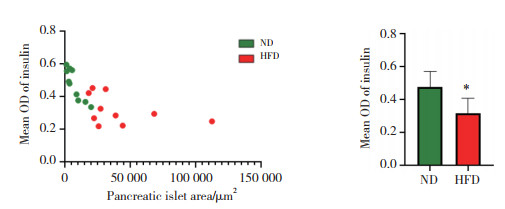
免疫组织化学染色结果显示,HFD组小鼠胰岛面积增大,胰岛素染色分布不均,阳性区域主要位于胰岛边缘位置,越向中心,染色越淡,而ND组小鼠胰岛素染色分布较为均匀一致。见图 6。与ND组相比,HFD组小鼠胰岛面积显著增加,但胰岛素含量显著降低(P < 0.01)。见图 7。
|
| 图 6 2组小鼠胰岛中胰岛素免疫组织化学染色 Fig.6 Immunohistochemical staining of insulin in the pancreatic islets of mice in the two groups |
|
| * P < 0.05 vs. ND group. 图 7 小鼠胰岛中胰岛素含量与胰岛面积的关系 Fig.7 Relationship between insulin levels and pancreatic islet area |
2.6 高脂饮食对小鼠胰岛组织中CD11c+细胞以及TLR2、TLR4表达水平的影响
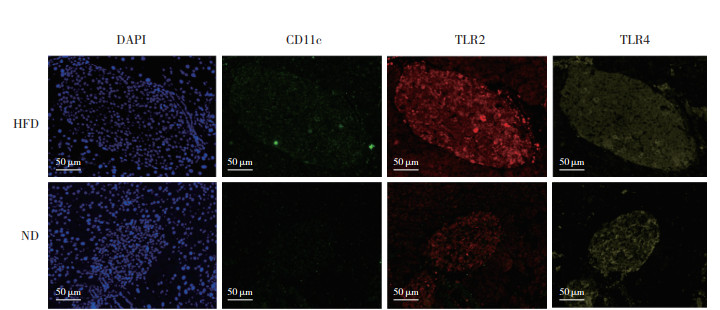
免疫荧光染色结果显示,HFD组小鼠胰岛CD11c+细胞数量显著大于ND组,TLR2荧光强度显著高于ND组;2组比较,TLR4荧光强度无明显差异。见图 8。
|
| 图 8 2组小鼠胰岛中CD11c+、TLR2、TLR4免疫荧光染色 Fig.8 Immunofluorescence staining of CD11c+, TLR2, and TLR4 in the pancreatic islets of mice in the two groups |
3 讨论
2型糖尿病作为一种复杂的代谢性疾病,其发病机制涉及遗传、环境、生活方式等多种因素[7]。目前尚无根治方法,尤其在疾病进展至典型糖尿病阶段后,胰岛β细胞功能往往已发生不可逆的损害,功能恢复极为困难[8]。相比之下,糖尿病前期为2型糖尿病的重要过渡阶段,处于此阶段的患者数量多,且在此阶段胰岛β细胞功能尚未完全丧失,为实施早期干预、延缓甚至阻断疾病进展提供了关键时间窗口[9-10]。
本研究采用高脂饲料长期喂养C57BL/6J小鼠,模拟人类高热量摄入状态,成功构建了糖耐量受损的小鼠模型。结果显示,经过12个月的高脂饲料喂养,HFD组小鼠虽未达到糖尿病诊断标准,但随机血糖已显著升高,糖耐量曲线整体上移,曲线下面积显著增大,提示胰岛对血糖的调节功能已出现明显障碍。值得注意的是,尽管HFD组小鼠的胰岛面积显著增大,约为ND组的5.77倍,但这种结构上的代偿性增生并未带来功能的同步提升,反而伴随细胞密度下降、胰岛素合成和分泌功能受损,说明长期高脂负荷下胰岛β细胞可能出现功能耗竭或去分化现象。
组织病理学结果进一步揭示,HFD组小鼠胰岛细胞核增大、淡染,并出现异形核和空泡变性等退行性病变,这可能是细胞密度下降的结构基础。此外,高脂饮食可能促进胰岛β细胞内胰岛淀粉样蛋白的异常沉积,后者具有细胞毒性,可进一步加剧β细胞损伤和凋亡,形成恶性循环。
胰岛作为高度血管化的微器官,其功能高度依赖于健全的微循环灌注[11]。本研究发现,2组小鼠的血管主要分布于胰岛周边,而HFD组小鼠胰岛内部的血管密度和血管面积占比均显著降低,VEGFA表达下降,提示高脂饮食损害了胰岛内的血管生成。由于胰岛细胞对缺氧极为敏感,血管密度下降会导致氧和营养物质扩散距离增加,代谢废物清除能力减弱,进而影响胰岛素的合成和分泌效率[12]。相关分析结果显示,胰岛血管密度与糖耐量曲线的曲线下面积呈显著负相关,进一步证实胰岛微循环障碍在糖耐量受损中的重要作用。
在分子机制层面,本研究发现HFD组小鼠胰岛内CD11c+细胞浸润增加,TLR2表达上调,而TLR4变化不明显。CD11c+细胞通常为炎症性巨噬细胞或树突状细胞,其增多提示胰岛局部炎症反应激活。TLR2作为先天免疫模式识别受体,其上调可能通过核因子κB等信号通路促进炎性细胞因子释放,参与胰岛β细胞功能障碍和胰岛素抵抗的进程[13]。这一发现为理解从营养过剩到炎症激活,再到胰岛损伤的连锁反应,提供了新的实验依据。
综上所述,长期高脂饮食通过诱导胰岛结构代偿性增生伴功能失代偿、破坏胰岛微循环、引发局部炎症反应等多重途径,共同导致小鼠糖耐量异常和胰岛功能进行性下降。本研究从形态、功能、血管和炎症角度系统揭示了高脂饮食对胰岛的综合影响,为深入探讨糖尿病前期的病理机制以及开发早期干预策略提供了重要的实验依据和理论支撑。
| [1] |
SUN H, SAEEDI P, KARURANGA S, et al. IDF diabetes atlas: glo-bal, regional and country-level diabetes prevalence estimates for 2021 and projections for 2045[J]. Diabetes Res Clin Pract, 2022, 183: 109119. DOI:10.1016/j.diabres.2021.109119 |
| [2] |
TINAJERO MG, MALIK VS. An update on the epidemiology of type 2 diabetes: a global perspective[J]. Endocrinol Metab Clin North Am, 2021, 50(3): 337-355. DOI:10.1016/j.ecl.2021.05.013 |
| [3] |
TABÁK AG, HERDER C, RATHMANN W, et al. Prediabetes: a high-risk state for diabetes development[J]. Lancet, 2012, 379(9833): 2279-2290. DOI:10.1016/S0140-6736(12)60283-9 |
| [4] |
TAN BL, NORHAIZAN ME. Effect of high-fat diets on oxidative stress, cellular inflammatory response and cognitive function[J]. Nutrients, 2019, 11(11): 2579. DOI:10.3390/nu11112579 |
| [5] |
ROHR MW, NARASIMHULU CA, RUDESKI-ROHR TA, et al. Negative effects of a high-fat diet on intestinal permeability: a review[J]. Adv Nutr, 2020, 11(1): 77-91. DOI:10.1093/advances/nmz061 |
| [6] |
ALY RH, AHMED AE, HOZAYEN WG, et al. Patterns of Toll-like receptor expressions and inflammatory cytokine levels and their implications in the progress of insulin resistance and diabetic nephropathy in type 2 diabetic patients[J]. Front Physiol, 2020, 11: 609223. DOI:10.3389/fphys.2020.609223 |
| [7] |
EDWARDS CM, CUSI K. Prediabetes: a worldwide epidemic[J]. Endocrinol Metab Clin North Am, 2016, 45(4): 751-764. DOI:10.1016/j.ecl.2016.06.007 |
| [8] |
NG XW, CHUNG YH, PISTON DW. Intercellular communication in the islets of Langerhans during health and disease[J]. Compr Physiol, 2021, 11(3): 2191-2225. DOI:10.1002/cphy.c200026 |
| [9] |
BLENCOWE M, FURTERER A, WANG Q, et al. IAPP-induced beta cell stress recapitulates the islet transcriptome in type 2 diabetes[J]. Diabetologia, 2022, 65(1): 173-187. DOI:10.1007/s00125-021-05569-2 |
| [10] |
MONTANE J, KLIMEK-ABERCROMBIE A, POTTER KJ, et al. Metabolic stress, IAPP and islet amyloid[J]. Diabetes Obes Metab, 2012, 14(Suppl 3): 68-77. DOI:10.1111/j.1463-1326.2012.01657.x |
| [11] |
KOMATSU H, KANDEEL F, MULLEN Y. Impact of oxygen on pancreatic islet survival[J]. Pancreas, 2018, 47(5): 533-543. DOI:10.1097/MPA.0000000000001050 |
| [12] |
LAMMERT E, GU GQ, MCLAUGHLIN M, et al. Role of VEGF-A in vascularization of pancreatic islets[J]. Curr Biol, 2003, 13(12): 1070-1074. DOI:10.1016/s0960-9822(03)00378-6 |
| [13] |
BRISSOVA M, SHOSTAK A, SHIOTA M, et al. Pancreatic islet production of vascular endothelial growth factor: a is essential for islet vascularization, revascularization, and function[J]. Diabetes, 2006, 55(11): 2974-2985. DOI:10.2337/db06-0690 |
 2026, Vol. 55
2026, Vol. 55