文章信息
- 王昀, 张洋, 杨贺然, 成永霞, 司云飞
- WANG Yun, ZHANG Yang, YANG Heran, CHENG Yongxia, SI Yunfei
- 酸枣仁皂苷A调节PINK1/Parkin信号通路介导的线粒体自噬对糖尿病大鼠心肌损伤的影响
- Effects of jujuboside A on myocardial injury in diabetic rats via regulation of PINK1/Parkin signaling pathway-mediated mitochondrial autophagy
- 中国医科大学学报, 2026, 55(4): 341-347, 353
- Journal of China Medical University, 2026, 55(4): 341-347, 353
-
文章历史
- 收稿日期:2025-02-14
- 网络出版时间:2026-04-15 11:20:02
2. 牡丹江医科大学基础医学院病理教研室, 黑龙江 牡丹江 157011;
3. 牡丹江市肿瘤医院腹外科, 黑龙江 牡丹江 157009
2. Department of Pathology, Mudanjiang Medical University, Mudanjiang 157011, China;
3. Department of Abdominal Surgery, Mudanjiang Tumor Hospital, Mudanjiang 157009, China
糖尿病心肌病(diabetic cardiomyopathy,DCM)是糖尿病(diabetes mellitus,DM)的主要并发症之一[1]。持续的高血糖可导致心肌细胞中线粒体损伤,其后通过线粒体自噬维持细胞稳态,但在此过程中会产生过量的活性氧(reactive oxygen species,ROS),进一步加剧心肌细胞的氧化应激和损伤[2]。研究[3-5]表明,DCM可通过上调线粒体自噬关键蛋白PTEN诱导假定激酶1(PTEN-induced putative kinase 1,PINK1)和Parkin的表达水平,恢复线粒体自噬功能,从而减轻心肌细胞的氧化应激和损伤。酸枣仁皂苷A(jujuboside A,JuA)是一种从酸枣仁中提取的化学物质,具有镇静催眠、降血脂、抗心肌缺血、改善糖尿病肾病等作用[6-8]。然而,JuA能否通过PINK1/Parkin介导的线粒体自噬对DCM发挥保护作用仍未可知。因此,本研究利用DM大鼠模型探讨了JuA对DM大鼠心肌损伤的影响,并分析其潜在机制。
1 材料与方法 1.1 材料 1.1.1 实验动物雄性8周龄SPF级SD大鼠80只,体重(200±20)g,购自黑龙江中医药大学[许可证号:SCXK(黑)2023-001],在12 h光照/黑暗循环、温度24 ℃、湿度55%的动物房中饲养。本研究获得牡丹江医科大学附属红旗医院伦理委员会批准(20240394)。
1.1.2 主要试剂与仪器JuA购自上海源叶生物科技有限公司;线粒体自噬抑制剂Mdivi-1购自美国MCE公司;链脲佐菌素(streptozotocin,STZ)购自美国Sigma-Aldrich公司;盐酸二甲双胍片(国药准字H20023370,规格0.5 g/片)购自中美上海施贵宝制药有限公司。苏木素-伊红(hematoxylin and eosin,HE)染色试剂盒(C0105S)、Masson三色染色试剂盒(C0189S)购自上海碧云天生物科技股份有限公司;ROS MitosOX红色荧光测定试剂盒(超氧阴离子)(GMS10460.2)购自深圳子科生物科技有限公司;乳酸脱氢酶(lactate dehydrogenase,LDH)(A020-2-2)、肌酸激酶同工酶(creatine kinase MB,CK-MB)(H197-1-2)、超氧化物歧化酶(superoxide dismutase,SOD)(A001-3-2)、丙二醛(malondialdehyde,MDA)(A003-1-2)检测试剂盒购自南京建成生物工程研究所;兔源一抗PINK1(PA1-16604)、Parkin(PA1-751)购自美国Thermo Fisher Scientific公司;兔源一抗微管相关蛋白1轻链3B(microtubule associated protein 1 light chain 3B,LC3B)(ab192890)、p62(ab109012)、GAPDH(ab181602)购自英国abcam公司。Vevo 2100超高分辨率小动物彩色多普勒超声仪购自加拿大VisualSonics公司;LSM 900激光共聚焦扫描显微镜购自德国Carl Zeiss公司;Multiskan FC酶标仪购自美国Thermo Fisher Scientific公司;HT7820透射电子显微镜购自株式会社日立制作所。
1.2 方法 1.2.1 模型建立及实验分组大鼠适应性喂养1周后,随机选取12只设为对照组,给予普通饲料喂养4周。其余68只大鼠采用高糖高脂饲料喂养4周,随后一次性腹腔注射STZ(35 mg/kg)建立DM模型,分别在注射3 d和7 d后从大鼠尾部取血,检测大鼠空腹血糖(fasting blood glucose,FBG),若连续2次FBG≥16.7 mmol/L,并出现多饮、多食、多尿和体重降低,则视为造模成功[9]。将60只造模成功大鼠分为模型组、二甲双胍组[9]、JuA低剂量组、JuA高剂量组[8]、JuA高剂量+Mdivi-1组[10],每组12只。二甲双胍组大鼠给予67.5 mg/kg二甲双胍混悬液灌胃,JuA低、高剂量组大鼠分别给予20 mg/kg、40 mg/kg的JuA混悬液灌胃,JuA高剂量+Mdivi-1组大鼠在灌胃40 mg/kg的JuA混悬液前30 min,腹腔注射10 mg/kg Mdivi-1;对照组和模型组大鼠给予等量溶剂灌胃和腹腔注射,1次/d。共给药8周。
1.2.2 超声心动图评估大鼠心功能用异氟醚麻醉大鼠后,将大鼠以仰卧位置于超声检查台上,剃除胸部毛发。将温偶联剂均匀涂抹在其心前区。将超声探头(频率22~55 MHz)调整到合适位置,确保胸腔成像清晰。测量左心室舒张末内径(left ventricular end-diastolic diameter,LVEDd)、左心室收缩末内径(left ventricular end-systolic diameter,LVESd)、左室射血分数(left ventricular ejection fraction,LVEF)和左室缩短分数(left ventricular fractional shortening,LVFS)。
1.2.3 ELISA检测大鼠血清中LDH、CK-MB含量大鼠心功能检测完成后,腹主动脉取血,3 000 r/min离心10 min以分离血清,用ELISA法检测血清LDH、CK-MB含量。
1.2.4 HE染色观察大鼠心肌组织病理学变化处死大鼠后,迅速取出心脏组织,并用生理盐水冲洗。分离左心室组织,取部分组织用4%多聚甲醛固定48 h,石蜡包埋,制4 µm厚切片,HE染色,在光学显微镜下观察心肌组织病理学变化。
1.2.5 Masson染色观察大鼠心肌纤维化程度取心肌组织石蜡切片,按照Masson染色试剂盒说明书进行常规染色。染色后,在光学显微镜下观察组织切片,用Image-Pro Plus 5.0软件分析大鼠心肌胶原面积,计算胶原容积分数(collagen volume fraction,CVF)。
1.2.6 比色法检测大鼠心肌组织中MDA水平和SOD活性取部分心肌组织,加入预冷的生理盐水,研磨制备10%的组织匀浆,离心后取上清,按照试剂盒说明书检测MDA水平和SOD活性。
1.2.7 大鼠心肌组织中线粒体ROS测定取部分心肌组织,制备心肌组织冰冻切片,室温下用预冷的清理液清洗切片表面后,将MitoSOX染液均匀覆盖在切片表面,在37 ℃下避光孵育10 min后,用清理液清洗切片表面,以去除多余的染色液。在激光共聚焦显微镜下观察切片,用Image J软件计算相对荧光强度。
1.2.8 透射电镜观察大鼠心肌细胞线粒体超微结构及自噬小体数量将心肌组织切成1 mm×1 mm×1 mm大小,用2.5%戊二醛和1%四氧化锇分别固定2 h,梯度乙醇脱水、环氧树脂包埋、切片(厚60 nm)后,用3%枸橼酸铅和醋酸铀双染。在透射电镜下观察线粒体形态,计数自噬小体数量。
1.2.9 Western blotting检测大鼠心肌组织PINK1、Parkin和自噬相关蛋白LC3B、p62表达取部分左心室组织,用RIPA裂解液匀浆,提取总蛋白,用BCA试剂盒测定蛋白浓度后,通过10%SDS-PAGE分离蛋白,电转移至PVDF膜。用5%脱脂牛奶封闭1 h,4 ℃下与一抗[PINK1(1∶1 000)、Parkin(1∶1 000)、p62(1∶10 000)、LC3B(1∶1 000)、GAPDH(1∶2 000)]孵育过夜。用TBST洗膜3次(5 min/次),室温下用二抗(1∶5 000)孵育1 h。显影检测蛋白条带,用ImageJ软件定量分析。
1.3 统计学分析采用SPSS 26.0软件进行统计分析。计量资料以x±s表示,符合正态分布时,多组间比较采用单因素方差分析,组间有差异则进一步采用SNK-q检验进行两两比较;不符合正态分布时,组间比较采用Mann-Whitney U秩和检验。P < 0.05为差异有统计学意义。
2 结果 2.1 各组大鼠心功能指标比较与对照组相比,模型组大鼠LVEDd、LVESd升高,LVEF、LVFS降低(P < 0.05);与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠LVEDd、LVESd降低,LVEF、LVFS升高(P < 0.05);与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠LVEDd、LVESd升高,LVEF、LVFS降低(P < 0.05)。见表 1。
| Group | n | LVEF(%) | LVFS(%) | LVEDd(mm) | LVESd(mm) |
| Control | 12 | 75.73±5.02 | 63.60±4.88 | 2.35±0.29 | 2.10±0.24 |
| Model | 12 | 39.20±3.941) | 25.72±3.091) | 5.94±0.401) | 3.56±0.381) |
| Metformin | 12 | 62.68±4.652) | 54.13±4.472) | 2.88±0.322) | 2.30±0.292) |
| Low-dose JuA | 12 | 50.35±4.312)3) | 39.29±3.522),3) | 4.53±0.362),3) | 2.92±0.322),3) |
| High-dose JuA | 12 | 61.90±4.822) | 51.85±4.702) | 3.01±0.352) | 2.35±0.262) |
| High-dose JuA+Mdivi-1 | 12 | 42.53±4.723) | 31.66±3.593) | 5.22±0.383) | 3.19±0.353) |
| 1)P<0.05 vs. control group;2)P<0.05 vs. model group;3)P<0.05 vs. high-dose JuA group. LVEF,left ventricular ejection fraction;LVFS,left ventricular fractional shortening;LVEDd,left ventricular end-diastolic diameter;LVESd,left ventricular end-systolic diameter. | |||||
2.2 各组大鼠血清CK-MB、LDH水平比较
与对照组相比,模型组大鼠血清CK-MB、LDH水平升高(P < 0.05);与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠血清CK-MB、LDH水平降低(P < 0.05);与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠血清CK-MB、LDH水平升高(P < 0.05)。见表 2。
| Group | n | CK-MB | LDH |
| Control | 12 | 48.21±7.50 | 121.59±20.06 |
| Model | 12 | 195.43±12.141) | 577.24±36.741) |
| Metformin | 12 | 76.08±9.362) | 200.39±24.182) |
| Low-dose JuA | 12 | 144.30±11.092),3) | 435.60±30.552),3) |
| High-dose JuA | 12 | 80.12±10.452) | 211.08±27.292) |
| High-dose JuA+Mdivi-1 | 12 | 163.74±12.033) | 512.47±32.503) |
| 1)P<0.05 vs. control group;2)P<0.05 vs. model group;3)P<0.05 vs. high-dose JuA group. CK-MB,creatine kinase MB;LDH,lactate dehydrogenase. | |||
2.3 各组大鼠心肌组织病理学变化比较
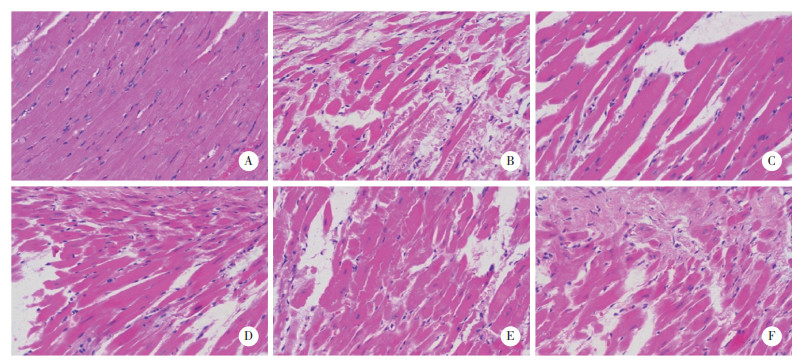
对照组大鼠心肌纤维结构正常,心肌细胞排列紧密、有规律,细胞核清晰可见;模型组大鼠心肌纤维严重断裂,心肌细胞大面积水肿,细胞间隙增大,细胞核不清,甚至融合;与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠心肌改变明显减轻,部分心肌纤维断裂,心肌细胞轻微水肿,排列更有规律;与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠心肌纤维断裂增多,心肌细胞排列较紊乱。见图 1。
|
| A, control group; B, model group; C, metformin group; D, low-dose JuA group; E, high-dose JuA group; F, high-dose JuA+Mdivi-1 group. 图 1 各组大鼠心肌组织病理变化HE ×200 Fig.1 Pathological changes of myocardial tissue in rats of each group HE ×200 |
2.4 各组大鼠心肌纤维化程度比较
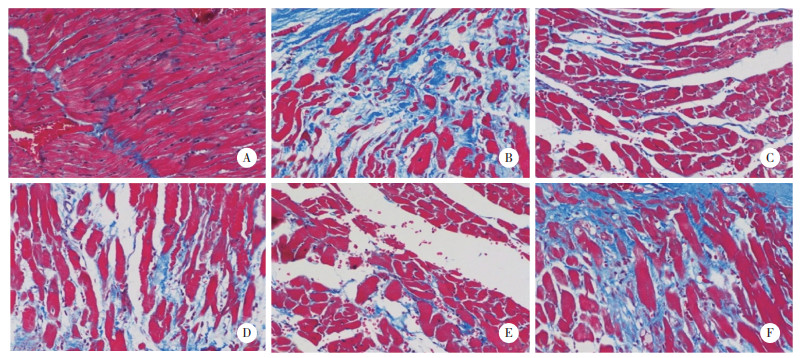
对照组大鼠心肌组织可见少量蓝色胶原纤维,未见结构异常;与对照组相比,模型组大鼠心肌有大量蓝色胶原纤维沉积,CVF升高至7.89%±0.60%;与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠心肌组织蓝色胶原纤维沉积减少,CVF降低,分别为3.64%±0.42 %、6.25%±0.53%、3.80%±0.45%;与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠心肌组织蓝色胶原纤维沉积增加,CVF升高至6.57%±0.58%,差异均有统计学意义(均P < 0.05)。见图 2。
|
| A, control group; B, model group; C, metformin group; D, low-dose JuA group; E, high-dose JuA group; F, high-dose JuA+Mdivi-1 group. 图 2 各组大鼠心肌纤维化程度Masson ×200 Fig.2 Degree of myocardial fibrosis in each group of rats Masson ×200 |
2.5 各组大鼠心肌组织MDA水平和SOD活性比较
与对照组相比,模型组大鼠心肌组织MDA水平升高,SOD活性降低(P < 0.05);与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠心肌组织MDA水平降低,SOD活性升高(P < 0.05);与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠心肌组织MDA水平升高,SOD活性降低(P < 0.05)。见表 3。
| Group | n | MDA(nmol/mg) | SOD(U/mg) |
| Control | 12 | 5.20±0.79 | 148.66±17.31 |
| Model | 12 | 14.65±1.231) | 51.42±9.291) |
| Metformin | 12 | 7.83±0.852) | 110.75±15.402) |
| Low-dose JuA | 12 | 10.70±1.062),3) | 86.13±11.362),3) |
| High-dose JuA | 12 | 7.91±0.942) | 105.80±14.752) |
| High-dose JuA+Mdivi-1 | 12 | 12.38±1.153) | 71.04±10.823) |
| 1)P<0.05 vs. control group;2)P<0.05 vs. model group;3)P<0.05 vs. high-dose JuA group. MDA,malondialdehyde;SOD,superoxide dismutase. | |||
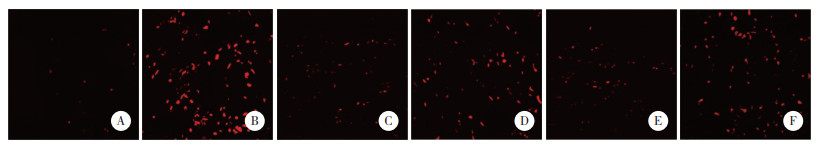
2.6 各组大鼠心肌组织线粒体ROS水平比较(图 3)
|
| A, control group; B, model group; C, metformin group; D, low-dose JuA group; E, high-dose JuA group; F, high-dose JuA+Mdivi-1 group. 图 3 各组大鼠心肌组织线粒体ROS水平MitoSOX ×200 Fig.3 Mitochondrial ROS levels in myocardial tissue of rats in each group MitoSOX ×200 |
与对照组[(1.00±0.00)μmol/mg]相比,模型组大鼠心肌组织线粒体ROS水平[(3.45±0.37)μmol/mg]升高(P < 0.05);与模型组相比,二甲双胍组[(1.69±0.25)μmol/mg]和JuA低剂量组、JuA高剂量组大鼠心肌组织线粒体ROS水平[(2.81±0.30)μmol/mg、(1.74±0.28)μmol/mg]降低(P < 0.05);与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠心肌组织线粒体ROS水平[(2.99±0.34)μmol/mg]升高(P < 0.05)。
2.7 各组大鼠心肌细胞线粒体超微结构及自噬小体数量比较对照组大鼠心肌组织线粒体排列整齐,线粒体膜完整,线粒体嵴结构清晰,线粒体中无明显双层膜的自噬小体形成,自噬小体数量为0.25±0.45;与对照组相比,模型组大鼠心肌线粒体双模结构破坏,线粒体肿胀,线粒体嵴紊乱,线粒体自噬小体增多至1.08±0.29;与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠心肌组织线粒体排列较整齐,线粒体肿胀减轻,线粒体嵴少量断裂,自噬小体数量分别增加至2.58±0.51、1.92±0.79、2.42±0.51;与JuA高剂量组相比,JuA高剂量+Mdivi-1组大鼠心肌组织线粒体肿胀,线粒体嵴断裂增加,自噬小体数量减少至1.33±0.49,差异均有统计学意义(均P < 0.05)。见图 4。

|
| A, control group; B, model group; C, metformin group; D, low-dose JuA group; E, high-dose JuA group; F, high-dose JuA+Mdivi-1 group. 图 4 各组大鼠心肌细胞线粒体超微结构和自噬情况TEM×20 000 Fig.4 Mitochondrial ultrastructure and autophagy of myocardial cells of rats in each group TEM×20 000 |
2.8 各组大鼠心肌组织PINK1、Parkin和自噬相关蛋白LC3B、p62表达比较
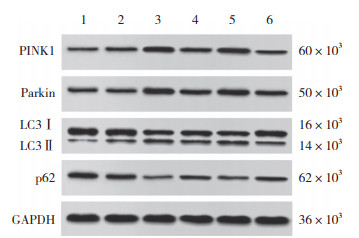
与对照组相比,模型组大鼠心肌组织PINK1蛋白表达水平升高(P < 0.05),Parkin、LC3Ⅱ/Ⅰ蛋白表达水平略有升高,但差异无统计学意义(P > 0.05),p62蛋白表达水平降低(P < 0.05);与模型组相比,二甲双胍组和JuA低剂量组、JuA高剂量组大鼠心肌组织PINK1、Parkin、LC3Ⅱ/Ⅰ蛋白表达水平升高,p62蛋白表达水平降低(P < 0.05);与JuA高剂量组相比,JuA高剂量+Mdivi-1组心肌组织PINK1、Parkin、LC3Ⅱ/Ⅰ蛋白表达水平降低,p62蛋白表达水平升高(P < 0.05),见表 4、图 5。
| Group | n | PINK1 | Parkin | LC3Ⅱ/Ⅰ | p62 |
| Control | 12 | 0.17±0.03 | 0.24±0.04 | 0.19±0.03 | 0.48±0.06 |
| Model | 12 | 0.25±0.041) | 0.28±0.04 | 0.23±0.04 | 0.40±0.051) |
| Metformin | 12 | 0.64±0.062) | 0.73±0.082) | 0.55±0.062) | 0.18±0.032) |
| Low-dose JuA | 12 | 0.39±0.052),3) | 0.50±0.062),3) | 0.37±0.052),3) | 0.31±0.042),3) |
| High-dose JuA | 12 | 0.60±0.062) | 0.69±0.072) | 0.52±0.052) | 0.20±0.042) |
| High-dose JuA+Mdivi-1 | 12 | 0.32±0.043) | 0.40±0.053) | 0.29±0.043) | 0.33±0.053) |
| 1)P<0.05 vs. control group;2)P<0.05 vs. model group;3)P<0.05 vs. high-dose JuA group. | |||||
|
| 1, control group; 2, model group; 3, metformin group; 4, low-dose JuA group; 5, high-dose JuA group; 6, high-dose JuA+Mdivi-1 group. 图 5 各组大鼠心肌组织PINK1、Parkin和自噬相关蛋白LC3B、p62表达 Fig.5 Expression of PINK1, Parkin, and autophagy-related proteins LC3B and p62 expression in myocardial tissue of rats in each group |
3 讨论
DCM是DM的并发症之一。DCM心脏结构改变和功能受损使心脏被迫重塑,心输出量减少,导致心力衰竭和死亡。其特征是心脏功能和结构异常,包括心肌肥大、间质纤维化、心肌细胞凋亡和舒张功能障碍[11-12]。
JuA作为酸枣仁的主要有效成分,长期以来被认为是一种镇静催眠药物。近年来研究[13-15]发现,JuA对缺血缺氧再灌注损伤等引发的心肌细胞损伤具有改善作用。此外,JuA还可通过改善肝脏脂质积累、炎症和氧化应激,缓解2型DM相关的脂肪肝[16],因此,JuA可能是DM及其相关并发症的一种候选治疗药物。本研究结果显示,JuA可降低DM大鼠血清CK-MB和LDH水平,改善DM大鼠心功能,减轻心肌病理变化和间质纤维化,表明JuA可减轻DM大鼠的心肌损伤,并再次证实了JuA的心脏保护作用。
线粒体自噬是指通过自噬溶酶体途径特异性清除受损、老化和ROS过量的线粒体,以确保细胞的能量供应和正常功能[17]。JuA对恢复心肌细胞ATP酶活性也具有一定作用[18]。在本研究中,DM大鼠心肌组织中SOD活性降低,MDA水平升高,线粒体ROS水平升高,同时线粒体出现肿胀、融合及空泡化,线粒体膜断裂,线粒体嵴断裂、消失,存在自噬现象,提示DM大鼠心肌细胞中线粒体受损,出现氧化应激损伤;而给予JuA干预后,DM大鼠心肌组织中SOD活性升高,MDA水平降低,线粒体ROS水平降低,线粒体空泡化及线粒体嵴断裂情况改善,膜结构相对完整,自噬小体数量增加,表明JuA可诱导线粒体自噬,清除受损的线粒体,抑制心肌细胞氧化应激损伤。
PINK1/Parkin信号通路是线粒体自噬的经典机制之一[19-20]。ZHONG等[8]发现,JuA可通过激活PINK1/Parkin信号通路增强线粒体自噬,改善高脂饮食和STZ诱导的糖尿病肾病。在本研究中,JuA可增加DM大鼠心肌组织中PINK1、Parkin、LC3Ⅱ/Ⅰ蛋白表达水平,降低p62蛋白表达水平,由此推测JuA对DM大鼠心肌损伤的改善作用可能与激活PINK1/Parkin信号通路介导的线粒体自噬有关。为了进一步验证此推测,本研究采用线粒体自噬抑制剂Mdivi-1进行干预,结果显示,Mdivi-1明显减弱了JuA对DM大鼠心肌损伤的改善作用。提示JuA可能通过激活PINK1/Parkin信号通路介导的线粒体自噬,清除受损的线粒体,抑制心肌细胞氧化应激损伤,改善DM大鼠心肌损伤。
综上所述,本研究发现,JuA可能通过激活PINK1/Parkin信号通路介导的线粒体自噬,清除受损的线粒体,抑制心肌细胞氧化应激损伤,改善DM大鼠心肌损伤。本研究从线粒体自噬的角度初步探讨了JuA对DM大鼠心肌损伤的改善作用,为DM治疗药物的研发提供了新的思路。但本研究仍存在不足之处,如仅针对PINK1/Parkin这一信号通路进行探究,但JuA能否通过其他通路或靶点发挥心肌保护作用仍需进一步探索。
| [1] |
RADZIOCH E, DĄBEK B, BALCERCZYK-LIS M, et al. Diabetic cardiomyopathy-from basics through diagnosis to treatment[J]. Biomedicines, 2024, 12(4): 765. DOI:10.3390/biomedicines12040765 |
| [2] |
LIN JG, DUAN JL, WANG QQ, et al. Mitochondrial dynamics and mitophagy in cardiometabolic disease[J]. Front Cardiovasc Med, 2022, 9: 917135. DOI:10.3389/fcvm.2022.917135 |
| [3] |
ZHENG HX, ZHU HL, LIU XY, et al. Mitophagy in diabetic cardiomyopathy: roles and mechanisms[J]. Front Cell Dev Biol, 2021, 9: 750382. DOI:10.3389/fcell.2021.750382 |
| [4] |
MU J, ZHANG DH, TIAN YL, et al. BRD4 inhibition by JQ1 prevents high-fat diet-induced diabetic cardiomyopathy by activating PINK1/Parkin-mediated mitophagy in vivo[J]. J Mol Cell Cardiol, 2020, 149: 1-14. DOI:10.1016/j.yjmcc.2020.09.003 |
| [5] |
YANG CR, XIAO C, DING ZR, et al. Canagliflozin mitigates diabetic cardiomyopathy through enhanced PINK1-parkin mitophagy[J]. Int J Mol Sci, 2024, 25(13): 7008. DOI:10.3390/ijms25137008 |
| [6] |
WANG W, WANG Y, PEI HY, et al. The mechanism of simultaneous intake of Jujuboside A and B in the regulation of sleep at the hypothalamic level[J]. Aging, 2023, 15(18): 9426-9437. DOI:10.18632/aging.204995 |
| [7] |
WANG Z, XIAO DR, JI QQ, et al. Jujuboside A attenuates sepsis-induced cardiomyopathy by inhibiting inflammation and regulating autophagy[J]. Eur J Pharmacol, 2023, 947: 175451. DOI:10.1016/j.ejphar.2022.175451 |
| [8] |
ZHONG YJ, LUO RL, LIU Q, et al. Jujuboside A ameliorates high fat diet and streptozotocin induced diabetic nephropathy via suppressing oxidative stress, apoptosis, and enhancing autophagy[J]. Food Chem Toxicol, 2022, 159: 112697. DOI:10.1016/j.fct.2021.112697 |
| [9] |
张亚楠, 丁英钧, 徐华洲, 等. 加味桃核承气汤对糖尿病心肌病大鼠NLRP3炎症小体的影响[J]. 中国实验方剂学杂志, 2022, 28(16): 59-65. DOI:10.13422/j.cnki.syfjx.20220780 |
| [10] |
SUN EY, ZHANG J, DENG Y, et al. Docosahexaenoic acid alleviates brain damage by promoting mitophagy in mice with ischaemic stroke[J]. Oxid Med Cell Longev, 2022, 2022: 3119649. DOI:10.1155/2022/3119649 |
| [11] |
谷君, 许峥嵘, 史丽, 等. circFAT1调节miR-211-5p/CCND2轴对糖尿病心肌病大鼠心肌损伤的影响[J]. 中国医科大学学报, 2024, 53(6): 516-524. DOI:10.12007/j.issn.0258-4646.2024.06.006 |
| [12] |
PAN KL, HSU YC, CHANG ST, et al. The role of cardiac fibrosis in diabetic cardiomyopathy: from pathophysiology to clinical diagnostic tools[J]. Int J Mol Sci, 2023, 24(10): 8604. DOI:10.3390/ijms24108604 |
| [13] |
胡怡然, 瞿惠燕, 郭佳莹, 等. 酸枣仁皂苷A对缺血缺氧再灌注的H9C2细胞CD38/NAD+信号通路相关因子表达的影响[J]. 中国老年学杂志, 2024, 44(2): 382-387. DOI:10.3969/j.issn.1005-9202.2024.02.037 |
| [14] |
李会涛, 李剑男, 张桐, 等. 酸枣仁皂苷A对抑郁小鼠行为及突触可塑性相关蛋白的作用[J]. 现代食品科技, 2024, 40(2): 36-43. DOI:10.13982/j.mfst.1673-9078.2024.2.0294 |
| [15] |
LIU YY, LI L, JI B, et al. Jujuboside A ameliorates tubulointerstitial fibrosis in diabetic mice through down-regulating the YY1/TGF-β1 signaling pathway[J]. Chin J Nat Med, 2022, 20(9): 656-668. DOI:10.1016/S1875-5364(22)60200-0 |
| [16] |
ZHANG WJ, CHENG Q, YIN LX, et al. Jujuboside A through YY1/CYP2E1 signaling alleviated type 2 diabetes-associated fatty liver disease by ameliorating hepatic lipid accumulation, inflammation, and oxidative stress[J]. Chem Biol Interact, 2024, 400: 111157. DOI:10.1016/j.cbi.2024.111157 |
| [17] |
李雨珊, 王鹏皓. 白藜芦醇介导SIRT2干预地塞米松诱导的骨髓间充质干细胞线粒体自噬[J]. 中国医科大学学报, 2024, 53(8): 731-735. DOI:10.12007/j.issn.0258-4646.2024.08.010 |
| [18] |
冯庭宇, 许晓伍. 酸枣仁皂苷A促进心肌线粒体COX表达介导膜电位恢复ATP酶活性改善失眠[J]. 解剖学研究, 2022, 44(4): 307-312. DOI:10.20021/j.cnki.1671-0770.2022.04.01 |
| [19] |
GUAN ZJ, CHEN J, WANG LH, et al. Nuanxinkang prevents the development of myocardial infarction-induced chronic heart failure by promoting PINK1/Parkin-mediated mitophagy[J]. Phytomedicine, 2023, 108: 154494. DOI:10.1016/j.phymed.2022.154494 |
| [20] |
KATAURA T, OTTEN EG, RABANAL-RUIZ Y, et al. NDP52 acts as a redox sensor in PINK1/Parkin-mediated mitophagy[J]. EMBO J, 2023, 42(5): e111372. DOI:10.15252/embj.2022111372 |
 2026, Vol. 55
2026, Vol. 55