文章信息
- 余粲, 秦志伟, 承泽农, 张磊, 陆进
- YU Can, QIN Zhiwei, CHENG Zenong, ZHANG Lei, LU Jin
- TOP2A-TTK-KIF2C基因网络在肝细胞癌免疫微环境和靶向治疗中的作用
- Role of TOP2A-TTK-KIF2C network in the immune microenvironment and its application in targeted therapy for hepatocellular carcinoma
- 中国医科大学学报, 2026, 55(4): 315-322
- Journal of China Medical University, 2026, 55(4): 315-322
-
文章历史
- 收稿日期:2025-03-03
- 网络出版时间:2026-04-15 13:28:53
2. 蚌埠医科大学第一附属医院病理科, 安徽 蚌埠 233030;
3. 蚌埠医科大学第二附属医院普外科, 安徽 蚌埠 233030;
4. 蚌埠医科大学数字医学与智慧健康安徽省重点实验室, 安徽 蚌埠 233030
2. Department of Pathology, First Affiliated Hospital, Bengbu Medical University, Bengbu 233030, China;
3. Department of General Surgery, Second Affiliated Hospital, Bengbu Medical University, Bengbu 233030, China;
4. Anhui Key Laboratory of Digital Medicine and Smart Health, Bengbu Medical University, Bengbu 233030, China
肝细胞癌(hepatocellular carcinoma,HCC)是最常见的原发性肝癌,约占肝癌的90%[1-3]。乙型肝炎病毒和丙型肝炎病毒慢性感染、酗酒和代谢综合征是HCC的常见病因[4-5]。目前手术切除仍是HCC的主要治疗手段,但术后复发转移率高[6],且多数患者确诊时已至中晚期,5年生存率仅为18%[7],需探索更有效的诊疗新策略。
DNA拓扑异构酶Ⅱα(topoisomerase Ⅱ alpha,TOP2A)是一种关键的DNA解旋酶[8],它在多种肿瘤中高表达,且与不良预后密切相关[9-11]。研究[12-13]表明,TOP2A在HCC中表达上调。目前对其在HCC中的分子调控网络,特别是在肿瘤免疫微环境中的作用机制尚不明确。近期研究[14]证实,整合生物信息学与机器学习策略可有效筛选肝癌关键基因。因此,本研究基于上述研究基础、整合多组学数据与实验验证,系统构建TOP2A核心调控网络,鉴定关键节点基因,深入探讨其在HCC免疫微环境调控及靶向治疗中的价值,为HCC精准诊疗提供理论依据。
1 材料与方法 1.1 数据来源数据来源于癌症基因组图谱(The Cancer Genome Atlas,TCGA)数据库(https://portal.gdc.cancer.gov)和基因表达综合(Gene Expression Omnibus,GEO)数据库(https://www.ncbi.nlm.nih.gov/geo)。选取TCGA-LIHC(374例HCC样本,50例正常样本)用于探索TOP2A及相关基因的表达与预后,并利用GSE41804(20例HCC样本,20例非肿瘤组织样本)和GSE78737(107例HCC样本)数据集进行验证。此外,收集蚌埠医科大学第一附属医院2019年1月至2021年12月存档的HCC组织60例及癌旁组织30例。本研究获得蚌埠医科大学伦理委员会批准(伦科批字[2024]第156号,伦科批字[2025]第310号)。所有患者知情同意。
1.2 方法 1.2.1 TOP2A表达与临床分析利用UALCAN数据库(https://ualcan.path.uab.edu)分析TOP2A mRNA表达与临床特征(分期、分级、TP53突变状态)的相关性及预后价值,并利用GEO数据集(GSE41804、GSE78737)进行外部验证。
1.2.2 免疫组织化学(immunohistochemistry,IHC)采用IHC验证TOP2A蛋白表达。用甲醛固定待检组织,石蜡包埋,切片,进行抗原修复及一抗(1∶200)孵育,DAB显色,苏木素复染。阳性判定标准为染色强度(0~3分)与阳性细胞比例(1~4分)总和 > 3。
1.2.3 TOP2A相关基因筛选与功能分析基于Linked-Omics数据库(https://linkedomics.org),筛选与TOP2A显著相关的差异表达基因(differentially expressed gene,DEG)(|cor| > 0.8,FDR < 0.001),并进行基因本体论(Gene Ontology,GO)和京都基因和基因组数据库(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析。
1.2.4 蛋白质-蛋白质相互作用(protein-protein inte-raction,PPI)网络与Hub基因鉴定利用STRING数据库(https://cn.string-db.org)构建PPI网络,通过Cytoscape软件及4种算法(MCC、MNC、EPC、Degree)筛选前20位基因,进一步取交集确定核心Hub基因。
1.2.5 关键基因筛选与模型构建采用LASSO回归及Cox回归从Hub基因中筛选关键基因,构建风险模型,并通过Kaplan-Meier生存分析和时间依赖性受试者操作特征(receiver operating characteristic,ROC)曲线的曲线下面积(area under the curve,AUC)评估模型预测效能。
1.2.6 多维度基因验证与分析基于TCGA、CPTAC及GEO数据库验证关键基因在mRNA和蛋白水平的表达,分析其与临床病理特征及预后的关系;利用cBioPortal和SangerBox分析基因突变、微卫星不稳定性(microsatellite instability,MSI)及肿瘤突变负荷(tumor mutation burden,TMB)。
1.2.7 免疫浸润与药物敏感性分析使用TIMER数据库(https://cistrome.shinyapps.io/timer/)分析关键基因表达与免疫细胞浸润水平的相关性,通过GSCA平台(https://guolab.wchscu.cn/GSCA/)整合的GDSC与CTRP数据库,评估其与药物敏感性的关系。
1.2.8 分子对接验证从PDB数据库(https://www.rcsb.org)获取TOP2A、TTK、KIF2C蛋白结构,从PubChem获取Sorafenib、Lenvatinib、PD-L1配体结构,利用CB-Dock2平台进行分子对接,评估结合能与相互作用模式。
1.3 统计学分析研究数据来源于TCGA与GEO数据库,统计分析均基于相应数据库平台或R语言(V4.3.1)完成。组间比较采用Mann-Whitney U检验;生存分析采用log-rank检验;相关性分析采用Spearman秩相关;关键基因筛选采用LASSO与Cox回归分析。P < 0.05为差异有统计学意义。
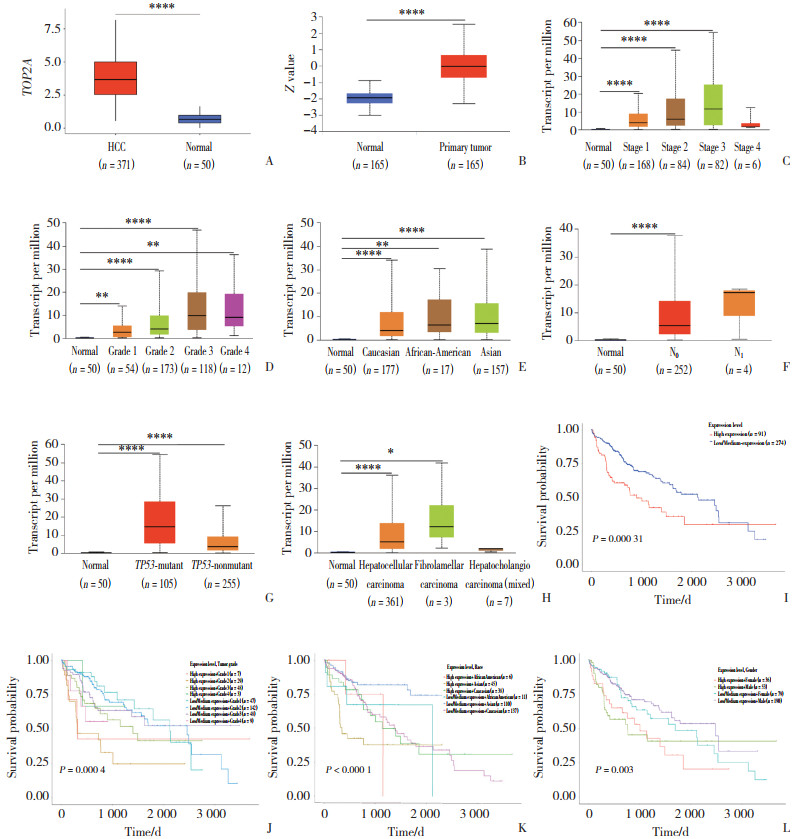
2 结果 2.1 TOP2A的表达与预后UALCAN数据库分析结果显示,TOP2A在HCC组织中高表达(图 1A、1B),且在肿瘤分期晚、组织学分级高、存在TP53突变等临床亚组中的表达水平进一步升高(图 1C~1G);TOP2A的表达在不同的HCC类型间有显著差异(图 1H)。TOP2A高表达组患者的总生存期(overall survival,OS)显著低于低表达组(图 1I~1L)。
|
| A, TOP2A mRNA in HCC vs. normal tissues; B, TOP2A protein in HCC (CPTAC dataset); C, TOP2A mRNA by tumor stage (Ⅰ to Ⅳ); D, TOP2A mRNA by histologic grade (1 to 4);E, TOP2A mRNA by race (Caucasian, African-American, Asian); F, TOP2A mRNA by lymph node metastasis status (N0 vs. N1);G, TOP2A mRNA by TP53 status (wild-type vs. mutant); H, TOP2A mRNA by histologic subtype (HCC, fibrolamellar carcinoma, cholangiocarcinoma); I, correlation between TOP2A expression and overall survival (OS); J, effect of TOP2A expression and tumor grade on OS; K, effect of TOP2A expression and race on OS; L, effect of TOP2A expression and sex on OS. * P < 0.05, ** P < 0.01, **** P < 0.000 1. 图 1 基于TCGA的TOP2A在HCC中的表达及生存分析 Fig.1 Expression and survival analysis of TOP2A in HCC based on TCGA |
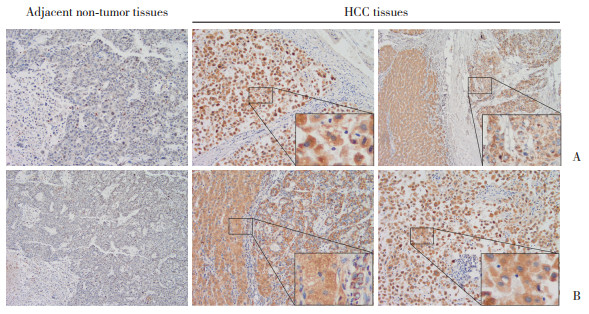
通过GEO数据集(GSE41804和GSE78737)进一步验证了TOP2A在HCC组织中的过表达现象,ROC曲线分析显示其对HCC的诊断效能较高(AUC分别为0.912和0.832)。IHC结果进一步证实了TOP2A蛋白在肿瘤组织中的表达水平显著高于癌旁组织(图 2)。
|
| A, case 1;B, case 2. 图 2 TOP2A在HCC及癌旁组织中的表达IHC ×100 Fig.2 TOP2A protein expression in HCC and adjacent non-tumor tissues IHC ×100 |
2.2 TOP2A相关基因的富集分析
结果显示,KIF18B、BUB1B和KIF23等基因与TOP2A表达呈正相关,而NDUFAF1、CCL14和PINK1等基因则与TOP2A表达呈负相关。GO和KEGG通路富集分析显示,TOP2A及其相关基因在生物过程(biological process,BP)方面主要涉及生物调节、代谢过程以及刺激反应等;在细胞成分(cellular component,CC)方面主要包括细胞膜、细胞核以及膜封闭腔等;在分子功能(molecular function,MF)方面主要涉及蛋白质结合、离子结合以及核酸结合等;在细胞周期、肿瘤相关微RNA、剪接体以及RNA运输等信号通路上存在显著富集。
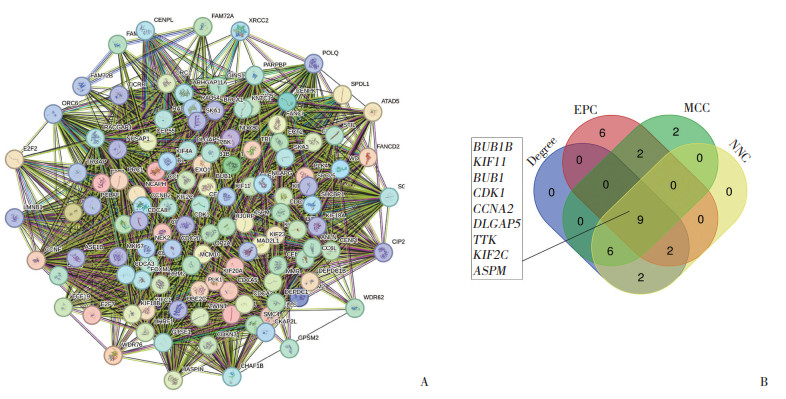
2.3 PPI网络构建及Hub基因确认通过STRING数据库构建PPI网络(图 3A),并通过Cytoscape软件Cytohubba插件识别其中相互作用最广泛的前20位基因。通过VENN图最终确定9个核心Hub基因(BUB1B、KIF11、BUB1、CDK1、CCNA2、DLGAP5、TTK、KIF2C、ASPM,图 3B)。
|
| A, protein-protein interaction (PPI) network from the STRING database; B, Venn diagram illustrating the intersection of the four algorithms, identifying nine core Hub genes. 图 3 PPI网络构建及Hub基因确认 Fig.3 Construction of the protein-protein interaction network and identification of Hub genes |
2.4 关键基因的筛选与确认
LASSO回归分析显示,与HCC预后最相关的关键基因为TTK和KIF2C。基于上述基因构建风险模型,Kaplan-Meier生存分析结果显示,高风险组患者OS显著缩短(P < 0.001)。时间依赖性ROC曲线分析表明,该模型预测3年及5年生存率的AUC分别为0.689和0.745。进一步通过单因素及多因素Cox回归分析验证,TTK和KIF2C被证实是HCC患者的独立预后风险因素(P < 0.05)。
2.5 关键基因验证基于TCGA、CPTAC及GEO数据库对关键基因TTK与KIF2C进行系统验证。结果显示,HCC组织中TTK与KIF2C mRNA及蛋白表达水平均显著高于正常组织。两者的表达量与肿瘤的恶性程度密切相关,在临床分期晚、组织学分级高的HCC中表达量更高。生存分析进一步证实,TTK或KIF2C高表达的HCC患者OS显著缩短,提示其与不良预后密切相关。在GEO外部验证集中,TTK与KIF2C不仅同样呈显著过表达,且诊断效能良好。
2.6 关键基因突变HCC组织中与TTK与KIF2C最相关的共突变基因均为TP53(分别为44.2%与42.5%)与CTNNB1(分别为37.2%与35.8%)。在TCGA队列的372例HCC患者中,TTK与KIF2C本身的突变频率(9%、5%)较低,其突变谱包括错义突变、基因扩增及深度缺失等多种类型。生存分析表明,携带TTK或KIF2C突变的患者,其OS、无进展生存期、疾病特异性生存期及无病生存期均显著缩短(P < 0.05)。此外,TTK与KIF2C的突变状态与MSI呈显著正相关,但与TMB无显著关联。
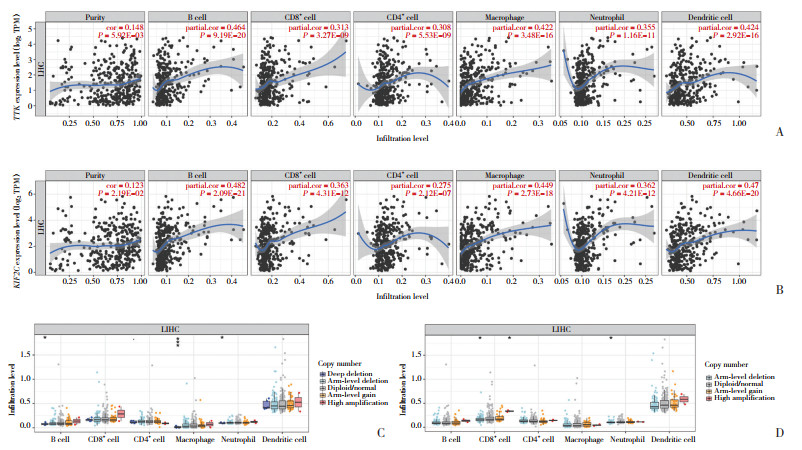
2.7 关键基因与免疫微环境的关联及预后意义TIMER数据库分析结果显示,TTK和KIF2C的表达水平与多种免疫细胞(包括B细胞、CD8+T细胞、CD4+T细胞、巨噬细胞、中性粒细胞和树突状细胞)的浸润水平均呈显著正相关(P < 0.001),而与肿瘤纯度相关性较弱(图 4A、4B)。TTK深度缺失突变会显著降低B细胞、巨噬细胞和中性粒细胞的浸润水平,KIF2C突变导致CD8+T细胞和中性粒细胞的浸润显著减少(图 4C、4D)。生存分析显示,中性粒细胞高浸润或TTK/KIF2C高表达均与患者1年生存率降低显著相关,巨噬细胞高浸润或TTK/KIF2C高表达同样与5年生存率下降密切相关。
|
| A, correlation of TTK expression with tumor purity and immune cell infiltration in HCC; B, correlation of KIF2C expression with tumor purity and immune cell infiltration in HCC; C, impact of TTK copy number alteration (CNA) on immune cell infiltration; D, impact of KIF2C CNA on immune cell infiltration. 图 4 关键基因与免疫细胞的相关性分析 Fig.4 Analysis of the correlation between key genes and immune cells |
2.8 关键基因的药物敏感性
GSCA平台分析结果显示,TTK与KIF2C的表达水平与包括selumetinib在内的13种抗癌药物敏感性呈正相关,而与包括NPK76-II-72-1在内的其他17种药物呈负相关。提示TTK与KIF2C可能作为预测HCC靶向治疗反应的潜在生物标志物。
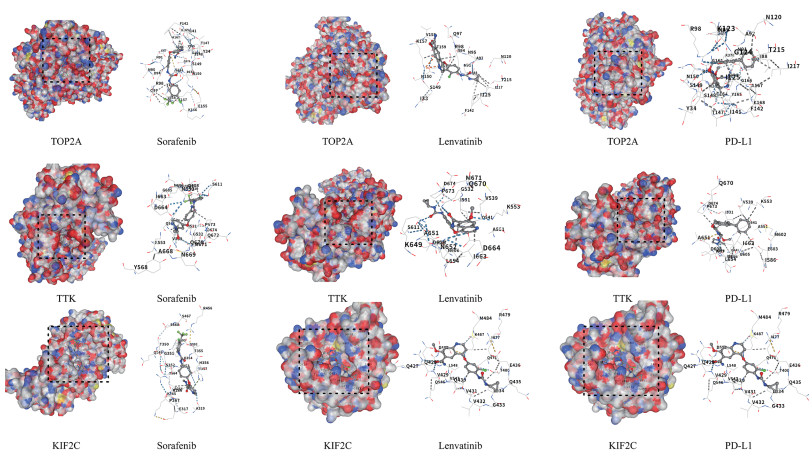
2.9 药物分子对接分析分子对接分析结果显示,Sorafenib、Lenvatinib和PD-L1与TOP2A、TTK、KIF2C这3种靶标蛋白的结合能均 < -7 kcal/mol(表 1),结合模式分析显示,药物与靶标蛋白的关键氨基酸残基形成了稳定的氢键和疏水相互作用(图 5)。
| Drug | TOP2A | TTK | KIF2C |
| Sorafenib | -10.3 | -9.5 | -8.1 |
| Lenvatinib | -9.5 | -8.9 | -8.3 |
| PD-L1 | -9.6 | -8.9 | -7.3 |
|
| Left, binding pockets on receptor proteins (black dashed boxes); right, drug-amino acid residue interactions. Colored dashed lines indicate hydrogen bonds or hydrophobic interactions. 图 5 Sorafenib、Lenvatinib和PD-L1与TOP2A、TTK、KIF2C的分子对接分析 Fig.5 Molecular docking analysis of Sorafenib, Lenvatinib and PD-L1 with TOP2A, TTK and KIF2C |
3 讨论
TOP2A是Ⅱ型DNA拓扑异构酶的关键异构体,在DNA复制和细胞分裂中发挥关键作用。TOP2A在HCC中的高表达及不良预后预测价值已被多项研究证实。CAI等 [15]通过多组学技术证实,TOP2A在HCC组织中表达显著上调,并将其确立为独立的预后危险因子。WANG等[16]则进一步揭示其通过调控CHK1磷酸化推动细胞周期进程与上皮-间质转化。此外,竞争性内源RNA机制研究[17-18]亦发现多个长链非编码RNA可通过竞争性结合miR-139-5p调控TOP2A表达,进而影响HCC进展与免疫微环境。然而,这些研究多聚焦于TOP2A的单基因功能,TOP2A作为关键调控因子,如何通过构建核心基因网络协同驱动HCC进展及免疫微环境重塑仍未明确。本研究创新性地从基因网络视角出发,构建了以TOP2A为核心的相互作用网络,并筛选出2个关键基因TTK与KIF2C,明确了它们在HCC中的关键地位。本研究还发现TOP2A在HCC中呈显著高表达,并与不良预后紧密相关,模型构建与药物敏感性分析结果共同提示,靶向TOP2A-TTK-KIF2C基因网络在HCC治疗中有重要潜力。
TTK是有丝分裂纺锤体装配检查点的主要成分,可磷酸化苏氨酸、丝氨酸和酪氨酸,从而调节细胞周期,确保有丝分裂的顺利进行。LIANG等[19]报道TTK在绝大多数肿瘤样本中表达升高,且突变事件罕见;CHOI等 [20]基于TCGA队列分析,进一步明确了TTK高表达与HCC患者OS缩短显著相关。另有研究[21]显示,TTK在HCC中的高风险评分与肿瘤分期、病理分级和OS显著相关。KIF2C又称有丝分裂着丝粒相关驱动蛋白,通过促进微管解聚参与纺锤体组装与染色体分离。KIF2C还可通过激活mTORC1与Wnt/β-catenin信号通路,促进肿瘤细胞增殖、迁移与侵袭,是影响HCC患者预后的独立危险因素[22]。这些证据共同提示,TTK与KIF2C可作为HCC潜在的治疗靶点。
本研究进一步揭示了TOP2A网络中的关键组分TTK与KIF2C的高表达与多种免疫细胞(包括CD8+ T细胞、B细胞、巨噬细胞等)浸润水平呈正相关,鉴于二者在有丝分裂调控中的核心作用,推测这种相关性可能源于其功能异常所引发的次级效应。TTK/KIF2C介导的染色体不稳定性可能增加TMB与新抗原产生,从而募集T细胞等效应免疫细胞[23];同时,异常活跃的细胞周期信号可能上调特定趋化因子(如CXCLs、CCLs)的表达,直接参与免疫微环境塑造[24]。提示TOP2A可能通过协调其网络成员TTK与KIF2C的表达,在更深层次上影响HCC免疫微环境的组成与功能状态。HCC免疫微环境由多种免疫细胞构成,它们在免疫监视与免疫逃逸中扮演关键角色[25]。本研究结果进一步支持以TOP2A为核心的基因网络在协调HCC进展与免疫应答中的重要作用,与JIANG等[26]的研究一致。尽管CD8+ T细胞浸润通常与较好预后相关[27],在TOP2A网络异常激活的背景下,其伴随的免疫浸润可能反映了一种代偿性抗肿瘤免疫与免疫抑制并存的复杂状态。TTK与KIF2C的突变亦会改变免疫细胞浸润模式,可能通过影响免疫细胞功能及肿瘤微环境组成而促进免疫逃逸[28]。生存分析显示,中性粒细胞高浸润与患者1年生存率下降相关,提示其在肿瘤早期可能通过促血管生成等机制加速疾病进展[29]。巨噬细胞高浸润则与5年生存率降低显著相关,表明肿瘤相关巨噬细胞可能通过分泌转化生长因子β、血管内皮生长因子、白细胞介素-10等因子,促进肿瘤的增殖、血管生成、转移并介导免疫抑制,在长期病程中导致不良预后[30]。这些发现提示,靶向TOP2A-TTK-KIF2C调控轴或其下游的免疫相关通路可能成为重塑HCC免疫微环境的新策略。
本研究首次揭示了TTK和KIF2C基因表达水平与特定药物敏感性的相关性。结果显示,二者高表达与药物敏感性呈负相关,提示其过表达可能降低治疗效果。这为未来研究基因对药物敏感性的影响提供了重要依据。
本研究通过整合多组学数据与实验验证,首次系统阐释了TOP2A-TTK-KIF2C基因网络在HCC中的重要作用。该调控网络在HCC中异常激活,其关键组分TTK和KIF2C不仅与患者不良预后显著相关,还通过影响免疫细胞浸润和药物敏感性,参与肿瘤恶性进展,可作为HCC潜在的新型生物标志物和治疗靶点,为临床诊疗提供新的思路。
| [1] |
LLOVET JM, KELLEY RK, VILLANUEVA A, et al. Hepatocellular carcinoma[J]. Nat Rev Dis Primers, 2021, 7: 6. DOI:10.1038/s41572-020-00240-3 |
| [2] |
SUNG H, FERLAY J, SIEGEL RL, et al. Global cancer statistics 2020:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [3] |
吴景, 姜玉, 毕京浩, 等. 2002-2019年上海市长宁区肝癌伤残调整寿命年的趋势分析[J]. 中国肿瘤, 2023, 32(9): 683-690. DOI:10.11735/j.issn.1004-0242.2023.09.A006 |
| [4] |
GAO Q, ZHU HW, DONG LQ, et al. Integrated proteogenomic cha- racterization of HBV-related hepatocellular carcinoma[J]. Cell, 2019, 179(2): 561-577. e22. DOI:10.1016/j.cell.2019.08.052 |
| [5] |
YANG JD, HAINAUT P, GORES GJ, et al. A global view of hepatocellular carcinoma: trends, risk, prevention and management[J]. Nat Rev Gastroenterol Hepatol, 2019, 16(10): 589-604. DOI:10.1038/s41575-019-0186-y |
| [6] |
MAN SL, LUO C, YAN MY, et al. Treatment for liver cancer: from sorafenib to natural products[J]. Eur J Med Chem, 2021, 224: 113690. DOI:10.1016/j.ejmech.2021.113690 |
| [7] |
VOGEL A, MEYER T, SAPISOCHIN G, et al. Hepatocellular carcinoma[J]. Lancet, 2022, 400(10360): 1345-1362. DOI:10.1016/S0140-6736(22)01200-4 |
| [8] |
WANG K, JIANG XL, JIANG Y, et al. EZH2-H3K27me3-mediated silencing of mir-139-5p inhibits cellular senescence in hepatocellular carcinoma by activating TOP2A[J]. J Exp Clin Cancer Res, 2023, 42(1): 320. DOI:10.1186/s13046-023-02855-2 |
| [9] |
马俊杰, 安韶光, 梅静宇, 等. 肾透明细胞癌中拓扑异构酶Ⅱα与免疫浸润的关系及相关基因分析[J]. 中国医科大学学报, 2023, 52(10): 871-878. DOI:10.12007/j.issn.0258-4646.2023.10.002 |
| [10] |
KOU F, SUN HF, WU L, et al. TOP2A promotes lung adenocarcinoma cells' malignant progression and predicts poor prognosis in lung adenocarcinoma[J]. J Cancer, 2020, 11(9): 2496-2508. DOI:10.7150/jca.41415 |
| [11] |
DE RESENDE MF, VIEIRA S, CHINEN LTD, et al. Prognostication of prostate cancer based on TOP2A protein and gene assessment: TOP2A in prostate cancer[J]. J Transl Med, 2013, 11: 36. DOI:10.1186/1479-5876-11-36 |
| [12] |
MENG JL, WEI YC, DENG Q, et al. Study on the expression of TOP2A in hepatocellular carcinoma and its relationship with patient prognosis[J]. Cancer Cell Int, 2022, 22(1): 29. DOI:10.1186/s12935-021-02439-0 |
| [13] |
WU ZH, YANG DL, WANG L, et al. Epigenetic and immune-cell infiltration changes in the tumor microenvironment in hepatocellular carcinoma[J]. Front Immunol, 2021, 12: 793343. DOI:10.3389/fimmu.2021.793343 |
| [14] |
LU J, MA J, YU C, et al. Identification of the key gene for hepato- cellular carcinoma based on bioinformatics and machine learning and experimental verification[J]. Transl Cancer Res, 2025, 14(11): 7995-8011. DOI:10.21037/tcr-2025-1067 |
| [15] |
CAI HY, ZHU XH, QIAN F, et al. High expression of TOP2A gene predicted poor prognosis of hepatocellular carcinoma after radical hepatectomy[J]. Transl Cancer Res, 2020, 9(2): 983-992. DOI:10.21037/tcr.2019.12.46 |
| [16] |
WANG T, LU J, WANG RR, et al. TOP2A promotes proliferation and metastasis of hepatocellular carcinoma regulated by miR-144-3p[J]. J Cancer, 2022, 13(2): 589-601. DOI:10.7150/jca.64017 |
| [17] |
WANG XQ, LI LL, LOU P, et al. Noval CeRNA axis-mediated high expression of TOP2A correlates with poor prognosis and tumor immune infiltration of hepatocellular carcinoma[J]. Transl Cancer Res, 2023, 12(12): 3486-3502. DOI:10.21037/tcr-23-755 |
| [18] |
卢兴浩, 俞鹏, 陶恒, 等. 拓扑异构酶Ⅱα (TOP2A) 基因的表达与CD4+ T细胞在肝细胞癌中的数量相关性及临床预后意义[J]. 细胞与分子免疫学杂志, 2022, 38(1): 24-31. DOI:10.13423/j.cnki.cjcmi.009283 |
| [19] |
LIANG XD, DAI YC, LI ZY, et al. Expression and function analysis of mitotic checkpoint genes identifies TTK as a potential therapeutic target for human hepatocellular carcinoma[J]. PLoS One, 2014, 9(6): e97739. DOI:10.1371/journal.pone.0097739 |
| [20] |
CHOI M, MIN YH, PYO J, et al. TC Mps112, a novel Mps1 inhibitor, suppresses the growth of hepatocellular carcinoma cells via the accumulation of chromosomal instability[J]. Br J Pharmacol, 2017, 174(12): 1810-1825. DOI:10.1111/bph.13782 |
| [21] |
WANG T, DAI LQ, SHEN S, et al. Comprehensive molecular analyses of a macrophage-related gene signature with regard to prognosis, immune features, and biomarkers for immunotherapy in hepatocellular carcinoma based on WGCNA and the LASSO algorithm[J]. Front Immunol, 2022, 13: 843408. DOI:10.3389/fimmu.2022.843408 |
| [22] |
WEI S, DAI MM, ZHANG C, et al. KIF2C: a novel link between Wnt/β-catenin and mTORC1 signaling in the pathogenesis of hepatocellular carcinoma[J]. Protein Cell, 2021, 12(10): 788-809. DOI:10.1007/s13238-020-00766-y |
| [23] |
SCHUMACHER TN, SCHREIBER RD. Neoantigens in cancer immunotherapy[J]. Science, 2015, 348(6230): 69-74. DOI:10.1126/science.aaa4971 |
| [24] |
NAGARSHETH N, WICHA MS, ZOU WP. Chemokines in the cancer microenvironment and their relevance in cancer immunothe- rapy[J]. Nat Rev Immunol, 2017, 17(9): 559-572. DOI:10.1038/nri.2017.49 |
| [25] |
沈锋, 林间, 王海波. 肝细胞癌免疫微环境研究进展及未来方向[J]. 中国实用外科杂志, 2021, 41(1): 42-47. DOI:10.19538/j.cjps.issn1005-2208.2021.01.06 |
| [26] |
JIANG Y, LIN LJ, LV HM, et al. Immune cell infiltration and immunotherapy in hepatocellular carcinoma[J]. Math Biosci Eng, 2022, 19(7): 7178-7200. DOI:10.3934/mbe.2022339 |
| [27] |
LIU GJ, WU DM, WEN YY, et al. Immune-associated molecular occurrence and prognosis predictor of hepatocellular carcinoma: an integrated analysis of GEO datasets[J]. Bioengineered, 2021, 12(1): 5253-5265. DOI:10.1080/21655979.2021.1962147 |
| [28] |
DONG LQ, PENG LH, MA LJ, et al. Heterogeneous immunogenomic features and distinct escape mechanisms in multifocal hepatocellular carcinoma[J]. J Hepatol, 2020, 72(5): 896-908. DOI:10.1016/j.jhep.2019.12.014 |
| [29] |
SANGHERA C, TEH JJ, PINATO DJ. The systemic inflammatory response as a source of biomarkers and therapeutic targets in hepatocellular carcinoma[J]. Liver Int, 2019, 39(11): 2008-2023. DOI:10.1111/liv.14220 |
| [30] |
魏芳, 宗世烨, 周静, 等. 肿瘤相关巨噬细胞通过诱导肝癌细胞自噬降低索拉菲尼的促凋亡作用[J]. 南方医科大学学报, 2019, 39(3): 264-270. DOI:10.12122/j.issn.1673-4254.2019.03.02 |
 2026, Vol. 55
2026, Vol. 55