文章信息
- 吴培, 李东东, 杜雨楠, 张希倩, 刘亚楠, 夏楠楠
- WU Pei, LI Dongdong, DU Yunan, ZHANG Xiqian, LIU Yanan, XIA Nannan
- 血竭提取物通过激活caspase-3/GSDME信号通路诱导人食管癌细胞焦亡
- Sanguis Draconis extract induces pyroptosis in human esophageal cancer cells by activating the caspase-3/GSDME signaling pathway
- 中国医科大学学报, 2026, 55(4): 301-307
- Journal of China Medical University, 2026, 55(4): 301-307
-
文章历史
- 收稿日期:2025-03-17
- 网络出版时间:2026-04-15 11:19:05
2. 河南省中医院(河南中医药大学第二附属医院)肿瘤科, 郑州 450053;
3. 河南省中医院(河南中医药大学第二附属医院)消化内科, 郑州 450053
2. Department of Oncology, Henan Provincial Hospital of Traditional Chinese Medicine (The Second Affiliated Hospital of Henan University of Chinese Medicine), Zhengzhou 450053, China;
3. Department of Gastroenterology, Henan Provincial Hospital of Traditional Chinese Medicine (The Second Affiliated Hospital of Henan University of Chinese Medicine), Zhengzhou 450053, China
食管癌是全球最常见的恶性肿瘤之一。目前,手术、化疗和联合治疗是食管癌常用的治疗方法,然而食管癌患者总体5年生存率仍然不足20%[1-2]。越来越多的研究表明[3-5]细胞焦亡在癌症的发生和治疗中起着重要作用。因此,开发新的药物来调控细胞焦亡对于食管癌的治疗意义重大。血竭提取物(Sanguis Draconis extract,SDE)是从中药血竭中提取的,以血竭为主要成分。已有研究[6]报道,以血竭为主要药物成分的通道开结丸可降低食管癌患者肿瘤标志物水平,提升患者生存质量。研究[7]显示,激活天冬氨酸特异性半胱氨酸蛋白酶-3(cysteinyc aspartate specific protease-3,caspase-3)/消皮素E(gasdermin E,GSDME)信号通路可诱导食管癌细胞焦亡。SDE是否通过调控caspase-3/GSDME信号通路影响食管癌细胞焦亡尚不明确。本研究探讨SDE对食管癌细胞焦亡的影响及作用机制。
1 材料与方法 1.1 细胞与主要试剂人食管癌细胞系(EC109)购自通派(上海)生物科技有限公司。培养时采用含10%胎牛血清的RPMI 1640培养基,置于37℃、5%CO2、饱和湿度的CO2培养箱中培养,培养箱放置于平稳通风、远离阳光直射及热源的无菌实验区域,定期更换培养基以维持细胞正常生长,传代时采用胰酶消化法,严格遵循无菌操作规范。主要试剂包括:SDE(西安千草生物技术有限公司);caspase-3抑制剂(Ac-DEVD-CHO,美国MedChemExpress公司);CCK-8试剂盒(武汉艾迪抗生物科技有限公司);Hoechst 33342-碘化丙啶(propidium iodide,PI)试剂盒(上海时代生物科技有限公司);乳酸脱氢酶(lactate dehydrogenase,LDH)细胞毒性检测试剂盒(上海玉博生物科技有限公司);2’,7’-二氯二氢荧光素二乙酸酯(2’,7’-dichlorodihydrofluorescein diacetate,DCFH-DA,北京普西唐生物科技有限公司);兔源一抗裂解的天冬氨酸特异性半胱氨酸蛋白酶-3(cleaved cysteinyl aspartate specific proteinase-3,cleaved caspase-3)、GSDME的N端片段(N-terminal fragment of gasdermin E,GSDME-N)、白细胞介素(interleukin,IL)-1β、IL-18,辣根过氧化物酶标记的山羊抗兔IgG二抗(英国abcam公司)。
1.2 方法 1.2.1 利用网络药理学获取血竭活性成分、细胞焦亡潜在的基因靶点利用Herb数据库(http://herb.ac.cn/v2)获取血竭的活性成分,通过Swiss tareget数据库(http://www.swisstargetprediction.ch)获取血竭活性成分的潜在基因靶点。以“pyroptosis”为关键词,通过Genecard数据库(https://www.genecards.org/)获取细胞焦亡的潜在基因靶点,利用Venny 2.1在线软件(https://bioinfogp.cnb.csic.es/tools/venny/index.html)获取交集靶点后,用Cytoscapse软件制作血竭-活性成分-基因靶点关系图。将交集靶点导入STRING在线数据分析(https://string-db.org/)平台,得到交集靶点的蛋白质-蛋白质相互作用图,筛选度值≥28的核心靶点进行基因本体论(Gene Ontology,GO)和京都基因与基因组数据库(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析。
1.2.2 细胞分组将EC109细胞分为低、中、高浓度SDE组(用15、30、60 mg/L SDE处理细胞48 h[8]),Ac-DEVD-CHO组(用15 μmol/L Ac-DEVD-CHO处理细胞48 h[9]),高浓度SDE +Ac-DEVD-CHO组(用60 mg/L SDE和15 μmol/L Ac-DEVD-CHO共同处理细胞48 h),对照组(未处理)。
1.2.3 各组细胞活力检测将各组细胞按照1×104/孔接种在96孔板中。每孔加入10 μL CCK-8溶液,并在培养箱中孵育2 h。使用酶标仪在450 nm处检测各孔光密度(optical density,OD)值,并计算细胞活力。细胞活力(%)=(OD处理组-OD空白组)/(OD对照组-OD空白组)×100。
1.2.4 各组细胞焦亡情况使用扫描电镜观察各组细胞焦亡形态变化。
1.2.5 Hoechst 33342-PI染色检测各组细胞中PI阳性率将各组细胞按照1×106/孔接种于6孔板中,向各孔加等量的Hoechst 33342-PI染色液(1 mL Hoechst 33342-PI染色液含5 μL Hoechst染色液和5 μL PI染色液)孵育30 min后,观察图像并计算PI阳性率,PI阳性率(%)=PI阳性细胞数/ Hoechst 33342阳性细胞数×100。
1.2.6 各组细胞上清液中LDH水平检测收集各组细胞上清液,使用LDH细胞毒性检测试剂盒检测上清液中LDH水平,按照试剂盒说明书进行操作。
1.2.7 DCFH-DA法检测各组细胞中活性氧(reactive oxygen species,ROS)相对荧光强度将各组细胞与10 μmoL DCFH-DA在37 ℃下孵育20 min,然后洗涤2次。使用倒置荧光显微镜观察细胞中ROS相对荧光强度。
1.2.8 各组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达检测使用RIPA裂解试剂从各组细胞中提取总蛋白,采用BCA法对蛋白进行定量。取30 μg蛋白进行电泳分离,然后以电子方式转移到PVDF膜上。随后,在室温下用5%脱脂牛奶封闭膜1 h,加入一抗cleaved caspase-3(1∶5 000)、GSDME-N(1∶3 000)、IL-1β(1∶2 000)、GAPDH(1∶5 000)、IL-18(1∶1 000)4 ℃下孵育过夜。然后洗涤膜3次,并与二抗(1∶4 000)在室温下孵育3 h。ECL试剂用于可视化蛋白条带,使用ImageJ软件分析蛋白相对表达量。
1.3 统计学分析使用GraphPad Prism 9.0软件进行统计分析。计量资料采用x±s表示,多组间比较使用单因素方差分析,然后使用SNK-q事后检验。P < 0.05为差异有统计学意义。
2 结果 2.1 网络药理学分析结果利用Herb数据库对血竭(编号为HERB006290)的主要成分进行查询,结合PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)显示,血竭中具有Canonical SMILES结构的主要成分为(2s)-5-methoxy-6-methyl-flavan-7-ol、(2s)-5-methoxy-flavan-7-ol、4-dihydroxy-6-methoxy-chalcone、abietic acid、dehydroa-bietic acid、dracorhodin、dracorubin、isopimaric acid、nordracorhodin、nordracorubin、oleanolic acid、oleano-nic aldehyde、pimaric acid、sandaracopimaric acid、ursonic aldehyde 15种,其对应的基因靶点去冗余后共439个。细胞焦亡基因靶点共885个,二者交集靶点53个。通过Cytoscape软件制作血竭-主要成分-基因靶点图。
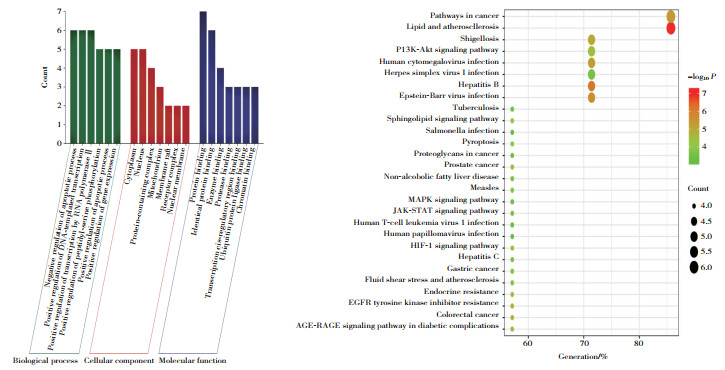
2.2 蛋白质-蛋白质相互作用及GO、KEGG富集分析将53个交集靶点导入STRING在线数据分析平台,得到交集靶点蛋白质-蛋白质相互作用图。根据度值≥28筛选出核心靶点7个,包括AKT1、TNF、IL6、TP53、EGFR、PPARG、BCL2。GO和KEGG富集分析结果显示,GO富集中生物过程有115条途径,细胞成分有7条途径,分子功能有16条途径;KEGG富集94条途径,选择Count值排名靠前进行可视化,其中,caspase-3/GSDME通路参与焦亡途径。见图 1。
|
| 图 1 GO和KEGG富集分析 Fig.1 GO and KEGG enrichment analysis |
2.3 SDE对各组细胞活力的影响
结果显示,对照组,低、中、高浓度SDE组,Ac-DEVD-CHO组和高浓度SDE+Ac-DEVD-CHO组细胞活力分别为(100.00±0.00)%、(86.65±4.19)%、(75.58±3.34)%、(52.28±2.16)%、(116.67±5.02)%、(77.76±3.15)%。与对照组相比,低、中、高浓度SDE组细胞活力显著降低(P < 0.05);而Ac-DEVD-CHO组细胞活力显著升高(P < 0.05)。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞活力显著升高(P < 0.05)。
2.4 SDE对各组细胞焦亡形态的影响与对照组相比,低、中、高浓度SDE组出现胀大破裂等焦亡特征的细胞增多;而Ac-DEVD-CHO组出现胀大破裂等焦亡特征的细胞减少。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组出现胀大破裂等焦亡特征的细胞减少,见图 2。

|
| A, control group; B, low-concentration SDE group; C, medium-concentration SDE group; D, high-concentration SDE group; E, Ac-DEVD-CHO group; F, high-concentration SDE + Ac-DEVD-CHO group. 图 2 各组细胞焦亡形态比较×10 000 Fig.2 Comparison of pyroptosis morphology in cells of each group ×10 000 |
2.5 SDE对各组细胞中PI阳性率的影响
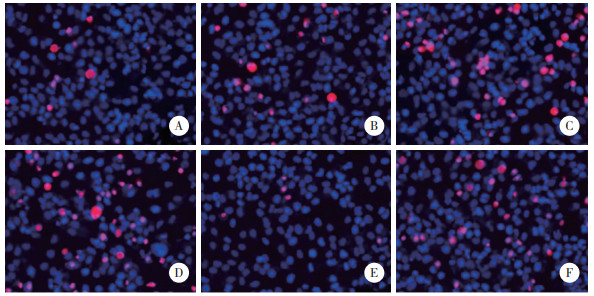
结果显示,对照组,低、中、高浓度SDE组,Ac-DEVD-CHO组和高浓度SDE+Ac-DEVD-CHO组细胞中PI阳性率分别为(5.15±0.12)%、(10.66±0.43)%、(23.19±1.13)%、(41.68±2.08)%、(3.02±0.12)%、(18.54±0.81)%。与对照组相比,低、中、高浓度SDE组细胞中PI阳性率显著升高(P < 0.05);而Ac-DEVD-CHO组细胞中PI阳性率显著降低(P < 0.05)。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞中PI阳性率显著降低(P < 0.05),见图 3。
|
| A, control group; B, low-concentration SDE group; C, medium-concentration SDE group; D, high-concentration SDE group; E, Ac-DEVD-CHO group; F, high-concentration SDE + Ac-DEVD-CHO group. 图 3 Hoechst 33342-PI染色检测各组细胞PI阳性率×200 Fig.3 Detection of PI positive rate in cells of each group by Hoechst 33342-PI staining ×200 |
2.6 SDE对各组细胞上清液中LDH水平的影响
结果显示,对照组,低、中、高浓度SDE组,Ac-DEVD-CHO组和高浓度SDE+Ac-DEVD-CHO组细胞上清液中LDH水平分别为(123.36±5.89)U/L、(178.83±8.52)U/L、(267.55±12.29)U/L、(335.57±16.65)U/L、(98.85±4.12)U/L、(232.56±10.58)U/L。与对照组相比,低、中、高浓度SDE组细胞上清液中LDH水平显著升高(P < 0.05);而Ac-DEVD-CHO组细胞上清液中LDH水平显著降低(P < 0.05)。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞上清液中LDH水平显著降低(P < 0.05)。
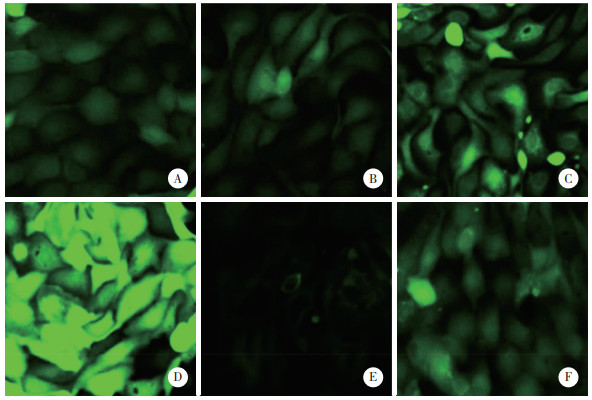
2.7 SDE对各组细胞中ROS相对荧光强度的影响结果显示,对照组,低、中、高浓度SDE组,Ac-DEVD-CHO组和高浓度SDE+Ac-DEVD-CHO组细胞中ROS相对荧光强度分别为1.00±0.00、1.84±0.27、3.61±0.35、7.23±0.32、0.39±0.02、2.78±0.16。与对照组相比,低、中、高浓度SDE组细胞中ROS相对荧光强度显著升高(P < 0.05);而Ac-DEVD-CHO组细胞中ROS相对荧光强度显著降低(P < 0.05)。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞中ROS相对荧光强度显著降低(P < 0.05),见图 4。
|
| A, control group; B, low-concentration SDE group; C, medium-concentration SDE group; D, high-concentration SDE group; E, Ac-DEVD-CHO group; F, high-concentration SDE + Ac-DEVD-CHO group. 图 4 各组细胞中ROS水平的免疫荧光检测结果×400 Fig.4 Results of ROS levels in cells of each group by immunofluorescence detection ×400 |
2.8 SDE对各组细胞中caspase-3/GSDME信号通路相关蛋白表达的影响
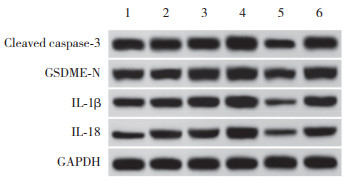
结果显示,与对照组相比,低、中、高浓度SDE组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达显著升高(P < 0.05);而Ac-DEVD-CHO组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达显著降低(P < 0.05)。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达显著降低(P < 0.05),见图 5、表 1。
|
| 1, control group; 2, low-concentration SDE group; 3, medium-concentration SDE group; 4, high-concentration SDE groups; 5, Ac-DEVD-CHO group; 6, high-concentration SDE +Ac-DEVD-CHO group. 图 5 Western blotting检测各组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达 Fig.5 Expression of cleaved caspase-3, GSDME-N, IL-1β, and IL-18 proteins in cells of each group by Western blotting |
| Group | n | Cleaved caspase-3 | GSDME-N | IL-1β | IL-18 |
| Control | 6 | 0.87±0.07 | 0.58±0.04 | 0.39±0.03 | 0.21±0.01 |
| Low-concentration SDE | 6 | 0.98±0.081) | 0.75±0.061) | 0.52±0.051) | 0.32±0.021) |
| Medium-concentration SDE | 6 | 1.23±0.111),2) | 0.94±0.081),2) | 0.79±0.061),2) | 0.46±0.041),2) |
| High-concentration SDE | 6 | 1.79±0.141),2),3) | 1.32±0.131),2),3) | 1.13±0.111),2),3) | 0.85±0.071),2),3) |
| Ac-DEVD-CHO | 6 | 0.61±0.051) | 0.40±0.031) | 0.19±0.011) | 0.10±0.011) |
| High-concentration SDE +Ac-DEVD-CHO | 6 | 1.13±0.104) | 0.81±0.074) | 0.60±0.054) | 0.36±0.034) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. low-concentration SDE group;3)P < 0.05 vs. medium-concentration SDE group;4)P < 0.05 vs. high-concentration SDE group. | |||||
3 讨论
细胞焦亡是一种非传统的程序性细胞死亡,其特征是在质膜上形成孔隙,导致细胞增大和质膜破坏,进而导致细胞内容物(LDH等)渗出[10-11]。因此,诱导细胞焦亡可能是治疗食管癌的一种新策略。网络药理学分析结果显示,血竭与细胞焦亡相关的交集靶点共53个,提示血竭可能通过调控这些靶点作用于细胞焦亡通路。本研究中,与对照组相比,低、中、高浓度SDE组细胞活力降低,表现出胀大破裂等焦亡特征的细胞增多,PI阳性率及细胞上清液中LDH水平升高,且SDE浓度越高趋势越明显,表明SDE可诱导EC109细胞焦亡。此外,有研究[12]显示,ROS过量产生可能导致氧化还原失衡和氧化应激,从而诱导食管癌细胞焦亡。本研究中低、中、高浓度SDE组EC109细胞中ROS相对荧光强度高于对照组,表明SDE诱导EC109细胞焦亡的机制与ROS介导的氧化应激有关,与以往研究结果一致。提示SDE可能是治疗食管癌的潜在有效药物。以往研究结果显示,含有血竭的通道开结丸治疗食管癌疗效显著[13];以血竭为主要成分的通道开结丸可以改善食管癌患者消化道反应,且不增加肝肾功能损害[14]。本研究的结果与其一致,表明SDE具有抗食管癌作用。
caspase-3/GSDME信号通路是细胞焦亡的经典通路,与本研究KEGG富集分析结果中的焦亡途径相对应,提示caspase-3/GSDME信号通路可能参与SDE调控细胞焦亡。caspase-3裂解GSDME可释放GSDME-N结构域,该结构域也通过促进膜孔的形成诱导细胞焦亡,释放促炎性细胞因子IL-1β、IL-18[15-16]。研究显示,激活caspase-3/GSDME信号通路可诱导肺癌、胃癌细胞焦亡[17-18]。本研究结果显示,与对照组相比,低、中、高浓度SDE组细胞中cleaved caspase-3、GSDME-N、IL-1β、IL-18蛋白表达显著升高,细胞焦亡现象明显,推测SDE可能通过诱导细胞焦亡而发挥抗食管癌作用。本研究用caspase-3抑制剂Ac-DEVD-CHO干预高浓度SDE处理的EC109细胞来验证,结果显示,Ac-DEVD-CHO逆转了高浓度SDE对EC109细胞焦亡的促进作用。与高浓度SDE组相比,高浓度SDE+Ac-DEVD-CHO组细胞活力升高,焦亡细胞比例、LDH及ROS水平均显著下降。这一方面证实了SDE通过激活caspase-3/GSDME信号通路诱导EC109细胞焦亡,另一方面也提示,在SDE处理导致的焦亡作用下,抑制caspase-3活性可能通过阻断细胞死亡程序而产生短暂的促细胞存活效应。此外,单独使用Ac-DEVD-CHO处理时,GSDME-N的表达水平亦低于对照组。这提示在EC109细胞的基础水平下,可能存在一定程度的caspase-3基础活性,介导了部分GSDME的切割,而Ac-DEVD-CHO通过抑制该基础活性,使GSDME-N进一步回落至低于对照组的水平。这一现象印证了基础水平的GSDME-N产生也依赖于caspase-3。这进一步强调了caspase-3在焦亡过程中的核心地位。
综上所述,SDE可能通过激活caspase-3/GSDME信号通路诱导EC109细胞焦亡,本研究为食管癌的治疗提供了新的参考依据。SDE对食管癌具有一定的抗癌作用,但未在动物体内进行实验验证,后续将继续深入探究。
| [1] |
南海峰, 何明, 李海霞, 等. STAT3调控P13K/Akt信号通路对食管癌细胞增殖、侵袭、迁移的影响[J]. 中国免疫学杂志, 2023, 39(11): 2343-2347. DOI:10.3969/j.issn.1000-484X.2023.11.017 |
| [2] |
ZHU X, HUANG NN, JI Y, et al. Brusatol induces ferroptosis in oesophageal squamous cell carcinoma by repressing GSH synthesis and increasing the labile iron pool via inhibition of the NRF2 pathway[J]. Biomedecine Pharmacother, 2023, 167: 115567. DOI:10.1016/j.biopha.2023.115567 |
| [3] |
HSU SK, LI CY, LIN IL, et al. Inflammation-related pyroptosis, a novel programmed cell death pathway, and its crosstalk with immune therapy in cancer treatment[J]. Theranostics, 2021, 11(18): 8813-8835. DOI:10.7150/thno.62521 |
| [4] |
HUANG Y, WANG JW, HUANG J, et al. Pyroptosis, a target for cancer treatment[J]. Apoptosis, 2022, 27(1/2): 1-13. DOI:10.1007/s10495-021-01703-y |
| [5] |
王珏, 何欣, 徐忠玲, 等. miR-651-3p调控乳腺癌细胞中免疫抑制因子IL-10与TGFβ1表达的机制研究[J]. 免疫学杂志, 2023, 39(12): 1050-1057. DOI:10.13431/j.cnki.immunol.j.20230125 |
| [6] |
李吉磊, 李洪霖, 许彦超, 等. 消痰化瘀通噎颗粒配合通道开结丸联合化疗治疗食管癌的临床疗效研究[J]. 中国全科医学, 2023, 26(30): 3759-3764. DOI:10.12114/j.issn.1007-9572.2023.0185 |
| [7] |
WU AL, LI ZY, WANG YL, et al. Recombinant measles virus vaccine rMV-Hu191 exerts an oncolytic effect on esophageal squamous cell carcinoma via caspase-3/GSDME-mediated pyroptosis[J]. Cell Death Discov, 2023, 9(1): 171. DOI:10.1038/s41420-023-01466-2 |
| [8] |
黄惠铭, 田颖颖, 庞道然, 等. 血竭石油醚提取物对人胃癌HGC-27和MGC-803细胞的抗肿瘤作用[J]. 中国实验方剂学杂志, 2022, 28(1): 85-91. DOI:10.13422/j.cnki.syfjx.20212124 |
| [9] |
骆长亮, 张秋红, 孙林春. Caspase-3抑制剂所致氧化应激状态下肾小管上皮细胞差异表达基因的筛选及功能验证[J]. 南京医科大学学报(自然科学版), 2023, 43(1): 17-26. DOI:10.7655/NYDXBNS20230103 |
| [10] |
WANG HG, WANG D, SARFRAZ M, et al. Endogenous hydrogen sulfide inhibition suppresses tumor growth by promoting apoptosis and pyroptosis in esophageal cancer cells[J]. Transl Oncol, 2023, 38: 101770. DOI:10.1016/j.tranon.2023.101770 |
| [11] |
汤宏超, 郑曦, 张玲阁, 等. CB-103通过ROS/caspase-3/GSDME信号通路对口腔鳞状细胞癌细胞焦亡的影响[J]. 中国医科大学学报, 2025, 54(6): 553-558. DOI:10.12007/j.issn.0258-4646.2025.06.013 |
| [12] |
TANG D, ZHENG YC, WANG GZ, et al. HPV18 E6 inhibits α-ketoglutarate-induced pyroptosis of esophageal squamous cell carcinoma cells via the P53/MDH1/ROS/GSDMC pathway[J]. FEBS Open Bio, 2023, 13(8): 1522-1535. DOI:10.1002/2211-5463.13666 |
| [13] |
李吉磊. 消痰化瘀通噎颗粒配合通道开结丸联合化疗治疗Ⅲ-Ⅳ期痰瘀互结型食管癌的临床观察[D]. 郑州: 河南中医药大学, 2021.
|
| [14] |
郭军辉, 王园园, 朱甜甜, 等. 中药联合化疗治疗痰气交阻型食管癌的临床观察[J]. 中医肿瘤学杂志, 2022, 4(2): 13-19. DOI:10.19811/j.cnki.ISSN2096-6628.2022.03.003 |
| [15] |
PAN TT, JIN SQ, HUANG XX, et al. Fenbendazole induces pyroptosis in breast cancer cells through HK2/caspase-3/GSDME signaling pathway[J]. Front Pharmacol, 2025, 16: 1596694. DOI:10.3389/fphar.2025.1596694 |
| [16] |
HAN ZY, JIA YT, YAN DC, et al. Hydrogen sulfide attenuates cisplatin-induced acute kidney injury via dual inhibition of apoptosis and pyroptosis[J]. Biomedicines, 2025, 13(11): 2696. DOI:10.3390/biomedicines13112696 |
| [17] |
HAN JC, CHENG C, ZHANG JX, et al. Myricetin activates the Caspase-3/GSDME pathway via ER stress induction of pyroptosis in lung cancer cells[J]. Front Pharmacol, 2022, 13: 959938. DOI:10.3389/fphar.2022.959938 |
| [18] |
XIA Y, JIN Y, CUI DX, et al. Antitumor effect of simvastatin in combination with DNA methyltransferase inhibitor on gastric cancer via GSDME-mediated pyroptosis[J]. Front Pharmacol, 2022, 13: 860546. DOI:10.3389/fphar.2022.860546 |
 2026, Vol. 55
2026, Vol. 55