文章信息
- 翟明慧, 袁殿宝, 吴文娟
- ZHAI Minghui, YUAN Dianbao, WU Wenjuan
- 紫草素调控AMPK/mTOR信号通路对人食管癌细胞增殖、凋亡、迁移、侵袭和顺铂耐药的影响
- Impact of shikonin on proliferation, apoptosis, migration, invasion, and cisplatin resistance of human esophageal cancer cells through AMPK/mTOR signaling pathway regulation
- 中国医科大学学报, 2026, 55(4): 295-300
- Journal of China Medical University, 2026, 55(4): 295-300
-
文章历史
- 收稿日期:2025-03-13
- 网络出版时间:2026-04-15 13:14:39
2. 河北北方学院附属第一医院消化内镜科, 河北 张家口 075061
2. Department of Gastroentero- logy and Endoscopy, The First Affiliated Hospital of Hebei North University, Zhangjiakou 075061, China
食管癌主要包括食管腺癌及食管鳞状细胞癌,可能发生在食管的任何部位,其中食管鳞状细胞癌是主要类型[1]。食管癌早期发病症状不明显,诊断时通常已发展到晚期,且临床治疗方法有限,患者预后极差[2-3],因此探讨其发展机制以寻求药物对食管癌患者的早期诊断和治疗有重要意义。
紫草素是从传统草药紫草科植物中提取一种萘醌色素,具有广泛的生物活性和抗肿瘤作用[4],但具体作用机制尚未完全阐明。AMP活化蛋白激酶(adenosine 5-monophosphate-activated protein kinase,AMPK)是一种高度保守的细胞能量状态传感器,在肿瘤发生和发展过程中,该分子以双链形式存在,发挥肿瘤抑制作用。AMPK通过抑制雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)激活导致细胞周期停滞、抑制肿瘤生长[5],在包括食管癌在内的肿瘤治疗中发挥关键作用[6]。本研究旨在探讨紫草素对人食管癌细胞增殖、凋亡、迁移、侵袭和顺铂耐药的影响及其潜在作用机制。
1 材料与方法 1.1 细胞来源人食管癌细胞系KYSE150由中国科学院(上海)细胞库提供,细胞在37 ℃、5% CO2环境中孵育,RPMI1640培养基以链霉素(100 mg/L)、青霉素(100 U/mL)与10%胎牛血清维持,选取对数生长期细胞进行研究。
1.2 主要材料及仪器紫草素(纯度≥98%)购自上海源叶生物科技有限公司;AMPK抑制剂-化合物C购自上海伟寰生物科技有限公司;多药耐药相关蛋白1(multidrug resistance-associated protein 1,MRP1)、端粒酶抑制因子(PIN2/TERF1-interacting telomerase inhibitor 1,PINX1)、增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)、Bcl-2相关X蛋白(Bcl-2 associated X protein,Bax)、AMPK、mTOR、p-AMPK、p-mTOR抗体购自英国abcam公司;逆转录试剂盒购自美国Fermentas International公司;膜联蛋白V-异硫氰酸荧光素(Annexin V-Fluorescein isothiocyanate,Annexin V-FITC)凋亡试剂盒购自德国默克集团;注射用顺铂购自锦州九泰药业有限责任公司。Multiskan GO酶标仪、Quant StudioTM荧光定量PCR仪购自美国ThermoFisher Scien-tific公司。
1.3 细胞分组及处理取对数生长期的KYSE150细胞。对照组常规培养;低浓度紫草素(低-紫草素)组、高浓度紫草素(高-紫草素)组分别以0.5 mol/L、2.0 mol/L紫草素处理KYSE150细胞[7];化合物C组以10 μmol/L化合物C处理KYSE150细胞[8];高-紫草素+化合物C组以10 μmol/L化合物C及2.0 mol/L紫草素同时处理KYSE150细胞。
1.4 MTT法检测细胞增殖率收集对数生长期的KYSE150细胞,将其接种到96孔板(3×103/孔)中。培养箱中培养细胞后,然后按照1.3中分组处理,孵育24 h后,加入MTT溶液(5 mg/mL,10 μL/孔),吸出上清液,加入二甲基亚砜(100 μL/孔),使用酶标仪测量490 nm波长处的吸光度(optical density,OD)值。
1.5 耐药性评估分别在培养基中依次加入2.5、5、10、20、40、80 μmol/L顺铂培养48 h[9],随后按照1.4中细胞增殖步骤进行操作,计算半数抑制浓度(half maximal inhibitory concentration,IC50)。
1.6 流式细胞术检测细胞凋亡将KYSE150细胞(1.5×105/孔)在6孔板中过夜,然后按照1.3中分组处理24 h。使用PBS洗涤细胞2次,通过Annexin V-FITC细胞凋亡试剂盒评估细胞凋亡,流式细胞仪评估凋亡细胞百分比。
1.7 Transwell实验检测细胞迁移、侵袭将细胞(迁移实验为5×104/孔,侵袭实验为1×105/孔)与无血清RPMI 1640培养基(0.2 mL)接种在孔径为8 μm上室中(侵袭实验涂有200 μg/mL基质胶,迁移实验无基质胶),下室加入RPMI 1640培养基(0.6 mL),其中含有10%胎牛血清。孵育24 h后,去除上室表面的非侵袭细胞及非迁移细胞,同时使用0.5%结晶紫、95%乙醇固定及染色底部迁移或侵袭性细胞,倒置显微镜下观察,用ImageJ分析染色细胞数量。
1.8 实时定量PCR检测自噬相关基因P62、LC3 mRNA表达水平采用TRIzol®试剂及逆转录酶试剂盒分别进行提取及逆转录,获得互补脱氧核糖核酸(complementary deoxyribonucleic acid,cDNA),混合PerfectStart Green qPCR SuperMix与cDNA、基因引物,在QuantStudio6系统中扩增cDNA,在StepOnePlusTM实时荧光定量PCR系统中进行PCR反应,使用2-ΔΔCt分析计算基因的相对表达,以β-actin为内参。引物序列如下:LC3,正向5’-TCCGAGAAGACCTTCAACAAGC-3’,反向5’-AAGAAGGCTTGGTTAGCATTGAG-3’;β-actin,正向5’-CTTCGCGGGCGACGAT-3’,反向5’-CCACATAGGAATCCTTCTGACC-3’;P62,正向5’-TTGAGAAGATTCAGAAGGGAGAGTC-3’,反向5’-TCTTCCTCCTTGGCTTTGTCTCTC -3’;初始变性步骤为94 ℃ 3 min,变性94 ℃ 30 s,退火56 ℃ 30 s,延伸72 ℃ 30 s,72 ℃ 7 min。
1.9 Western blotting检测相关蛋白表达水平按照1.3中分组处理24 h。使用磷酸盐缓冲液洗涤细胞2次,并通过添加放射免疫沉淀测定缓冲液进行裂解,在4 ℃下16 000 g离心20 min,用移液管轻轻吸出上清液,测量上清液中的总蛋白含量。通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离20 μg蛋白质,并转移到聚偏氟乙烯膜上,封闭膜30 min,并在4℃下在摇床上与特异性一抗孵育过夜,其中PINX1(稀释比1∶1 000)、PCNA(稀释比1∶500)、MRP1(稀释比1∶1 000)、Bax(稀释比1∶1 000)以及β-actin(稀释比1∶1 000),洗涤膜3次,室温下加入二抗孵育,化学发光溶液作为显影液,ChemiDoc成像系统进行蛋白质条带成像,ImageJ用于检测相应蛋白质条带的灰度值。
1.10 统计学分析采用SPSS 26.0软件进行统计分析,数据以x±s表示,多组间比较采用单因素方差分析,进一步进行SNK-q检验。P < 0.05为差异有统计学意义。
2 结果 2.1 紫草素对KYSE150细胞增殖的影响与对照组(0.85±0.09)相比,低-紫草素组(0.64±0.07)、高-紫草素组(0.38±0.04)OD490值降低,化合物C组OD490值(1.31±0.15)增加(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组OD490值(0.59±0.06)增加(P < 0.05);与化合物C组相比,高-紫草素+化合物C组OD490值降低(P < 0.05)。
2.2 紫草素对KYSE150细胞IC50变化的影响与对照组(28.86 μmol/L±2.91 μmol/L)相比,低-紫草素组(19.54 μmol/L±2.03 μmol/L)、高-紫草素组(11.14 μmol/L±1.15 μmol/L)IC50降低,化合物C组IC50(39.42 μmol/L±4.05 μmol/L)增加(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组IC50(20.08 μmol/L±2.06 μmol/L)增加(P < 0.05);与化合物C组相比,高-紫草素+化合物C组IC50降低(P < 0.05)。
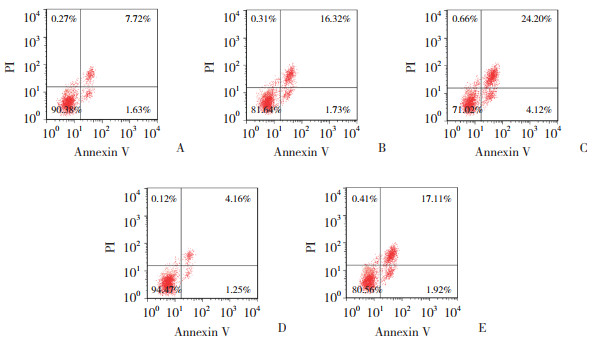
2.3 紫草素对KYSE150细胞凋亡的影响与对照组(9.42%±0.10%)相比,低-紫草素组(17.85%±1.82%)、高-紫草素组(28.05%±2.86%)凋亡率增加,化合物C组(5.47%±0.56%)凋亡率降低(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组(18.06%±1.82%)凋亡率降低(P < 0.05);与化合物C组相比,高-紫草素+化合物C组凋亡率增加(P < 0.05),见图 1。
|
| A, control group; B, low-shikonin group; C, high-shikonin group; D, compound C group; E, high-shikonin+compound C group. 图 1 各组细胞凋亡变化 Fig.1 Changes of apoptosis in cells of different groups |
2.4 紫草素对KYSE150细胞迁移、侵袭数的影响
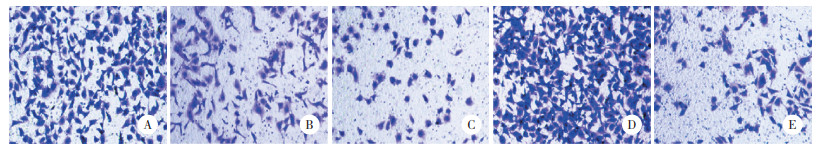
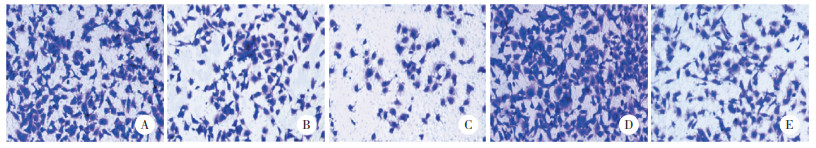
与对照组相比,低-紫草素组、高-紫草素组侵袭、迁移数降低,化合物C组侵袭、迁移数增加(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组侵袭、迁移数增加(P < 0.05);与化合物C组相比,高-紫草素+化合物C组侵袭、迁移数降低(P < 0.05),见图 2、3,表 1。
|
| A, control group; B, low-shikonin group; C, high-shikonin group; D, compound C group; E, high-shikonin+compound C group. 图 2 各组细胞侵袭变化×200 Fig.2 Changes in cell invasion of different groups ×200 |
|
| A, control group; B, low-shikonin group; C, high-shikonin group; D, compound C group; E, high-shikonin+compound C group. 图 3 各组细胞迁移变化×200 Fig.3 Changes in cell migration of different groups ×200 |
| Group | n | Invasion | Migration |
| Control | 6 | 152.06±15.31 | 188.64±18.92 |
| Low-shikonin | 6 | 91.52±9.211) | 126.34±12.711) |
| High-shikonin | 6 | 60.21±6.091),2) | 77.34±7.811),2) |
| Compound C | 6 | 225.34±22.641) | 271.54±27.221) |
| High-shikonin+compound C | 6 | 91.06±9.183),4) | 127.04±12.813),4) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. low-shikonin group;3)P < 0.05 vs. high-shikonin group;4)P < 0.05 vs. compound C group. | |||
2.5 紫草素对KYSE150细胞P62及LC3 mRNA表达的影响
与对照组相比,低-紫草素组、高-紫草素组P62 mRNA表达降低,LC3 mRNA表达增加,但化合物C组P62 mRNA表达增加,LC3 mRNA表达降低(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组P62 mRNA表达增加,LC3 mRNA表达降低(P < 0.05);与化合物C组相比,高-紫草素+化合物C组P62 mRNA表达降低,LC3 mRNA表达增加(P < 0.05),见表 2。
| Group | n | P62 mRNA | LC3 mRNA |
| Control | 6 | 0.98±0.10 | 1.08±0.11 |
| Low-shikonin | 6 | 0.63±0.071) | 1.52±0.161) |
| High-shikonin | 6 | 0.37±0.041),2) | 2.19±0.221),2) |
| Compound C | 6 | 1.42±0.151) | 0.67±0.071) |
| High-shikonin+compound C | 6 | 0.59±0.063),4) | 1.48±0.153),4) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. low-shikonin group;3)P < 0.05 vs. high-shikonin group;4)P < 0.05 vs. compound C group. | |||
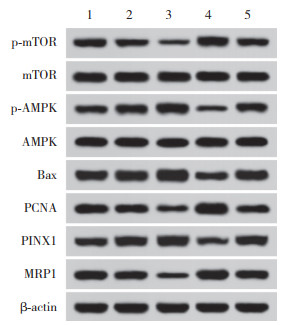
2.6 紫草素对KYSE150细胞MRP1、PINX1、PCNA、Bax、AMPK、mTOR、p-AMPK、p-mTOR表达的影响
与对照组相比,低-紫草素组、高-紫草素组p-mTOR/mTOR、MRP1、PCNA表达降低,p-AMPK/AMPK、PINX1、Bax表达增加,但化合物C组p-mTOR/mTOR、MRP1、PCNA表达增加,p-AMPK/AMPK、PINX1、Bax表达降低(P < 0.05);与高-紫草素组相比,高-紫草素+化合物C组p-mTOR/mTOR、MRP1、PCNA表达增加,p-AMPK/AMPK、PINX1、Bax表达降低(P < 0.05);与化合物C组相比,高-紫草素+化合物C组p-mTOR/mTOR、MRP1、PCNA表达降低,p-AMPK/AMPK、PINX1、Bax表达增加(P < 0.05),见表 3。图 4、
| Group | n | p-mTOR/mTOR | p-AMPK/AMPK | Bax/β-actin | PCNA/β-actin | PINX1/β-actin | MRP1/β-actin |
| Control | 6 | 0.52±0.06 | 0.37±0.04 | 0.75±0.08 | 0.79±0.08 | 0.48±0.05 | 0.71±0.08 |
| Low-shikonin | 6 | 0.31±0.041) | 0.61±0.071) | 1.03±0.111) | 0.52±0.061) | 0.77±0.081) | 0.49±0.051) |
| High-shikonin | 6 | 0.15±0.021),2) | 0.84±0.091),2) | 1.48±0.151),2) | 0.27±0.031),2) | 1.15±0.121),2) | 0.22±0.031),2) |
| Compound C | 6 | 0.79±0.081) | 0.18±0.021) | 0.48±0.051) | 1.24±0.131) | 0.23±0.031) | 1.04±0.111) |
| High-shikonin+compound C | 6 | 0.37±0.043),4) | 0.59±0.063),4) | 0.98±0.103),4) | 0.49±0.053),4) | 0.71±0.083),4) | 0.50±0.053),4) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. low-shikonin group;3)P < 0.05 vs. high-shikonin group;4)P < 0.05 vs. compound C group. | |||||||
|
| 1, control group; 2, low-shikonin group; 3, high-shikonin group; 4, compound C group; 5, high-shikonin+compound C group. 图 4 各组细胞中MRP1、PINX1、PCNA、Bax、AMPK、mTOR、p-AMPK、p-mTOR蛋白表达的Western blotting结果 Fig.4 Western blotting results of MRP1, PINX1, PCNA, Bax, AMPK, mTOR, p-AMPK, and p-mTOR expressions in cells of different groups |
3 讨论
PCNA是一种参与DNA合成和修复的酸性核蛋白,是细胞增殖的组织学标志物,参与DNA复制、DNA损伤修复、细胞周期调节等广泛细胞过程,并在各种肿瘤组织和细胞中过表达[10]。细胞凋亡或程序性细胞死亡是细胞停止生长和分裂并在基因水平上受到精细调节的过程,促进癌细胞凋亡是阻止肿瘤发展的关键[11]。
紫草素作为一类重要的天然分子,在抗癌治疗中显示出巨大的潜力,在许多肿瘤细胞中具有抗增殖和促凋亡作用。研究[12]发现紫草素可促进细胞凋亡并减弱食管癌细胞迁移和侵袭,提示紫草素可能是治疗食管癌的新药。顺铂是食管癌患者常用的化疗药物,可引起DNA损伤并诱导细胞凋亡。顺铂耐药会大大降低化疗方案的疗效,是患者预后不良和5年生存率低的主要原因[13]。PINX1作为抑癌基因,与肿瘤细胞顺铂敏感性有关[14]。本研究发现紫草素对KYSE150细胞显示出抗增殖、侵袭与迁移,并促凋亡的作用。Western blotting结果进一步证实紫草素能显著下调KYSE150细胞中PCNA表达,上调Bax表达,促进KYSE150细胞耐药,下调耐药蛋白MRP1表达,上调PINX1表达,提示紫草素不仅可以抑制KYSE150细胞的恶性发展,还可提高KYSE150细胞的顺铂敏感性。
自噬用于维持细胞的能量平衡并清除废物,与肿瘤发生、侵袭、转移、肿瘤免疫和化疗耐药等有关,已成为多种肿瘤发病机制和靶向治疗研究的重点,自噬细胞内稳态过程受LC3、p62等自噬相关蛋白的影响,增加食管癌细胞的自噬水平可抑制癌细胞增殖,减缓食管癌进展[15]。AMPK/mTOR信号通路是自噬的主要调节因子,mTOR是一种信号转导分子,可以调节蛋白质翻译和细胞生长等各种生理活动,从而影响自噬和细胞凋亡等活动,如结肠癌治疗中,AMPK可负向调节mTOR表达在体内和体外诱导癌细胞自噬和凋亡[16]。本研究发现,紫草素处理KYSE150食管癌细胞后,不仅显著上调AMPK磷酸化水平、下调mTOR磷酸化表达,更通过该通路激活诱导自噬发生,进而在功能层面抑制肿瘤细胞增殖、侵袭与迁移能力,并诱导细胞凋亡,同时促进顺铂耐药表型的形成,提示紫草素的抗食管癌作用可能与调控AMPK/mTOR信号通路密切相关。从分子机制层面分析,紫草素可能通过直接或间接激活AMPK激酶活性,引发下游mTOR信号通路的抑制,打破自噬相关蛋白LC3与p62的动态平衡,推动细胞自噬流的激活,通过诱导肿瘤细胞进入自噬性死亡程序,直接抑制KYSE150细胞增殖并促进凋亡,削弱肿瘤细胞的侵袭与迁移。为进一步验证上述机制假说,本研究通过AMPK特异性抑制剂化合物C进行干预实验,结果显示化合物C可显著逆转紫草素对AMPK磷酸化的激活作用,同时减弱紫草素诱导的自噬活性,并恢复KYSE150细胞的增殖、侵袭与迁移能力,这一结果直接证实紫草素需依赖AMPK/mTOR信号通路的激活,才能发挥其对食管癌的抗肿瘤生物学效应,表明紫草素通过上调AMPK/mTOR信号通路发挥抗食管癌的作用。
综上所述,紫草素通过上调AMPK/mTOR信号通路抑制人食管癌细胞增殖、迁移、侵袭,促进其凋亡,提高顺铂敏感性,相关机制的体内验证实验仍在进一步开展中。
| [1] |
熊飞. 腔镜lvor-Lewis术在胸中下段食管癌患者中的应用及对术后生活质量的影响[J]. 沈阳药科大学学报, 2021, 38(S2): 99-100. |
| [2] |
QIAO ZS, DAI CC, WANG ZQ, et al. Epiplakin1 promotes the progression of esophageal squamous cell carcinoma by activating the PI3K-AKT signaling pathway[J]. Thorac Cancer, 2022, 13(8): 1117-1125. DOI:10.1111/1759-7714.14366 |
| [3] |
刘双双, 朱正帅, 杨子林, 等. 积雪草苷调节HIF-1α/VEGF信号通路对食管癌细胞上皮-间质转化和放疗敏感性的影响[J]. 中国医科大学学报, 2025, 54(2): 150-155. DOI:10.12007/j.issn.0258‐4646.2025.02.010 |
| [4] |
DU WZ, HAO XH, YUAN ZL, et al. Shikonin potentiates paclitaxel antitumor efficacy in esophageal cancer cells via the apoptotic pathway[J]. Oncol Lett, 2019, 18(3): 3195-3201. DOI:10.3892/ol.2019.10662 |
| [5] |
ZHOU H, LI GL, KAN LY, et al. Synergistic induction of autophagy in gastric cancer by targeting CDK4/6 and MEK through AMPK/mTOR pathway[J]. Heliyon, 2024, 10(9): e30475. DOI:10.1016/j.heliyon.2024.e30475 |
| [6] |
HENG YQ, LIANG YP, ZHANG JQ, et al. Camptothecin inhibits neddylation to activate the protective autophagy through NF-κB/AMPK/mTOR/ULK1 axis in human esophageal cancer cells[J]. Front Oncol, 2021, 11: 671180. DOI:10.3389/fonc.2021.671180 |
| [7] |
杨双, 俞思全. 紫草素促进食管癌细胞凋亡及细胞周期阻滞的作用机制研究[J]. 安徽医药, 2023, 27(1): 79-82. DOI:10.3969/j.issn.1009-6469.2023.01.017 |
| [8] |
雷轩, 罗丹, 卢梁杰, 等. 芹菜素通过AMPK/mTOR通路调控肺癌A549细胞自噬[J]. 2024(1): 6-10. DOI: 10.3969/j.issn.1672-3511.2024.01.002.
|
| [9] |
卢万里, 金哲, 段东奎, 等. PVT1通过调节miR-486-3p/MAPK14轴降低食管癌细胞的化学敏感性[J]. 中国免疫学杂志, 2021, 37(24): 2999-3004. DOI:10.3969/j.issn.1000-484X.2021.24.012 |
| [10] |
WENDEL SO, SNOW JA, GU L, et al. The potential of PCNA inhibition as a therapeutic strategy in cervical cancer[J]. J Med Virol, 2023, 95(11): e29244. DOI:10.1002/jmv.29244 |
| [11] |
杨懿, 胡艳娥, 赵茂源, 等. 紫花前胡素通过PI3K/Akt信号通路影响结直肠癌细胞增殖、凋亡及迁移[J]. 中国中药杂志, 2023, 48(9): 2334-2342. DOI:10.19540/j.cnki.cjcmm.20230117.703 |
| [12] |
HUANG JR, ZHAO L, GONG CX, et al. Shikonin promotes apoptosis and attenuates migration and invasion of human esophageal cancer cells by inhibiting tumor necrosis factor receptor-associated protein 1 expression and AKT/mTOR signaling pathway[J]. Evid Based Complement Alternat Med, 2021, 2021: 5386050. DOI:10.1155/2021/5386050 |
| [13] |
XU T, MA XL, WEI Y, et al. Integrin-linked kinase affects the sensitivity of esophageal squamous cell carcinoma cells to chemotherapy with cisplatin via the Wnt/beta-catenin signaling pathway[J]. Bioengineered, 2022, 13(5): 12532-12547. DOI:10.1080/21655979.2022.2076497 |
| [14] |
LIU YY, GONG PG, ZHOU N, et al. Insufficient PINX1 expression stimulates telomerase activation by direct inhibition of EBV LMP1-NF-κB axis during nasopharyngeal carcinoma development[J]. Biochem Biophys Res Commun, 2019, 514(1): 127-133. DOI:10.1016/j.bbrc.2019.04.104 |
| [15] |
LI XZ, LIU S, JIN LY, et al. NOD2 inhibits the proliferation of esophageal adenocarcinoma cells through autophagy[J]. J Cancer Res Clin Oncol, 2023, 149(2): 639-652. DOI:10.1007/s00432-022-04354-x |
| [16] |
HU CX, CAO YB, LI P, et al. Oleanolic acid induces autophagy and apoptosis via the AMPK-mTOR signaling pathway in colon cancer[J]. J Oncol, 2021, 2021: 8281718. DOI:10.1155/2021/8281718 |
 2026, Vol. 55
2026, Vol. 55