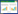文章信息
- 冯勇, 李义帅, 魏巍, 李萌
- FENG Yong, LI Yishuai, WEI Wei, LI Meng
- 1个中国Birt-Hogg-Dubé综合征相关的家族性自发性气胸家系新型致病性卵泡蛋白基因突变鉴定及文献复习
- Identification of a novel pathogenic folliculin mutant in a Chinese family with Birt-Hogg-Dubé syndrome-related familial spontaneous pneumothorax and literature review
- 中国医科大学学报, 2026, 55(3): 278-282
- Journal of China Medical University, 2026, 55(3): 278-282
-
文章历史
- 收稿日期:2025-03-24
- 网络出版时间:2026-03-24 15:21:28
2. 河北省胸科医院胸外科, 石家庄 050011;
3. 河北医科大学第四医院门诊部, 石家庄 050011;
4. 河北医科大学第四医院CT/MRI科, 石家庄 050011
Birt-Hogg-Dubé综合征(Birt-Hogg-Dubé syndrome,BHDS)(OMIM#135150),也称为Hornstein-Knickenberg综合征,是一种罕见的常染色体显性遗传性疾病,以肺囊肿、自发性气胸、皮肤纤维毛囊瘤和各种类型的肾肿瘤为特征。德国HORNSTEIN等[1]于1975年首次报道了一种新型常染色体显性遗传疾病,其特征是“皮肤毛囊周围维瘤病”、多发皮赘和多个易癌变的结肠息肉。1977年,加拿大BIRT等[2]报告了1个家系,其中多个家庭成员患有纤维毛囊瘤。随后,这种疾病被命名为“BHDS”[3]。原发性自发性气胸(primary spontaneous pneumothorax,PSP)中约有10%为家族性自发气胸(familial spontaneous pneumothorax,FSP)[4-5]。目前,BHDS相关的FSP的发病机制尚不清楚。已知的BHDS致病基因是位于染色体17p11.2、由14个外显子组成的卵泡蛋白(folliculin,FLCN)基因[6]。FLCN基因外显子11中极易变异的多胞嘧啶(C8)区域中,胞嘧啶的种系插入或缺失为不同国家或种族中最常见的突变[7-11]。本研究分析了1个BHDS相关的FSP家系的临床特征,探讨了该家系中FLCN基因的突变情况,并进行相关文献复习。
1 材料与方法 1.1 研究对象回顾性分析了河北医科大学第四医院胸外科收治的1个患有BHDS相关的FSP家系的临床资料。通过询问病史发现此家系中有8人曾患PSP,经询问先证者及其家属获得患者的一般信息及诊断治疗经过。以“家族性自发性气胸”为关键词,检索中国知网和万方数据库1998年1月至2024年1月间所有关于FSP的文献。排除临床资料不全的病例,共获得相关文献25篇,78个家系,加上本病例,共79个家系,275例FSP。选取河北医科大学第四医院同期健康体检者作为健康对照。
1.2 研究方法收集此家系8例FSP患者和10例健康对照者的外周血样品,使用DNeasy Blood & Tissue Kit(美国Qiagen公司)制备基因组DNA,-20 ℃保存。通过PCR扩增具有FLCN基因侧翼序列的编码外显子(PCR引物序列见表 1)。PCR反应体系:PCR Mix 5 μL,上下游引物各1 μL,基因组DNA 0.5 μL,加RNase-free水至20 μL。PCR反应条件:95 ℃ 2 min变性,94 ℃ 1 min,60 ℃ 1 min退火,72 ℃ 15 min延伸,30个循环。用ABI3100分析仪(美国ThermoFisher Scientific公司)确定。使用基于illumina测序平台的靶区探针捕获技术和下一代测序(next-generation sequencing technology,NGS)方法检测该家系中8例气胸患者和10例健康对照者的FLCN基因情况,并将结果在大型人群数据库中进行比对。本研究获得河北医科大学第四医院医学伦理委员会批准(2021KY011)。所有研究对象签署知情同意书。
| 外显子 | 正向引物 | 反向引物 | 产物(bp) |
| 4 | 5’-GGGAGGTTTCATGGAGTCAA-3’ | 5’-CTCTCAGGTCCTCCTGTCCAT-3’ | 402 |
| 5 | 5’-CCGAGCTCAGATTTGCATAAA-3’ | 5’-AGAAAATGCTCAGCAAGTCCA-3’ | 437 |
| 6 | 5’-ATTAACGCTGGCTGATTTGTG-3’ | 5’-CAGCTCTGAAGCCAAGAGACT-3’ | 486 |
| 7 | 5’-CTCAACCGATTTCTGTTCTCG-3’ | 5’-GCCAACCAATGTATCGTGACT-3’ | 446 |
| 8 | 5’-AAGGACCTTGGTCGTTGACTT-3’ | 5’-GCAAACGAGACAGGAAATCAC-3’ | 463 |
| 9 | 5’-CCATGAAGTATCTTGGGCTGA-3’ | 5’-GAGGCTGTCAGTCACTTCCTG-3’ | 393 |
| 10 | 5’-CTGAGCCCTGTCTTTGCTCTA-3’ | 5’-CCCACAAAGAAGCTTTTACCA-3’ | 497 |
| 11 | 5’-GGTAGTAGAGCATGGATGGCC-3’ | 5’-GGTTCCACTTTGGGCCTGAG-3’ | 270 |
| 12 | 5’-ATTGATTTGGGCCAGTCTTTT-3’ | 5’-CATCCACAGACAGGTTCTGGT-3’ | 427 |
| 13 | 5’-AGGATGACCAGTCTCTCAGCA-3’ | 5’-AGCTCCTCTTTTGGAAACAGC-3’ | 345 |
| 14 | 5’-GCTCGAGGGATTGTGCTGT-3’ | 5’-ATTGCCATCTTCAGCGATTC-3’ | 470 |
2 结果 2.1 FSP患者的临床特征
本研究家系中8例气胸患者的临床资料见表 2。谱系图(配偶省略)见图 1。
| 家系 | 性别 | 年龄(岁) | 身高(cm) | 体重(kg) | 吸烟史 | 胸部CT | 治疗方法 | |
| 左肺 | 右肺 | |||||||
| Ⅰ-1 | 男 | 97 | 172 | 65 | 有 | 不适用 | 胸腔穿刺术 | - |
| Ⅱ-1 | 男 | 78 | 174 | 73 | 有 | 不适用 | 胸腔闭式引流术,开胸肺大疱切除术 | 胸腔闭式引流术,开胸肺大疱切除术 |
| Ⅱ-2 | 男 | 73 | 178 | 78 | 无 | 不适用 | - | 胸腔穿刺术 |
| Ⅱ-6 | 女 | 71 | 160 | 66 | 有 | 多发肺囊肿 | 胸腔闭式引流术,胸腔镜肺大疱切除术 | - |
| Ⅲ-2 | 男 | 54 | 173 | 77 | 无 | 多发肺囊肿 | 胸腔闭式引流术 | 胸腔闭式引流术,开胸肺大疱切除术 |
| Ⅲ-14 | 男 | 52 | 177 | 82 | 有 | 多发肺囊肿 | 开胸肺大疱切除术 | 开胸肺大疱切除术 |
| Ⅲ-16 | 女 | 51 | 165 | 58 | 无 | 多发肺囊肿 | 胸腔穿刺术,胸腔穿刺术+胸膜固定术 | - |
| Ⅳ-25 | 男 | 28 | 177 | 63 | 无 | 多发肺囊肿 | 胸腔穿刺术+胸膜固定术 | 胸腔闭式引流术 |
结合文献,在来自79个家系的275例FSP患者中,男∶女为1.46∶1。第一次发病年龄≤40岁者140例(50.91%),年龄 > 40岁135例(49.09%)。同代发病率为17.72%(14/79),2代发病率为67.09%(53/79),3代发病率为13.92%(11/79),4代发病率为1.27%(1/79)。未发现隔代遗传的现象。保守治疗(卧床休息、吸氧)38例,复发率23.68%(9/38);胸腔穿刺65例,复发率50.77%(33/65);胸腔闭式引流98例,复发率41.84%(41/98);手术治疗107例,复发率3.74%(4/107)。
2.2 FLCN基因序列分析FLCN基因序列分析结果显示,患者第6外显子有1个新的无义突变(c.558G > A),该家系的8例气胸患者携带相同的突变,见图 2,证明了该基因突变位点的多样性。健康对照者中未发现FLCN基因突变。

|
| 图 2 气胸患者FLCN基因测序结果 |
3 讨论
BHDS的典型症状包括复发性气胸、多发性肺囊肿、纤维毛囊瘤和肾细胞癌。然而,这些症状通常单独出现且不典型[12]。超过80%的BHDS相关气胸患者有多个双侧肺囊肿,约22.5%~38%的患者有单发或复发的自发性气胸病史,可表现为首发症状[13]。此类患者通常被误诊为普通的PSP,而忽略了是否存在家族性,尤其是在仅存在孤立的肺囊肿/气胸的病例[14]。通过文献复习发现,BHDS相关的FSP与PSP的临床表现显著不同,PSP多见于10~30岁高瘦男性,而FSP多为40岁以上发病,且FSP的男女比例为1.46∶1 [15-16]。
有肺囊肿的年轻BHDS患者可能没有明显的症状,但当其中年时,肺囊肿常发生破裂,导致自发性气胸,且复发率很高[13, 17-18]。有研究[19]发现,BHDS患者的肺实质内多有双侧、多发性肺大疱。由于肺大疱较深,破裂引起气胸的时间往往比其他浅表部位气胸的时间晚,这是FSP患者首次气胸发病年龄较大的原因。FSP家族中还有相当一部分患者的亲属患有肺大疱但尚未发病,需密切监测。
本研究的家系中,同代家庭14个(17.72%),2代家庭53个(67.09%),3代家庭11个(13.92%)。此家系为4代家庭,共有8人患气胸,提示可能与遗传因素有关。研究[13, 20]显示,BHDS中FSP与FLCN基因突变密切相关。FLCN通过增加肺泡上皮细胞的通透性和诱导凋亡,减少肺泡表面活性物质的分泌,导致肺泡表面张力发生致病性变化,动态顺应性降低,对机械应力(甚至呼吸运动)的抵抗力增加,从而导致囊壁扩张和表面破裂的可能性增加[14, 21-22]。在BHDS相关气胸患者中,囊壁破裂可引发气胸形成,而继发性气胸主要分布在肺部张力最大的部位[23-25]。本研究在先证者和家系中其他气胸患者中发现了FLCN基因的新无义突变。此外,还发现FLCN基因编码第186位氨基酸由色氨酸的序列突变为终止子。过早出现的终止子可能导致无义介导的mRNA降解,蛋白质表达缺失。该突变尚未在大型人群数据库(包括gnomad、exac、1000 genomes等)中发现,是一种罕见的新型突变。其他家族成员是否存在FLCN突变,尚需进一步基因检测确定。
本研究结果结合文献复习显示,手术治疗FSP效果最好,复发率仅为3.74%,其次是内科保守治疗,复发率为23.68%,而胸腔穿刺和胸腔闭式引流的复发率较高,分别为50.77%和41.84%。研究[20, 26-27]表明,与常规保守治疗相比,肺大疱切除术和胸膜固定术在控制复发率方面效果更好。LIU等[27]报道,BHDS相关气胸手术和保守治疗的复发率分别为9.1%和53.1%,与本研究结果相似。对疑似BHDS的复发性气胸患者的早期诊断对于及时做出手术决策至关重要。
此外,BHDS患者常发生肾脏、肝脏和其他器官的囊性肿瘤,且具有较高的恶变风险[17, 28-31]。因此,临床医生应注意复发性气胸与BHDS之间的相关性,并考虑进行全面检查和早期干预。
本研究只对1个家系中的气胸患者进行了基因检测,未检测家属的基因。因此,需要多中心、更大样本量的前瞻性研究以进一步验证。
综上所述,本研究首次发现了BHDS的1个新型致病性FLCN基因突变,该突变可能引起肺囊肿和气胸。本研究结果扩大了中国人群FLCN基因的突变谱。与PSP的散发病例相比,BHDS相关气胸的临床特征包括女性气胸发病率明显较高,气胸发病年龄较晚,多为两代发病,可能与遗传有关,手术治疗效果最好。
| [1] |
HORNSTEIN OP, KNICKENBERG M. Perifollicular fibromatosis cutis with polyps of the colon: a cutaneo-intestinal syndrome Sui ge-neris[J]. Arch Dermatol Res, 1975, 253(2): 161-175. DOI:10.1007/BF00582068 |
| [2] |
BIRT AR, HOGG GR, DUBÉ WJ. Hereditary multiple fibrofolliculomas with trichodiscomas and acrochordons[J]. Arch Dermatol, 1977, 113(12): 1674-1677. |
| [3] |
HAPPLE R. Hornstein-Knickenberg syndrome vs. Birt-Hogg-Dubé syndrome: a critical review of an unjustified designation[J]. J Eur Acad Dermatol Venereol, 2020, 34(4): 885-887. DOI:10.1111/jdv.16190 |
| [4] |
BOONE PM, SCOTT RM, MARCINIAK SJ, et al. The genetics of pneumothorax[J]. Am J Respir Crit Care Med, 2019, 199(11): 1344-1357. DOI:10.1164/rccm.201807-1212ci |
| [5] |
SCOTT RM, HENSKE EP, RABY B, et al. Familial pneumothorax: towards precision medicine[J]. Thorax, 2018, 73(3): 270-276. DOI:10.1136/thoraxjnl-2017-211169 |
| [6] |
SCHMIDT LS, LINEHAN WM. FLCN The causative gene for Birt-Hogg-Dubé syndrome[J]. Gene, 2018, 640: 28-42. DOI:10.1016/j.gene.2017.09.044 |
| [7] |
KHOO SK, GIRAUD S, KAHNOSKI K, et al. Clinical and genetic studies of Birt-Hogg-Dubé syndrome[J]. J Med Genet, 2002, 39(12): 906-912. DOI:10.1136/jmg.39.12.906 |
| [8] |
SCHMIDT LS, NICKERSON ML, WARREN MB, et al. Germline BHD-mutation spectrum and phenotype analysis of a large cohort of families with Birt-Hogg-Dubé syndrome[J]. Am J Hum Genet, 2005, 76(6): 1023-1033. DOI:10.1086/430842 |
| [9] |
FURUYA M, YAO M, TANAKA R, et al. Genetic, epidemiologic and clinicopathologic studies of Japanese Asian patients with Birt-Hogg-Dubé syndrome[J]. Clin Genet, 2016, 90(5): 403-412. DOI:10.1111/cge.12807 |
| [10] |
LIU KQ, XU WS, TIAN XL, et al. Genotypic characteristics of Chinese patients with BHD syndrome and functional analysis of FLCN variants[J]. Orphanet J Rare Dis, 2019, 14(1): 223. DOI:10.1186/s13023-019-1198-y |
| [11] |
LIU YP, XU ZY, FENG RE, et al. Clinical and genetic characteristics of Chinese patients with Birt-Hogg-Dubé syndrome[J]. Orphanet J Rare Dis, 2017, 12(1): 104. DOI:10.1186/s13023-017-0656-7 |
| [12] |
HAN JZ, HAO JC, LIU RQ, et al. Birt-Hogg-Dubé syndrome caused by a mutation of FLCN gene in a CVST patient: a case report[J]. Int J Neurosci, 2020, 130(5): 438-442. DOI:10.1080/00207454.2019.1691204 |
| [13] |
SATTLER EC, SYUNYAEVA Z, MANSMANN U, et al. Genetic risk factors for spontaneous pneumothorax in Birt-Hogg-Dubé syndrome[J]. Chest, 2020, 157(5): 1199-1206. DOI:10.1016/j.chest.2019.12.019 |
| [14] |
MIN HY, MA DH, ZOU W, et al. FLCN-regulated miRNAs suppressed reparative response in cells and pulmonary lesions of Birt-Hogg-Dubé syndrome[J]. Thorax, 2020, 75(6): 476-485. DOI:10.1136/thoraxjnl-2019-213225 |
| [15] |
SAHN SA, HEFFNER JE. Spontaneous pneumothorax[J]. N Engl J Med, 2000, 342(12): 868-874. DOI:10.1056/nejm200003233421207 |
| [16] |
WILSON WG, AYLSWORTH AS. Familial spontaneous pneumothorax[J]. Pediatrics, 1979, 64(2): 172-175. DOI:10.1542/peds.64.2.172 |
| [17] |
DACCORD C, GOOD JM, MORREN MA, et al. Birt-Hogg-Dubé syndrome[J]. Eur Respir Rev, 2020, 29(157): 200042. DOI:10.1183/16000617.0042-2020 |
| [18] |
GUPTA N, KOPRAS EJ, HENSKE EP, et al. Spontaneous pneumothoraces in patients with birt-Hogg-Dubé syndrome[J]. Annals Am Thorac Soc, 2017, 14(5): 706-713. DOI:10.1513/Annalsats.201611-886oc |
| [19] |
刘彦国, 何博, 姜冠潮, 等. 家族性自发性气胸临床特点分析[J]. 中华胸心血管外科杂志, 2015, 31(2): 93-95. DOI:10.3760/cma.j.issn.1001-4497.2015.02.007 |
| [20] |
HU XW, ZHANG GF, CHEN XM, et al. Birt-Hogg-Dubé syndrome in Chinese patients: a literature review of 120 families[J]. Orphanet J Rare Dis, 2021, 16(1): 223. DOI:10.1186/s13023-021-01848-8 |
| [21] |
GONCHAROVA EA, GONCHAROV DA, JAMES ML, et al. Folliculin controls lung alveolar enlargement and epithelial cell survival through E-cadherin, LKB1, and AMPK[J]. Cell Rep, 2014, 7(2): 412-423. DOI:10.1016/j.celrep.2014.03.025 |
| [22] |
CHU L, LUO YF, CHEN H, et al. Mesenchymal folliculin is required for alveolar development: implications for cystic lung disease in Birt-Hogg-Dubé syndrome[J]. Thorax, 2020, 75(6): 486-493. DOI:10.1136/thoraxjnl-2019-214112 |
| [23] |
JOHANNESMA PC, HOUWELING AC, VAN WAESBERGHE JTM, et al. The pathogenesis of pneumothorax in Birt-Hogg-Dubé syndrome: a hypothesis[J]. Respirology, 2014, 19(8): 1248-1250. DOI:10.1111/resp.12405 |
| [24] |
KENNEDY JC, KHABIBULLIN D, HENSKE EP. Mechanisms of pulmonary cyst pathogenesis in Birt-Hogg-Dubé syndrome: the stretch hypothesis[J]. Semin Cell Dev Biol, 2016, 52: 47-52. DOI:10.1016/j.semcdb.2016.02.014 |
| [25] |
YANG JJ, HU XW, LI JJ, et al. Correlative analysis of lung CT fin-dings in patients with Birt-Hogg-Dubé Syndrome and the occurrence of spontaneous pneumothorax: a preliminary study[J]. BMC Med Imaging, 2022, 22(1): 22. DOI:10.1186/s12880-022-00743-3 |
| [26] |
TORO JR, PAUTLER SE, STEWART L, et al. Lung cysts, spontaneous pneumothorax, and genetic associations in 89 families with Birt-Hogg-Dubé syndrome[J]. Am J Respir Crit Care Med, 2007, 175(10): 1044-1053. DOI:10.1164/rccm.200610-1483OC |
| [27] |
LIU YG, XING HJ, HUANG Y, et al. Familial spontaneous pneumothorax: importance of screening for Birt-Hogg-Dubé syndrome[J]. Eur J Cardiothorac Surg, 2020, 57(1): 39-45. DOI:10.1093/ejcts/ezz171 |
| [28] |
HINDMAN NM. Imaging of cystic renal masses[J]. Urol Clin N Am, 2018, 45(3): 331-349. DOI:10.1016/j.ucl.2018.03.006 |
| [29] |
KAY FU, PEDROSA I. Imaging of solid renal masses[J]. Urol Clin N Am, 2018, 45(3): 311-330. DOI:10.1016/j.ucl.2018.03.013 |
| [30] |
STEINLEIN OK, REITHMAIR M, SYUNYAEVA Z, et al. Delayed diagnosis of Birt-Hogg-Dubé syndrome might be aggravated by gender bias[J]. EClinicalMedicine, 2022, 51: 101572. DOI:10.1016/j.eclinm.2022.101572 |
| [31] |
KURATA K, MATSUMOTO H, JIMBO N, et al. Lymphoplasmacytic lymphoma in a patient with Birt-Hogg-Dubé syndrome[J]. Int J Hematol, 2020, 112(6): 864-870. DOI:10.1007/s12185-020-02970-2 |
 2026, Vol. 55
2026, Vol. 55