文章信息
- 熊和然, 赵欣, 王松, 向超, 万骐, 程思玲, 何生华
- XIONG Heran, ZHAO Xin, WANG Song, XIANG Chao, WAN Qi, CHENG Siling, HE Shenghua
- miR-224-3p调控JAK/STAT信号通路对LPS诱导的椎间盘退变髓核细胞增殖、凋亡和炎症反应的影响
- Effects of miR-224-3p regulating JAK/STAT signaling pathway on proliferation, apoptosis, and inflammatory response of LPS-induced nucleus pulposus cells in intervertebral disc degeneration
- 中国医科大学学报, 2026, 55(3): 265-271
- Journal of China Medical University, 2026, 55(3): 265-271
-
文章历史
- 收稿日期:2025-01-14
- 网络出版时间:2026-03-24 15:13:23
椎间盘退变是一种起源于椎间盘的脊柱退行性疾病,可导致脊柱不稳、椎间盘突出和颈椎病[1]。髓核细胞是椎间盘的重要组成部分,其行为学的变化会影响椎间盘的功能[2]。研究[3]发现髓核组织的炎症反应与腰椎间盘退变密切相关,主要表现为炎症介质促使细胞凋亡并促进各种细胞外基质降解酶的合成,从而导致细胞外基质降解。Janus激酶/信号转导和转录激活因子(janus kinase/signal transducer and activator of transcription,JAK/STAT)是介导细胞增殖、凋亡及炎症反应的关键信号通路[4]。研究[5]表明通过下调JAK/STAT信号通路活性,可减少髓核细胞外基质降解,保护椎间盘结构的完整性。微RNA(microRNA,miRNA)与椎间盘退变的增殖、凋亡、炎症和细胞外基质相关[6]。目前对miR-224-3p的研究主要集中在肿瘤和免疫细胞[7],关于其在椎间盘退变中的作用鲜有报道。
本研究通过ENCORI数据库预测发现miR-224-3p和JAK1之间存在结合位点,提示二者可能存在靶向调控关系。基于此,本研究旨在探究miR-224-3p通过调控JAK/STAT信号通路对人椎间盘退变髓核细胞增殖、凋亡和炎症反应的影响,以期为椎间盘退变的治疗提供理论参考。
1 材料与方法 1.1 材料 1.1.1 细胞与试剂人髓核细胞购自武汉赛奥斯生物科技有限公司;脂多糖(lipopolysaccharide,LPS)购自北京伊塔生物科技有限公司;DMEM培养基(含10%胎牛血清)购自武汉佰瑞得生物技术有限公司;细胞凋亡检测试剂盒购自上海雅吉生物科技有限公司;实时定量PCR试剂盒购自艾美捷科技有限公司;CCK-8试剂盒购自上海谱析生物科技有限公司;lipofectamine 2000转染试剂购自上海恒斐生物科技有限公司;miR-224-3p空载体、miR-224-3p模拟物、JAK1过表达空载体和JAK1过表达质粒由吉满生物科技(上海)有限公司构建并提供;基因引物序列由北京擎科生物科技有限公司合成并提供;AnnexinV-FITC/PI双染细胞凋亡检测试剂盒购自浙江麦飞生物科技有限公司;肿瘤坏死因子α(tumor necrosis factor α,TNF-α)、白细胞介素(interleukin,IL)-6、IL-8、IL-1β试剂盒均购自北京索莱宝科技有限公司;BCA蛋白浓度测定试剂盒购自武汉伊莱瑞特生物科技股份有限公司;JAK1、p-JAK1、STAT1、p-STAT1、Bax、Bcl-2、caspase-3、aggrecan、CollagenⅡ抗体购自英国abcam公司。
1.1.2 主要仪器Thermo BB15CO2细胞培养箱购自上海远耀生物科技有限公司;GenoSens S2 Pro/Ultra凝胶成像仪购自上海勤翔科学仪器有限公司;Q3200实时荧光定量PCR仪购自杭州柏恒科技有限公司;DMi1显微镜购自北京普瑞赛司仪器有限公司;NanoDrop 8000分光光度计购自美国赛默飞世尔科技公司;SpectraMax Mini多功能酶标仪购自美谷分子仪器(上海)有限公司。
1.2 方法 1.2.1 细胞培养将冷冻保存的人髓核细胞解冻后,接种于DMEM培养基(含10%胎牛血清),在37 ℃,5% CO2的细胞培养箱中培养,定期更换培养液(间隔2~3 d),观察细胞的颜色以及生长状态,当细胞融合度达到80%左右时进行传代,并取3代细胞经LPS诱导24 h后进行后续实验研究。
1.2.2 miR-224-3p、JAK1和STAT1 mRNA表达水平检测用TRIzol试剂盒提取正常人髓核细胞和经LPS干预后髓核细胞的总RNA,NanoDrop 8000核酸分光光度计测定其浓度和纯度后将其逆转录为cDNA,随后进行实时定量PCR。以U6作为miR-224-3p的内参,GAPDH作为JAK1和STAT1的内参,用2-ΔΔCt法计算相对表达量。引物由北京擎科生物技术有限公司生成。引物序列见表 1。
| Gene | Primer sequence |
| miR-224-3p | Forward:5’-CTTCATGTGGCTGATGACCTATG-3’ |
| Reverse:5’-TAGACAATTGGGACGCTGAAGA-3’ | |
| U6 | Forward:5’-TTAGCATGGCCCCTGC-3’ |
| Reverse:5’-TGCGTGTCGTGGAGTC-3’ | |
| JAK1 | Forward:5’-TGGAGGTAACCACATAGC-3’ |
| Reverse:5’-CCGAGAACCCAAATAGTC-3’ | |
| STAT1 | Forward:5’-GGTAATTGACCTCGAGACGACCTCTC-3’ |
| Reverse:5’-GGAAGAAGGACAGATTCCTGGGTTCC-3’ | |
| TNF-α | Forward:5’-AATGGCGTGGAGCTGAGA-3’ |
| Reverse:5’-ATGCGGCTGATGGTGTGG-3’ | |
| IL-6 | Forward:5’-ATCTGGATTCAATGAGGAGA-3’ |
| Reverse:5’-TCTGGCTTGTTCCTCACTAC-3’ | |
| Aggrecan | Forward:5’-CTACCAGTGGATCGGCCTGAA-3’ |
| Reverse:5’-CGTGCCAGATCATCACCACA-3’ | |
| CollagenⅡ | Forward:5’-GGCAATAGCAGGTTCACGTACA-3’ |
| Reverse:5’-CGATAACAGTCTTGCCCCACTT-3’ | |
| GAPDH | Forward:5’-GGTGAAGGTCGGAGTCAACG-3’ |
| Reverse:5’-CAAAGTTGTCATGGATGACC-3’ |
1.2.3 细胞转染
将人髓核细胞分为对照(Control)组、模型(Model)组、miR-224-3p空载体(miR-NC)组、miR-224-3p模拟物(miR-224-3p mimics)组、miR-224-3p模拟物+JAK1过表达空载体(miR-224-3p mimics+pcDNA-NC)组、miR-224-3p模拟物+JAK1过表达粒(miR-224-3p mimics+JAK1)组。其中Control组细胞正常培养,Model组细胞以LPS(200 μg/mL)[8]诱导24 h,其他各组细胞经LPS(200 μg/mL)诱导24 h后,使用lipofectamine 2000转染试剂分别将miR-NC、miR-224-3p mimics、miR-224-3p mimics和pcDNA-NC、miR-224-3p mimics和JAK1转染至各组细胞,48 h后收集细胞并检测相关指标。
1.2.4 实时定量PCR检测目的基因相对表达收集各组髓核细胞,按照1.2.2的方法检测miR-224-3p、TNF-α、IL-6、aggrecan和CollagenⅡ的相对表达水平。引物序列见表 1。
1.2.5 CCK-8法检测各组髓核细胞活性收集1.2.3中各组培养至对数生长期的髓核细胞接种于96孔板中,以未处理的髓核细胞作为空白对照组。在标准环境的细胞培养箱(37 ℃,5% CO2)中培养24 h后,向每孔加入CCK-8试剂。孵育后取含待测液的样板,用酶标仪检测各组细胞450 nm的吸光度(optical density,OD)值。
1.2.6 流式细胞术检测各组髓核细胞的凋亡情况收集各组髓核细胞,用预冷的PBS清洗,离心弃上清(3 000 r/min 5 min),加入结合缓冲液重悬细胞,再分别加入AnnexinV-FITC和PI,均匀混合后避光反应10 min。用流式细胞仪进行检测。
1.2.7 ELISA法检测各组炎性细胞因子水平收集各组髓核细胞,离心后(3 000 r/min 5 min)收集上清液,按照试剂盒说明书检测TNF-α、IL-6、IL-8水平。
1.2.8 Western blotting检测髓核细胞JAK/STAT信号通路蛋白表达情况收集髓核细胞,加入RIPA裂解液反应后离心取上清,提取并定量总蛋白。蛋白经变性、电泳分离、转膜、封闭后与JAK1、p-JAK1、STAT1、p-STAT1、Bax、Bcl-2、caspase-3、aggrecan和Collagen Ⅱ一抗在4℃孵育过夜,HRP标记的山羊抗兔二抗IgG室温孵育1 h。可视化处理后使用ImageJ分析蛋白条带灰度值。
1.2.9 双萤光素酶报告基因检测利用在线网站(https://rnasysu.com)对miR-224-3p与JAK1的结合位点进行预测,并构建JAK1-WT、JAK1-MUT双萤光素酶报告基因表达载体。分别与miR-NC和miR-224-3p mimics共转染于髓核细胞,进行48 h培养后,对其萤光素酶活性进行检测。
1.3 统计学分析采用SPSS 24.0软件进行统计分析。数据以x±s表示,多组间比较采用单因素方差分析,组间两两比较采用t检验。P < 0.05为差异有统计学意义。
2 结果 2.1 miR-224-3p、JAK1和STAT1 mRNA表达水平与Control组(0.91±0.05,0.25±0.02,0.17±0.01)相比,Model组髓核细胞miR-224-3p表达水平(0.47±0.04)显著下调,JAK1 mRNA(0.79±0.07)和STAT1 mRNA(0.68±0.06)表达水平显著上调(P < 0.05)。
2.2 各组髓核细胞中miR-224-3p、TNF-α、IL-6、aggrecan和CollagenⅡ表达水平与Control组相比,Model组miR-224-3p表达水平明显降低,TNF-α mRNA和IL-6 mRNA表达水平明显升高(P < 0.05),提示人椎间盘退变髓核细胞模型构建成功;与miR-NC组相比,miR-224-3p mimics组miR-224-3p、aggrecan和CollagenⅡ mRNA表达水平显著升高,TNF-α、IL-6表达水平明显降低(P < 0.05);与miR-224-3p mimics+pcDNA-NC组相比,miR-224-3p mimics+JAK1组aggrecan和CollagenⅡ mRNA表达水平降低,TNF-α、IL-6 mRNA表达水平显著升高(P < 0.05)。见表 2。
| Group | n | miR-224-3p | TNF-α | IL-6 | aggrecan | CollagenⅡ |
| Control | 6 | 0.98±0.02 | 0.25±0.02 | 0.17±0.01 | 0.97±0.06 | 0.92±0.07 |
| Model | 6 | 0.46±0.051) | 0.54±0.051) | 0.42±0.041) | 0.41±0.041) | 0.55±0.041) |
| miR-NC | 6 | 0.47±0.04 | 0.57±0.05 | 0.45±0.04 | 0.43±0.04 | 0.52±0.05 |
| miR-224-3p mimics | 6 | 0.75±0.062) | 0.36±0.032) | 0.24±0.032) | 0.82±0.082) | 0.86±0.072) |
| miR-224-3p mimics+pcDNA-NC | 6 | 0.76±0.07 | 0.38±0.04 | 0.25±0.02 | 0.80±0.08 | 0.84±0.08 |
| miR-224-3p mimics+JAK1 | 6 | 0.77±0.06 | 0.49±0.053) | 0.38±0.043) | 0.54±0.053) | 0.67±0.063) |
| 1)P < 0.05 vs. Control group;2)P < 0.05 vs. miR-NC group;3)P < 0.05 vs. miR-224-3p mimics+pcDNA-NC group. | ||||||
2.3 各组髓核细胞活性比较
与Control组相比,Model组髓核细胞活性显著降低(96.51±8.65 vs. 51.53±5.07,P < 0.05);与miR-NC组相比,miR-224-3p mimics组髓核细胞活性显著升高(50.39±5.04 vs. 69.81±5.01,P < 0.05);与miR-224-3p mimics+pcDNA-NC组相比,miR-224-3p mi-mics+JAK1组髓核细胞活性显著降低(66.45±4.52 vs. 57.49±3.30,P < 0.05)。
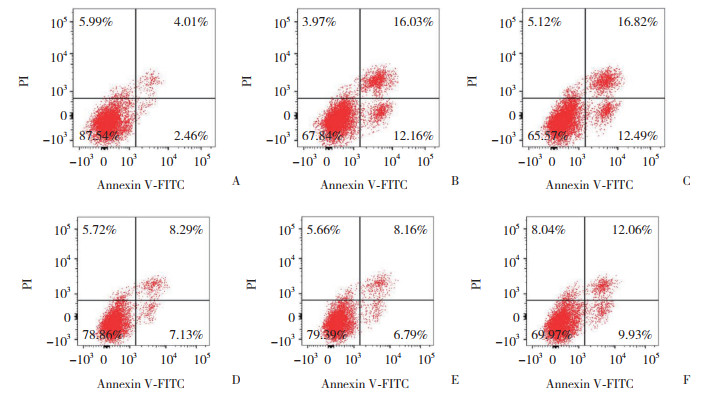
2.4 各组髓核细胞凋亡率比较与Control组(6.39%±0.76%)相比,Model组髓核细胞凋亡率(27.41%±2.38%)显著升高(P < 0.05);与miR-NC组(28.64%±2.71%)相比,miR-224-3p mi-mics组髓核细胞凋亡率(15.20%±1.24%)显著降低(P < 0.05);与miR-224-3p mimics+pcDNA-NC组(14.67%±1.38%)相比,miR-224-3p mimics+JAK1组髓核细胞凋亡率(21.89%±1.91%)显著升高(P < 0.05)。见图 1。
|
| A, Control group; B, Model group; C, miR-NC group; D, miR-224-3p mimics group; E, miR-224-3p mimics+pcDNA-NC; F, miR-224-3p mimics+JAK1 group. 图 1 流式细胞术检测各组髓核细胞凋亡情况 Fig.1 Detection of nucleus pulposus cell apoptosis in each group using flow cytometry |
2.5 各组炎性细胞因子水平比较
与Control组相比,Model组炎性细胞因子水平显著升高(P < 0.05);与miR-NC组相比,miR-224-3p mimics组炎性细胞因子水平显著降低(P < 0.05);与miR-224-3p mimics+pcDNA-NC组相比,miR-224-3p mimics+JAK1组炎性细胞因子水平显著升高(P < 0.05)。见表 3。
| Group | n | TNF-α | IL-6 | IL-8 |
| Control | 6 | 126.39±12.50 | 76.80±7.21 | 98.18±8.41 |
| Model | 6 | 227.41±21.431) | 161.70±12.251) | 173.26±15.171) |
| miR-NC | 6 | 231.64±20.26 | 158.32±15.40 | 178.31±16.35 |
| miR-224-3p mimics | 6 | 155.20±15.202) | 97.46±9.122) | 115.33±10.102) |
| miR-224-3p mimics+pcDNA-NC | 6 | 159.70±15.51 | 100.23±10.05 | 119.14±11.45 |
| miR-224-3p mimics+JAK1 | 6 | 201.89±17.913) | 135.70±12.283) | 151.74±14.633) |
| 1)P < 0.05 vs. Control group;2)P < 0.05 vs. miR-NC group;3)P < 0.05 vs. miR-224-3p mimics+pcDNA-NC group. | ||||
2.6 各组髓核细胞JAK/STAT信号通路相关蛋白表达水平比较
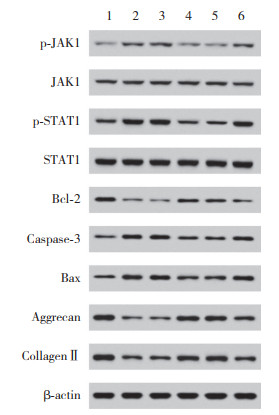
与Control组相比,Model组p-JAK1/JAK1、p-STAT1/STAT1、caspase-3和Bax蛋白表达水平显著升高、Bcl- 2、aggrecan和CollagenⅡ蛋白表达水平显著降低(P < 0.05);与miR-NC组相比,miR-224-3p mimics组p- JAK1/JAK1、p-STAT1/STAT1、caspase-3和Bax蛋白表达水平显著下降、Bcl-2、aggrecan和CollagenⅡ蛋白表达水平显著升高(P < 0.05);与miR-224-3p mimics+pcDNA-NC组相比,miR-224-3p mimics+JAK1组p-JAK1/JAK1、p-STAT1/STAT1、caspase-3和Bax蛋白表达水平显著升高、Bcl-2、aggrecan和CollagenⅡ蛋白表达水平显著降低(P < 0.05)。见表 4、图 2。
| Group | p-JAK1/JAK1 | p-STAT1/STAT1 | Bcl-2 | Caspase-3 | Bax | Aggrecan | CollagenⅡ |
| Control | 0.41±0.04 | 0.32±0.03 | 0.71±0.07 | 0.35±0.03 | 0.47±0.05 | 0.99±0.02 | 0.92±0.07 |
| Model | 0.75±0.071) | 0.80±0.081) | 0.26±0.031) | 0.72±0.071) | 0.85±0.081) | 0.34±0.031) | 0.47±0.041) |
| miR-NC | 0.72±0.07 | 0.78±0.07 | 0.29±0.03 | 0.71±0.06 | 0.87±0.08 | 0.36±0.04 | 0.45±0.04 |
| miR-224-3p mimics | 0.53±0.052) | 0.47±0.052) | 0.61±0.062) | 0.50±0.052) | 0.63±0.062) | 0.87±0.082) | 0.81±0.082) |
| miR-224-3p mimics+pcDNA-NC | 0.50±0.04 | 0.49±0.05 | 0.60±0.05 | 0.52±0.05 | 0.60±0.05 | 0.85±0.07 | 0.78±0.07 |
| miR-224-3p mimics+JAK1 | 0.69±0.063) | 0.71±0.073) | 0.34±0.033) | 0.63±0.063) | 0.77±0.073) | 0.60±0.053) | 0.58±0.053) |
| 1)P < 0.05 vs. Control group;2)P < 0.05 vs. miR-NC group;3)P < 0.05 vs. miR-224-3p mimics+pcDNA-NC group. n = 6. | |||||||
|
| 1, Control group; 2, Model group; 3, miR-NC group; 4, miR-224-3p mimics group; 5, miR-224-3p mimics+pcDNA-NC group; 6, miR-224-3p mimics+JAK1 group. 图 2 各组髓核细胞JAK/STAT信号通路相关蛋白表达 Fig.2 JAK/STAT signaling pathway-related protein expressions in nucleus pulposus cells of each group |
2.7 miR-224-3p与JAK1的靶向关系验证
网站预测结果显示,miR-224-3p与JAK1之间存在互补结合位点。双萤光素酶报告基因实验进一步显示,与阴性对照miR-NC相比,miR-224-3p mimics可显著抑制JAK1-WT质粒的萤光素酶活性(1.01±0.05 vs. 0.52±0.05,P < 0.05),证明miR-224-3p与JAK1之间存在靶向关系。见图 3。
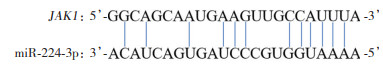
|
| 图 3 miR-224-3p与JAK1的靶向结合位点 Fig.3 Target binding sites of miR-224-3p and JAK1 |
3 讨论
衰老、遗传、营养、代谢因素、炎性细胞因子、感染、机械因素、信号通路等多种因素都会导致髓核细胞凋亡、椎间盘退变[9]。髓核中的髓核细胞可产生aggrecan、CollagenⅡ,从而形成细胞外基质,在维持椎间盘的结构和健康中发挥关键作用[10]。髓核细胞凋亡是椎间盘退变潜在病理之一,而细胞凋亡的主要诱因是细胞受到刺激发生强烈的炎症反应。因此,抑制髓核细胞炎症和凋亡现象是缓解椎间盘退变的有效途径。
既往研究[11]表明,miRNA是基因表达的调控因子,在椎间盘退变的预防和治疗中发挥重要作用。ZHENG等[12]指出,miRNA通过调节髓核细胞的凋亡和内质网应激反应影响椎间盘退变的发生和发展。miR-224-3p作为一种短的非编码RNA,已被证实在股骨头创伤性骨坏死组织中显著下调[13],但在椎间盘退变疾病中尚未有研究。本研究结果显示,髓核细胞经LPS干预后,miR-224-3p表达水平显著下调,过表达miR-224-3p可抑制细胞凋亡和炎性细胞因子的表达,提高细胞活力及aggrecan、CollagenⅡ的表达量。以上结果表明miR-224-3p对椎间盘退变髓核细胞具有保护作用。
miRNA通过与靶基因互补结合发挥其生物学功能[14]。本研究预测miR-224-3p与JAK1存在的结合位点。JAK/STAT信号通路是调节机体炎症反应的典型通路。炎性细胞因子的过表达使JAK磷酸化,进而使下游的STAT磷酸化,再通过与相应的位点结合,诱导该信号通路的进一步激活,促进炎症和细胞凋亡[15]。本研究结果显示,经LPS干预髓核细胞后,miR-224-3p表达水平显著下调、JAK1和STAT表达上调,猜测JAK/STAT信号通路介导椎间盘退变的病理进程,而miRNA可能影响JAK/STAT信号通路活性。细胞转染实验结果显示,过表达miR-224-3p可抑制细胞凋亡和炎性细胞因子水平、增加aggrecan和CollagenⅡ的表达量从而减少细胞外基质降解,同时p-JAK1/JAK1和p-STAT1/STAT1的蛋白表达水平显著下降。这可能说明miR-224-3p通过抑制JAK1/STAT1信号通路的活性发挥对髓核细胞的调节作用。本研究结果显示,过表达JAK1可逆转过表达miR-224-3p对椎间盘退变髓核细胞的凋亡和炎症的改善作用,从而证明了miR-224-3p通过抑制JAK1/STAT1通路活性发挥对髓核细胞的改善作用。
综上所述,人椎间盘退变髓核细胞中miR-224-3p的表达水平显著下调,过表达miR-224-3p可通过靶向JAK1抑制JAK/STAT信号通路活性,从而抑制LPS诱导的人髓核细胞凋亡、炎症反应和细胞外基质降解,提高细胞活力。miR-224-3p可能是椎间盘退变治疗的潜在靶点。本文只是对miR-224-3p在椎间盘退变中作用的初步研究,为了阐明miR-224-3p在椎间盘退变中的具体作用机制,还需要开展大量深入的实验及临床研究进一步验证。
| [1] |
SAMANTA A, LUFKIN T, KRAUS P. Intervertebral disc degeneration-current therapeutic options and challenges[J]. Front Public Health, 2023, 11: 1156749. DOI:10.3389/fpubh.2023.1156749 |
| [2] |
CHEN SL, LEI LC, LI ZM, et al. Grem1 accelerates nucleus pulposus cell apoptosis and intervertebral disc degeneration by inhibiting TGF-β-mediated Smad2/3 phosphorylation[J]. Exp Mol Med, 2022, 54(4): 518-530. DOI:10.1038/s12276-022-00753-9 |
| [3] |
TIAN Z, GAO HR, XIA WJ, et al. S1PR3 suppresses the inflammatory response and extracellular matrix degradation in human nucleus pulposus cells[J]. Exp Ther Med, 2024, 27(6): 265. DOI:10.3892/etm.2024.12553 |
| [4] |
DU XX, WANG XY, CUI KY, et al. TanshinoneⅡA and astragaloside Ⅳ inhibit miR-223/JAK2/STAT1 signalling pathway to alleviate lipopolysaccharide-induced damage in nucleus pulposus cells[J]. Dis Markers, 2021, 2021: 6554480. DOI:10.1155/2021/6554480 |
| [5] |
DONG XW, HU FQ, YI J, et al. DPSCs protect architectural integrity and alleviate intervertebral disc degeneration by regulating nucleus pulposus immune status[J]. Stem Cells Int, 2022, 2022: 7590337. DOI:10.1155/2022/7590337 |
| [6] |
DONG L, DONG B. miR-489-3p overexpression inhibits lipopolysaccharide-induced nucleus pulposus cell apoptosis, inflammation and extracellular matrix degradation via targeting Toll-like receptor 4[J]. Exp Ther Med, 2021, 22(5): 1323. DOI:10.3892/etm.2021.10758 |
| [7] |
陈泉润, 蒋玉芹, 刘鹏, 等. miR-224-3p靶向肿瘤坏死因子超家族成员14抑制脂质积累和动脉粥样硬化的研究[J]. 实用医院临床杂志, 2022, 19(6): 1-6. |
| [8] |
唐盼, 刘渤. 锌指蛋白A20对LPS刺激时人退变髓核细胞衰老与凋亡的影响[J]. 陆军军医大学学报, 2022, 44(16): 1613-1620. DOI:10.16016/j.2097-0927.202203143 |
| [9] |
CHIU AP, CHIA C, ARENDT-NIELSEN L, et al. Lumbar intervertebral disc degeneration in low back pain[J]. Minerva Anestesiol, 2024, 90(4): 330-338. DOI:10.23736/S0375-9393.24.17843-1 |
| [10] |
SHI ZT, HE J, HE J, et al. High hydrostatic pressure (30 atm) enhances the apoptosis and inhibits the proteoglycan synthesis and extracellular matrix level of human nucleus pulposus cells via promoting the Wnt/β-catenin pathway[J]. Bioengineered, 2022, 13(2): 3070-3081. DOI:10.1080/21655979.2022.2025518 |
| [11] |
GHAFFARPASAND F, SARHADI S, ALAVI MH, et al. Modifications of miRNAs in intervertebral disc degeneration: a key to the future development of genetic-based therapies[J]. Epigenomics, 2023, 15(5): 271-281. DOI:10.2217/epi-2022-0277 |
| [12] |
ZHENG YC, CHEN XS, LAN T, et al. Panax notoginseng saponin reduces IL-1β-stimulated apoptosis and endoplasmic reticulum stress of nucleus pulposus cells by suppressing miR-222-3p[J]. Ann Transl Med, 2022, 10(13): 748. DOI:10.21037/atm-22-3203 |
| [13] |
XU HJ, LIAO W, LIU XZ, et al. Down-regulation of exosomal microRNA-224-3p derived from bone marrow-derived mesenchymal stem cells potentiates angiogenesis in traumatic osteonecrosis of the femoral head[J]. FASEB J, 2019, 33(7): 8055-8068. DOI:10.1096/fj.201801618RRR |
| [14] |
WANG CL, CUI LQ, GU QW, et al. The mechanism and function of miRNA in intervertebral disc degeneration[J]. Orthop Surg, 2022, 14(3): 463-471. DOI:10.1111/os.13204 |
| [15] |
周怡锦, 祝志朋, 田新磊, 等. 益气温肺通窍方通过调节JAK1/STAT3信号通路减轻肺气虚寒型变应性鼻炎大鼠炎症反应[J]. 中国医科大学学报, 2025, 54(9): 826-831. DOI:10.12007/j.issn.0258-4646.2025.09.011 |
 2026, Vol. 55
2026, Vol. 55