文章信息
- 陈艳林, 张晓敏, 刘娜, 袁慧敏, 邢珍, 姚杰
- CHEN Yanlin, ZHANG Xiaomin, LIU Na, YUAN Huimin, XING Zhen, YAO Jie
- 异氟醚调节AMPK/mTOR信号通路减轻大鼠缺氧/复氧所致的心肌细胞损伤
- Isoflurane alleviates hypoxia/reoxygenation-induced cardiomyocyte injury in rats via regulating AMPK/mTOR signaling pathway
- 中国医科大学学报, 2026, 55(3): 259-264, 271
- Journal of China Medical University, 2026, 55(3): 259-264, 271
-
文章历史
- 收稿日期:2025-01-24
- 网络出版时间:2026-03-24 16:58:40
缺氧/复氧(hypoxia/reoxygenation,H/R)可诱导活性氧(reactive oxygen species,ROS)和炎性细胞因子大量产生,引发心肌细胞氧化应激及炎症损伤,是缺血性心脏病及缺血/再灌注所致心肌损伤发生的主要病理基础,抑制炎症和脂质过氧化可减轻心肌损伤[1-2]。AMPK/mTOR可通过调控细胞凋亡、炎症与脂质过氧化等介导心血管疾病发病过程,上调磷酸化AMPK并下调磷酸化mTOR可减轻H/R诱导的心肌细胞损伤,激活AMPK/mTOR信号通路是防治心肌缺血/再灌注损伤的有效策略[3-4]。
异氟醚是一种常用的吸入麻醉剂,有心脏保护作用,可通过抑制氧化应激和心肌炎症减轻缺血/再灌注引发的心肌细胞凋亡和心肌损伤[5],还可通过激活AMPK信号通路改善脑缺血/再灌注损伤大鼠神经功能和认知障碍[6],因此推测异氟醚可能通过激活AMPK/mTOR信号通路来防治心肌缺血/再灌注损伤。本研究旨在探讨异氟醚调节AMPK/mTOR信号通路对H/R诱导的心肌细胞的保护作用,为异氟醚合理应用于心肌缺血/再灌注损伤的临床防治提供理论依据。
1 材料与方法 1.1 细胞及培养基大鼠心肌细胞系H9c2、DMEM培养基(无血清和葡萄糖)、DMEM完全培养基(含10%胎牛血清、1 000 mg/L葡萄糖),购自武汉普诺赛生命科技有限公司。
1.2 主要试剂及仪器异氟醚(液体,蒸汽压238 mmHg)购自美国Sigma-Aldrich公司;AMPK抑制剂化合物C(compound C,CC)购自美国Glpbio公司;HRP-二抗、CCK-8试剂盒、线粒体膜电位(mitochondrial membrance proteintial,∆Ψm)检测(JC-1法)试剂盒、大鼠肿瘤坏死因子α(tumor necrosis factor α,TNF-α)与白细胞介素-6(interleukin-6,IL-6)酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)试剂盒、过氧化氢酶(catalase,CAT)与超氧化物歧化酶(superoxide dismutase,SOD)活性检测试剂盒、ROS检测试剂盒、Annexin V-FITC凋亡检测试剂盒、p-AMPK、GAPDH、AMPK、p-mTOR、mTOR一抗购自英国abcam公司。
流式细胞仪、全自动酶标仪(型号Attune NxT、Multiskan FC)购自美国ThermoFisher Scientific公司;倒置荧光显微镜(型号Ⅸ71)购自日本Olympus公司;超薄切片机(型号UC7)购自德国Leica公司;透射电子显微镜(型号H-7500)购自日本HITACHI公司;含基础电源、垂直槽、转印槽的垂直电泳转印套装(型号1658033)购自美国Bio-Rad公司。
1.3 方法 1.3.1 异氟醚作用浓度筛选H9c2细胞快速解冻复苏,在95%空气、5%CO2和37 ℃条件下用DMEM完全培养基进行传代培养,取第3代细胞接种于96孔板培养24 h,用0.5%、1%、2%、3%异氟醚干预20 min[7],然后进行H/R处理[7]。在95% N2、5%CO2和37 ℃条件下用DMEM培养基缺氧培养6 h,然后将培养基替换为DMEM完全培养基并在95%空气、5%CO2和37 ℃条件下复氧3 h,取出细胞,用CCK-8试剂孵育2 h后按CCK-8试剂盒操作说明测定各组吸光度(absorbance,A)值。
1.3.2 心肌细胞H/R处理与药物处理取第3代H9c2细胞接种于24孔板培养24 h,随机分为空白组、H/R组、异氟醚组、CC组、异氟醚+CC组。空白组细胞不做任何干预,其余各组按照缺氧6 h后复氧3 h进行H/R处理。在H/R处理前异氟醚组用2%异氟醚干预20 min,CC组用5 μg/mL的CC干预20 min[8],异氟醚+CC组用2%异氟醚和5 μg/mL的CC联合干预20 min,H/R组不进行药物干预。各组细胞于复氧3 h后进行后续检测。
1.3.3 CCK-8法、JC-1荧光染色、流式细胞术分别检测各组细胞活力、∆Ψm及凋亡率 1.3.3.1 细胞活力检测取第3代细胞接种于96孔板培养24 h,参照1.3.2中方法分组并进行H/R处理与药物处理,用CCK-8法检测各组细胞活力。
1.3.3.2 ∆Ψm检测取1.3.2中处理后的各组H9c2细胞,洗涤、固定后加入JC-1荧光探针,按线粒体膜电位检测试剂盒说明书中方法进行JC-1荧光染色后荧光显微镜下拍照、定量荧光强度,用红/绿荧光强度比值评测∆Ψm。
1.3.3.3 凋亡率检测取1.3.2中处理后的各组H9c2细胞,用PBS缓冲液洗涤、重悬制为单细胞悬液,以5×105/mL的细胞密度孵育Annexin V-FITC和PI,按Annexin V-FITC凋亡检测试剂盒说明书中方法,用流式细胞术检测各组细胞凋亡率。
1.3.4 透射电镜观察各组H9c2细胞超微结构取1.3.2中处理后的各组H9c2细胞进行消化、离心后,用2.5%戊二醛固定离心管底部细胞团2 h,取出细胞团用1%四氧化锇再次固定15 min,用丙酮脱水后包埋制备超薄切片,进行柠檬酸铅/醋酸双氧铀双染后,在透射电镜下观察细胞超微结构。
1.3.5 流式细胞术检测各组H9c2细胞ROS水平取1.3.2中处理后的各组H9c2细胞进行消化、离心后,用DCFDA工作液重悬、孵育,按细胞ROS检测试剂盒说明书中方法用流式细胞术检测各组细胞ROS水平。
1.3.6 测定各组H9c2细胞抗氧化酶活性与炎性细胞因子水平取1.3.2中处理后的各组H9c2细胞及其培养基,用RIPA裂解液裂解、离心。按照CAT与SOD活性检测试剂盒说明书中方法,用酶标仪测定上清中CAT与SOD活性水平;按照ELISA说明书中方法用酶标仪测定上清中IL-6与TNF-α水平。
1.3.7 Westernblotting检测各组H9c2细胞AMPK/mTOR信号通路蛋白表达:取1.3.2处理后的各组H9c2细胞及其培养基,用RIPA裂解液裂解、离心后用BCA法测定上清中蛋白浓度,煮沸变性蛋白后上样(20 µg/孔)上样,于120 V恒压下进行电泳后在40 mA稳定电流下做全湿电转,膜上蛋白封闭后,于4 ℃下孵育p-AMPK、GAPDH、AMPK、p-mTOR、mTOR一抗过夜后,洗膜,37 ℃下孵育二抗,2 h后洗膜、显色、拍照、定量蛋白灰度值,以GAPDH为内参,计算各蛋白相对表达量。
1.4 统计学分析采用SPSS 26.0软件进行统计分析,数据以x±s表示,多组间比较采用单因素方差分析,事后进一步两两比较采用SNK-q检验,P < 0.05为差异有统计学意义。
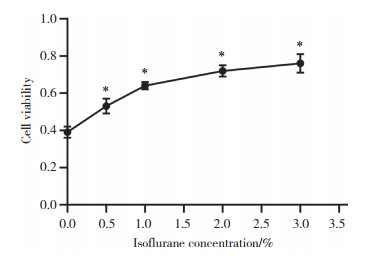
2 结果 2.1 异氟醚对H/R诱导的H9c2细胞活力的影响0.5%、1%、2%、3%异氟醚均可提高H/R诱导的H9c2细胞活力,且细胞活力随异氟醚浓度的升高逐渐提升,在浓度为2%时进入平台期,因而选择2%异氟醚进行后续细胞实验。见图 1。
|
| *P < 0.05 vs. 0% isoflurane. 图 1 不同浓度异氟醚对H/R诱导的H9c2细胞活力的影响 Fig.1 Effect of different isoflurane concentrations on H/R-induced H9c2 cell viability |
2.2 异氟醚对H/R诱导的H9c2细胞活力、∆Ψm及凋亡率的影响
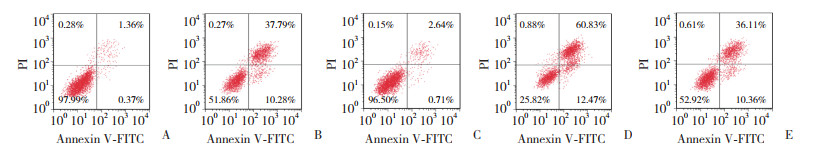
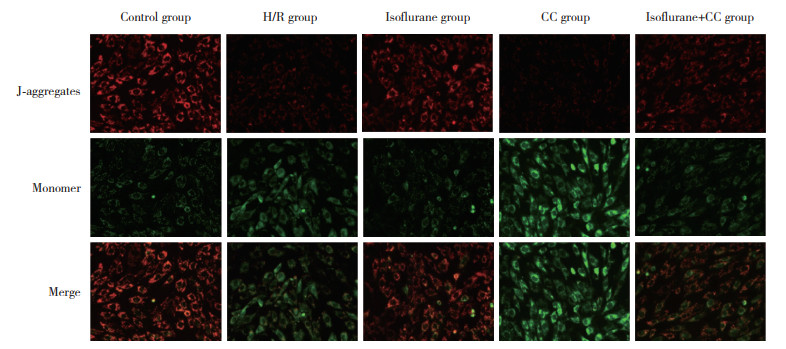
与空白组相比,H/R组细胞活力、∆Ψm降低,凋亡率升高(P均 < 0.05)。与H/R组相比,异氟醚组细胞活力、∆Ψm升高,凋亡率降低;CC组细胞活力、∆Ψm降低,凋亡率升高(P均 < 0.05)。与异氟醚组相比,异氟醚+CC组细胞活力、∆Ψm降低,凋亡率升高(P均 < 0.05)。见图 2、3,表 1。
|
| A, control group; B, H/R group; C, isoflurane group; D, CC group; E, isoflurane+CC group. 图 2 流式细胞术检测各组H9c2细胞凋亡率 Fig.2 Apoptosis rate of H9c2 cells detected using flow cytometry in each group |
|
| 图 3 JC-1荧光染色检测各组H9c2细胞∆Ψm ×200 Fig.3 JC-1 fluorescence staining for determining ∆Ψm of H9c2 cells in each group ×200 |
| Group | n | Cell viability(A value) | ∆Ψm | Apoptosis rate(%) |
| Control | 6 | 0.84±0.05 | 0.89±0.07 | 1.65±0.53 |
| H/R | 6 | 0.41±0.041) | 0.57±0.041) | 47.49±1.321) |
| Isoflurane | 6 | 0.81±0.062) | 0.85±0.062) | 3.27±0.802) |
| CC | 6 | 0.23±0.032) | 0.29±0.032) | 73.14±1.652) |
| Isoflurane+CC | 6 | 0.43±0.073) | 0.60±0.053) | 45.76±1.293) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. H/R group;3)P < 0.05 vs. isoflurane group. | ||||
2.3 异氟醚对H/R诱导的H9c2细胞超微结构的影响
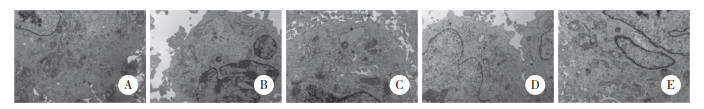
空白组细胞膜清晰、连续、完整,线粒体结构完好,细胞超微结构正常无病变;H/R组细胞膜破裂、模糊不清,线粒体肿胀且结构破损、模糊,线粒体嵴部分溶解、断裂且排列紊乱细胞超微结构发生明显病变;异氟醚组细胞膜结构相对完整,线粒体肿胀减轻,线粒体嵴基本恢复正常,细胞超微结构病变明显减轻;CC组细胞膜破损程度和线粒体肿胀更为严重,线粒体嵴大部分溶解、断裂,细胞超微结构病变加重;异氟醚+CC组细胞超微结构病变比异氟醚组严重,病变程度与H/R组相仿。见图 4。
|
| A, control group; B, H/R group; C, isoflurane group; D, CC group; E, isoflurane+CC group. 图 4 透射电镜观察各组H9c2细胞超微结构×15 000 Fig.4 Transmission electron microscopy images of ultrastructure of H9c2 cells in each group ×15 000 |
2.4 异氟醚对H/R诱导的H9c2细胞ROS水平的影响
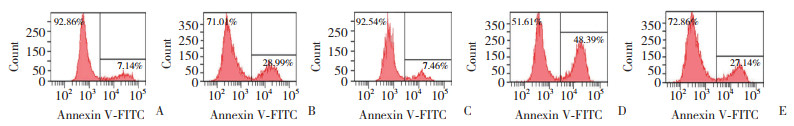
与空白组(7.06±1.83)相比,H/R组细胞ROS水平(28.54±2.65)升高(P < 0.05)。与H/R组相比,异氟醚组细胞ROS水平(7.91±1.72)降低;CC组细胞ROS水平(47.86±2.47)升高(P均 < 0.05)。与异氟醚组相比,异氟醚+CC组细胞ROS水平(26.79±2.30)升高(P < 0.05)。见图 5。
|
| A, control group; B, H/R group; C, isoflurane group; D, CC group; E, isoflurane+CC group. 图 5 流式细胞术检测各组H9c2细胞ROS水平 Fig.5 ROS levels in H9c2 cells in each group detected with flow cytometry |
2.5 异氟醚对H/R诱导的H9c2细胞抗氧化酶活性与炎性细胞因子水平的影响
与空白组相比,H/R组细胞CAT、SOD活性降低,IL-6、TNF-α水平升高(P均 < 0.05)。与H/R组相比,异氟醚组细胞CAT、SOD活性升高,IL-6、TNF-α水平降低(P均 < 0.05);CC组细胞CAT、SOD活性降低,IL-6、TNF-α水平升高(P均 < 0.05)。与异氟醚组相比,异氟醚+CC组细胞CAT、SOD活性降低,IL-6、TNF-α水平升高(P均 < 0.05)。见表 2。
| Group | n | CAT(U/mg prot) | SOD(U/mg prot) | IL-6(pg/mL) | TNF-α(pg/mL) |
| Control | 6 | 69.74±4.32 | 81.03±5.01 | 260.86±51.32 | 86.14±13.61 |
| H/R | 6 | 14.50±2.941) | 22.54±3.521) | 615.21±62.601) | 334.27±22.801) |
| Isoflurane | 6 | 64.82±3.962) | 76.39±5.132) | 283.15±54.792) | 97.05±16.142) |
| CC | 6 | 3.90±1.252) | 6.82±2.212) | 976.54±68.252) | 565.34±20.972) |
| Isoflurane+CC | 6 | 17.13±3.173) | 25.76±3.603) | 580.37±61.543) | 318.52±21.353) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. H/R group;3)P < 0.05 vs. isoflurane group. | |||||
2.6 异氟醚对H/R诱导的H9c2细胞AMPK/mTOR信号通路蛋白表达的影响
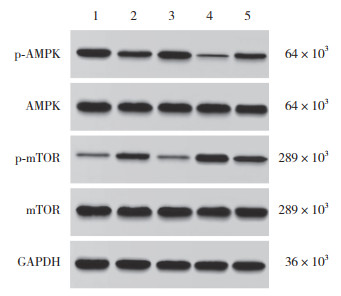
与空白组相比,H/R组细胞p-AMPK/AMPK降低,p-mTOR/mTOR升高(P均 < 0.05)。与H/R组相比,异氟醚组细胞p-AMPK/AMPK升高,p-mTOR/mTOR降低(P均 < 0.05);CC组细胞p-AMPK/AMPK降低,p-mTOR/mTOR升高(P均 < 0.05)。与异氟醚组相比,异氟醚+CC组细胞p-AMPK/AMPK降低,p-mTOR/mTOR升高(P均 < 0.05)。见图 6、表 3。
|
| 1, control group; 2, H/R group; 3, isoflurane group; 4, CC group; 5, isoflurane+CC group. 图 6 Western blotting检测各组H9c2细胞AMPK/mTOR信号通路蛋白表达 Fig.6 Western blotting of AMPK/mTOR signaling pathway protein expression levels in H9c2 cells in each group |
| Group | n | p-AMPK/AMPK | p-mTOR/mTOR |
| Control | 6 | 0.93±0.04 | 0.11±0.02 |
| H/R | 6 | 0.51±0.051) | 0.49±0.061) |
| Isoflurane | 6 | 0.91±0.082) | 0.12±0.032) |
| CC | 6 | 0.14±0.032) | 0.90±0.072) |
| Isoflurane+CC | 6 | 0.53±0.063) | 0.47±0.053) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. H/R group;3)P < 0.05 vs. isoflurane group. | |||
3 讨论
冠状动脉介入治疗和旁路移植等心脏血液再灌注治疗是缺血性心脏病的主要治疗手段,但可能会造成继发性心肌损伤,防止心肌缺血再灌注损伤发生是治疗缺血性心脏病的关键环节[9-10]。H/R处理的心肌细胞可在细胞水平上模拟心肌缺血/再灌注损伤病理过程[2, 11]。本研究对体外培养的大鼠心肌细胞系H9c2进行H/R处理,引发ROS、IL-6、TNF-α水平升高及抗氧化酶(CAT、SOD)活性明显降低,诱发严重细胞炎症与氧化应激,导致H9c2细胞活力、∆Ψm降低及凋亡率升高,最终造成心肌细胞大量凋亡和线粒体损伤,揭示心肌缺血/再灌注损伤体外细胞模型构建成功。
异氟醚作为临床常用的一种吸入性麻醉药物,表现出明显清除氧自由基、抗炎和抗凋亡作用,可通过减轻H/R诱导的心肌细胞凋亡和炎性损伤而发挥心肌保护作用[12-13]。本研究结果显示,用2%异氟醚预先干预H/R处理的H9c2细胞,可降低细胞凋亡率,ROS、IL-6与TNF-α水平,升高细胞活力和∆Ψm,并减轻其超微结构损伤,表明异氟醚预处理可减少H/R诱导的ROS与炎性细胞因子,提高抗氧化酶活性,抵抗H/R引发的心肌细胞凋亡与损伤,进一步证实了异氟醚在心肌缺血/再灌注损伤过程中的心肌保护作用。
AMPK/mTOR信号通路可通过调控炎症与氧化应激反应在心血管疾病中发挥关键作用。刺激其信号激活可发挥心脏保护作用[14],增强AMPK磷酸化可降低mTOR磷酸化水平,进而对抗缺氧诱导的心肌细胞损伤[15];并可通过抑制细胞凋亡、炎症与氧化应激而减轻心肌缺血/再灌注损伤[3-4]。本研究结果显示,H/R处理的H9c2细胞AMPK磷酸化水平相比正常培养细胞降低而mTOR磷酸化减弱,用2%异氟醚预处理H/R诱导的H9c2细胞可逆转AMPK/mTOR信号通路蛋白磷酸化变化趋势,提示AMPK/mTOR信号通路与异氟醚对H/R诱导心肌细胞损伤的保护作用密切相关;用异氟醚和AMPK抑制剂CC联合预处理H/R诱导的H9c2细胞,可减弱异氟醚预处理对H/R诱导的H9c2细胞凋亡的抑制作用及对其细胞活力的升高作用,逆转异氟醚预处理对H/R诱导心肌细胞损伤的缓解作用,揭示异氟醚预处理可通过激活AMPK信号通路对H/R诱导心肌细胞损伤发挥保护作用。
综上所述,异氟醚预处理可阻止H/R诱导的炎症与氧化应激反应,从而减轻H/R诱导的心肌细胞损伤与凋亡,激活AMPK/mTOR信号通路可能是异氟醚对H/R诱导心肌细胞发挥上述保护作用的药理机制,本研究为异氟醚用于心肌缺血/再灌注损伤的临床防治提供了新的理论依据,并初步阐明了其药理机制,有助于异氟醚在缺血性心脏病临床治疗中的应用。
| [1] |
XIANG Q, YI X, ZHU XH, et al. Regulated cell death in myocardial ischemia-reperfusion injury[J]. Trends Endocrinol Metab, 2024, 35(3): 219-234. DOI:10.1016/j.tem.2023.10.010 |
| [2] |
XU SJ, WU BX, ZHONG BY, et al. Naringenin alleviates myocardial ischemia/reperfusion injury by regulating the nuclear factor-erythroid factor 2-related factor 2 (Nrf2)/System xc-/glutathione peroxidase 4 (GPX4) axis to inhibit ferroptosis[J]. Bioengineered, 2021, 12(2): 10924-10934. DOI:10.1080/21655979.2021.1995994 |
| [3] |
SHEN LY, ZHU YW, CHEN ZF, et al. Isoliquiritigenin attenuates myocardial ischemia reperfusion through autophagy activation mediated by AMPK/mTOR/ULK1 signaling[J]. BMC Cardiovasc Disord, 2024, 24(1): 415. DOI:10.1186/s12872-024-04054-z |
| [4] |
YANG ZJ, ZHANG WF, JIN QQ, et al. Lactate contributes to remote ischemic preconditioning-mediated protection against myocardial ischemia reperfusion injury by facilitating autophagy via the AMP-activated protein kinase-mammalian target of rapamycin-transcription factor EB-connexin 43 axis[J]. Am J Pathol, 2024, 194(10): 1857-1878. DOI:10.1016/j.ajpath.2024.07.005 |
| [5] |
WANG XY, WANG YP, YUAN YW, et al. Isoflurane pretreatment protects against myocardial ischemia/reperfusion injury via mediating lncRNA CASC15/miR-542-3p axis[J]. Toxicol Mech Methods, 2024, 34(6): 694-702. DOI:10.1080/15376516.2024.2327057 |
| [6] |
ZHAI JW, LI N, ZHANG X, et al. Isoflurane enhances autophagy by activating AMPK/ULK1, inhibits NLRP3, and reduces cognitive impairment after cerebral ischemia-reperfusion injury in rats[J]. J Mol Neurosci, 2023, 73(7-8): 549-562. DOI:10.1007/s12031-023-02135-w |
| [7] |
QI KK, CAO F, WANG J, et al. miR-652-3p suppressed the protective effects of isoflurane against myocardial injury in hypoxia/reoxygenation by targeting ISL1[J]. Cardiovasc Toxicol, 2024, 24(7): 646-655. DOI:10.1007/s12012-024-09870-5 |
| [8] |
周云洁, 常红波, 王新洲. 龙牙楤木总皂苷通过调控AMPK/Nrf2信号抑制缺氧/复氧诱导的心肌细胞铁死亡[J]. 中药材, 2023, 46(12): 3091-3096. DOI:10.13863/j.issn1001-4454.2023.12.030 |
| [9] |
SAGRIS M, APOSTOLOS A, THEOFILIS P, et al. Myocardial ischemia-reperfusion injury: unraveling pathophysiology, clinical manifestations, and emerging prevention strategies[J]. Biomedicines, 2024, 12(4): 802. DOI:10.3390/biomedicines12040802 |
| [10] |
李柳, 李敏, 郑庆厚, 等. 应用D-SPECT评估远程缺血预适应联合腺苷注射液在PCI患者中的作用[J]. 中国医科大学学报, 2024, 53(8): 725-730. DOI:10.12007/j.issn.0258-4646.2024.08.009 |
| [11] |
LI SN, LI FM, WANG Y, et al. Multiple delivery strategies of nanocarriers for myocardial ischemia-reperfusion injury: current strategies and future prospective[J]. Drug Deliv, 2024, 31(1): 2298514. DOI:10.1080/10717544.2023.2298514 |
| [12] |
HAN XF, KAN HY, SHI JY, et al. Isoflurane preconditioning alleviates hypoxia/reoxygenation-induced cardiomyocyte injury by inhibiting miR-195-3p expression[J]. Cardiovasc Toxicol, 2024, 24(7): 637-645. DOI:10.1007/s12012-024-09869-y |
| [13] |
ZHANG DB, WU QL, LIU FF, et al. Isoflurane preconditioning attenuates OGD/R-induced cardiomyocyte cytotoxicity by regulating the miR-210/BNIP3 axis[J]. J Appl Toxicol, 2024, 44(11): 1761-1772. DOI:10.1002/jat.4674 |
| [14] |
HUANG HF, WANG TL, WANG LP, et al. Saponins of Panax japonicus ameliorates cardiac aging phenotype in aging rats by enhancing basal autophagy through AMPK/mTOR/ULK1 pathway[J]. Exp Gerontol, 2023, 182: 112305. DOI:10.1016/j.exger.2023.112305 |
| [15] |
HU TH, WEN L, WANG L, et al. Luteoloside pretreatment attenuates anoxia-induced damage in cardiomyocytes by regulating autophagy mediated by 14-3-3η and the AMPKα-mTOR/ULK1 pathway[J]. Mol Cell Biochem, 2023, 478(7): 1475-1486. DOI:10.1007/s11010-022-04611-0 |
 2026, Vol. 55
2026, Vol. 55