文章信息
- 崔畅婉, 路一平, 鲍艺文, 吴思, 孙峥嵘
- CUI Changwan, LU Yiping, BAO Yiwen, WU Si, SUN Zhengrong
- SLC7A5促进TGF-β1诱导的小鼠胚胎成纤维细胞活化和增殖
- SLC7A5 promotes TGF-β1-induced activation and proliferation of mouse embryonic fibroblasts
- 中国医科大学学报, 2026, 55(3): 240-244
- Journal of China Medical University, 2026, 55(3): 240-244
-
文章历史
- 收稿日期:2025-04-29
- 网络出版时间:2026-03-24 15:21:31
慢性肾脏病的发病率逐年升高,目前已超过10%。肾纤维化是一个动态的、趋同的过程,是慢性肾脏病进展为终末期肾病的最终共同结局[1]。现有的研究表明,包括缺氧诱导因子[2]、转化生长因子β1(transforming growth factor β1,TGF-β1)[3]介导的信号通路参与缺氧诱导的间质纤维化的发病机制,而肾纤维化几乎是所有具有多种病因的晚期肾脏疾病的共同病理标志。肾纤维化的特征为成纤维细胞增殖、聚集并活化为肌成纤维细胞,细胞外基质合成增加,最终导致肾功能损害[4]。在糖尿病肾病、急性肾损伤、慢性肾脏病、肾病综合征中,均有多种机制触发活性氧(reactive oxygen species,ROS)的产生,因此研究氧化应激信号调节通路可能有助于找到治疗肾纤维化的有效靶点,进而抑制肾纤维化进展[5]。溶质载体(solute carrier,SLC)家族成员近年来受到广泛关注[6],溶质运载家族7成员5(solute carrier family 7 member 5,SLC7A5)是必需氨基酸(包括亮氨酸和苯丙氨酸)的膜转运蛋白,在细胞生长、增殖、分化等多种生命活动中发挥重要作用[7]。SLC7A5在慢性肾脏病进展中的作用有待进一步验证。本研究采用TGF-β1诱导的成纤维细胞体外模型,检测通过干扰SLC7A5基因表达,检测成纤维细胞增殖活化指标α平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)、波形蛋白(vimentin,Vim)、Ⅰ型胶原(typeⅠcollagen,COL-Ⅰ)和细胞增殖速率,探讨SLC7A5在促进成纤维细胞活化和增殖中的作用,为寻找肾纤维化的治疗靶点提供理论依据。
1 材料与方法 1.1 材料NIH3T3细胞,购自武汉普诺赛生命科技有限公司;PCR阵列(PCR array)检测试剂盒、RNA提取试剂盒,购自德国Qiagen公司;TGF-β1,购自北京义翘神州科技股份有限公司;CCK-8试剂盒,购自汉恒生物科技(上海)有限公司;ROS检测试剂盒、谷胱甘肽(glutathione,GSH)检测试剂盒,购自武汉赛维尔生物科技有限公司;SLC7A5、α-SMA,购自美国Immunoway公司;COL-Ⅰ、Vim、β-actin,购自英国abcam公司;反转录试剂盒和预混Ex TaqTM Ⅱ荧光定量试剂盒,购自日本TaKaRa公司;高速离心机(型号Sorvall ST8),购自美国ThermoFisher Scientific公司;Gel DocTM XR凝胶成像分析系统、PCR扩增仪(型号T100),购自美国Bio-Rad有限公司;实时荧光定量PCR仪(型号7500),购自美国Applied Biosystems公司。
1.2 实验方法 1.2.1 细胞模型建立将NIH-3T3细胞分为对照组(PBS组)和模型组(TGF-β1组)。将细胞以2×105/mL的密度接种于6孔板中,每组4个孔。在含10%胎牛血清和1%青链霉素双抗的DMEM培养基中培养12 h,细胞贴壁,更换无血清培养基继续培养24 h。PBS组和TGF-β1组分别加入终浓度5 ng/mL PBS和5 ng/mL TGF-β1培养24 h,刮取细胞,于-80 ℃冰箱中保存。
1.2.2 细胞转染将NIH-3T3细胞分为对照组(Con组)、沉默慢病毒组(sh-SLC组)、重表达慢病毒组(r-SLC组)。将细胞以2×105/mL的密度接种于6孔板中。Con组不进行病毒转染;sh-SLC组使用SLC7A5基因沉默慢病毒sh-SLC [汉恒生物科技(上海)有限公司]转染细胞;r-SLC组使用重表达慢病毒r-SLC [汉恒生物科技(上海)有限公司]转染细胞。在37 ℃、5%CO2条件下转染慢病毒72 h后,用嘌呤霉素(8 μg/mL)筛选稳定转染的细胞,刮取NIH-3T3细胞。Western blotting验证沉默和再表达的结果。慢病毒转染时,培养基中不含抗生素。
1.2.3 PCR array将从NIH-3T3细胞中提取的总RNA反转录为cDNA,使用德国Qiagen公司RT2 Profiler PCR Array Mouse Drug Transporters试剂盒,通过Qiagen RT2 Profiler PCR阵列数据分析网站(https://geneglobe.qiagen.com/us/analyze),分析NIH-3T3细胞中药物转运相关基因的表达变化。
1.2.4 ROS检测将DCFH-DA探针按1∶1 000的比例稀释,制备工作溶液。采用LSR Ⅱ流式细胞仪检测DCF荧光光谱,激发波长为488 nm,发射波长为525 nm,对细胞内ROS水平进行定量。
1.2.5 GSH检测收集1×107个细胞,加入200 μL蛋白去除剂进行超声裂解。按照说明书,制备检测探针溶液。搅拌后室温孵育5 min,采用酶标仪测定波长412 nm处的吸光度。
1.2.6 CCK-8法将2 000个细胞(总体积100 μL)接种于96孔板中。连续5 d,每天采用CCK-8试剂盒检测细胞增殖情况。采用SpectraMax iD5酶标仪测定波长450 nm处的吸光度。
1.2.7 Western blotting使用RIPA裂解液提取肾组织蛋白,按照说明书添加蛋白酶抑制剂和磷酸酶抑制剂,抑制蛋白降解。提取细胞蛋白质,用预冷PBS清洗细胞,按1×106个细胞与1 mL RIPA裂解液的比例,超声破碎,冰上孵育1 h。应用BCA检测试剂盒,对裂解产物中的蛋白质含量进行定量。使用预制PAGE凝胶,进行蛋白电泳。随后将蛋白转移到PVDF膜上,PVDF膜与一抗在4 ℃孵育过夜。次日,室温下孵育二抗1 h。利用ECL显色液对所需蛋白条带进行显色。使用GelDocTM XR成像分析系统对印迹进行可视化处理。使用ImageJ软件对波段强度进行量化。
1.2.8 实时定量PCR使用RNA提取试剂盒提取成纤维细胞中总RNA。利用反转录试剂盒,将RNA逆转录为cDNA。采用预混Ex TaqTMⅡ荧光定量试剂盒进行实时PCR。所有实验步骤均按照说明书进行。PCR扩增:95 ℃ 30 s预变性,95 ℃ 5 s,60 ℃ 34 s,40个循环。采用2-ΔΔCt法测定靶基因的相对表达量,以β-actin为内参,计算靶基因的循环时间Ct值。引物序列:α-SMA,正向5’-GTCCCAGACATCAGGGAGTAA-3’,反向5’-TCGGATACTTCAGCGTCAGGA-3’;COL-Ⅰ,正向5’-GCTCCTCTTAGGGGC CACT-3’,反向5’-CCACGTCTCACCATTGGGG-3’;β-actin,正向5’-GGCTGTATTCCCCTCCATCG-3’,反向5’-CCAGTTGGTAACAATGCCAT GT-3’;Vim,正向5’-CGTCCACACGCACCTACAG-3’,反向5’-GGGGGATGAGGAATAGAGGCT-3’;SLC7A5,正向5’-ATATCACGCTGCTCAAC GGTG-3’,反向5’-CTCCAGCATGTAGGCGxTAGTC-3’。
1.3 统计学分析采用GraphPad Prism 8.0.2软件进行统计学分析。数据进行归一化处理,以对照组均值为基准,各实验组数据除以该均值,所得数值即为相对于照组的倍数变化。符合正态分布的计量资料用x±s表示,2组间比较采用t检验,多组间比较采用单因素方差分析,进一步两两比较采用Tukey法。P < 0.05为差异有统计学意义。
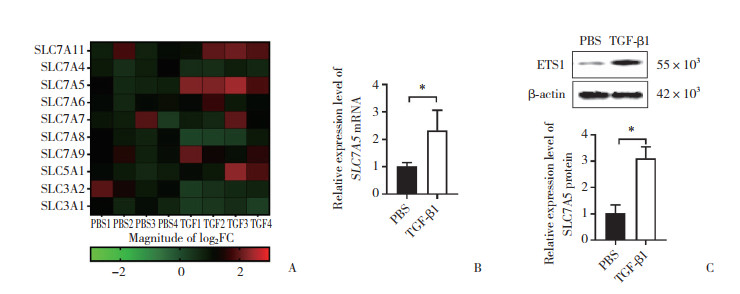
2 结果 2.1 PCR array、实时定量PCR、Western blotting验证TGF-β1孵育的成纤维细胞中SLC7A5高表达与PBS组相比,TGF-β1组NIH-3T3成纤维细胞中SLC7A5 mRNA和蛋白表达水平显著升高(P < 0.05)。见图 1。
|
| A, a PCR array was used to detect the differentially expressed genes of NIH-3T3 fibroblasts in the PBS and TGF-β1 groups; B, real-time quantitative PCR was used to determine the difference in SLC7A5 transcript levels between the PBS and TGF-β1 groups; C, Western blotting was used to detect the difference in SLC7A5 protein levels between the PBS and TGF-β1 groups. *P < 0.001. 图 1 PCR array、实时定量PCR、Western blotting验证TGF-β1孵育的成纤维细胞中SLC7A5高表达 Fig.1 High expression of SLC7A5 in the fibroblasts incubated with TGF-β1, as verified using a PCR array, real-time PCR, and Western blotting |
2.2 慢病毒转染细胞效率验证和成纤维细胞增殖活化指标改变
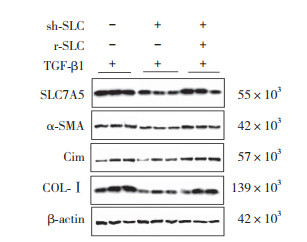
与Con组相比,sh-SLC组细胞中SLC7A5以及成纤维细胞活化增殖指标α-SMA、Vim和COL-Ⅰ mRNA和蛋白表达水平显著下降(P < 0.05);与sh-SLC组相比,r-SLC组细胞中SLC7A5、α-SMA、Vim和COL-Ⅰ mRNA和蛋白表达水平显著升高(P < 0.05)。见表 1、图 2。
| Item | Con group(n = 3) | sh-SLC group(n = 3) | r-SLC group(n = 3) |
| SLC7A5 | |||
| mRNA | 1.000±0.118 | 0.376±0.2521) | 1.251±0.2162) |
| Protein | 1.000±0.229 | 0.476±0.1931) | 1.242±0.2052) |
| α-SMA | |||
| mRNA | 1.000±0.159 | 0.476±0.0941) | 1.192±0.1682) |
| Protein | 1.000±0.135 | 0.526±0.1671) | 1.159±0.1472) |
| Vim | |||
| mRNA | 1.000±0.2201) | 0.501±0.1001) | 1.192±0.2092) |
| Protein | 1.000±0.248 | 0.448±0.0931) | 1.231±0.1792) |
| COL-Ⅰ | |||
| mRNA | 1.000±0.122 | 0.526±0.0771) | 1.092±0.1962) |
| Protein | 1.000±0.302 | 0.521±0.0951) | 1.037±0.1642) |
| GSH | 1.000±0.199 | 0.506±0.1011) | 1.154±0.1382) |
| ROS | 1.000±0.198 | 1.429±0.1921) | 0.931±0.2282) |
| 1)P < 0.05 vs. Con group;2)P < 0.05 vs. sh-SLC group. | |||
|
| 图 2 Western blotting检测SLC7A5、α-SMA、Vim和COL-Ⅰ蛋白的表达 Fig.2 Expression of SLC7A5, α-SMA, Vim, and COL-Ⅰ proteins, as detected by Western blotting |
2.3 慢病毒转染对成纤维细胞氧化应激和增殖效率影响
与Con组相比,sh-SLC组细胞中ROS累积量显著增加,GSH含量显著下降(P < 0.05);与sh-SLC组相比,r-SLC组细胞中ROS累积量显著减少,GSH含量显著增加(P < 0.05)。见表 1。
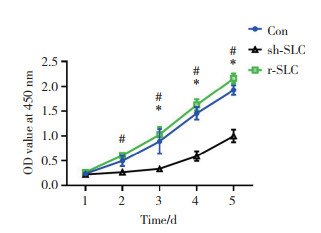
与Con组相比,sh-SLC组细胞增殖速率显著降低(P < 0.05);与sh-SLC组相比,r-SLC组细胞增殖速率显著升高(P < 0.05)。见图 3。
|
| * P < 0.05 vs. Con group; # P < 0.05 vs. sh-SLC group. 图 3 CCK-8法检测各组细胞增殖速率 Fig.3 Cell proliferation rate in each group, as detected by CCK-8 assay |
3 讨论
肾纤维化是所有慢性肾脏病进展过程中的共同病理表现,但目前仍缺乏有效的治疗方法。因此,研究肾纤维化的发病机制,寻找新的抗纤维化治疗靶点,具有重要意义。本研究着重探究药物转运相关基因在成纤维细胞活化和增殖中的作用,为慢性肾脏病临床治疗寻找新的靶点。
成纤维细胞在肾纤维化中起关键作用。成纤维细胞和肾小管上皮细胞通常相互进行信息传递,可在生理条件下促进肾脏组织修复,但当损伤持续存在时,成纤维细胞则过度增殖活化成为肌成纤维细胞,产生Vim和α-SMA,导致大量细胞外基质的分泌,促进肾纤维化[8]。因此,抑制成纤维细胞增殖对于缓解肾纤维化具有重要意义。本研究通过TGF-β1诱导纤维化体外模型,探究调控成纤维细胞活化和增殖的关键靶点,并通过慢病毒转染改变靶基因SLC7A5表达效率,进而探究SLC7A5在成纤维细胞活化和增殖中的作用。
细胞增殖所需的底物通过特定的转运蛋白从细胞外转运到细胞内。这些转运蛋白在促进细胞增殖中起关键作用。SLC最初被鉴定为是一组广泛表达于细胞膜上的转运蛋白。现有研究表明,SLC7A5基因的表达水平由于组织部位和细胞类型不同而不同,如在正常的胎盘[9]、睾丸[10]、大脑[11]等组织中呈高表达,可能为这些组织细胞的快速增殖提供所需的必需氨基酸。此外,SLC7A5在肿瘤细胞中也大量表达,在SLC7A5被抑制的肿瘤细胞中,克隆形成受到限制,表明SLC7A5在细胞增殖中可能具有重要作用[12]。而SLC7A5对肾纤维化疾病进展的影响仍不明确。本研究通过PCR array筛选目标基因SLC7A5,并在体外实验中证明SLC7A5与成纤维细胞的增殖速率有关,表明SLC7A5可能影响成纤维细胞增殖,进而影响纤维化进展。
ROS通过激活胞外信号调节激酶、活化B细胞的核因子κ轻链增强子等通路促进纤维化进展[13]。GSH具有抗氧化作用和整合解毒作用,能够保护细胞免受自由基、重金属、毒素等有害物质的损伤,维持细胞内氧化还原平衡,同时GSH可以通过调节细胞信号传导途径,影响细胞的增殖、分化和凋亡[14]。GSH的抗氧化作用主要表现在以下几个方面:直接清除体内产生的过氧化氢、过氧化脂质、羟基自由基等ROS物质,减少它们对细胞的损害[15]。本研究中,沉默SLC7A5促进ROS累积,抑制GSH合成,而恢复SLC7A5表达能够逆转这种现象。结果提示,SLC7A5可能通过调节成纤维细胞氧化应激状态调节细胞增殖。
综上所述,本研究证明,SLC7A5能够促进成纤维细胞中Vim和α-SMA表达,诱导成纤维细胞活化和增殖,并且能够调节成纤维细胞内氧化还原状态,影响细胞增殖速率。抑制SLC7A5表达能够降低成纤维细胞在TGF-β1诱导纤维化体外模型中增殖和活化。进一步探究SLC7A5作为治疗靶点在人类慢性肾脏病中的预防或辅助治疗作用,是未来的研究方向。
| [1] |
RAYEGO-MATEOS S, VALDIVIELSO JM. New therapeutic targets in chronic kidney disease progression and renal fibrosis[J]. Expert Opin Ther Targets, 2020, 24(7): 655-670. DOI:10.1080/14728222.2020.1762173 |
| [2] |
DI W, LI Y, ZHANG L, et al. The hippo-YAP1/HIF-1α pathway mediates arsenic-induced renal fibrosis[J]. Environ Res, 2024, 257: 119325. DOI:10.1016/j.envres.2024.119325 |
| [3] |
YAO M, LIAN D, WU M, et al. Isoliensinine attenuates renal fibrosis and inhibits TGF-β1/Smad2/3 signaling pathway in spontaneously hypertensive rats[J]. Drug Des Devel Ther, 2023, 17: 2749-2762. DOI:10.2147/DDDT.S414179 |
| [4] |
MENG XM. Inflammatory mediators and renal fibrosis[J]. Adv Exp Med Biol, 2019, 1165: 381-406. DOI:10.1007/978-981-13-8871-2_18 |
| [5] |
LI L, LU Z, PENG Y, et al. Oxidatively stressed extracellular microenvironment drives fibroblast activation and kidney fibrosis[J]. Redox Biol, 2023, 67: 102868. DOI:10.1016/j.redox.2023.102868 |
| [6] |
张凤英, 汤永红, 谢言青, 等. 过表达Slc1a2调节Glu/GABA平衡抑制铁死亡改善睡眠剥夺小鼠的认知功能障碍[J]. 中国医科大学学报, 2025, 54(11): 967-976. DOI:10.12007/j.issn.0258-4646.2025.11.002 |
| [7] |
DUNLAP KN, BENDER A, BOWLES A, et al. SLC7A5 is required for cancer cell growth under arginine-limited conditions[J]. Cell Rep, 2025, 44(1): 115130. DOI:10.1016/j.celrep.2024.115130 |
| [8] |
LIVINGSTON MJ, SHU S, FAN Y, et al. Tubular cells produce FGF2 via autophagy after acute kidney injury leading to fibroblast activation and renal fibrosis[J]. Autophagy, 2023, 19(1): 256-277. DOI:10.1080/15548627.2022.2072054 |
| [9] |
SCHROEDER M, FUENZALIDA B, YI N, et al. LAT1-dependent placental methionine uptake is a key player in fetal programming of metabolic disease[J]. Metabolism, 2024, 153: 155793. DOI:10.1016/j.metabol.2024.155793 |
| [10] |
HUTCHINSON K, SCHLESSINGER A. Comprehensive characterization of LAT1 cholesterol-binding sites[J]. J Chem Theory Comput, 2024, 20(8): 3349-3358. DOI:10.1021/acs.jctc.3c01391 |
| [11] |
KNAUS LS, BASILICO B, MALZL D, et al. Large neutral amino acid levels tune perinatal neuronal excitability and survival[J]. Cell, 2023, 186(9): 1950-1967.e25. DOI:10.1016/j.cell.2023.02.037 |
| [12] |
ZAUGG J, HUANG X, ZIEGLER F, et al. Small molecule inhibitors provide insights into the relevance of LAT1 and LAT2 in materno-foetal amino acid transport[J]. J Cell Mol Med, 2020, 24(21): 12681-12693. DOI:10.1111/jcmm.15840 |
| [13] |
SUN Z, JI Z, MENG H, et al. Lactate facilitated mitochondrial fission-derived ROS to promote pulmonary fibrosis via ERK/DRP-1 signaling[J]. J Transl Med, 2024, 22(1): 479. DOI:10.1186/s12967-024-05289-2 |
| [14] |
WEI Q, XIAO X, HUO E, et al. Hypermethylation and suppression of microRNA219a-2 activates the ALDH1L2/GSH/PAI-1 pathway for fibronectin degradation in renal fibrosis[J]. Mol Ther, 2025, 33(1): 249-262. DOI:10.1016/j.ymthe.2024.09.020 |
| [15] |
LAPENNA D. Glutathione and glutathione-dependent enzymes: from biochemistry to gerontology and successful aging[J]. Ageing Res Rev, 2023, 92: 102066. DOI:10.1016/j.arr.2023.102066 |
 2026, Vol. 55
2026, Vol. 55