文章信息
- 范晨, 陈维鹏, 张晓玲, 朱依谆
- FAN Chen, CHEN Weipeng, ZHANG Xiaoling, ZHU Yizhun
- CT影像组学对肾上腺非结节样增生患者高血压发生风险的预测价值
- Predictive value of computed tomography radiomics for thie risk of hypertension in patients with non-nodular adrenal hyperplasia
- 中国医科大学学报, 2026, 55(3): 227-233
- Journal of China Medical University, 2026, 55(3): 227-233
-
文章历史
- 收稿日期:2025-02-14
- 网络出版时间:2026-03-24 15:46:52
2. 珠海市人民医院医学影像中心, 广东 珠海 519000
2. Medical Imaging Center, Zhuhai People's Hospital, Zhuhai 519000, China
肾上腺性高血压约占继发性高血压的5%~10%,尽管其发病率较低,但通常较为顽固,且常伴有严重的并发症,因此早期识别与治疗至关重要[1-3]。研究[4]发现,肾上腺结节样增生是肾上腺性高血压的高危因素,以计算机断层扫描(computed tomography,CT)为核心的医学影像技术以及临床激素水平检测等手段有助于早期确诊、及时干预。但由于图像分辨率的限制,尽管肾上腺CT影像表现为非结节样增生,实际仍可能存在肉眼无法察觉的微小结节,这些隐匿微小结节依然会导致亚临床肾上腺功能障碍,从而增加心血管疾病的风险[5-6]。因此,如何早期识别这些隐匿的病变已成为临床亟待解决的难题。随着医学影像技术的不断进步和影像组学的兴起,通过影像组学手段分析CT影像中肾上腺非结节样增生与高血压患病风险之间的潜在关联变得愈加可行,有望为早期识别和有效预防高血压提供新的思路。
1 材料与方法 1.1 研究对象选取2018年1月1日至2023年7月1日在珠海市人民医院接受腹部CT门静脉期增强图像检查的住院患者,收集其临床资料和薄层重建图像。纳入标准:入院行腹部CT肾上腺增强检查,层厚1 mm、1.25 mm;门静脉期可清晰显示双侧肾上腺形态,肾上腺无明确结节样病变;临床病史(有无高血压病史)明确。高血压诊断采用世界卫生组织标准:未服用降压药的情况下,非同日3次测量血压,收缩压≥140 mmHg和(或)舒张压≥90 mmHg。排除标准:患有会导致肾上腺肿大的明确或疑似疾病,如脓毒血症、创伤和恶性肿瘤等;图像质量不佳,存在伪影干扰。本研究获得珠海市人民医院伦理委员会审查批准(ZH2025097)。本研究为回顾性设计,遵循《赫尔辛基宣言》原则,对所有数据进行了去标识化处理,获得了知情同意的豁免。
1.2 CT扫描方法采用3台不同型号的多层螺旋CT机(uCT780,上海联影医疗科技股份有限公司;SOMATOM Defintion Flash CT,德国西门子医疗系统有限公司;GE New Revolution 256层能谱CT,美国通用电气公司)进行腹部CT增强扫描。CT图像扫描参数如下:管电压,体重指数≤28 kg/m2的患者采用100 kVp,体重指数 > 28 kg/m2的患者采用120 kVp;管电流,自动管电流设置,与体型自动适配;视场(field of view,FOV),FOV与患者的体型大小相适应;造影剂,碘海醇以1.3 mL/kg计算,注药时间固定为30 s,注药流速根据患者体重、用药剂量和注药时间进行相应计算,造影剂最大用量≤100 mL;重建层厚与间距,uCT780和SOMATOM Defintion Flash CT的层厚为1.5 mm,间距为0.75 mm,GE New Revolution 256层能谱CT的层厚为1.25 mm,间距0.625 mm。增强时相统一采用肝门水平层面的腹主动脉作为触发层面,采用智能追踪法,相对CT值升高100 HU后,延时13 s扫描动脉期,动脉期后延时30 s扫描门脉期,门脉期后延时120 s扫描延时期。
1.3 CT形态学特征与影像组学特征提取由1位初级放射科医生(具有2年以上工作经验)在后处理工作站对肾上腺侧肢形态进行临床常规测量,主要包括双侧肾上腺体积、面积及内侧肢、外侧肢、结合部的厚度测量,每个部分的厚度均在检查时肾上腺最大的横轴位图像上确定;随后使用ITK-SNAP v3.6.0软件(https://www.itksnap.org/pmwiki/pmwiki.php)在每个CT图像中分别勾画左右肾上腺,并由1位正高级职称的放射科医生进行检查。然后,使用Pyradiomics(https://pyradiomics.readthedocs.io)影像组学特征提取包提取肾上腺相关的影像组学特征,主要包括统计学特征和高阶纹理特征,如灰度均值、肾上腺表面积、灰度共生矩阵、灰度大小区域矩阵、灰度游程矩阵、相邻灰度差矩阵、灰度相关矩阵等高阶影像组学特征。左、右肾上腺分别提取了1 223个特征,共提取了2 446个影像组学特征。
1.4 特征选择与模型构建将数据按照8∶2的比例随机拆分为训练集和验证集。为减少特征冗余,使用单因素逻辑回归分析对CT形态学特征筛选风险因素;运用LASSO回归模型对影像组学特征进行特征选择。然后使用逻辑回归算法对筛选的特征进行相应的模型构建。构建的模型包括基于CT形态学特征建立的CT形态学模型,基于CT增强图像的影像组学特征构建影像组学模型;结合CT形态学特征和影像组学特征建立的综合模型。所有模型均在训练集进行建模,并在验证集进行评估和验证。
1.5 统计学分析使用R(4.3.2)软件进行统计学分析。对于基线资料特征,计数资料以率(%)表示,组间比较采用χ2检验;正态分布计量资料采用x±s表示,2组间比较采用t检验;非正态分布计量资料则采用M(P25~P75)表示,2组间比较采用Mann-Whitney U检验。采用多因素逻辑回归分析构建预测模型,并通过受试者操作特征(receiver operating characteristic,ROC)曲线、曲线下面积(area under the curve,AUC)、校准曲线、决策曲线评价模型的性能,同时使用Delong检验对模型性能进行比较。最后,分别进行年龄和性别的亚组分析,以验证最优模型的稳定性与泛化能力。P < 0.05为差异有统计学意义。
2 结果 2.1 患者一般资料本研究共纳入452例患者,按照8∶2的比例随机分为训练集(360例,其中高血压136例;男174例,女186例)和验证集(92例,其中高血压35例;男47例,女45例)。2组患者的一般资料比较无统计学差异(P > 0.05),见表 1。
| Item | Training set(n = 360) | Validation set(n = 92) | P |
| Baseline | |||
| Hypertension [n(%)] | 136(37.78) | 35(38.04) | 0.963 |
| Age(year) | 57.00(47.00-66.00) | 56.00(46.00-62.25) | 0.224 |
| Male [n(%)] | 174(48.33) | 47(51.09) | 0.638 |
| Adrenal morphology | |||
| Left medial limb thickness(mm) | 4.94(4.10-5.69) | 5.01(3.95-5.82) | 0.934 |
| Left lateral limb thickness(mm) | 3.46(2.91-4.08) | 3.55(2.72-4.22) | 0.783 |
| Left junction thickness(mm) | 7.96(6.81-9.17) | 8.35(6.93-9.05) | 0.790 |
| Left adrenal area(mm2) | 162.61(133.54-208.25) | 180.94(141.16-221.27) | 0.182 |
| Left adrenal volume(mm3) | 3 523.76(2 953.38-4 239.75) | 2 458.07(3 037.00-4 459.30) | 0.268 |
| Right medial limb thickness(mm) | 3.69(3.22-4.32) | 3.77(3.08-4.43) | 0.560 |
| Right lateral limb thickness(mm) | 2.93(2.46-3.66) | 3.05(2.45-3.83) | 0.867 |
| Right junction thickness(mm) | 7.12(6.02-8.39) | 7.62(5.86-8.20) | 0.314 |
| Right adrenal area(mm2) | 159.75(133.90-192.94) | 167.55(132.37-196.80) | 0.782 |
| Right adrenal volume(mm3) | 2 340.33(2 006.41-3 006.30) | 2 672.26(1 977.31-3 148.59) | 0.606 |
2.2 特征筛选及模型构建
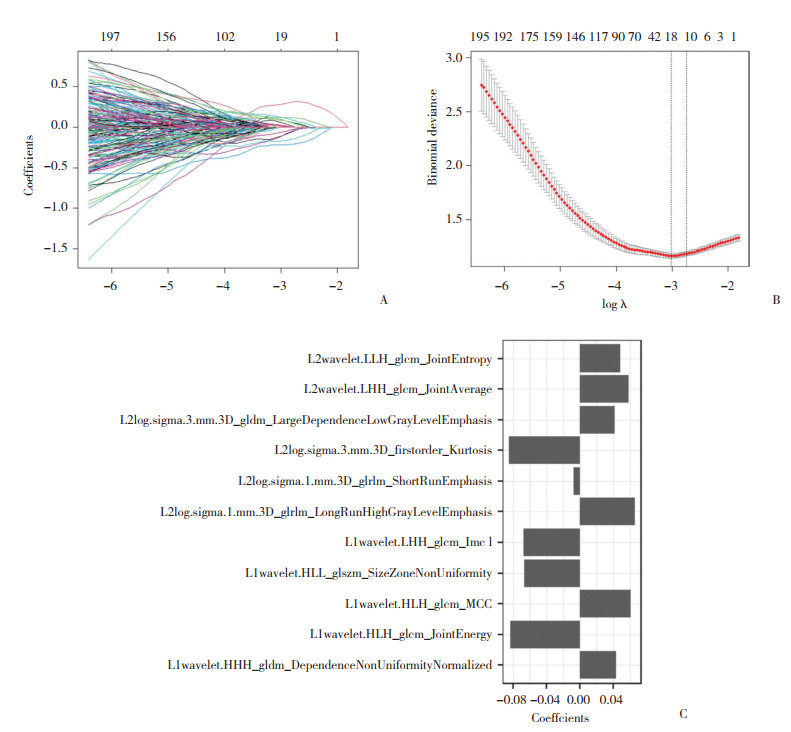
以有无高血压病史为因变量、肾上腺的形态学特征为自变量,进行单因素逻辑回归分析,最终确定了6个高血压相关的危险因素:左、右侧肾上腺的面积、体积及结合部厚度(表 2),并以此作为自变量,通过多因素logistic回归构建CT形态学模型。通过LASSO算法对提取的2 446个影像组学特征进行特征筛选,最终保留了11个关键影像组学特征,并据此构建影像组学模型(图 1)。最后联合上述2类(共17个)特征作为自变量,构建综合模型。
| Variable | Hypertension | ||
| OR | 95%CI | P | |
| Left adrenal area | 1.32 | 1.06-1.63 | 0.013 |
| Left adrenal volume | 1.39 | 1.12-1.72 | 0.003 |
| Left medial limb thickness | 1.20 | 0.97-1.49 | 0.089 |
| Left lateral limb thickness | 1.13 | 0.91-1.39 | 0.271 |
| Left junction thickness | 1.39 | 1.12-1.73 | 0.003 |
| Right adrenal area | 1.33 | 1.33-1.65 | 0.010 |
| Right adrenal volume | 1.35 | 1.08-1.67 | 0.007 |
| Right medial limb thickness | 1.02 | 0.83-1.02 | 0.843 |
| Right lateral limb thickness | 1.09 | 0.88-1.34 | 0.436 |
| Right junction thickness | 1.29 | 1.04-1.73 | 0.022 |
|
| A, radiomic features were selected by LASSO regression; B, 10-fold cross-validation was used to select adjustment parameters; C, selected features and their coefficients. 图 1 利用LASSO算法进行影像组学特征选择 Fig.1 Radiomics features were selected by LASSO regression |
2.3 模型的性能比较
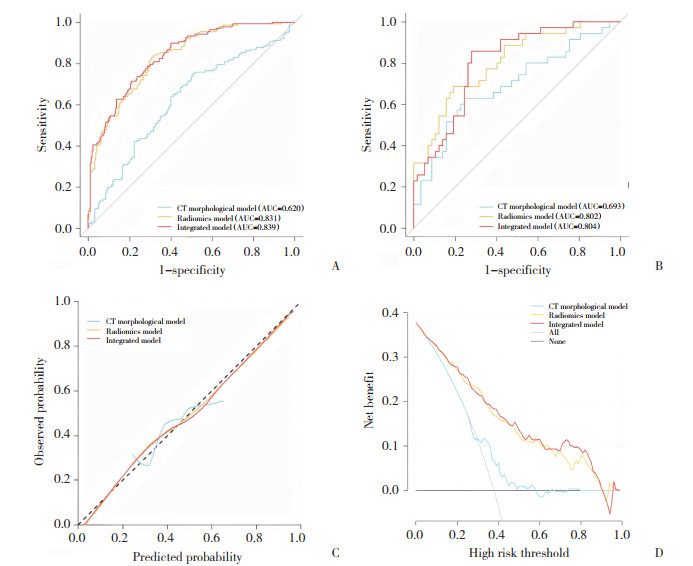
CT形态学、影像组学和综合模型的高血压预测性能比较分析结果见图 2。进一步对3个模型的AUC两两进行Delong检验,结果如表 3所示,影像组学模型和综合模型的预测性能更好,其AUC高于CT形态学模型,差异有统计学意义(P < 0.05)。影像组学模型和综合模型的AUC比较差异无统计学意义(P < 0.05)。
|
| A, ROC curves of different models in the training set; B, ROC curves of different models in the validation set; C, calibration curve in the training set; D, decision curve in the training set. 图 2 模型的性能比较 Fig.2 Performance comparison of the models |
| Model comparison | Training set(P) | Validation set(P) |
| CT morphological model vs. radiomics model | 1.64E-09 | 0.106 |
| CT morphological model vs. radiomics model | 2.03E-11 | 0.078 |
| Radiomics model vs. integrated model | 0.245 | 0.916 |
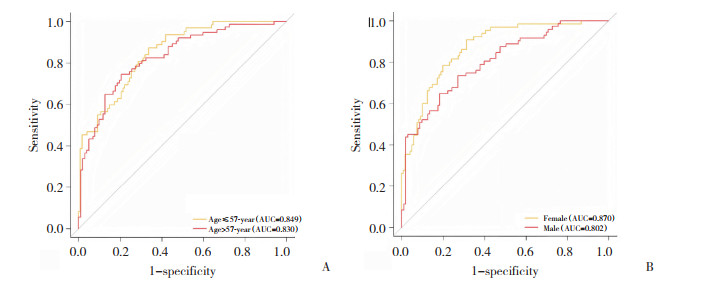
校准曲线表明综合模型在预测高血压患病风险方面与实际观测结果之间高度一致。决策曲线表明综合模型相较于单一的影像组学模型及临床模型具有更好的净收益。综合模型的亚组分析结果显示,模型在多个亚组中的预测性能均较为一致,不会因患者的年龄(P = 0.660)或性别(P = 0.110)等因素而显著偏离(图 3)。
|
| 图 3 综合模型在各年龄(A)和性别(B)亚组中的表现 Fig.3 Performance of the model in subgroups of age (A) and sex (B) |
3 讨论
肾上腺疾病是继发性高血压的常见原因之一,通过治疗肾上腺的原发疾病,大多数肾上腺源性高血压都可获得显著改善或治愈[7]。本研究根据患者的肾上腺CT影像,提取形态学特征以及影像组学特征,探讨了肾上腺非结节样增生与高血压患病风险的关联,旨在助力早期识别并预防肾上腺增生患者的高血压发展。
目前,肾上腺增生的放射学诊断主要依赖于肾上腺测量的主观评估。肾上腺体积已被提议作为下丘脑-垂体-肾上腺(hypothalamus-pituitary-adrenal,HPA)轴活动标准测量(如24 h尿游离皮质醇)的替代方法[8-9],用于评估各种精神疾病和恶性肿瘤患者的HPA轴功能[10-12]。本研究结果也证明,肾上腺形态学(两侧结合部厚度、面积、体积)增大会增加高血压的患病风险,这些形态学变化可能反映了肾上腺在高血压状态下的结构性改变,提示肾上腺非结节样增生在高血压中的潜在作用机制,这可能与醛固酮或皮质醇等激素的过量分泌有关,其通过影响HPA轴,导致激素(如醛固酮和皮质醇)的分泌异常,从而引发水钠潴留和血管收缩,进而维持高血压状态[13]。其次,高血压患者的肾上腺形态学变化可能是长期内分泌激素刺激的反应性表现,即肾上腺在持续的高血压环境中通过非结节样增生进行代偿性调节[14-15]。这种结构性变化可能在影像学上表现为厚度、面积和体积的增加,但并不形成明显的结节结构。
影像组学可用于捕获图像中深层次的病变纹理特征[16],以供进一步分析。在模型比较方面,本研究结果表明,影像组学模型和综合模型的性能在训练集中优于CT形态学模型。这些结果提示肾上腺的影像组学特征在预测高血压的发生中具有重要价值。在纳入的影像组学指标中,灰度共生矩阵特征描述了肾上腺图像中灰度强度的空间分布;灰度依赖矩阵特征量化肾上腺图像中的灰度级依赖关系;灰度区域大小矩阵特征通过量化左侧肾上腺图像灰度区域来表示区域中灰度等级的随机性;灰度游程矩阵特征用于计算右侧肾上腺具有相同灰度级值的连续体素的数量,并描述任何方向上不同灰度级强度的灰度级运行长度[17]。这些特征描述了肾上腺内体素密度的空间分布、纹理特性等,描述了肉眼难以在图像中感知的病变异质性信息。这表明肾上腺的异质性越大,高血压的患病风险越高。这些结果与ZHANG等[18]的研究结果一致,使用CT纹理分析显示,嗜铬细胞瘤比低脂肾上腺皮质腺瘤更具异质性。此外,尽管肾上腺CT形态学特征对高血压的识别能力相对有限,肾上腺的CT形态学特征和影像组学特征相结合具有提升模型性能的潜力,可视化的形态学特征和深层次的纹理特征相辅相成,有望为肾上腺非结节样增生合并高血压的临床诊疗提供辅助依据。
综上所述,本研究结果显示,CT所提示的肾上腺非结节样增生是高血压发生与进展的独立影响因素,肾上腺形态学的增大及纹理异质性的增加会增加高血压的患病风险。肾上腺影像组学模型具有较好的高血压预测价值。但本研究为单中心回顾性分析,数据量相对有限,未来仍需通过多中心大样本的数据库来进一步验证模型性能。
| [1] |
中华医学会老年医学分会, 中国医疗保健国际交流促进会高血压病分会. 老年高血压特点及临床诊治流程专家共识(2024)[J]. 中华老年医学杂志, 2024, 43(3): 257-268. DOI:10.3760/cma.j.issn.0254-9026.2024.03.001 |
| [2] |
REINCKE M, BANCOS I, MULATERO P, et al. Diagnosis and treatment of primary aldosteronism[J]. Lancet Diabetes Endocrinol, 2021, 9(12): 876-892. DOI:10.1016/S2213-8587(21)00210-2 |
| [3] |
FLESERIU M, AUCHUS R, BANCOS I, et al. Consensus on diagnosis and management of Cushing's disease: a guideline update[J]. Lancet Diabetes Endocrinol, 2021, 9(12): 847-875. DOI:10.1016/S2213-8587(21)00235-7 |
| [4] |
MORANI AC, JENSEN CT, HABRA MA, et al. Adrenocortical hyperplasia: a review of clinical presentation and imaging[J]. Abdom Radiol, 2020, 45(4): 917-927. DOI:10.1007/s00261-019-02048-6 |
| [5] |
TANG YZ, BHARWANI N, MICCO M, et al. Prevalence of incidentally detected adrenal enlargement on CT[J]. Clin Radiol, 2014, 69(1): e37-e42. DOI:10.1016/j.crad.2013.08.017 |
| [6] |
崔钟秀. 高血压伴肾上腺增生临床探讨[J]. 临床医药文献电子杂志, 2020, 7(21): 53. DOI:10.16281/j.cnki.jocml.2020.21.048 |
| [7] |
李星, 朱云鹏, 汪静, 等. 高血压伴无肾上腺激素生化异常的肾上腺偶发瘤外科治疗疗效及预后因素分析[J]. 临床泌尿外科杂志, 2021, 36(7): 513-518. DOI:10.13201/j.issn.1001-1420.2021.07.002 |
| [8] |
KIM TM, KIM JH, JANG HN, et al. Adrenal morphology as an indicator of long-term disease control in adults with classic 21-hydroxylase deficiency[J]. Endocrinol Metab, 2022, 37(1): 124-137. DOI:10.3803/EnM.2021.1278 |
| [9] |
赵志敏. 肾上腺性高血压影像学研究进展[J]. 实用放射学杂志, 2022, 38(1): 156-159. DOI:10.3969/j.issn.1002-1671.2022.01.037 |
| [10] |
HANTSOO L, JAGODNIK KM, NOVICK AM, et al. The role of the hypothalamic-pituitary-adrenal axis in depression across the female reproductive lifecycle: current knowledge and future directions[J]. Front Endocrinol, 2023, 14: 1295261. DOI:10.3389/fendo.2023.1295261 |
| [11] |
SWAINSON J, REESON M, MALIK U, et al. Diet and depression: a systematic review of whole dietary interventions as treatment in patients with depression[J]. J Affect Disord, 2023, 327: 270-278. DOI:10.1016/j.jad.2023.01.094 |
| [12] |
LI Y, ZHAO YN, YANG P, et al. Adrenal volume quantitative visualization tool by multiple parameters and an nnU-net deep learning automatic segmentation model[J]. J Imaging Inform Med, 2025, 38(1): 47-59. DOI:10.1007/s10278-024-01158-y |
| [13] |
MORANI AC, JENSEN CT, HABRA MA, et al. Adrenocortical hyperplasia: a review of clinical presentation and imaging[J]. Abdom Radiol, 2020, 45(4): 917-927. DOI:10.1007/s00261-019-02048-6 |
| [14] |
BOURDEAU I, PARISIEN-LA SALLE S, LACROIX A. Adrenocortical hyperplasia: a multifaceted disease[J]. Best Pract Res Clin Endocrinol Metab, 2020, 34(3): 101386. DOI:10.1016/j.beem.2020.101386 |
| [15] |
CHEVALIER B, VANTYGHEM MC, ESPIARD S. Bilateral adrenal hyperplasia: pathogenesis and treatment[J]. Biomedicines, 2021, 9(10): 1397. DOI:10.3390/biomedicines9101397 |
| [16] |
管超, 李梦玲, 蒋礼青, 等. 构建CT影像组学模型预测肺鳞状细胞癌肿瘤突变负荷[J]. 中国医科大学学报, 2022, 51(6): 481-485, 491. DOI:10.12007/j.issn.0258-4646.2022.06.001 |
| [17] |
LAFATA KJ, WANG YQ, KONKEL B, et al. Radiomics: a primer on high-throughput image phenotyping[J]. Abdom Radiol, 2022, 47(9): 2986-3002. DOI:10.1007/s00261-021-03254-x |
| [18] |
ZHANG GMY, SHI B, SUN H, et al. Differentiating pheochromocytoma from lipid-poor adrenocortical adenoma by CT texture analysis: feasibility study[J]. Abdom Radiol, 2017, 42(9): 2305-2313. DOI:10.1007/s00261-017-1118-3 |
 2026, Vol. 55
2026, Vol. 55