文章信息
- 杨燕梅, 任炜, 岳永生, 王丽影, 杨占君
- YANG Yanmei, REN Wei, YUE Yongsheng, WANG Liying, YANG Zhanjun
- 香青兰总黄酮对缺氧诱导损伤致HT22细胞铁死亡的影响及其作用机制
- Effects of total flavonoids of Dracocephalum moldavica L. on ferroptosis in HT22 cells caused by hypoxia-induced injury and its acting mechanism
- 中国医科大学学报, 2026, 55(3): 212-220
- Journal of China Medical University, 2026, 55(3): 212-220
-
文章历史
- 收稿日期:2025-09-12
- 网络出版时间:2026-03-24 13:12:43
2. 简阳市人民医院康复科, 成都 641400;
3. 赤峰学院人体解剖学教研室, 内蒙古 赤峰 024005
2. Department of Rehabilitation Medicine, Jianyang People's Hospital, Chengdu 641400, China;
3. Department of Human Anatomy, Chifeng University, Chifeng 024005, China
老年群体中血管性痴呆(vascular dementia,VaD)与心脑血管系统疾病患病率较高,给家庭和社会带来严重的经济压力[1]。脑血管疾病是VaD最常见的病因之一,并且根据血管病变的性质和程度、颅外和颅内血管受累的程度、受累脑区的解剖位置以及脑血管事件发生初始时间将VaD分为不同的亚型[2]。目前,VaD的具体发病机制仍未阐明。衰老导致机体多系统功能紊乱,在神经系统中可能与过度的氧化应激反应、神经慢性炎症、凋亡及神经元退行性病变有关[3]。研究[4]表明,在正常衰老过程中,铁在大脑特定功能区特定神经元与胶质细胞亚型中渐进性积累,铁积累最显著的大脑区域往往与多种神经系统疾病的发病及进展密切相关;游离铁的积累可通过凋亡和铁死亡等多种程序性细胞死亡途径导致神经元死亡。在阿尔茨海默病、帕金森病、亨廷顿病、运动神经元病及多发性硬化患者的脑组织与脑脊液中,铁水平升高和脂质过氧化加剧[5-6]。此外,铁死亡抑制剂去铁胺、Ferrostatin-1及脂氧抑素-1能有效阻止RSL3抑制GPX4引发的神经元线粒体损伤及自由基生成[7]。特异性敲除神经元GPX4基因可导致海马CA3区中间神经元选择性丢失,并诱发海马区神经退行性病变[8]。这些研究证实铁死亡驱动多种神经病理过程中的组织损伤与神经元丢失;靶向干预相关铁死亡效应分子,有望成为神经元损伤与神经退行性疾病治疗的新策略。
香青兰总黄酮(total flavonoids of Dracocephalum moldavica L.,TFDM)作为唇形科青兰属香青兰植株中的主要活性成分,广泛分布于内蒙古、新疆等地区[9]。已有研究[10]表明,TFDM能抑制血管性认知障碍大鼠模型TNF-α/NF-κB p65信号通路,减轻神经炎症,改善慢性低灌注引起的血脑屏障破坏等作用。课题组前期实验[11]表明在Aβ1-42诱导的阿尔茨海默病细胞模型中,TFDM能通过调控Nrf2/NF-κB通路抑制星型胶质细胞活化及神经炎症,从而发挥神经保护功能。本研究通过细胞实验探讨TFDM对缺氧诱导损伤致HT22细胞铁死亡的影响,旨在为明确VaD的发病机制以及防治提供实验依据。
1 材料与方法 1.1 细胞、药物及主要试剂与仪器小鼠海马神经元永生化细胞系HT22购于武汉普诺赛生命科技有限公司。香青兰植株由内蒙古科技大学包头医学院药园种植,TFDM由南京普怡生物科技有限公司提纯,最终浓度为78.53%(货号PY241213XQL)。
Gibco高糖培养基、Gibco 0.25%胰酶购自上海赛默飞世尔科技公司,特级胎牛血清购自武汉普诺赛生命科技有限公司,青链霉素混合液、电泳液、转膜液、TBST、一抗稀释液、DMSO购自北京索莱宝科技有限公司,Quant cDNA第一链合成试剂盒和Talent荧光定量检测试剂盒购自天根生化科技(北京)有限公司,COX2、GPX4、β-actin引物由生工生物工程(上海)股份有限公司设计,谷胱甘肽(glutathione,GSH)检测试剂盒(A006-2-1)购自南京建成生物工程研究所,CCK-8试剂盒(CK04)、Ferro Orange(Fe2+检测探针,F374)购自东仁化学科技(上海)有限公司,一抗COX2(12282T)购自美国Cell Signaling公司、GPX4(30388-1-AP)购自武汉三鹰生物技术有限公司,β-actin(21338)、二抗(L3016)购自英国Signalway Antibody公司,铁死亡抑制剂(Ferrostatin-1,HY-100579)、铁死亡诱导剂(Erastin,HY-15763)购自美国MedChemExpress公司,JC-1(增强型线粒体膜电位检测试剂盒,C2003S)、活性氧检测试剂盒(S003M)购自上海碧云天生物技术有限公司。
主要仪器包括酶标仪(瑞士TECAN公司),蛋白成像分析系统(上海天能生命科学有限公司),荧光定量PCR仪(西安天隆科技有限公司),冷冻离心机(美国Sigma-Aldrich公司),垂直电泳仪、转印槽(美国Bio-Rad公司),激光共聚焦显微镜(日本尼康公司),BD流式细胞仪(美国BD公司)。
1.2 方法 1.2.1 细胞培养按照90%DMEM+10%FBS+1%青链霉素配置完全培养基,将细胞培养于37 ℃、5%CO2培养箱中,隔日观察换液,待细胞密度生长至85%~90%时,根据实验需求传代或冻存,传代比例1∶4,冻存液按90%血清+10%DMSO配置,于梯度冻存盒中置于-80 ℃冰箱,隔日转移至液氮保存。
1.2.2 缺氧诱导HT22损伤细胞建立造模方法参照文献[12],细胞复苏、传代至生长密度为对数期时,根据实验分组按需转移至37 ℃恒温缺氧培养箱中进行缺氧诱导。缺氧培养箱气体为90%N2+5%CO2+5%O2。
1.2.3 细胞分组和给药实验分组按实验设计分为3部分,分别是缺氧诱导时效筛选分组(正常组,模型组,12 h、24 h、36 h、48 h组)、TFDM给药浓度筛选分组(正常组,模型组,2.5 μg/mL、5 μg/mL、7 μg/mL、10 μg/mL组)以及铁死亡诱导剂(Erastin)和抑制剂(Ferrostatin-1)干预分组(正常组、模型组、TFDM组、Erastin组、模型+Erastin组、模型+Erastin+TFDM组、Ferrostatin-1组、模型+Ferrostatin-1组、模型+Ferrostatin-1+TFDM组)。Erastin和Ferrostatin-1给药浓度参考文献[12]和试剂说明书,设置为20 μmol/L,实验所用药物均在37 ℃、5%CO2培养箱预处理1 h后放入缺氧培养箱中同步孵育。
1.2.4 CCK-8检测细胞活力细胞96孔板铺板培养,在给予缺氧诱导以及不同浓度给药干预后弃旧培养基,PBS洗涤2次,每孔加入100 μL新培养基和10 μL CCK-8溶液,分为空白孔组(只含培养基)、正常对照孔组和实验孔组(含细胞+培养基+CCK-8试剂),每组均设3复孔,于培养箱内避光孵育2.5 h,使用酶标仪于450 nm波长处测定各孔光密度(optical density,OD)值。
1.2.5 GSH检测收集各组细胞并计数,用PBS清洗2次,再加入500 μL等渗PBS重悬,超声破碎后4 ℃离心取上清,按试剂盒说明书进行显色反应,然后使用酶标仪于405 nm处测定各孔OD值。
1.2.6 实时定量PCR收集各组细胞,采用TRIzol法抽提总RNA后进行浓度测定,根据Fasking cDNA试剂盒说明书进行反转录,根据荧光定量试剂盒说明书进行荧光定量扩增反应检测mRNA相对表达水平,采用2-ΔΔCt计算基因的相对表达量。引物序列见表 1。
| Gene | Primer sequences(5’→3’) | Length(bp) |
| COX2 | Forward:GTGCCTGGTCTGATGATGTATGC | 23 |
| Reverse:TGAGTCTGCTGGTTTGGAATAGTTG | 25 | |
| GPX4 | Forward:GCAGGAGCCAGGAAGTAATCAAG | 23 |
| Reverse:ACAGTGGGTGGGCATCGTC | 19 | |
| β-actin | Forward:GATGGTGGGAATGGGTCAGAAGG | 23 |
| Reverse:TTGTAGAAGGTGTGGTGCCAGATC | 24 |
1.2.7 Western blotting
细胞干预结束后弃上清,PBS清洗2次,胰酶消化后给予适量裂解液,冰上裂解15 min后冰浴超声,高速冷冻离心机离心后取上清即为蛋白原液,BCA法进行蛋白浓度检测,通过标曲制作计算好上样量后-20 ℃冰箱保存备用;按相应蛋白分子量选择适宜分离胶浓度制胶,随后按步骤进行电泳、转模、封闭、抗体孵育、显影等操作。抗体稀释比例、电泳液、转膜液、TBST配置按试剂说明书进行操作。
1.2.8 细胞荧光染色及ROS检测细胞按分组干预结束后进行Fe2+荧光、线粒体膜电位和ROS检测,均按照对应试剂盒说明书进行操作,最后于激光倒置共聚焦显微镜下观察,ROS采用BD流式细胞仪检测。
1.3 统计学分析应用Graph Pad Prism 10.0进行数据统计分析。计量数据用x±s表示,2组间比较采用独立样本t检验,多组间比较采用单因素方差分析。P < 0.05为差异有统计学意义。
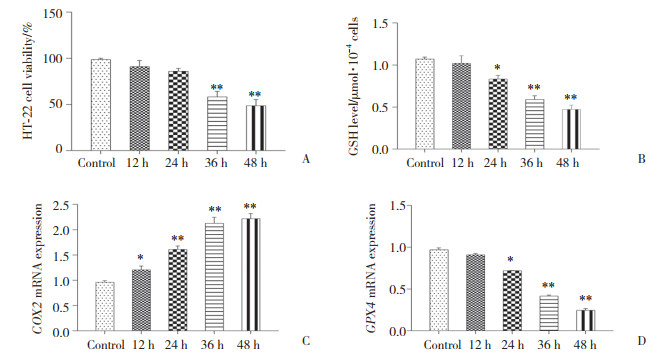
2 结果 2.1 缺氧诱导HT22细胞损伤最佳时间筛选如图 1所示,与Control组相比,随着缺氧时间的增加,HT22细胞活力以及胞内GSH含量呈现显著下降趋势,当缺氧36 h时细胞活力及GSH含量改变显著(P < 0.01)。实时定量PCR检测结果显示,COX2 mRNA表达水平随着缺氧时间的增加而显著升高(P < 0.01),GPX4 mRNA表达水平随着缺氧时间增加而显著减小(P < 0.01)。结合相关文献[12],后续实验细胞缺氧时间设为36 h。
|
| A, HT22 cell viability; B, GSH level; C, COX2 mRNA; D, GPX4 mRNA. *P < 0.05, **P < 0.01 vs.Control group. 图 1 缺氧不同时间对HT22细胞活力、GSH含量以及COX2、GPX4 mRNA表达的影响 Fig.1 Effects of different hypoxia durations on HT22 cell viability, GSH content, and mRNA expressions of COX2 and GPX4 |
2.2 TFDM干预最佳浓度筛选
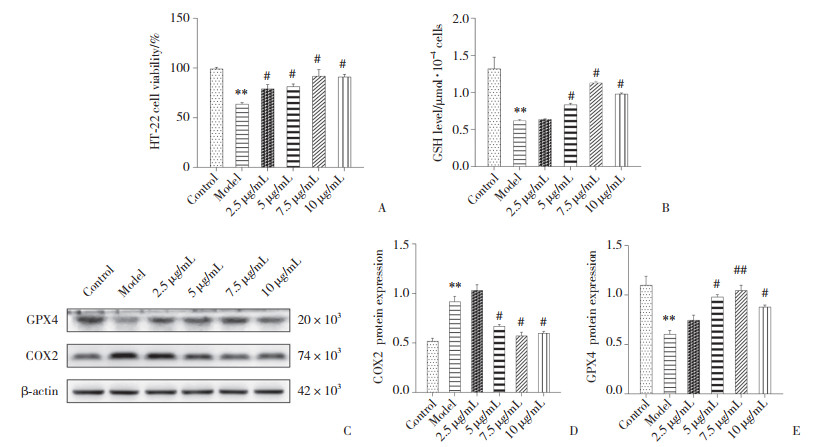
如图 2所示,在建立缺氧损伤模型后,随着不同浓度TFDM干预,HT22细胞活力、GSH含量、GPX4蛋白表达逐渐升高,而COX2蛋白表达逐渐下降,以浓度7.5 μg/mL时最为显著。结合课题组既往研究[11]及本实验结果,选择7.5 μg/mL作为后续实验的给药浓度。
|
| A, HT22 cell viability; B, GSH level; C-E, COX2, GPX4 protein expressions.**P < 0.01 vs. Control group; #P < 0.05, ##P < 0.01 vs. Model group. 图 2 不同浓度TFDM对HT22细胞活力、GSH含量以及COX2、GPX4蛋白表达的影响 Fig.2 Effects of different concentrations of TFDM on HT22 Cell viability, GSH content, and protein expressions of COX2 and GPX4 |
2.3 TFDM联合Erastin/Ferrostatin-1处理对缺氧诱导HT22细胞损伤后GSH含量的影响
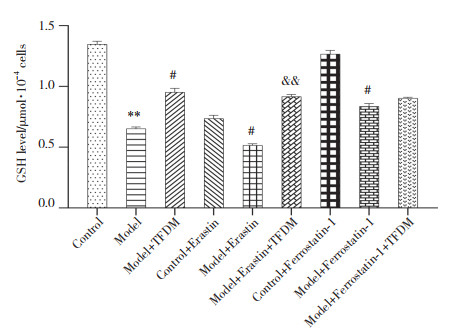
如图 3所示,与Control组相比,Model组GSH含量显著降低(P < 0.01)。与Model组相比,Model+TFDM组和Model+Ferrostatin-1组GSH含量显著升高,Model+Erastin组GSH含量降低(P < 0.05)。与Model+Erastin组相比,Model+Erastin+TFDM组GSH含量显著升高(P < 0.01)。与Model+Ferrostatin-1组相比,Model+Ferrostatin-1+TFDM组GSH含量差异无统计学意义(P > 0.05)。
|
| **P < 0.01 vs. Control group; #P < 0.05 vs. Model group; &&P < 0.01 vs. Model+Erastin group. 图 3 TFDM联合Erastin/Ferrostatin-1处理对缺氧诱导HT22细胞损伤后GSH含量的影响 Fig.3 Effects of TFDM combined with Erastin/Ferrostatin-1 on GSH content in HT22 cell after hypoxia-induced injury |
2.4 TFDM对缺氧诱导HT22细胞损伤后GPX4、COX2 mRNA和蛋白表达的影响
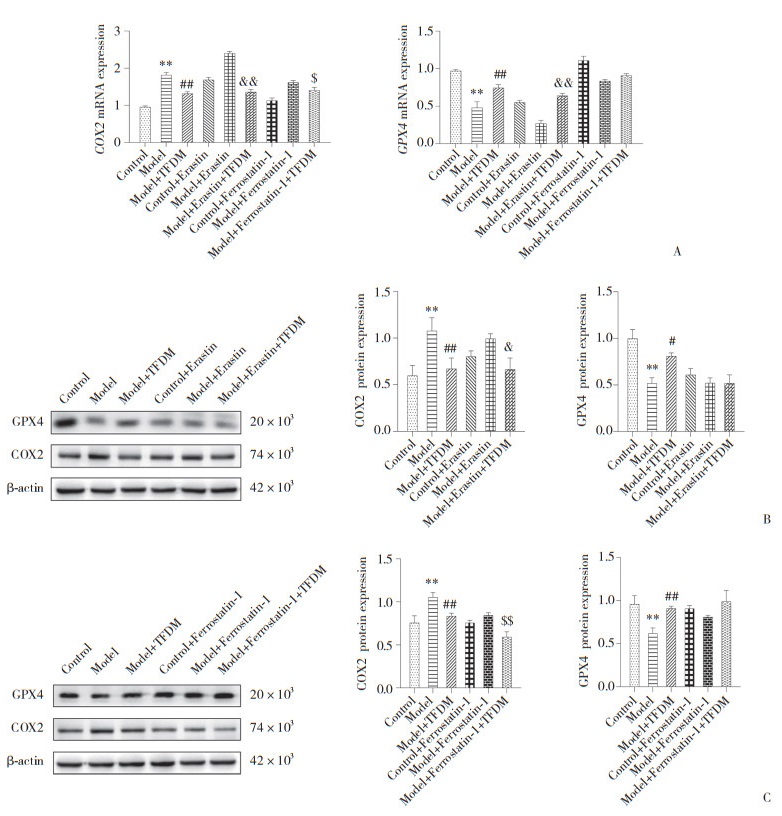
如图 4所示,与Control组相比,Model组COX2 mRNA和蛋白表达显著升高(P < 0.01),而GPX4 mRNA和蛋白表达显著降低(P < 0.01)。与Model组相比,Model+TFDM组COX2 mRNA和蛋白表达显著下降,GPX4 mRNA和蛋白表达显著升高(P < 0.05)。与Model+Erastin组相比,Model+Erastin+TFDM组COX2 mRNA和蛋白表达显著降低,GPX4 mRNA表达显著升高(P < 0.05),而GPX4蛋白表达差异无统计学意义(P > 0.05)。与Model+Ferrostatin-1组相比,Model+Ferrostatin-1+TFDM组COX2 mRNA和蛋白表达显著降低(P < 0.05),而GPX4 mRNA和蛋白表达差异无统计学意义(P > 0.05)。
|
|
A, COX2, GPX4 mRNA expression; B, TFDM combined with Erastin; C, TFDM combined with Ferrostatin-1. **P < 0.01 vs. Control group; #P < 0.05, ##P < 0.01 vs. Model group; & P < 0.05, &&P < 0.01 vs. Model+Erastin group; $P < 0.05, |
2.5 TFDM联合Erastin处理对缺氧诱导HT22细胞损伤后Fe2+含量的影响
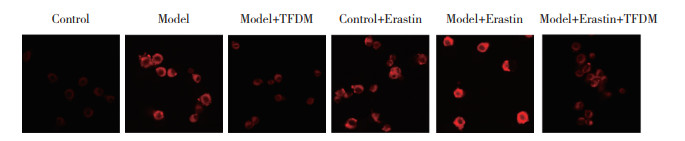
Control组、Model组、Model+TFDM组、Control+Erastin组、Model+Erastin组、Model+Erastin+TFDM组Fe2+平均荧光强度分别为1.00±0.09、3.74±0.18、2.62±0.12、3.11±0.21、5.08±0.36、3.22±0.31。与Control相比,Model组Fe2+平均荧光强度显著增强(P < 0.01)。与Model组相比,Model+TFDM组Fe2+平均荧光强度显著下降(P < 0.05)。与Model+Erastin相比,Model+Erastin+TFDM组Fe2+平均荧光强度显著降低(P < 0.05),见图 5。
|
| 图 5 TFDM联合Erastin处理对缺氧诱导HT22细胞损伤后Fe2+含量的影响×20 Fig.5 Effects of TFDM combined with Erastin on Fe2+ content in HT22 Cell after hypoxia-induced injury ×20 |
2.6 TFDM联合Erastin处理对缺氧诱导HT22损伤后线粒体膜电位的影响
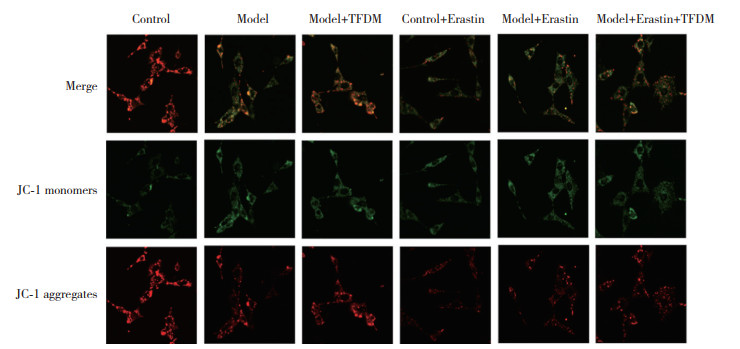
Control组、Model组、Model+TFDM组、Control+Erastin组、Model+Erastin组、Model+Erastin+TFDM组线粒体膜电位分别为0.96±0.17、0.51±0.03、0.77±0.06、0.43±0.04、0.36±0.06、0.46±0.08。与Control组相比,Model组线粒体膜电位显著下降(P < 0.01)。与Model组相比,Model+TFDM组线粒体膜电位显著升高(P < 0.05)。与Model+Erastin组相比,Model+Erastin+TFDM组线粒体膜电位变化差异无统计学意义。见图 6。
|
| 图 6 TFDM联合Erastin处理对缺氧诱导HT22损伤线粒体膜电位的影响×20 Fig.6 Effects of TFDM combined with Erastin on mitochondrial membrane potential in HT22 Cell after hypoxia-induced injury ×20 |
2.7 TFDM联合Erastin处理对缺氧诱导HT22细胞损伤后ROS的影响
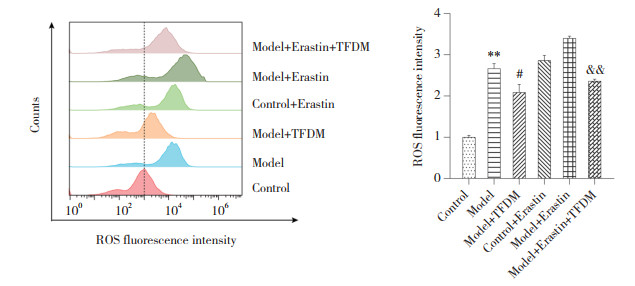
如图 7所示,与Control相比,Model组波峰右移,ROS水平明显升高(P < 0.01)。与Model组相比,Model+TFDM组波峰左移,ROS水平明显降低(P < 0.05)。与Model+Erastin相比,Model+Erastin+TFDM组波峰左移,ROS水平明显降低(P < 0.01)。
|
| **P < 0.01 vs. Control group; #P < 0.05 vs. Model group; &&P < 0.01 vs. Model+Erastin group. 图 7 TFDM联合Erastin处理对缺氧诱导HT22损伤ROS水平的影响 Fig.7 Effects of TFDM combined with Erastin on ROS levels in HT22 Cell after hypoxia-induced injury |
3 讨论
缺氧和低灌注可导致脑组织,特别是海马区神经元细胞缺氧损伤,从而导致神经元丢失和认知功能下降[13]。本实验选择小鼠海马神经元细胞作为研究对象,采用缺氧诱导损伤模拟VaD病理状态,其理论依据及实验依据均较充分。
铁死亡是一种调节性细胞死亡方式,它在形态、生物化学和遗传学方面与传统细胞死亡途径(如凋亡、坏死和自噬等)有所区别[14]。近年来研究[15]发现,启动铁死亡核心因素主要与GPX4功能丧失、Fe2+蓄积以及脂质过氧化增强等因素紧密相关。研究表明,当机体受到内部或外界应激刺激时,体内GSH及其依赖酶系统在发挥抵抗脂质过氧化反应中居于核心地位,特别是GPX4在GSH的辅助下能将膜脂质过氧化物还原为低反应活性的醇类物质,从而减少脂质过氧化物的蓄积,避免对蛋白质、核酸等大分子造成损伤[16]。本研究结果表明,在缺氧诱导损伤后,细胞内脂质过氧化反应明显增强,导致抗过氧化反应的过氧化物酶GPX4以及GSH减少,细胞活力明显下降。当TFDM干预后,细胞抗脂质过氧化能力增强,细胞活力回升,GPX4蛋白及GSH水平明显升高,COX2 mRNA及蛋白表达下降,这提示脂质过氧化反应的过度激活和抗过氧化反应物质的不足在VaD发病过程中发挥了重要作用,TFDM可能通过促进抗过氧化物酶类的表达来抑制过氧化物水平升高,从而发挥神经保护作用。而当TFDM联合Erastin和Ferrostatin-1干预时,COX2 mRNA及蛋白表达均下降,但GSH含量、GPX4 mRNA及蛋白表达无明显上调,提示药物联合干预的效果优劣存在差别,这可能与不同信号通路之间的串扰及药物作用靶点的饱和及特异性有关,后续还需展开进一步研究。
神经元对能量的高需求来源于其特殊的复杂功能,包括轴突间信号的处理、神经递质的合成释放及回收、维持线粒体膜电位的稳定以及神经系统的内环境稳定等[17]。本研究结果表明,当神经元在缺氧诱导损伤后,线粒体膜电位明显下降,表明缺氧导致了线粒体功能障碍,氧化磷酸化水平受阻,ATP生成不足,对神经元造成了不可逆损伤。这也提示线粒体功能障碍在VaD发病过程中的重要性,而TFDM干预后线粒体膜电位明显增高,提示TFDM可能对缺氧状态下的线粒体具有一定的保护作用,但具体机制需要进一步研究。
此外,研究[18]发现,随着年龄的增长,大脑内循环清除能力下降,铁在大脑中蓄积愈发明显,导致对铁死亡的易感性增加。当细胞处于应激条件下,Fe3+在细胞内还原为Fe2+,而胞内Fe2+的过量积累会通过Fenton反应促进氧自由基的生成,从而加剧脂质过氧化反应,大量ROS及脂质过氧化产物将进一步损伤细胞器,最终导致神经元死亡。另有研究[19]表明,一些小分子铁死亡抑制剂具有潜在的神经保护能力,可以改善神经退行性变导致的认知衰退。本研究结果表明,在缺氧损伤发生后,细胞内Fe2+水平明显升高,当缺氧损伤联合Erastin处理后,细胞内Fe2+水平升高更为明显,而给予TFDM干预后,Fe2+水平下降。与此同时,细胞ROS含量变化与上述结果一致,表明TFDM能降低缺氧诱导损伤神经元细胞Fe2+和ROS的水平,从而降低铁死亡的敏感性,发挥神经保护功能,也进一步提示TFDM可以作为铁死亡抑制剂备选的潜在可能。
综上所述,本研究通过检测铁死亡相关指标,并引入铁死亡诱导剂和抑制剂联合TFDM处理细胞,不同实验方法多重验证表明,脂质过氧化反应的过度激活引发的铁死亡病理过程在VaD发病机制中发挥了重要作用,与研究[20]发现铁死亡是多种脑部疾病发病机制结果一致。TFDM可上调GPX4表达、促进GSH合成、下调COX2表达、减少细胞Fe2+蓄积、降低ROS水平,抵抗脂质过氧化,从而降低铁死亡的敏感性,发挥神经保护功能。本研究为使用TFDM防治VaD提供了实验依据,但TFDM作为复方传统中药,其中的药效成分如何通过降低铁死亡的敏感性发挥神经保护作用仍需进一步论证。
| [1] |
田浩, 高爱社, 任金玲, 等. 铁死亡在血管性痴呆中的研究进展[J]. 中药新药与临床药理, 2023, 34(8): 1164-1170. DOI:10.19378/j.issn.1003-9783.2023.08.018 |
| [2] |
KALARIA RN. The pathology and pathophysiology of vascular dementia[J]. Neuropharmacology, 2018, 134: 226-239. DOI:10.1016/j.neuropharm.2017.12.030 |
| [3] |
吴振, 马晓俞. 瑞马唑仑通过调控BDNF/TrkB信号通路影响衰老大鼠模型术后认知功能[J]. 中国医科大学学报, 2025, 54(9): 781-785. DOI:10.12007/j.issn.0258-4646.2025.09.003 |
| [4] |
DIXON SJ, STOCKWELL BR. The role of iron and reactive oxygen species in cell death[J]. Nat Chem Biol, 2014, 10(1): 9-17. DOI:10.1038/nchembio.1416 |
| [5] |
BRADLEY-WHITMAN MA, LOVELL MA. Biomarkers of lipid peroxidation in Alzheimer disease (AD): an update[J]. Arch Toxicol, 2015, 89(7): 1035-1044. DOI:10.1007/s00204-015-1517-6 |
| [6] |
SUGIYAMA A, SUN J. Immunochemical detection of lipid hydroperoxide- and aldehyde-modified proteins in diseases[M]//Lipid hydroperoxide-derived modification of biomolecules. Dordrecht: Springer Netherlands, 2013: 115-125. DOI: 10.1007/978-94-007-7920-4_10.
|
| [7] |
JELINEK A, HEYDER L, DAUDE M, et al. Mitochondrial rescue prevents glutathione peroxidase-dependent ferroptosis[J]. Free Radic Biol Med, 2018, 117: 45-57. DOI:10.1016/j.freeradbiomed.2018.01.019 |
| [8] |
SEILER A, SCHNEIDER M, FÖRSTER H, et al. Glutathione peroxidase 4 senses and translates oxidative stress into 12/15-lipoxygenase dependent- and AIF-mediated cell death[J]. Cell Metab, 2008, 8(3): 237-248. DOI:10.1016/j.cmet.2008.07.005 |
| [9] |
陈丽, 曹星月, 王占黎, 等. 内蒙古香青兰总黄酮提取工艺优化及其抗氧化活性成分分析[J]. 中国现代应用药学, 2023, 40(9): 1187-1193. DOI:10.13748/j.cnki.issn1007-7693.20221039 |
| [10] |
马尚佳, 王璐, 李华, 等. 基于网络药理学和动物实验探讨香青兰总黄酮治疗血管性认知障碍的作用机制[J]. 安徽医科大学学报, 2025, 60(4): 675-684. DOI:10.19405/j.cnki.issn1000-1492.2025.04.013 |
| [11] |
REN W, YAN XS, FAN JC, et al. Effect of total flavonoids of Dracocephalum moldavica L. on neuroinflammation in Alzheimer's disease model amyloid-β (Aβ1-42) -peptide-induced astrocyte activation[J]. J Toxicol Environ Health Part A, 2024, 87(10): 436-447. DOI:10.1080/15287394.2024.2336570 |
| [12] |
LI Y, ZHANG ED, YANG H, et al. Gastrodin ameliorates cognitive dysfunction in vascular dementia rats by suppressing ferroptosis via the regulation of the Nrf2/Keap1-GPx4 signaling pathway[J]. Molecules, 2022, 27(19): 6311. DOI:10.3390/molecules27196311 |
| [13] |
KANG P, YING CW, CHEN YS, et al. Oxygen metabolic stress and white matter injury in patients with cerebral small vessel di-sease[J]. Stroke, 2022, 53(5): 1570-1579. DOI:10.1161/strokeaha.121.035674 |
| [14] |
URSINI F, MAIORINO M. Lipid peroxidation and ferroptosis: the role of GSH and GPx4[J]. Free Radic Biol Med, 2020, 152: 175-185. DOI:10.1016/j.freeradbiomed.2020.02.027 |
| [15] |
DIXON SJ, STOCKWELL BR. The hallmarks of ferroptosis[J]. Annu Rev Cancer Biol, 2019, 3: 35-54. DOI:10.1146/annurev-cancerbio-030518-055844 |
| [16] |
IMAI H, MATSUOKA M, KUMAGAI T, et al. Lipid peroxidation-dependent cell death regulated by GPx4 and ferroptosis[M]//Apoptotic and non-apoptotic cell death. Cham: Springer International Publishing, 2016: 143-170. DOI: 10.1007/82_2016_508.
|
| [17] |
王淑静, 黄冬梅, 王立, 等. 基于能量代谢分析白藜芦醇对H2O2诱导SH-SY5Y细胞保护作用[J]. 药学研究, 2023, 42(11): 870-874. DOI:10.13506/j.cnki.jpr.2023.11.004 |
| [18] |
HE YJ, LIU XY, XING L, et al. Fenton reaction-independent ferroptosis therapy via glutathione and iron redox couple sequentially triggered lipid peroxide generator[J]. Biomaterials, 2020, 241: 119911. DOI:10.1016/j.biomaterials.2020.119911 |
| [19] |
PLASCENCIA-VILLA G, PERRY G. Preventive and therapeutic strategies in Alzheimer's disease: focus on oxidative stress, redox metals, and ferroptosis[J]. Antioxid Redox Signal, 2021, 34(8): 591-610. DOI:10.1089/ars.2020.8134 |
| [20] |
张凤英, 汤永红, 谢言青, 等. 过表达Slc1a2调节Glu/GABA平衡抑制铁死亡改善睡眠剥夺小鼠的认知功能障碍[J]. 中国医科大学学报, 2025, 54(11): 967-976. DOI:10.12007/j.issn.0258-4646.2025.11.002 |
 2026, Vol. 55
2026, Vol. 55