文章信息
- 翟春清, 裴明, 温暖
- ZHAI Chunqing, PEI Ming, WEN Nuan
- 卫矛醇通过调控PPARA/ABCA1信号通路抑制氧化应激改善膜性肾病
- Ducitol ameliorates membranous nephropathy by activating the PPARA/ABCA1 signaling pathway to inhibit oxidative stress
- 中国医科大学学报, 2026, 55(3): 198-205
- Journal of China Medical University, 2026, 55(3): 198-205
-
文章历史
- 收稿日期:2025-09-15
- 网络出版时间:2026-03-24 13:09:43
2. 天津中医药大学第一附属医院肾科, 中医国家临床医学研究中心, 天津 300381;
3. 河北医科大学临床学院医学检验技术系, 石家庄 050031
2. Department of Nephrology, First Teaching Hospital of Tianjin University of Traditional Chinese Medicine, National Clinical Research Center for Chinese Medicine, Tianjin 300381, China;
3. Department of Medical Laboratory Technology, Clinical College of Hebei Medical University, Shijiazhuang 050031, China
膜性肾病以肾小球基底膜免疫复合物沉积为特征,可致蛋白尿和肾功能恶化,伴足细胞损伤,氧化应激在其发病中起关键作用[1-2]。卫矛醇(dulcitol,Dul)是具有抗炎、抗凋亡作用的植物提取物,可缓解肠道上皮细胞炎症损伤,但其在膜性肾病中的作用尚不明确[3-4]。过氧化物酶体增殖物激活受体α(peroxisome proliferator-activated receptor α,PPARA)主要调控脂质稳态,芯片数据提示PPARA在膜性肾病组织中表达下调,抑制PPARA可加重肾损伤[5]。其下游靶点ATP结合盒转运蛋白A1(ATP-binding cassette transporter A1,ABCA1)能维持足细胞脂质平衡,减轻糖尿病肾病氧化应激[6]。而抑制ABCA1会加重氧化应激损伤,PPARA则能够上调ABCA1,发挥协同保护作用[7-8]。本研究拟探讨Dul通过调控PPARA/ABCA1信号通路影响氧化应激介导的膜性肾病进展机制,以期为膜性肾病的靶向治疗提供依据。
1 材料与方法 1.1 材料 1.1.1 实验动物与细胞40只成年雄性SD大鼠,体重(225±20)g,购自豪威生物科技有限公司,许可证号SCXK(津)2024-0002。STR鉴定的小鼠肾小球足细胞系MPC-5,购自誉弛(上海)生物科技有限公司。本研究获得天津中医药大学实验动物伦理委员会审批(TCM-LAEC2023075)。
1.1.2 试剂与仪器Dul购自青岛多特糖醇科技有限公司;酵母多糖购自西格玛奥德里奇(上海)贸易有限公司;lipofectamin 3000转染试剂购自赛默飞世尔科技(中国)有限公司;pcDNA3.1、pcDNA3.1-PPARA及siNC、siABCA1载体购自上海吉玛制药技术有限公司;乳酸脱氢酶(lactic dehydrogenase,LDH)活性检测试剂盒、HE和Masson染色试剂盒购自北京索莱宝科技有限公司;CCK-8试剂盒、一步法TUNEL细胞凋亡检测试剂盒(绿色荧光)购自美国Med Chem Express公司;小鼠及大鼠超氧化物歧化酶(superoxide dismutase,SOD)、丙二醛(malondialdehyde,MDA)ELISA试剂盒购自上海江莱生物科技有限公司;DCFH-DA荧光探针购自优利科(上海)生命科学有限公司;实时定量PCR引物由生工生物工程(上海)股份有限公司合成;反转录试剂盒、SYBR Premix Ex Taq试剂盒购自宝日医生物技术(北京)有限公司;BCA蛋白测定试剂盒、PVDF膜购自上海碧云天生物技术股份有限公司;PPARA抗体购自武汉华美生物工程有限公司;ABCA1抗体、GAPDH抗体、HRP偶联的二抗购自艾博抗(上海)贸易有限公司;Immobilon蛋白质化学发光HRP底物购自武汉飞羿科技有限公司;阳离子牛血清蛋白(cationic bovine serum albumin,C-BSA)购自北京博蕾德生物科技有限公司。自动化学发光/荧光图像分析系统购自中国上海天能科技有限公司;全自动生化分析仪购自日本Hitachi公司。
1.2 方法 1.2.1 网络药理学与生物信息学分析利用PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)检索Dul(C6H14O6)获SMILES,用SwissTargetPrediction网站(http://www.swisstargetprediction.ch)与prediction网站(https://pre-diction.charite.de)预测靶点。从NCBI基因表达综合(gene expression omnibus,GEO)数据库(https://www.ncbi.nlm.nih.gov)获取GSE175759和GSE73953数据集,用GEO2R工具筛选差异基因(|logFC| > 1,P < 0.05)。从GeneCards数据库(https://www.genecards.org)筛选氧化应激靶点(评分≥6)[9]。通过Venn图取交集,用STRING数据库(https://cn.string-db.org)构建蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络,按中心性值与度值排名,从PDB数据库(https://www.rcsb.org)获取PPARA、NFKB1晶体,从PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)获取Dul SDF,用AutodockVina 1.2.2对接,用PLIP分析界面,PyMOL 2.5可视化。
1.2.2 细胞培养、转染与分组将MPC-5细胞于DMEM+10%FBS复苏后,37 ℃、5% CO2培养分化。参照文献[10]方法制备酵母多糖活化血清(zymosan activated serum,ZAS),用8% ZAS(100 μL,亚致死C5b-9)建立足细胞亚溶破模型。在模型构建前先以Dul(30、60、90、120、150、180、200 μmol/L)预处理MPC-5细胞1 h,通过CCK-8检测,确定Dul的最佳作用浓度为180 μmol/L。细胞转染pcDNA3.1、pcDNA3.1-PPARA、siNC、siABCA1并验证。将细胞分为对照、ZAS、ZAS+Dul、ZAS+pcDNA3.1、ZAS+pcDNA3.1-PPARA、ZAS+pcDNA3.1-PPARA+Dul、ZAS+pcDNA3.1-PPARA+siNC、ZAS+pcDNA3.1-PPARA+siABCA1组。转染48 h后各组进行相应干预,Dul预处理先于ZAS。
1.2.3 膜性肾病大鼠模型建立与分组随机取8只SD大鼠为Sham组,其余32只大鼠经尾静脉梯度注射C-BSA,第1周逐日增加剂量(1 mg、1 mg、1 mg、1.5 mg、1.5 mg、2 mg和2 mg),后3周固定2.5 mg,隔日1次,构建膜性肾病模型[11-12]。用Bradford测定试剂盒检测24 h尿蛋白(24-hour urinary protein,24 h-UTP),确认造模成功后,再随机分为Dul-L组、Dul-M组、Dul-H组及Model组,造模成功后第1天起,分别每日灌胃50 mg/kg Dul、100 mg/kg Dul、150 mg/kg Dul及等体积蒸馏水,连续4周。最后一次给药后检测24 h-UTP,全自动生化分析仪测血清肌酐(serum creatinine,Scr)、血尿素氮(blood urea nitrogen,BUN)。
1.2.4 LDH释放及细胞活力、凋亡检测超声破碎细胞(5×106/mL,冰浴200 W,3 s/10 s,30次)后,离心(4 ℃,8 000 g,10 min)取上清,按照试剂盒说明书检测LDH。将细胞接种至96孔板,培养24 h后加CCK-8孵育4 h,酶标仪450 nm测吸光度。另板接种细胞(1×104/孔),4% PFA固定10 min,Triton X-100通透后,TUNEL37 ℃孵育1 h,DAPI染核,荧光显微镜下采集图像,计算凋亡率。
1.2.5 氧化应激相关指标检测4 ℃下1 000 g离心细胞20 min,取上清。用PBS冲洗并剪碎肾组织,用含蛋白酶抑制剂PBS冰浴匀浆,5 000 g离心5~10 min,取上清。按照试剂盒说明书检测上清中SOD活性及MDA含量。收集各组细胞并将其接种至96孔板,加DCFH-DA荧光探针(1∶500)37 ℃孵育20 min,用PBS洗3次。荧光显微镜下采集图像,定量活性氧(reactive oxygen species,ROS)荧光强度。
1.2.6 药物亲和反应的靶点稳定性(drug affinity responsive target stability,DARTS)实验采用DARTS验证Dul与PPARA的结合。用裂解缓冲液处理MPC-5细胞30 min,提取蛋白后分为对照(含1 mL/L DMSO)组、链霉蛋白酶组、链霉蛋白酶+Dul(180 μmol/L)组,链霉蛋白酶与蛋白的混合比例为1∶20 000,室温静置10 min,加热5 min,进行Western blotting检测。
1.2.7 实时定量PCR用TRIzol法提取各组足细胞总RNA,反转录得cDNA后,以SYBR Premix Ex Taq进行实时定量PCR。反应体系25 μL:2×Premix 12.5 μL,10 μmol/L上下游引物各0.5 μL,探针1 μL,模板2 μL,无核酸水8.5 μL。反应条件:95 ℃ 30 s,95 ℃ 5 s、60 ℃ 30 s,40个循环。2-ΔΔCt法计算目标基因相对表达量。GAPDH作为内参照。引物序列如下:PPARA,正向5’-GTTTGAGGGGGTAACAGCAA-3’,反向5’-GCTAACTGCAGAGGGTGAGG-3’;ABCA1,正向5’-AACAGTTTGTGGCCCTTTTG-3’,反向5’- AGTTCCAGGCTGGGGTACTT-3’;GAPDH,正向5’-CGACCACTTTGTCAAGCTCA-3’,反向5’-AGGGGTCTACATGGCAACTG -3’。
1.2.8 Western blotting以含蛋白酶/磷酸酶抑制剂的RIPA裂解MPC-5细胞及肾组织,BCA定量后取30 μg蛋白变性,进行10% SDS-PAGE电泳并转膜,封闭后4 ℃孵育一抗(PPARA、ABCA1、GAPDH)过夜,二抗(1∶5 000)室温孵育2 h,ECL显影,以GAPDH为内参照。
1.2.9 肾组织病理与免疫组织化学分析用4%多聚甲醛固定肾组织,石蜡包埋,制5 μm厚切片,脱蜡再水化后行HE和Masson染色,光镜下观察。肾组织切片脱蜡、3% H2O2阻断、柠檬酸钠修复、BSA封闭,PPARA、ABCA1一抗(1∶100)4 ℃过夜,HRP二抗(1∶1 000)室温孵育1 h,DAB显色,苏木素复染,用Image-Pro Plus 6.0软件计算平均光密度(average optical density,AOD)。
1.3 统计学分析采用SPSS 26.0和GraphPad Prism 9.5软件进行统计学分析。计量资料以 x±s表示,2组比较采用t检验,多组比较采用单因素方差分析及LSD-t检验。P < 0.05为差异有统计学意义。
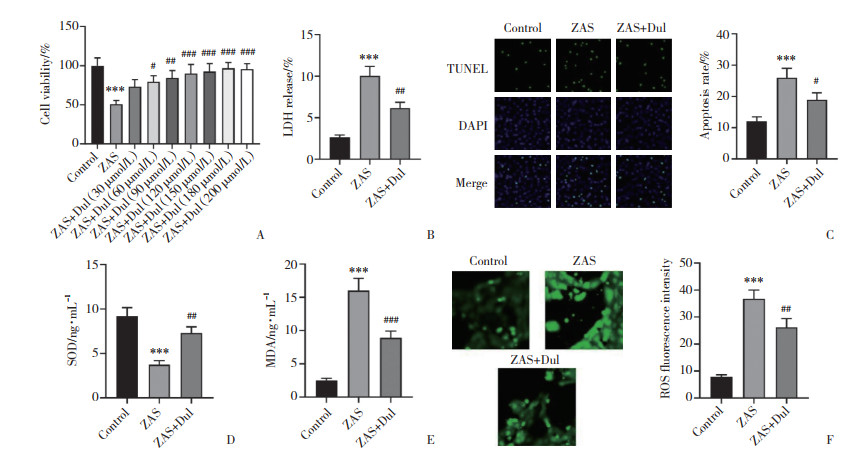
2 结果 2.1 Dul预防ZAS诱导的MPC-5细胞氧化应激损伤与对照组相比,ZAS组细胞增殖活力降低,LDH释放水平和细胞凋亡率升高,SOD活性下降,MDA和ROS水平升高(均P < 0.05)。与ZAS组比较,Dul呈浓度依赖性促进细胞增殖,180 μmol/L效果最佳,故将该浓度用于后续实验。Dul干预后,LDH释放和细胞凋亡减少,SOD活性增强,MDA和ROS降低(均P < 0.05)。见图 1。
|
| A, cell viability (CCK-8 results); B, LDH release; C, TUNEL results (×200);D, SOD activity; E, MDA level; F, ROS fluorescence intensity detected by DCFH-DA probe (×200). ***P < 0.001 vs. control group; #P < 0.05, ##P < 0.01, ###P < 0.001 vs. ZAS group. n = 3. 图 1 Dul改善ZAS诱导的MPC-5细胞氧化应激程度 Fig.1 Dul alleviates oxidative stress in MPC-5 cells under ZAS induction |
2.2 生物信息学分析结果
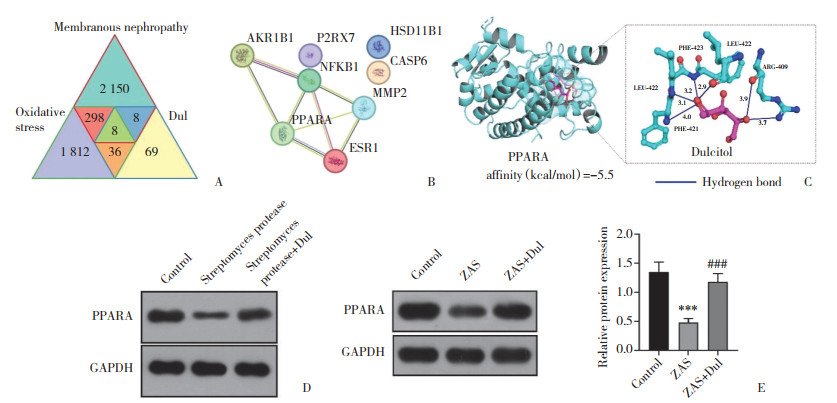
Venn图取Dul、氧化应激与膜性肾病差异基因交集获8个共同靶点(图 2A)。PPI网络按中心性值排序筛选出核心靶点NFKB1、PPARA(图 2B)。分子对接显示Dul与PPARA对接分数-5.5 kcal/mol,高于NFKB1,形成氢键,证实强结合(图 2C)。DARTS实验显示,蛋白酶组PPARA水解,Dul减少水解,证实二者结合(图 2D)。Western blotting结果显示,ZAS降低了PPARA表达水平,而Dul提高了PPARA表达水平(P < 0.001)(图 2E)。
|
| A, Venn diagram; B, STRING analysis; C, Dul-PPARA docking; D, DARTS assay results; E, Western blotting results. ***P < 0.001 vs. control group; ###P < 0.001 vs. ZAS group. n = 3. 图 2 生物信息学分析结果 Fig.2 Bioinformatics analysis results |
2.3 上调PPARA改善ZAS诱导的MPC-5细胞损伤与氧化应激
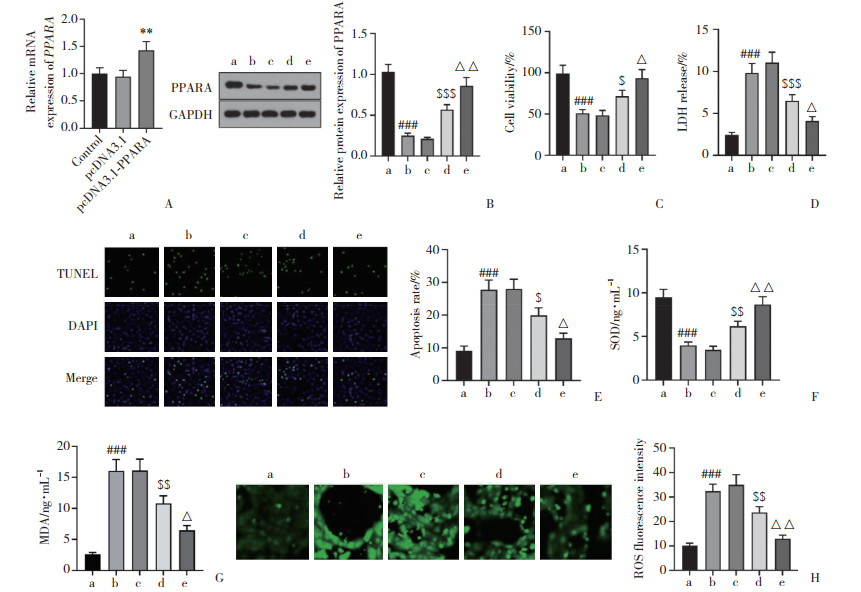
实时定量PCR结果显示,pcDNA3.1-PPARA转染显著上调PPARA mRNA表达水平(P < 0.05),证实转染成功。ZAS组较对照组PPARA蛋白表达减弱,细胞增殖活力降低、LDH水平升高、细胞凋亡增加、SOD活性下降、MDA和ROS水平升高(均P < 0.05);pcDNA3.1转染无改善作用。ZAS+pcDNA3.1-PPARA组较ZAS+pcDNA3.1组PPARA蛋白表达增强,增殖活力上调、LDH水平降低、细胞凋亡下降、SOD活性升高、MDA和ROS水平降低(均P < 0.05);联合Dul干预则进一步增强了以上保护作用(均P < 0.05)。见图 3。
|
|
A, real-time PCR results; B, Western blotting results; C, CCK-8 results; D, LDH release (podocytes); E, TUNEL results (×200);F, SOD activity; G, MDA level; H, ROS fluorescence intensity detected by DCFH-DA probe (×200). **P < 0.01 vs. pcDNA3.1 group; ###P < 0.001 vs. control group; $P < 0.05, |
2.4 敲减ABCA1逆转上调PPARA对ZAS诱导的MPC-5细胞损伤的保护作用
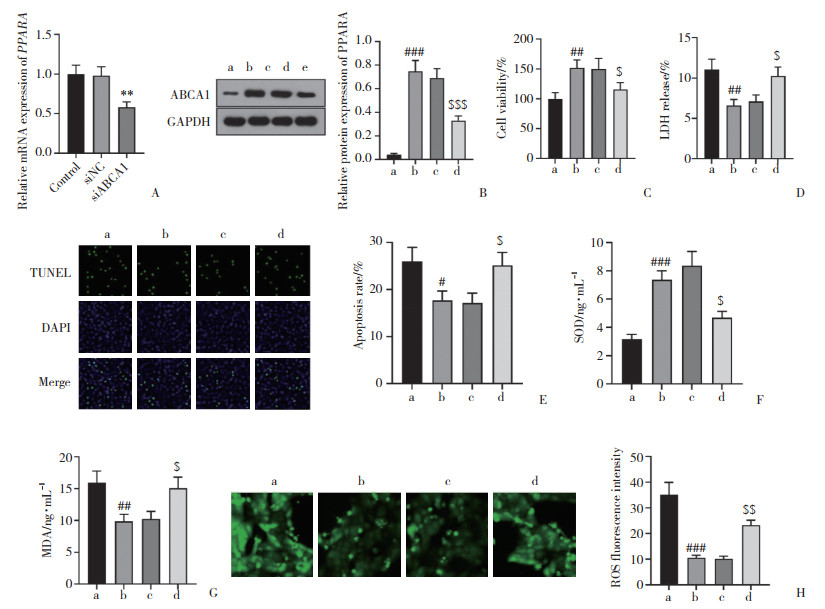
实时定量PCR结果显示,siABCA1使ABCA1 mRNA表达水平显著下调,siNC无此作用(P < 0.05)。ZAS+pcDNA3.1-PPARA组较ZAS+pcDNA3.1组ABCA1蛋白表达水平升高,细胞活力提高,LDH降低,细胞凋亡减少,SOD上调,MDA和ROS降低。ZAS+pcDNA3.1-PPARA+siABCA1组较ZAS+pcDNA3.1-PPARA+siNC组则呈相反效应(均P < 0.05)。见图 4。
|
|
A, real-time PCR results; B, Western blotting results; C, CCK-8 results; D, LDH release (podocytes); E, TUNEL results (×200);F, SOD activity; G, MDA level; H, ROS fluorescence intensity detected by DCFH-DA probe (×200). a, ZAS+pcDNA3.1 group; b, ZAS+pcDNA3.1-PPARA group; c, ZAS+pcDNA3.1-PPARA+siNC group; d, ZAS+pcDNA3.1-PPARA+siABCA1 group. **P < 0.01 vs. siNC group; #P < 0.05, ##P < 0.01, ###P < 0.001 vs. ZAS+pcDNA3.1 group; $P < 0.05, |
2.5 Dul改善膜性肾病大鼠模型肾损伤程度
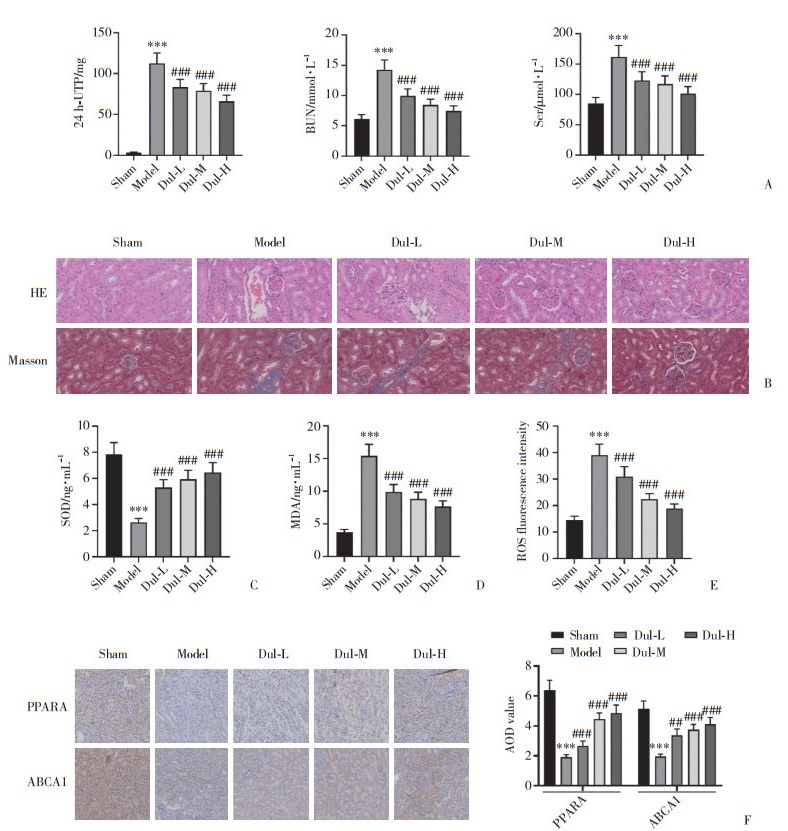
结果显示,Model组大鼠24 h-UTP及血清BUN与Scr均较Sham组升高,Dul干预后则显著降低(均P < 0.05)。HE和Masson染色显示,Sham组肾结构正常,Model组肾小球呈双轨征,肾小管变性、间质纤维化,Dul干预改善了以上病理损伤。此外,与Sham组比较,Model组肾组织SOD活性降低,MDA与ROS水平升高,PPARA与ABCA1 AOD值下降;Dul干预后SOD活性升高,MDA与ROS水平降低,PPARA、ABCA1 AOD值增加(均P < 0.05)。见图 5。
|
| A, 24 h-UTP, BUN, and Scr levels; B, renal pathology (HE & Masson staining, ×200);C to E, renal SOD, MDA, ROS levels; F, PPARA & ABCA1 (IHC, ×200). ***P < 0.001 vs. Sham group; ##P < 0.01, ###P < 0.001 vs. Model group. n = 8. 图 5 Dul改善模型大鼠肾损伤 Fig.5 Dul ameliorates renal injury in model rats |
3 讨论
ZAS诱导足细胞损伤模型的核心病理机制为补体激活产物C5b-9沉积,可在24 h内稳定复制膜性肾病关键表型,使足细胞特异性蛋白(podocin、nephrin、WT-1)表达下调,以及足突回缩、易脱落等[13]。C-BSA诱导的膜性肾病大鼠模型出现高脂血症、低蛋白血症和严重蛋白尿,可模拟人类疾病发展过程[14-15]。
本研究中,ZAS组细胞增殖活力降低、LDH释放与凋亡增加,Model组大鼠肾功能损伤加重,病理呈典型膜性肾病特征,证实模型构建成功。结合生物信息学分析结果,Dul可能通过调控PPARA/ABCA1信号通路减轻氧化应激和肾功能损害。
在膜性肾病中,炎症细胞过度产生ROS,可加剧炎症反应,导致组织和肾病进展;氧化应激影响足细胞功能,损害肾小球滤过屏障的完整性,导致蛋白尿;此外,包括SOD在内的抗氧化系统活性减弱,可导致氧化应激进一步增加,从而加剧慢性肾病进展[12]。在胶质瘤中,Dul能够通过诱导肿瘤细胞中的氧化应激,抑制细胞自噬,促进细胞凋亡,并提高胶质瘤模型大鼠的生存率[16]。本研究无论是在体外细胞模型还是大鼠模型中,均呈现SOD水平下降、MDA与ROS生成增加,这些变化加剧了细胞的氧化损伤和肾组织的病理损害。然而,Dul作为一种有效的抗氧化剂,能够显著抑制由ZAS诱导的氧化应激反应,不仅提升了SOD的活性,降低了MDA和ROS的水平,还有效改善了肾组织的病理状态,在体外和体内模型中均展现出对膜性肾病的保护作用。
PPARA是一种核转录因子,在近曲小管细胞中高度表达,具有调节脂质和葡萄糖代谢以及炎症反应的作用,在糖尿病肾病和膜性肾病纤维化组织中其表达下降[17-18]。ABCA1在足细胞中表达降低,可通过炎性小体途径促进肾损伤[19]。PPARA激活可增加ABCA1表达,促进胆固醇外流,改善糖脂紊乱[20]。此外,PPARγ与LXRα-ABCA1通路共同作用也可降低氧化应激水平[21]。本研究中分子对接结果显示,Dul与PPARA结合力较强,并促进PPARA蛋白表达。本研究还发现,当在足细胞中过表达PPARA时,ABCA1 mRNA表达水平显著增强,同时ZAS诱导的足细胞增殖活力改善、凋亡减少,氧化应激水平降低。提示PPARA可能通过某种机制促进ABCA1的表达,从而降低氧化应激程度。
综上所述,PPARA/ABCA1信号通路在膜性肾病中发挥着重要作用,而Dul可能通过促进PPARA/ABCA1信号通路的激活,抑制膜性肾病中的氧化应激,并改善肾损伤。因此,开发能够激活PPARA/ABCA1信号通路的药物,如Dul或其衍生物,可能有助于治疗膜性肾病,本研究结果为膜性肾病的药物研发提供了新的思路。
| [1] |
DANTAS M, SILVA LBB, PONTES BTM, et al. Membranous nephropathy[J]. Braz J Nephrol, 2023, 45(2): 229-243. DOI:10.1590/2175-8239-jbn-2023-0046en |
| [2] |
王媛媛, 周华. 抗磷脂酶A2受体抗体与原发性膜性肾病的临床特征和预后的相关性[J]. 中国医科大学学报, 2022, 51(2): 106-110. DOI:10.12007/j.issn.0258-4646.2022.02.003 |
| [3] |
LIU ZQ, WANG H, HAN H, et al. The protective effect of dulcitol on lipopolysaccharide-induced intestinal injury in piglets: mechanistic insights[J]. J Nutr Biochem, 2024, 133: 109719. DOI:10.1016/j.jnutbio.2024.109719 |
| [4] |
王晗, 刘正群, 朱龙博, 等. 卫矛醇通过调节Toll样受体4/髓样分化因子88/核因子-κB信号通路缓解脂多糖诱导的猪肠道上皮细胞损伤[J]. 动物营养学报, 2024, 36(6): 3952-3962. DOI:10.12418/CJAN2024.338 |
| [5] |
SU BX, HAN HB, JI CY, et al. miR-21 promotes calcium oxalate-induced renal tubular cell injury by targeting PPARA[J]. Am J Physiol Renal Physiol, 2020, 319(2): F202-F214. DOI:10.1152/ajprenal.00132.2020 |
| [6] |
ZUO FW, LIU ZY, WANG MW, et al. CCDC92 promotes podocyte injury by regulating PA28α/ABCA1/cholesterol efflux axis in type 2 diabetic mice[J]. Acta Pharmacol Sin, 2024, 45(5): 1019-1031. DOI:10.1038/s41401-023-01213-4 |
| [7] |
LUO ZS, YU XC, WANG C, et al. Trimethylamine N-oxide promotes oxidative stress and lipid accumulation in macrophage foam cells via the Nrf2/ABCA1 pathway[J]. J Physiol Biochem, 2024, 80(1): 67-79. DOI:10.1007/s13105-023-00984-y |
| [8] |
SONG J, QIU HR, DU P, et al. Polyphenols extracted from Shanxi-aged vinegar exert hypolipidemic effects on OA-induced HepG2 cells via the PPARα-LXRα-ABCA1 pathway[J]. J Food Biochem, 2022, 46(2): e14029. DOI:10.1111/jfbc.14029 |
| [9] |
WANG LL, LIU X. An oxidative stress-related signature for predic-ting the prognosis of liver cancer[J]. Front Genet, 2023, 13: 975211. DOI:10.3389/fgene.2022.975211 |
| [10] |
包能, 于翔, 顾鸣佳, 等. 联合液相色谱-质谱分析和网络药理学探讨益肾清利方治疗特发性膜性肾病的作用机制[J]. 世界科学技术-中医药现代化, 2024, 26(3): 797-807. DOI:10.11842/wst.20230305002 |
| [11] |
PAN Y, CHEN S, WU L, et al. Animal models of membranous nephropathy: more choices and higher similarity[J]. Front Immunol, 2024, 15: 1412826. DOI:10.3389/fimmu.2024.1412826 |
| [12] |
JIA SY, SI RH, LIU GZ, et al. Diosgenin protects against cationic bovine serum albumin-induced membranous glomerulonephritis by attenuating oxidative stress and renal inflammation via the NF-κB pathway[J]. Pharm Biol, 2024, 62(1): 285-295. DOI:10.1080/13880209.2024.2330602 |
| [13] |
MIAO H, WANG YN, SU W, et al. Sirtuin 6 protects against podocyte injury by blocking the renin-angiotensin system by inhibiting the Wnt1/β-catenin pathway[J]. Acta Pharmacol Sin, 2024, 45(1): 137-149. DOI:10.1038/s41401-023-01148-w |
| [14] |
WANG WD, SHENG L, CHEN YY, et al. Total coumarin derivates from Hydrangea paniculata attenuate renal injuries in cationized-BSA induced membranous nephropathy by inhibiting complement activation and interleukin 10-mediated interstitial fibrosis[J]. Phytomedicine, 2022, 96: 153886. DOI:10.1016/j.phymed.2021.153886 |
| [15] |
MA MC, PAN Y, ZHANG Y, et al. Metformin combined with rapamycin ameliorates podocyte injury in idiopathic membranous nephropathy through the AMPK/mTOR signaling pathway[J]. J Cell Commun Signal, 2023, 17(4): 1405-1415. DOI:10.1007/s12079-023-00781-8 |
| [16] |
ZHANG YL, WANG H, LI FJ, et al. Inhibitory effects of Dulcitol on rat C6 glioma by regulating autophagy pathway[J]. Nat Prod Res, 2020, 34(10): 1437-1441. DOI:10.1080/14786419.2018.1512994 |
| [17] |
GAO JJ, GU ZY. The role of peroxisome proliferator-activated receptors in kidney diseases[J]. Front Pharmacol, 2022, 13: 832732. DOI:10.3389/fphar.2022.832732 |
| [18] |
FU ZN, GENG XD, LIU C, et al. Identification of common and specific fibrosis-related genes in three common chronic kidney diseases[J]. Ren Fail, 2024, 46(1): 2295431. DOI:10.1080/0886022X.2023.2295431 |
| [19] |
ITO M, DUCASA GM, MOLINA JD, et al. ABCA1 deficiency contributes to podocyte pyroptosis priming via the APE1/IRF1 axis in diabetic kidney disease[J]. Sci Rep, 2023, 13(1): 9616. DOI:10.1038/s41598-023-35499-5 |
| [20] |
李翠茹, 郝媛媛, 刘妍, 等. 津力达对胰岛素抵抗大鼠糖脂代谢紊乱及对PPARα/ABCA1通路的影响[J]. 世界科学技术-中医药现代化, 2023, 25(4): 1382-1389. DOI:10.11842/wst.20220314016 |
| [21] |
李智, 高铸烨, 别玉龙, 等. 黄连素通过PPARγ-LXRα-ABCA1信号通路促进ApoE-/-小鼠胆固醇代谢的作用机制研究[J]. 中华中医药学刊, 2022, 40(10): 28-32, 260-261. DOI:10.13193/j.issn.1673-7717.2022.10.006 |
 2026, Vol. 55
2026, Vol. 55