文章信息
- 陈熹铭, 吴岑
- CHEN Ximing, WU Cen
- 前列腺素D2受体对肺腺癌细胞增殖、迁移及自噬的影响
- Effect of PTGDR2 on the proliferation, migration, and autophagy of lung adenocarcinoma cells
- 中国医科大学学报, 2025, 54(7): 638-642
- Journal of China Medical University, 2025, 54(7): 638-642
-
文章历史
- 收稿日期:2025-05-07
- 网络出版时间:2025-07-07 09:54:59
2. 中国医科大学附属盛京医院呼吸与危重症医学科, 沈阳 110004
2. Department of Respiratory and Critical Care Medicine, Shengjing Hospital of China Medical University, Shenyang 110004, China
肺腺癌(lung adenocarcinoma,LUAD)是非小细胞肺癌(non-small cell lung cancer,NSCLC)中最为常见的类型,近年来其发病率和死亡率持续上升[1-2]。肿瘤细胞的浸润和转移是导致LUAD治疗失败的主要原因,而肿瘤干细胞的存在则是肿瘤复发和耐药的根源[3-5]。与此同时,肿瘤细胞通过免疫逃逸机制抑制免疫系统的抗肿瘤作用,进一步加剧了治疗的困难[6]。此外,肿瘤微环境的复杂性,包括低氧、免疫抑制和基质改变,也使得LUAD的治疗更加艰难[7-8]。
前列腺素D2(prostaglandin D2,PGD2)能够通过激活其受体(prostaglandin D2 receptor,PTGDR2),抑制肿瘤细胞的增殖和转移,还可能通过减少肿瘤干细胞(cancer stem cells,CSC)相关的免疫逃逸和免疫抑制信号,改善肿瘤免疫微环境,提高机体对肿瘤的免疫应答能力[9-13]。因此,PGD2/PTGDR2通路可能成为抑制CSC及改善肿瘤免疫微环境的潜在治疗靶点。本研究拟探讨PTGDR2在LUAD进展中的作用及其通过自噬调控CSC干性的靶向潜力,以期为PTGDR2在临床治疗中的应用提供理论依据。
1 材料与方法 1.1 细胞培养用含10% FBS和10 mg/mL青霉素-链霉素的RPMI 1640培养基(美国Gibco公司),在37 ℃、5%CO2培养箱中,培养人LUAD细胞系A549(购自中国科学院细胞库)。每72 h换液1次。取对数生长期细胞用于本研究。
1.2 细胞转染及分组利用siRNA技术沉默PTGDR2,靶向PTGDR2的siRNA(大连瑞真生物技术有限公司)序列为5’-UCAACACGGUGCCCUAUUUTT-3 ’。转染前24 h接种A549细胞至24孔板(5×104/孔),待细胞生长达到30%~50%融合时,用lipofectamine 3000、Opti-MEM™培养基及50 nmol/L siPTGDR2或siNC进行细胞转染,在37 ℃、5%CO2培养箱中继续培养18~48 h。将A549细胞随机分为5组:(1)siNC组,仅转染siNC;(2)siNC+PGD2组,用2 μg/mL PGD2处理siNC转染细胞;(3)siPTGDR2组,仅转染siPTGDR2;(4)siPTGDR2+PGD2组,用2 μg/mL PGD2处理siPTGDR2转染细胞;(5)siPTGDR2+PGD2+RAPA组,用2 μg/mL PGD2及20 μmol/L细胞自噬激动剂RAPA处理siPTGDR2转染细胞。
1.3 细胞迁移能力检测将siNC组、siNC+PGD2组、siPTGDR2组、siPTGDR2+PGD2组细胞按照5×104/孔的密度,接种至Transwell上室。在Transwell上室添加无血清RPMI1640培养基,下室添加含1% FBS的培养基,培养24 h。取出小室,结晶紫染色,用PBS清洗。光学显微镜下观察并拍照,用ImageJ软件计算迁移细胞所占面积。
1.4 细胞增殖能力检测按照1×104/孔的密度,将siNC组、siNC+PGD2组、siPTGDR2组、siPTGDR2+PGD2组细胞接种至24孔板中,加入含10%胎牛血清的RPMI 1640培养基,在37 ℃、5% CO2培养箱中培养1、3、5 d。在显微镜下计数细胞数,并计算增殖率。细胞增殖率=(实验组细胞数-对照组细胞数)/对照组细胞数×100%。
1.5 CSC标志物分析siNC组、siNC+PGD2组、siPTGDR2组、siPTGDR2+PGD2组细胞培养3 d后,进行CSC表面抗原CD166染色,通过流式细胞术分析CSC标志物CD166阳性率。
1.6 实时PCR使用RNeasy Mini Kit(美国Qiagen公司)提取5组细胞总RNA,逆转录cDNA,进行实时PCR。PCR反应体系:2×SYBR® Green Pro Taq HS Premix 20 μL,cDNA 2 μL,Primer F(10 μmol/L)0.4 μL,Primer R(10 μmol/L)0.4 μL,RNase free water 7.2 μL。GAPDH作内参照。引物序列如下:LC3B,正向5’-AGCAGCATCCAACCAAAATC-3’,反向5’-CTGTGTCCGTTCACCAACAG-3’;CD166,正向5’-TGGCTGTGTTTGAGATTGCC-3’,反向5’-TGGCGTAGTGTTGGTTCTGA-3’;OCT4,正向5’-GAGGAGTCCCAGGACATGAA-3’,反向5’-GGAGACCCAGCAGCCTCAAA-3’;GAPDH,正向5’-TTCCACCTTTGATGCTGGGG-3’,反向5’-CCATGTAGGCCATGAGGTCC-3’。采用2-ΔΔCt法计算自噬及CSC相关基因的相对表达量。
1.7 统计学分析采用SPSS 25.0软件进行统计学分析。计量资料用x±s表示,组间比较采用两独立样本t检验,组内比较采用方差分析。计数资料用率(%)表示,采用χ2检验进行比较。P < 0.05为差异有统计学意义。
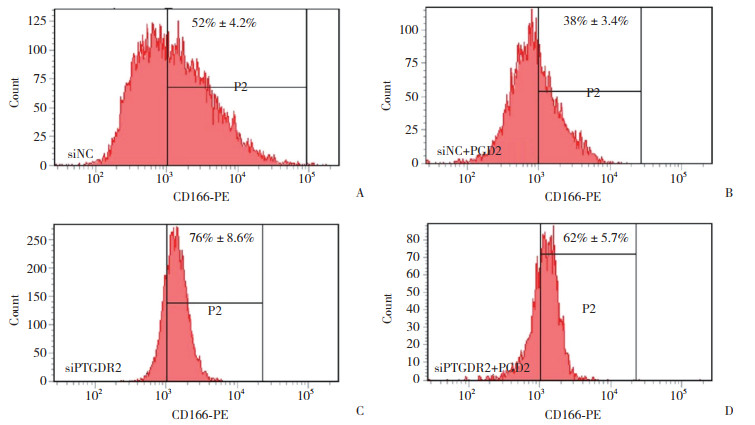
2 结果 2.1 CSC表面抗原CD166染色结果与siNC组细胞(52%±4.2%)相比,siNC+PGD2组细胞(38%±3.4%)CD166表达水平降低,siPTGDR2组细胞(76%±8.6%)和siPTGDR2+PDG2组细胞(62%±5.7%)CD166表达水平升高,差异均有统计学意义(均P < 0.05)。siPTGDR2+PDG2组细胞CD166表达水平与siPTGDR2组细胞比较无显著差异。提示PGD2可能通过其受体PTGDR2抑制CD166的表达,调控CSC特性。见图 1。
|
| A,siNC group;B,siNC+PGD2 group;C,siPTGDR2 group;D,siPTGDR2+PDG2 group. 图 1 CSC表面抗原CD166染色结果 Fig.1 Cancer stem cell surface marker CD166 through staining results |
2.2 PDG2/PTDGR2对A549细胞自噬及CSC相关基因表达的影响
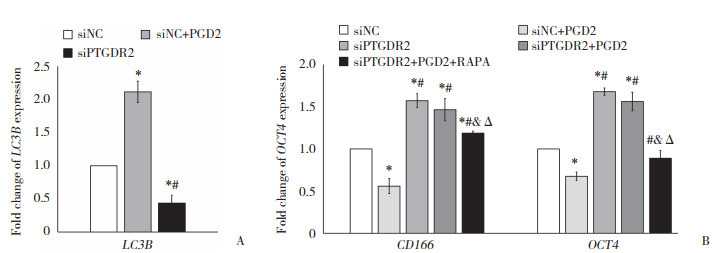
实时PCR结果显示,与siNC组相比,siNC+PGD2组自噬相关基因LC3B mRNA表达水平升高,siPTGDR2组LC3B mRNA表达水平降低,差异均有统计学意义(均P < 0.05)。提示PGD2/PTGDR2信号可促进LUAD细胞自噬。见图 2A。与siNC组相比,siNC+PGD2组CSC相关基因CD166、OCT4 mRNA表达水平降低;siPTGDR2组、siPTGDR2+PGD2组和siPTGDR2+PGD2+RAPA组CD166、OCT4 mRNA表达水较siNC+PGD2组升高;siPTGDR2+PGD2+RAPA组CD166、OCT4 mRNA表达水平则较siPTGDR2组、siPTGDR2+PGD2组降低,差异均有统计学意义(均P < 0.05)。说明PGD2诱导的CSC抑制作用由于敲低PTGDR2而消失,而自噬激活剂RAPA可增加CD166和OCT4的表达。提示自噬激动剂RAPA能够部分逆转PTGDR2缺失带来的CSC特性增强现象,进一步证实了PTGDR2在自噬与CSC特性调控中的重要作用,见图 2B。
|
| A,LC3B mRNA expression;B,CD166 and OCT4 mRNA expression. * P < 0.05 vs. siNC group;# P < 0.05 vs. siNC+PGD2 group;& P < 0.05 vs. siPTGDR2 group;Δ P < 0.05 vs. siPTGDR2+PGD2 group. 图 2 实时PCR结果 Fig.2 Real time PCR results |
2.3 PDG2/PDGR2对A549细胞迁移及增殖的影响
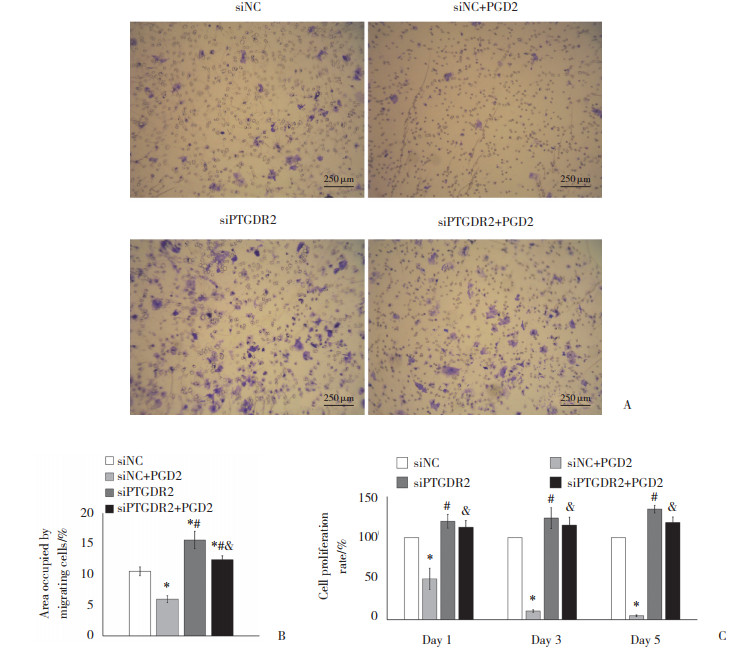
Transwell实验结果显示,与siNC组细胞比较,siNC+PGD2组细胞迁移能力下降,siPTGDR2组、siPTGDR2+PGD2组细胞迁移能力增加,siPTGDR2+PGD2组细胞迁移能力较siPTGDR2组降低,差异均有统计学意义(均P < 0.05)。见图 3A、3B。
|
| A and B,the Transwell system was used to assess the migrative ability of A549 cells in each group;C,cell proliferation rate of four groups on day 1,3,and 5. * P < 0.05 vs. siNC group;# P < 0.05 vs. siNC+PGD2 group;& P < 0.05 vs. siPTGDR2 group. 图 3 PGD2/PTGDR2信号通路对A549细胞增殖和迁移的影响 Fig.3 Effect of PGD2/PTGDR2 signaling pathway on the proliferation and migration of A549 cells |
对培养1、3、5 d的4组细胞进行计数并计算增殖率,结果显示,与siNC组比较,siNC+PGD2组细胞增殖率降低;与siNC+PGD2组比较,siPTGDR2组细胞增殖率升高;与siPTGDR2组比较,siPTGDR2+PGD2组细胞增殖率降低,差异均有统计学意义(均P < 0.05)。提示PGD2通过其受体PTGDR2抑制了LUAD细胞A549的增殖与迁移,而敲低PTGDR2可抵消这种抑制。见图 3C。
3 讨论PTGDR2作为G蛋白偶联受体家族成员,具有抗肿瘤特性。PTGDR2在LUAD、胃癌等实体肿瘤中普遍呈低表达,且其表达水平与患者的预后呈正相关[9-11]。PGD2能够通过激活其受体PTGDR2抑制CSC,主要机制包括以下2个方面:通过抑制STAT3的磷酸化和核转位,下调CSC相关基因的表达,削弱其自我更新能力;PTGDR2与E3泛素连接酶RNF5竞争结合ATG4B,促进自噬相关蛋白表达,激活自噬通路,从而进一步抑制CSC[10-13]。此外,PTGDR2的低表达还可能影响肿瘤微环境的免疫逃逸机制[14-17]。因此,PGD2/PTGDR2通路可能成为抑制CSC及改善肿瘤免疫微环境的潜在治疗靶点。
研究发现,胃癌组织中L-PTGDS/PTGDR2表达显著下调,且与CSC标志物(Sall4、Lgr5)的表达呈显著负相关。PTGDR2沉默可增强CSC自我更新能力,而外源性PGD2刺激或L-PTGDS过表达则能有效抑制CSC。PGD2/PTGDR2信号通路通过特异性阻断STAT3 Thr705位点磷酸化,抑制其核转位及转录激活功能,从而下调CSC相关基因表达[12]。本研究中,敲低PTGDR2后,A549细胞的CSC相关基因CD166和OCT4的表达上调,自噬相关基因LC3B表达下调,表明PTGDR2通过自噬调控轴抑制了A549细胞的CSC特性。自噬激动剂RAPA的干预能够部分逆转PTGDR2敲除带来的CSC干性增强,从而进一步证实了PTGDR2在自噬与CSC调控中的重要作用。相比以往在胃癌等肿瘤模型中关于PTGDR2调控STAT3磷酸化或维持CSC特性的研究[11-12],本研究结果拓展了PTGD2/PTGDR2信号通路在自噬调控方面的作用。
研究发现,PTGDR2的低表达与肿瘤增殖和转移相关,PGD2可通过PTGDR2依赖性方式显著抑制肿瘤生长及转移,且可被PTGDR2敲除完全逆转。因此,PTGDR2在PGD2介导的抗肿瘤效应中发挥着关键作用。本研究结果显示,PGD2通过PTGDR2抑制了LUAD细胞A549的增殖和迁移,而这一作用在PTGDR2敲除后被显著抵消。
综上所述,PTGDR2在LUAD的进展中发挥重要作用。PTGDR2能够通过激活PGD2/PTGDR2信号通路,抑制肿瘤细胞的增殖、迁移及CSC特性,并通过促进自噬抑制肿瘤进展。本研究结果为PTGDR2作为LUAD的治疗靶点提供了理论依据,并为PTGDR2激动剂在LUAD的临床治疗,尤其是在联合免疫治疗中的应用,提供了新的思路。
| [1] |
DONG HH, TIAN YH, XIN SW, et al. Diagnosis and management of multiple primary lung cancer[J]. Front Oncol, 2024, 14: 1392969. DOI:10.3389/fonc.2024.1392969 |
| [2] |
Olteanu GE, Kern I, Kalson L, et al. From morphology to molecules: advances in the distinction of multiple primary lung cancers from intrapulmonary metastases in non-small cell lung cancer[J]. Adv Anat Pathol, 2024, 31(5): 318-323. DOI:10.1097/PAP.0000000000000449 |
| [3] |
Fan L, Wang X, Cheng C, et al. Inhibitory effect and mechanism of ursolic acid on cisplatin-induced resistance and stemness in human lung cancer A549 cells[J]. Evid Based Complement Alternat Med, 2023, 14: 1307323. DOI:10.1155/2023/1307323 |
| [4] |
ZHANG HF, JIANG H, ZHU LC, et al. Cancer-associated fibroblasts in non-small cell lung cancer: recent advances and future perspectives[J]. Cancer Lett, 2021, 514: 38-47. DOI:10.1016/j.canlet.2021.05.009 |
| [5] |
DEL RE M, ARRIGONI E, RESTANTE G, et al. Concise review: resistance to tyrosine kinase inhibitors in non-small cell lung cancer: the role of cancer stem cells[J]. Stem Cells, 2018, 36(5): 633-640. DOI:10.1002/stem.2787 |
| [6] |
CASCONE T, FRADETTE J, PRADHAN M, et al. Tumor immunology and immunotherapy of non-small-cell lung cancer[J]. Cold Spring Harb Perspect Med, 2022, 12(5): a037895. DOI:10.1101/cshperspect.a037895 |
| [7] |
KACHLER K, BAILER M, HEIM L, et al. Enhanced acid sphingomye-linase activity drives immune evasion and tumor growth in non-small cell lung carcinoma[J]. Cancer Res, 2017, 77(21): 5963-5976. DOI:10.1158/0008-5472.CAN-16-3313 |
| [8] |
PENG HX, WU XR, LIU SP, et al. Multiplex immunofluorescence and single-cell transcriptomic profiling reveal the spatial cell interaction networks in the non-small cell lung cancer microenvironment[J]. Clin Transl Med, 2023, 13(1): e1155. DOI:10.1002/ctm2.1155 |
| [9] |
DELGIORNO KE, CHUNG CY, VAVINSKAYA V, et al. Tuft cells inhibit pancreatic tumorigenesis in mice by producing prostaglandin D2[J]. Gastroenterology, 2020, 159(5): 1866-1881.e8. DOI:10.1053/j.gastro.2020.07.037 |
| [10] |
SLANOVC J, MIKULČIĆ M, JAHN N, et al. Prostaglandin 15d-PGJ2 inhibits proliferation of lung adenocarcinoma cells by inducing ROS production and activation of apoptosis via sirtuin-1[J]. Biochim Biophys Acta Mol Basis Dis, 2024, 1870(1): 166924. DOI:10.1016/j.bbadis.2023.166924 |
| [11] |
ZHANG Q, TIAN HJ, GE KP, et al. PGD2/PTGDR2 signaling pathway affects the self-renewal capacity of gastric cancer stem cells by regulating ATG4B ubiquitination[J]. Front Oncol, 2024, 14: 1496050. DOI:10.3389/fonc.2024.1496050 |
| [12] |
ZHANG B, BIE QL, WU PP, et al. PGD2/PTGDR2 signaling restricts the self-renewal and tumorigenesis of gastric cancer[J]. Stem Cells, 2018, 36(7): 990-1003. DOI:10.1002/stem.2821 |
| [13] |
WANG FF, TIAN HJ, GAO PY, et al. PGD2/PTGDR2 signaling affects the stemness of gastric cancer stem cells by regulating autophagy[J]. Comb Chem High Throughput Screen, 2025. DOI:10.2174/0113862073372570250123091700 |
| [14] |
OOKI A, MALEKI Z, TSAY JJ, et al. A panel of novel detection and prognostic methylated DNA markers in primary non-small cell lung cancer and serum DNA[J]. Clin Cancer Res, 2017, 23(22): 7141-7152. DOI:10.1158/1078-0432.CCR-17-1222 |
| [15] |
MARCOS-VADILLO E, GARCÍA-SÁNCHEZ A, SANZ C, et al. PTGDR gene expression and response to dexamethasone treatment in an in vitro model[J]. PLoS One, 2017, 12(10): e0186957. DOI:10.1371/journal.pone.0186957 |
| [16] |
TIAN HJ, GE KP, WANG LL, et al. Advances in PGD2/PTGDR2 signaling pathway in tumors: a review[J]. Biomol Biomed, 2024, 24(5): 1055-1067. DOI:10.17305/bb.2024.10485 |
| [17] |
ZHANG Q, WANG FF, HUANG Y, et al. PGD2/PTGDR2 signal affects the viability, invasion, apoptosis, and stemness of gastric cancer stem cells and prevents the progression of gastric cancer[J]. Comb Chem High Throughput Screen, 2024, 27(6): 933-946. DOI:10.2174/1386207326666230731103112 |
 2025, Vol. 54
2025, Vol. 54