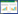文章信息
- 杨加敏, 刘艳君, 李响
- YANG Jiamin, LIU Yanjun, LI Xiang
- 超声诊断胆囊管低位汇入1例报道
- Diagnosis of low insertion of cystic duct using ultrasound: a case report
- 中国医科大学学报, 2025, 54(3): 273-275
- Journal of China Medical University, 2025, 54(3): 273-275
-
文章历史
- 收稿日期:2023-12-11
- 网络出版时间:2025-03-19 11:08:51
胆囊管低位汇入(low insertion of cystic duct,LICD)属于胆囊管汇入部位异常,是胆道变异中相对常见的一种变异类型,但关于胆囊管解剖变异的影像学诊断报道中鲜有关于LICD的超声诊断报道。本文报道了我院收治的1例LICD病例,旨在提高超声医生对该疾病的认识。
1 临床资料患者,女,66岁,因腹痛于外院诊断“胆总管末端结石”1月余后收入我院,欲行内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)取石治疗。术前实验室检查提示白细胞计数3.44×109/L,总胆红素(total bilirubin,TBIL)13.8 μmol/L,直接胆红素(direct bilirubin,DBIL)3.4 μmol/L。全腹增强CT检查提示胆总管略宽。超声检查提示胆总管内径约0.95 cm,胆总管上段管腔内条带状回声(图 1)。因不排除有胆总管小结石自行排出的可能,且为明确是否需行ERCP,进一步行内镜超声检查。内镜超声检查提示肝外胆管内未见强回声,故患者未行ERCP取石治疗。因患者自觉无明显不适,且无手术治疗指征,符合出院标准,医嘱建议其出院后3~6个月门诊复查超声、腹部CT或磁共振胰胆管成像(magnetic resonance cholangiopancreatography,MRCP),病情变化随诊。
|
| 箭头所示为胆总管内条带状回声. 图 1 首次超声检查图像 |
患者出院3个月后,于门诊复查超声,结果提示胆囊管内径约0.47 cm,长度约4.98 cm,肝总管内径约1.09 cm,长度约3.95 cm,胆总管内径约0.87 cm,长度约2.72 cm,胆囊管在肝外胆管下段汇入其内,综上判断为肝外胆管扩张,LICD可能性大(图 2)。结合既往MRCP检查见肝外胆管扩张,胆囊管汇入位置低,汇入点位于胆总管左侧壁(图 3),证实患者为胆囊管低位螺旋汇入。患者因自觉无明显不适,选择定期超声复查。本研究获得我院医学科学伦理委员会批准。
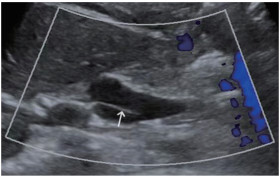
|
| A,与胆囊(GB)相连接冗长扩张的胆囊管(CD);B,胆囊管(CD)与扩张的肝总管(CHD)伴行,最终汇合成胆总管(CBD)进入胰头(PAH). 图 2 复查超声图像 |
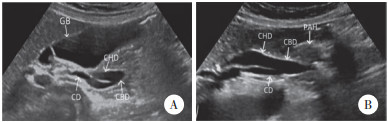
|
| 肝外胆管扩张. 箭头所示为胆囊管低位汇入,汇入点位于肝外胆管左侧壁. 图 3 3D-MRCP检查图像 |
2 讨论
胆囊管是控制胆汁流入和流出胆囊的管道,长度约2 cm。多数情况下胆囊管以锐角汇入肝外胆管上1/3处的右侧壁[1],若胆囊管汇入肝外胆管的下1/2段,肝总管的长度大于胆总管长度,即为LICD。LICD分为低位平行汇入和低位螺旋汇入2类,前者胆囊管与肝总管平行伴行汇入胆总管右侧壁,后者胆囊管环绕肝总管走行汇入胆总管左侧壁、前壁或后壁,二者常伴有胆囊管冗长扩张。
胆囊管解剖变异可影响胆汁从肝总管流入胆囊和流出胆囊所需的压力差,也可增加胆汁流动的阻力,在LICD中,冗长的胆囊管使胆汁排空障碍,导致胆汁淤滞和反流,是发生胆囊炎、胆囊结石和胆总管结石复发的危险因素[2-3]。胆管的解剖变异也是造成医源性胆管损伤的主要原因[4],腹腔镜胆囊切除术是目前胆囊切除的常规手术方式[5],而胆管损伤是腹腔镜胆囊切除术中的一种严重并发症,发生率约为开腹胆囊切除术的2~3倍,约70%~80%的胆管损伤是由于患者存在胆管的解剖变异而导致医生对胆管解剖结构识别错误。LICD中胆囊管与肝总管平行走行,或螺旋走行至胆总管前方、后方或左侧,使胆囊三角区的胆囊管、肝总管和胆总管难以区分,容易造成术中胆总管或肝总管被钳夹和离断,最终导致医源性胆管损伤。若无法早期识别LICD,也可造成ERCP操作失败,GEORGE等[6]最先报道了1例行ERCP下胆总管支架术的胆总管结石伴化脓性胆管炎病例,由于患者在术前未被诊断出患有LICD,导致术者将低位走行的胆囊管误认为胆总管,将应该放置于胆总管的支架误置于胆囊管内,导致最终开腹手术切除胆囊。此外,最近有研究[7]提出,LICD与胰腺癌和壶腹周围癌相关,可能与较短的胆总管远端腔内压力升高有关,压力升高导致胆汁反流至胰管和胆管周围腺体,从而启动致癌过程。因此,LICD的早期识别及诊断具有重要的临床意义,不仅可为临床医生指导患者预防胆道结石形成提供参考,也可在术前为临床医生提供有关胆管解剖结构的信息,从而避免医源性胆管损伤和ERCP操作失败的发生。
胆囊管解剖变异的诊断主要借助影像学检查,MRCP是目前胆道解剖学检查中侵入性最小、最可靠的检查方法[8],能全面地显示胰胆管的解剖结构及连接关系,可诊断包括LICD在内的胆管解剖变异[9],有文献[10]报道MRCP诊断胆管解剖变异的准确率高达96.9%。但MRCP对胆管周围组织的定性诊断较差,且易受伪影影响,目前仍不能作为胆道系统疾病的常规检查项目。超声检查是诊断胆道疾病的首选方法,但目前对于LICD的超声诊断报道较为罕见,这可能与未扩张的胆囊管在超声检查中显示困难及超声医生对胆囊管解剖变异认识不足有关。本例患者在既往超声检查中,由于初诊超声医生对LICD认识不足,将相互伴行的胆囊管和肝总管误认为胆总管上段,将胆囊管和肝总管二者相重叠的管壁回声误认为胆总管上段腔内的条带状回声(图 1),而复查超声时发现第一肝门处2条胆管回声,右侧的胆管向上与胆囊相连接,为冗长扩张的胆囊管(图 2A),左侧胆管与肝内的左右肝管相连接,为扩张的肝总管,最终二者汇合成胆总管进入胰头(图 2B),胆囊管在肝外胆管下段汇入,因此,超声诊断为LICD。但超声检查目前很难确定胆囊管汇入点的位置,还需借助MRCP进一步明确。本例LICD患者的3D-MRCP图像可清晰显示胆囊管汇入点位于胆总管的左侧壁(图 3),属LICD的低位螺旋汇入。
综上所述,LICD的早期识别和诊断具有重要的临床意义。当合并胆囊管扩张时,超声检查可以识别诊断LICD,超声医生应当熟知胆囊管解剖变异的类型,在超声检查发现肝外胆管扩张合并回声异常时,应动态检查胆管的走行和连接情况,明确是否存在胆管的解剖变异。当超声检查怀疑LICD时,应建议患者进一步行MRCP等影像学检查,为临床医生进一步诊治提供依据。
| [1] |
PRIYA A, GHOSH SK, WALOCHA JA, et al. Variations in extra-hepatic biliary tree morphology and morphometry: a narrative review of literature with focus on cystohepatic triangle[J]. Folia Morphol, 2023, 82(3): 498-506. DOI:10.5603/FM.a2022.0069 |
| [2] |
沈为光, 陈飞翔, 龚沈初. 胆囊管汇合变异的分型与胆囊结石相关性的MRCP研究[J]. 临床放射学杂志, 2019, 38(2): 270-275. DOI:10.13437/j.cnki.jcr.2019.02.021 |
| [3] |
CHOI SJ, YOON JH, KOH DH, et al. Low insertion of cystic duct increases risk for common bile duct stone recurrence[J]. Surg Endosc, 2022, 36(5): 2786-2792. DOI:10.1007/s00464-021-08563-2 |
| [4] |
YANG SH, HU S, GU XH, et al. Analysis of risk factors for bile duct injury in laparoscopic cholecystectomy in China: a systematic review and meta-analysis[J]. Medicine, 2022, 101(37): e30365. DOI:10.1097/MD.0000000000030365 |
| [5] |
黎鑫, 艾克拜尔·艾力, 阿力木江·麦斯依提, 等. 机器人辅助和腹腔镜袖状胃切除术联合胆囊切除术治疗肥胖合并胆囊结石患者的减重效果和安全性[J]. 中国医科大学学报, 2023, 52(3): 219-223, 229. DOI:10.12007/j.issn.0258-4646.2023.03.005 |
| [6] |
GEORGE RA, DEBNATH J, SINGH K, et al. Low insertion of a cystic duct into the common bile duct as a cause for a malpositioned biliary stent: demonstration with multidetector computed tomography[J]. Singapore Med J, 2009, 50(7): e243-e246. |
| [7] |
MURAKI T, REID MD, PEHLIVANOGLU B, et al. Variant ana- tomy of the biliary system as a cause of pancreatic and peri-ampullary cancers[J]. HPB, 2020, 22(12): 1675-1685. DOI:10.1016/j.hpb.2020.03.014 |
| [8] |
王敏, 石喻, 郭启勇. 慢性胰腺炎影像学诊断现状及研究进展[J]. 中国医科大学学报, 2019, 48(7): 652-656. DOI:10.12007/j.issn.0258-4646.2019.07.017 |
| [9] |
GARG S, DUTTA U, CHALUVASHETTY SB, et al. The anatomy of the cystic duct and its association with cholelithiasis: mr cholangiopancreatographic study[J]. Clin Anat, 2022, 35(7): 847-854. DOI:10.1002/ca.23856 |
| [10] |
JAGANATHAN S, RAY B, VELAGA J. Our experience in tracking the tract: normal biliary anatomy and variants on magnetic resonance cholangiopancreatography in living donor liver transplan-tation[J]. Cureus, 2023, 15(2): e34695. DOI:10.7759/cureus.34695 |
 2025, Vol. 54
2025, Vol. 54