文章信息
- 陈凯立, 王婷, 罗智浩
- CHEN Kaili, WANG Ting, LUO Zhihao
- PPARδ激动剂GW501516调控细胞自噬对脓毒症小鼠肠黏膜屏障的影响
- Effects of PPARδ agonist GW501516 on the intestinal mucosal barrier in septic mice by regulating autophagy
- 中国医科大学学报, 2025, 54(3): 246-250, 256
- Journal of China Medical University, 2025, 54(3): 246-250, 256
-
文章历史
- 收稿日期:2024-03-07
- 网络出版时间:2025-3-19 14:13:23
脓毒症常继发于严重的感染,是机体对感染反应失调从而导致危及生命的器官功能障碍,是一种高病死率的临床综合征。肠道作为体内最大的细菌库,是脓毒症的靶器官,其损伤会加重或诱发脓毒症[1]。肠黏膜屏障在脓毒症的发生和发展过程中起重要作用[2],因此,早期干预肠黏膜屏障损伤对抑制脓毒症恶化、改善预后具有重要意义。研究[3]显示,抑制过度的自噬可减轻炎症性肠病肠黏膜屏障损伤。过氧化物酶体增殖物激活受体(peroxisome proliferator activated receptor,PPAR) 是一类由配体激活的核转录因子,包含α、δ (或β)、γ亚基。目前,已明确PPARα和PPARγ参与调控脓毒症的病理进程[4-5]。PPARδ能通过调控机体炎症反应改善脓毒症模型动物生存率[6]。PPARδ可抑制自噬[7],但有关PPARδ对脓毒症肠黏膜屏障损伤的研究鲜有报道。因此,本研究拟探讨PPARδ激动剂GW501516干预对脓毒症模型小鼠肠黏膜屏障的影响及其作用机制,为脓毒症肠黏膜屏障损伤的发病机制和药物靶点开发提供实验依据。
1 材料与方法 1.1 实验动物SPF级C57BL/6J小鼠60只,雄性,8周龄,体重22~24 g,购自海南金港生物技术股份有限公司,动物生产许可证编号:SCXK (琼) 2020-0001。于23 ℃、55%相对湿度的SPF级条件下饲养,明暗光照各12 h。本研究获得广东省中医院海南医院实验动物管理与使用委员会批准(审批号IACUC-HPHCM- 2204014)。
1.2 方法 1.2.1 实验分组及脓毒症模型构建将C57BL/6J小鼠随机分为假手术组(sham组)、模型组(model组)、PPARδ激动剂GW501516组(GW501516组) 和GW501516+雷帕霉素组(GW501516+Rap组),每组15只。除sham组外,其他各组小鼠均采用盲肠结扎与穿孔术法建立脓毒症模型[8]。术后,GW501516组小鼠皮下注射GW501516 (0.5 mg/kg),GW501516+Rap组小鼠皮下注射GW501516 (0.5 mg/kg) 和雷帕霉素(5 mg/kg),1次/d;sham组和model组小鼠皮下注射等量溶媒。对各组小鼠进行大体观察。72 h后收集各组小鼠血清并于-20 ℃冻存。处死小鼠,采集近盲肠处小肠组织8 cm,取2 cm小肠组织置于4%多聚甲醛中固定,取3块1 mm×1 mm×1 mm小肠组织,置于2.5%戊二醛中固定,剩余小肠组织用PBS溶液洗净后于-80 ℃冻存。
1.2.2 HE染色将小肠组织固定、脱水、石蜡包埋后,进行组织切片,HE染色。由3位病理医师在光学显微镜下观察小肠组织病理改变,并按照CHIU’s病理学评分[9]判定小肠组织肠黏膜损伤程度。
1.2.3 ELISA检测取100 mg冻存的小肠组织研磨,离心收集上清液。取血清和小肠组织上清液按照ELISA试剂盒说明书进行操作,检测小鼠血清中D-乳酸(D-lactic acid,D-LA) 和二胺氧化酶(diamine oxidase,DAO) 水平,以及小肠组织中分泌型免疫球蛋白A (secreted immunoglobulin A,sIgA)、白细胞介素(interleukin,IL) -1β、肿瘤坏死因子α (tumor necrosis factor α,TNF-α)、IL-6水平。
1.2.4 透射电子显微镜观察自噬体小肠组织经脱水、包埋、固化,制备60 nm超薄切片,3 %醋酸铀-枸橼酸铅双染色。透射电子显微镜下观察小肠组织自噬体形成情况,计数3个视野中自噬体数量,取平均值。
1.2.5 Western blotting将剩余的小肠组织研磨匀浆后提取蛋白,测定总蛋白浓度。取40 μg蛋白样品进行电泳,转至PVDF膜,漂洗,封闭。加入PPARδ、Beclin-1、p62、LC-3和GAPDH一抗(均1∶1 000稀释),4 ℃孵育过夜,TBST充分洗涤,加入HRP标记的二抗(1∶10 000稀释),室温孵育1 h。TBST清洗后,ECL显色。以GAPDH为内参,使用ImageJ软件分析目标条带的光密度值,计算目的蛋白的相对表达量。
1.3 统计学分析采用SPSS 19.0统计软件进行分析。计量资料以x±s表示,多组间比较采用单因素方差分析,组间两两比较采用SNK-q检验。P < 0.05为差异有统计学意义。
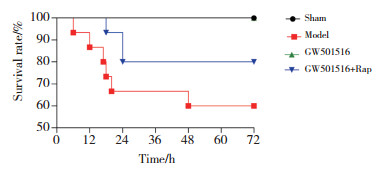
2 结果 2.1 各组小鼠大体情况sham组小鼠精神状态、饮食和排便均正常,毛发光泽。sham组、model组、GW501516组和GW501516+ Rap组小鼠72 h生存率分别为100%、60%、100%和80%。与sham组比较,model组小鼠精神萎靡,懒动,饮食和排便减少,毛发杂乱,72 h生存率显著降低(P < 0.01)。与model组比较,GW501516组小鼠饮食和排便增多,毛发和精神状态逐渐恢复正常,72 h生存率显著升高(P < 0.05)。与GW501516组比较,GW501516+Rap组小鼠精神、饮食、排便和毛发等情况均变差,72 h生存率降低,但差异无统计学意义(P > 0.05)。见图 1。
|
| 图 1 各组小鼠生存曲线 Fig.1 Survival curve of mice in each group |
2.2 GW501516对脓毒症小鼠小肠黏膜病理损伤的影响
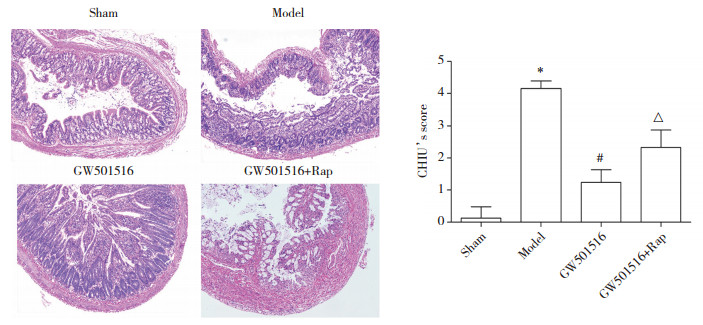
sham组小鼠小肠组织正常。与sham组比较,model组小鼠小肠绒毛肿胀、坏死,出现大面积脱落,CHIU’s病理学评分显著升高(P < 0.001)。与model组比较,GW501516组小鼠小肠绒毛顶端出现坏死、脱落,结构较为完整,CHIU’s病理学评分显著降低(P < 0.001)。与GW501516组比较,GW501516+Rap组小鼠小肠绒毛坏死和脱落程度加重,CHIU’s病理学评分显著升高(P < 0.001)。见图 2。
|
| *P < 0.001 vs. sham group; #P < 0.001 vs. model group; △P < 0.001 vs. GW501516 group. 图 2 小肠组织病理学变化HE ×200 Fig.2 Histopathological changes of intestinal tissue HE ×200 |
2.3 GW501516对脓毒症小鼠肠黏膜屏障损伤以及小肠组织炎症和免疫反应的影响
与sham组比较,model组小鼠血清中D-LA和DAO水平以及小肠组织中sIgA、IL-1β、TNF-α和IL-6水平显著升高(P < 0.001)。与model组比较,GW501516组小鼠血清中D-LA和DAO水平以及小肠组织中sIgA、IL-1β、TNF-α和IL-6水平显著降低(P < 0.001)。与GW501516组比较,GW501516+Rap组小鼠血清中D-LA和DAO水平以及小肠组织中sIgA、IL-1β、TNF-α和IL-6水平显著升高(P < 0.001)。见表 1。
| Group | n | D-LA (mg/L) | DAO (U/mL) | sIgA (μg/mL) | IL-1β (pg/mL) | TNF-α (pg/mL) | IL-6 (pg/mL) |
| Sham | 15 | 2.20±0.26 | 1.66±0.19 | 2.20±0.26 | 18.05±1.11 | 18.80±0.75 | 63.18±4.98 |
| Model | 9 | 6.88±0.471) | 5.72±0.351) | 6.88±0.471) | 47.63±1.801) | 31.34±1.001) | 196.89±8.521) |
| GW501516 | 15 | 3.47±0.432) | 2.62±0.252) | 3.47±0.432) | 24.25±1.092) | 21.05±1.062) | 86.07±5.592) |
| GW501516+Rap | 13 | 5.20±0.503) | 3.93±0.363) | 5.20±0.503) | 31.98±1.043) | 27.80±0.923) | 140.91±7.303) |
| F | 280.193 | 425.672 | 1 182.653 | 459.847 | 964.204 | 370.893 | |
| P | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | < 0.001 | |
| 1) P < 0.001 vs. sham group;2) P < 0.001 vs. model group;3) P < 0.001 vs. GW501516 group. | |||||||
2.4 GW501516对脓毒症小鼠小肠组织自噬体形成的影响
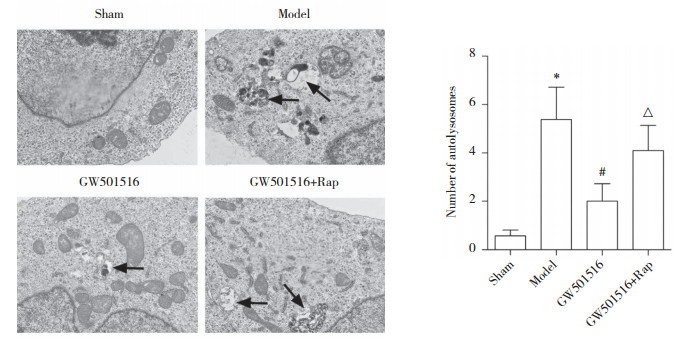
与sham组比较,model组小鼠小肠组织中自噬体数量显著升高(P < 0.001)。与model组比较,GW501516组小鼠小肠组织中自噬体数量显著降低(P < 0.001)。与GW501516组比较,GW501516+Rap组小鼠小肠组织中自噬体数量显著升高(P < 0.001)。见图 3。
|
| *P < 0.001 vs. sham group; #P < 0.001 vs. model group; △P < 0.001 vs. GW501516 group. The arrows show autolysosomes. 图 3 各组小鼠小肠组织内自噬体TEM ×8 000 Fig.3 Autophagosomes in intestinal tissue of mice in each group TEM ×8 000 |
2.5 GW501516对脓毒症小鼠小肠组织中PPARδ和自噬相关蛋白表达的影响
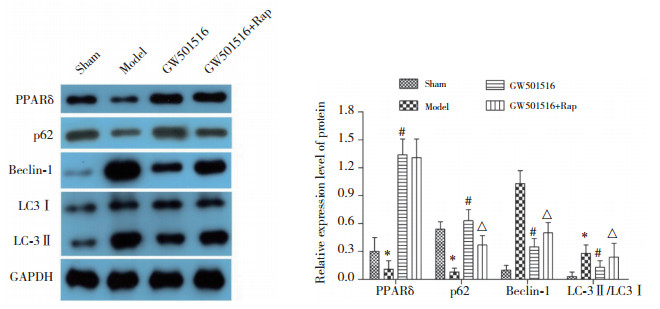
与sham组比较,model组小鼠小肠组织中PPARδ和p62蛋白表达水平显著降低,Beclin-1蛋白表达水平和LC-3Ⅱ/LC-3Ⅰ比值显著升高(P < 0.001)。与model组比较,GW501516组小鼠小肠组织中PPARδ和p62蛋白表达水平显著升高,Beclin-1蛋白表达水平和LC-3Ⅱ/LC-3Ⅰ比值显著降低(P < 0.001)。与GW501516组比较,GW501516+Rap组小鼠小肠组织中p62蛋白表达水平显著降低,Beclin-1蛋白表达水平和LC-3Ⅱ/LC-3Ⅰ比值显著升高(P < 0.001),而PPARδ蛋白表达水平无统计学差异(P > 0.05)。见图 4。
|
| *P < 0.001 vs. sham group; #P < 0.001 vs. model group; △P < 0.001 vs. GW501516 group. 图 4 各组小鼠小肠组织中PPARδ、Beclin-1、p62和LC-3蛋白表达水平 Fig.4 Expression levels of PPARδ, Beclin-1, p62, and LC-3 protein in intestinal tissue of mice in each group |
3 讨论
脓毒症发病机制复杂,涉及感染、炎症和免疫等,累及多个器官,其中肠道作为最大的免疫器官最先受损[10]。研究[11]发现,脓毒症时肠黏膜屏障损伤,通透性增加,大量释放炎性细胞因子,机体免疫力下降,启动全身炎症反应。本研究中,脓毒症模型小鼠精神萎靡,懒动,饮食和排便减少,毛发杂乱,72 h生存率显著降低,表明模型构建成功。
D-LA是细菌发酵的代谢产物,而DAO是小肠黏膜上层绒毛中的细胞内酶,小肠黏膜损伤时二者被释放入血,因此可用于反映肠黏膜通透性及肠道机械屏障的完整性和损伤程度[12]。sIgA作为肠黏膜中介导体液免疫的重要抗体,可通过免疫排斥作用吞噬肠上皮细胞黏附的病原菌[13]。另外,炎症也是导致肠黏膜屏障损伤的关键因素,TNF-α是调节免疫和炎症反应的核心指标,可促进炎性细胞因子IL-1β和IL-6产生,加重肠黏膜屏障损伤[14]。本研究结果发现,脓毒症小鼠血清中D-LA和DAO水平及小肠组织中sIgA、IL-1β、TNF-α和IL-6水平均升高,说明肠黏膜通透性增加,免疫功能被抑制,肠黏膜屏障损伤严重。
本研究还发现,脓毒症小鼠小肠组织内PPARδ呈低表达。PPAR参与脂质代谢、葡萄糖稳态、细胞增殖及分化、炎症反应和氧化应激等生理过程。文献[15]报道,PPARδ配体GW0742可通过上调PPARδ,抑制NF-κB转录活性,减少全身炎性细胞因子的释放及肺、肝脏和盲肠组织中性粒细胞的浸润,进而改善脓毒症大鼠全身炎症反应。给予PPARδ激动剂GW501516干预可显著提高脓毒症大鼠存活率,降低血清及肺组织中炎性细胞因子水平,改善脓毒症大鼠肺损伤[16]。本研究结果显示,经GW501516干预后,脓毒症模型小鼠小肠黏膜病理损伤明显减轻,小肠通透性和炎性细胞因子水平降低,免疫功能改善,脓毒症肠黏膜屏障损伤减轻,小鼠状态恢复正常,存活率升高。
自噬对脓毒症的影响是近年的研究热点,其在肠黏膜屏障中的作用不可忽视[17]。脓毒症早期可发生过度自噬,导致小肠黏膜受损[18];而抑制过度自噬可减轻肠损伤[19]。Beclin-1、p62和LC-3均为自噬的标志蛋白,其表达水平的变化可反映自噬的活性。p62是一种选择性的自噬受体,其表达水平与自噬呈负相关。本研究结果显示,脓毒症小鼠小肠组织自噬体数量增多,Beclin-1蛋白表达水平和LC-3Ⅱ/LC-3Ⅰ蛋白比值升高,p62蛋白表达水平降低,提示脓毒症引起小肠组织过度自噬。PPARδ作为新型的自噬调节剂,通过调控AMPK/mTOR通路介导自噬[20]。本研究中,经GW501516干预后,脓毒症模型小鼠小肠组织内PPARδ高表达,且明显抑制小肠组织过度自噬。雷帕霉素作为自噬激动剂,可抑制mTOR,导致自噬活性增强。本研究采用GW501516联合雷帕霉素干预,结果发现,雷帕霉素可显著抑制GW501516对脓毒症小鼠肠黏膜损伤的改善作用,且激活的PPARδ无法降低雷帕霉素引起的自噬活性。
综上所述,PPARδ激动剂GW501516可通过抑制细胞自噬改善脓毒症小鼠肠黏膜屏障损伤,但关于PPARδ介导自噬的分子机制仍需进一步研究。
| [1] |
何锐, 朱烨柯, 滕文彬, 等. 甘油可能通过水通道蛋白3减轻脓毒症小鼠肠黏膜屏障损伤[J]. 基础医学与临床, 2020, 40(5): 655-661. DOI:10.3969/j.issn.1001-6325.2020.05.013 |
| [2] |
HU QY, REN HJ, LI GW, et al. STING-mediated intestinal barrier dysfunction contributes to lethal sepsis[J]. EBioMedicine, 2019, 41: 497-508. DOI:10.1016/j.ebiom.2019.02.055 |
| [3] |
吴东升, 张彧, 陈大光, 等. 自噬在炎症性肠病肠黏膜屏障损伤中的作用[J]. 胃肠病学, 2018, 23(12): 755-758. DOI:10.3969/j.issn.1008-7125.2018.12.012 |
| [4] |
VANDEWALLE J, GARCIA B, TIMMERMANS S, et al. Hepatic peroxisome proliferator-activated receptor alpha dysfunction in porcine septic shock[J]. Cells, 2022, 11(24): 4080. DOI:10.3390/cells11244080 |
| [5] |
VON KNETHEN A, SOLLER M, BRÜNE B. Peroxisome proliferator-activated receptor gamma (PPAR gamma) and sepsis[J]. Arch Immunol Ther Exp, 2007, 55(1): 19-25. DOI:10.1007/s00005-007-0005-y |
| [6] |
BUSCH D, KAPOOR A, RADEMANN P, et al. Delayed activation of PPAR-β/δ improves long-term survival in mouse sepsis: effects on organ inflammation and coagulation[J]. Innate Immun, 2018, 24(4): 262-273. DOI:10.1177/1753425918771748 |
| [7] |
GOU Q, JIANG YD, ZHANG RY, et al. PPARδ is a regulator of autophagy by its phosphorylation[J]. Oncogene, 2020, 39(25): 4844-4853. DOI:10.1038/s41388-020-1329-x |
| [8] |
杨李旺, 杨蓉, 赵焕新, 等. 黄连解毒汤通过诱导自噬减轻脓毒症小鼠肝损伤[J]. 中国实验方剂学杂志, 2022, 28(5): 71-76. DOI:10.13422/j.cnki.syfjx.20220424 |
| [9] |
CHIU CJ, MCARDLE AH, BROWN R, et al. Intestinal mucosal lesion in low-flow states.Ⅰ. A morphological, hemodynamic, and metabolic reappraisa[J]. Arch Surg, 1970, 101(4): 478-483. DOI:10.1001/archsurg.1970.01340280030009 |
| [10] |
张俊亮, 曾其毅. 脓毒症与胃肠道功能损伤的关系及研究进展[J]. 实用医学杂志, 2016, 32(17): 2925-2927. DOI:10.3969/j.issn.1006-5725.2016.17.042 |
| [11] |
LEI XZ, TENG WB, FAN Y, et al. The protective effects of HIF-1α activation on sepsis induced intestinal mucosal barrier injury in rats model of sepsis[J]. PLoS One, 2022, 17(5): e0268445. DOI:10.1371/journal.pone.0268445 |
| [12] |
郭久冰, 王隽笙, 林锦洲, 等. 降钙素基因相关肽对脓毒症大鼠肠黏膜屏障的保护作用及机制[J]. 解放军医学杂志, 2019, 44(12): 1024-1029. DOI:10.11855/j.issn.0577-7402.2019.12.06 |
| [13] |
JIN SF, JIANG RL, LEI S, et al. Shenfu injection prolongs survival and protects the intestinal mucosa in rats with sepsis by modulating immune response[J]. Turk J Gastroenterol, 2019, 30(4): 364-371. DOI:10.5152/tjg.2019.18418 |
| [14] |
DU XJ, TIAN D, WEI J, et al. MiR-199a-5p exacerbated intestinal barrier dysfunction through inhibiting surfactant protein D and activating NF-κB pathway in sepsis[J]. Mediators Inflamm, 2020, 2020: 8275026. DOI:10.1155/2020/8275026 |
| [15] |
ZINGARELLI B, PIRAINO G, HAKE PW, et al. Peroxisome proliferator-activated receptor delta regulates inflammation via NF-kappa B signaling in polymicrobial sepsis[J]. Am J Pathol, 2010, 177(4): 1834-1847. DOI:10.2353/ajpath.2010.091010 |
| [16] |
WANG CR, ZHOU GP, ZENG Z. Effects of peroxisome proliferator-activated receptor-β/δ on sepsis induced acute lung injury[J]. Chin Med J, 2014, 127(11): 2129-2137. DOI:10.3760/cma.j.issn.0366-6999.20132972 |
| [17] |
XU SQ, LI LL, WU J, et al. Melatonin attenuates sepsis-induced small-intestine injury by upregulating SIRT3-mediated oxidative-stress inhibition, mitochondrial protection, and autophagy induction[J]. Front Immunol, 2021, 12: 625627. DOI:10.3389/fimmu.2021.625627 |
| [18] |
万晟霞, 张宏泽, 马爽, 等. 脓毒症大鼠肠上皮细胞自噬水平的研究[J]. 肠外与肠内营养, 2014, 21 (6): 368-371, 376. DOI: CNKI:SUN:CWCN.0.2014-06-018.
|
| [19] |
周彩华, 李国峰, 莫伟彬. 益生菌对力竭运动大鼠肠上皮细胞自噬的影响[J]. 现代预防医学, 2019, 46(7): 1238-1241, 1280. |
| [20] |
CHEN M, JING D, YE R, et al. PPARβ/δ accelerates bone regeneration in diabetic mellitus by enhancing AMPK/mTOR pathway-mediated autophagy[J]. Stem Cell Res Ther, 2021, 12(1): 566. DOI:10.1186/s13287-021-02628-8 |
 2025, Vol. 54
2025, Vol. 54