文章信息
- 杨彩云, 朱星瑶, 张睿祺, 刘玉华, 丁琪, 申舒琦, 林星辰, 李雁青, 邹泓
- YANG Caiyun, ZHU Xingyao, ZHANG Ruiqi, LIU Yuhua, DING Qi, SHEN Shuqi, LIN Xingchen, LI Yanqing, ZOU Hong
- 易误诊的低级别黏液表皮样癌2例报道并文献复习
- Misdiagnosed low-grade mucoepidermoid carcinoma: two case reports and literature review
- 中国医科大学学报, 2025, 54(12): 1146-1149
- Journal of China Medical University, 2025, 54(12): 1146-1149
-
文章历史
- 收稿日期:2025-01-07
- 网络出版时间:2025-12-15 11:40:22
2. 浙江大学医学院附属第二医院病理科,杭州 310009
黏液表皮样癌(mucoepidermoid carcinomas,MEC)是涎腺恶性肿瘤中最常见的类型之一[1]。典型MEC是由黏液细胞、中间型细胞、表皮样细胞构成,呈实性、囊性排列。MEC根据细胞恶性程度分为低、中、高级别,典型的中高级别MEC容易诊断,但低级别实体性、Warthin样MEC少见,而且缺乏典型的表皮样细胞及成片黏液细胞,细胞形态相对温和,恶性特征(如核分裂象、坏死)不明显,很容易误诊[2]。本研究回顾性分析浙江大学医学院附属第二医院收治的1例实体性、1例Warthin样低级别MEC患者的临床资料,总结其临床病理特征,并结合文献探讨低级别MEC的诊断要点,旨在提高临床医师对该病的认识。
1 临床资料病例1,女,28岁,2020年3月22日因“左颊黏膜肿物4月余”就诊于浙江大学医学院附属第二医院口腔科。查体结果显示左颊黏膜后缘直径2.5 cm肿物,中央增生破溃,无压痛;MRI检查结果显示左侧牙槽骨与上颌骨升支间隙内结节,倾向良性肿瘤。2020年3月30日行左颊部病损切除术+双侧拔牙术+下颌骨部分切除术。左颊病损组织全检,镜下肿瘤实性片状分布,可见纤维间质分割,边界尚清晰,局灶呈囊性变,肿瘤细胞呈透明、嗜酸。高倍镜下,肿瘤细胞大部分胞质丰富、嗜酸,可见核仁,可见鳞状分化上皮细胞,局灶见体积小、嗜碱性似中间型细胞,细胞温和,未见明确核分裂(图 1A)。本院及美国加州大学洛杉矶分校医学中心(UCLA Health)会诊,均考虑为良性唾液腺肿瘤。3年后原部位复发,2023年2月27日再次就诊于浙江大学医学院附属第二医院口腔科,复发肿物MRI检查结果显示术区结节(5 mm×9 mm),增强明显强化。2023年3月22日行左颊部病损切除术+带蒂皮瓣迁徙术+备27拔牙术。患者再次切除的左颊病损组织送病理活检。低倍镜下,肿瘤实性片状分布,边界清晰。高倍镜下,细胞形态温和,可见鳞状细胞呈巢状或片状排列,局部细胞胞质透亮,可见核仁,小灶细胞胞质少、体积小,似基底细胞,肿瘤巢团间散在黏液细胞(图 1B)。复阅初诊切片,仔细观察后可见少许散在黏液细胞及中间样细胞。会诊讨论认为初诊时肿瘤细胞异型性不明显、核分裂象罕见,且典型的诊断性结构(如显著的黏液细胞巢、角化鳞状上皮)匮乏,导致误诊为良性唾液腺肿瘤。免疫组织化学及特殊染色显示,肿瘤细胞CK7、CK(AE1/AE3)、CK5/6和P63阳性表达,散在S-100和SOX10阳性表达,CK20、Calponin、SMA和CD117均呈阴性表达,P53野生型表达,Ki-67增殖指数为3%~10%。AB/PAS染色存在散在或灶性黏液细胞。FISH检测结果显示MAML2基因断裂重排阳性(图 1C)。综合临床、形态、免疫组织化学及分子病理检测结果,确诊为实体性低级别MEC。术后6月后随访未再复发。
|
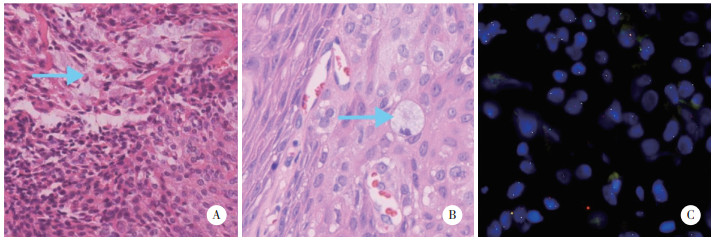
| A,初诊时细胞形态温和,复阅时在实性上皮巢团内见少许黏液细胞(箭头指示,×20);B,复发时仍以实性成分为主,见散在灶状中间型细胞与小灶黏液细胞(箭头指示,×20);C,FISH检测示MAML2基因断裂重排阳性(红绿信号分离距离超过2个信号长度). 图 1 病例1检查结果 |
病例2,女,56岁,2023年7月5日因“发现右耳垂下肿物2月余”就诊于浙江大学医学院附属第二医院口腔科。查体结果显示右耳垂下颌后区3 cm×2 cm膨隆,质软、边界不清、无压痛,基底触摸不清。外院腮腺MRI检查结果显示右侧腮腺占位性病变。于2023年7月7日全身麻醉下行右腮腺肿物切除术+腮腺部分切除+面神经解剖+生物膜置入。右腮腺肿物组织全检,低倍镜下显示,肿瘤边界尚清晰,局灶可见囊性扩张的腺体,周围有伴生发中心的慢性炎症形成明确套状结构,腺体被覆鳞状上皮为多层、嗜酸性,似Warthin瘤。高倍镜下显示,囊壁非典型Warthin瘤样的双层高柱状上皮,囊壁内可见局灶不典型上皮巢团,囊壁细胞轻度异型,囊壁及巢团间散在黏液细胞及局灶似中间细胞(图 2A)。免疫组织化学结果显示,上皮标志物CK5/6(图 2B)、CK7、CK(AE1/AE3)、CK8、CK18、P63、P40、EMA阳性表达,SMA、Calponin及S-100阴性表达,P53野生型,Ki-67增殖指数为2%,AB/PAS染色显示黏液细胞阳性(图 2C)。FISH检测结果显示MAML2基因断裂重排阳性。综合临床、形态、免疫组织化学及分子病理检测结果,诊断为Warthin样低级别MEC。术后6月后随访未复发,复查超声显示右侧腮腺术后改变,残余腺体及淋巴结未见异常。
|
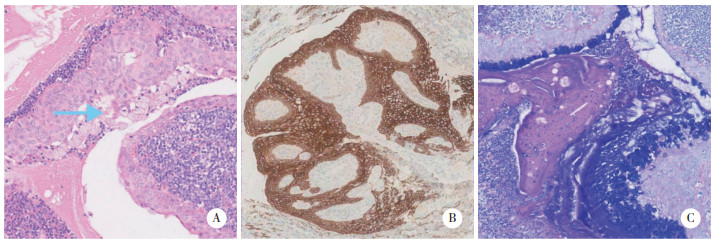
| A,低倍镜下形态似良性Warthin瘤,但高倍镜下可见囊壁内散在不典型上皮巢团,其中散在黏液细胞(箭头指示)及中间型细胞(×20);B,免疫组织化学染色显示中间型细胞CK5/6阳性,提示其鳞状分化(×10);C,AB/PAS染色证实存在散在或灶性黏液细胞(×10). 图 2 病例2检查结果 |
本研究获得浙江大学医学院附属第二医院医学伦理委员会批准,批号为(2024)伦审研第(1390)号。研究对象均同意参加本研究并签署知情同意书。
2 讨论利用PubMed、中国知网、万方数据库,以“黏液表皮样癌”“mucoepidermoid carcinoma”“Warthin-like” “WT-MEC”“MAML2 gene rearrangement”为关键词进行检索,检索时间截止至2025年1月1日。筛选出相关文献[2, 3-24] 23篇。共获得有完整病理检查的69例实体型MEC与52例Warthin样MEC患者的临床资料。
2.1 实体性与Warthin样MEC的临床病理特征和分子诊断实体性MEC分布范围较广,以肺部最常见(62.3%,43/69),其次为腮腺(13.1%,9/69)及腭部、下颌骨、乳腺等部位(24.6%,17/69)。患者中位年龄45.5(24~69)岁。组织学典型表现为表皮样细胞、黏液细胞及中间细胞构成的实性片巢结构,但黏液细胞与鳞状上皮细胞稀少,以中间型细胞为主,易误诊。本研究例1患者的误诊具有典型提示意义。患者较为年轻,肿瘤细胞呈实性片状分布,细胞温和,缺乏核分裂像,缺乏典型鳞状上皮细胞,黏液细胞稀少,因此误诊为良性唾液腺肿瘤。复发肿瘤细胞仍较温和,但因有复发病史,引起医生高度警惕,仔细观察发现存在中间型细胞和小巢黏液细胞,并与原发肿瘤切片进行比对,发现黏液细胞比例轻度升高,故进行免疫组织化学及特殊染色检查,证实伴鳞状上皮细胞与黏液分化;FISH检测结果显示MAML2基因断裂重排阳性,最终确诊为实体性低级别MEC。
Warthin样MEC集中分布于腮腺(92.3%,48/52),且女性高发(男∶女=1∶1.65)。组织学为肿瘤边界清楚,呈多房囊性,间质富含淋巴细胞及淋巴滤泡,低倍镜下形态极似良性Warthin瘤,但高倍镜下可见囊壁内散在不典型上皮巢团及散在黏液细胞与中间型细胞。因此,低倍镜下需评估其是否缺乏典型的Warthin瘤所具备的双层嗜酸性上皮结构,高倍镜下寻找是否存在非典型囊壁(局灶不典型上皮巢团、散在黏液细胞及中间细胞浸润,囊壁细胞轻度异型),如有此类结构,需进行免疫组织化学及特殊染色检查证实其鳞状上皮细胞与黏液细胞分化。另外,92.0%(46/50)患者存在MAML2基因断裂重排阳性。
2.2 实体性与Warthin样MEC的鉴别诊断实体性与Warthin样MEC需与涎腺多形性腺瘤、Warthin瘤、具有基底样形态的淋巴上皮癌、皮脂腺淋巴腺瘤及淋巴上皮囊肿进行鉴别诊断[25-26]。
2.3 治疗与预后实体性和Warthin样低级别MEC治疗以腺叶切除和颈部淋巴结清扫术为主,若存在高级别成分或阳性切缘等情况,可考虑辅助术后放疗[27]。本组2例均未进行术后放疗,1例复发。文献报道有随访记录的40例患者中[2, 3-24],中位随访28(1~166)个月;3例(7.5%)在6、12和48个月后复发,37例无复发。虽然多数患者预后良好,但仍需定期随诊。另外,由于病例较少、资料有限,生物学行为尚不能完全肯定,治疗和远期预后评估有待于进一步观察研究。
综上所述,低级别实体性与Warthin样MEC由于缺乏典型MEC形态特点,易误诊,仔细寻找黏液细胞及中间细胞,结合FISH检测其特异性MAML2基因断裂重排可提高诊断准确性。
| [1] |
王玺, 李斌斌. 唾液腺Warthin瘤样黏液表皮样癌临床病理研究进展[J]. 中华病理学杂志, 2020, 49(11): 1209-1213. DOI:10.3760/cma.j.cn112151-20200221-00119 |
| [2] |
ISHIBASHI K, ITO Y, MASAKI A, et al. Warthin-like mucoepidermoid carcinoma: a combined study of fluorescence in situ hybridization and whole-slide imaging[J]. Am J Surg Pathol, 2015, 39(11): 1479-1487. DOI:10.1097/PAS.0000000000000507 |
| [3] |
师晨阳, 李文才, 李彦鹏, 等. 原发性肺黏液表皮样癌64例临床病理分析[J]. 郑州大学学报(医学版), 2017, 52(1): 92-95. DOI:10.13705/j.issn.1671-6825.2017.01.024 |
| [4] |
杨丽娟, 曾祥菲, 于佳秀, 等. 乳腺黏液表皮样癌1例[J]. 中华病理学杂志, 2023, 52(2): 172-174. DOI:10.3760/cma.j.cn112151-20220512-00404 |
| [5] |
赵建民, 谷宛蓉, 张彦宁, 等. 原发性食管黏液表皮样癌4例临床病理观察[J]. 临床与实验病理学杂志, 2022, 38(10): 1256-1259. DOI:10.13315/j.cnki.cjcep.2022.10.023 |
| [6] |
霍双杰, 温俊秀, 宋慧茹, 等. 透明细胞变异型黏液表皮样癌2例并临床病理特征分析[J]. 诊断病理学杂志, 2023, 30(6): 557-559, 570. DOI:10.3969/j.issn.1007-8096.2023.06.010 |
| [7] |
宋汉香, 文双雪, 郭乔楠. MAML2重排阴性腮腺Warthin瘤样黏液表皮样癌1例并文献复习[J]. 临床与实验病理学杂志, 2024, 40(4): 433-435. DOI:10.13315/j.cnki.cjcep.2024.04.020 |
| [8] |
鄢丽敏, 董郁红, 张志勇, 等. Warthin瘤样黏液表皮样癌与Warthin瘤伴鳞状与黏液上皮化生的临床病理学观察[J]. 临床与实验病理学杂志, 2023, 39(10): 1259-1261. DOI:10.13315/j.cnki.cjcep.2023.10.024 |
| [9] |
赵好为, 韩琪, 孙小钦, 等. Warthin样黏液表皮样癌、Warthin瘤合并黏液表皮样癌及伴黏液化生3例[J]. 华西口腔医学杂志, 2022, 40(1): 106-110. DOI:10.7518/hxkq.2022.01.016 |
| [10] |
颜晓晓, 欧阳小娟, 齐兴峰, 等. 唾液腺Warthin瘤样黏液表皮样癌3例临床病理分析[J]. 临床与实验病理学杂志, 2022, 38(3): 318-322. DOI:10.13315/j.cnki.cjcep.2022.03.013 |
| [11] |
GARCÍA JJ, HUNT JL, WEINREB I, et al. Fluorescence in situ hybridization for detection of MAML2 rearrangements in oncocytic mucoepidermoid carcinomas: utility as a diagnostic test[J]. Hum Pathol, 2011, 42(12): 2001-2009. DOI:10.1016/j.humpath.2011.02.028 |
| [12] |
NODA Y, ISHIDA M, OKANO K, et al. Fine-needle aspiration cytology of Warthin-like mucoepidermoid carcinoma: a case report with cytological review[J]. Mol Clin Oncol, 2022, 16(1): 5. DOI:10.3892/mco.2021.2438 |
| [13] |
YANG Y, LEI Z, LANG YX, et al. Case report: the diagnostic pitfall of Warthin-like mucoepidermoid carcinoma[J]. Front Oncol, 2024, 14: 1391616. DOI:10.3389/fonc.2024.1391616 |
| [14] |
HANG JF, SHUM CH, ALI SZ, et al. Cytological features of the Warthin-like variant of salivary mucoepidermoid carcinoma[J]. Diagn Cytopathol, 2017, 45(12): 1132-1136. DOI:10.1002/dc.23785 |
| [15] |
NAKANO S, OKUMURA Y, MURASE T, et al. Salivary mucoepidermoid carcinoma: histological variants, grading systems, CRTC1/3-MAML2 fusions, and clinicopathological features[J]. Histopathology, 2022, 80(4): 729-735. DOI:10.1111/his.14586 |
| [16] |
BIEŃKOWSKI M, KUNC M, ILISZKO M, et al. MAML2 rearrangement as a useful diagnostic marker discriminating between Warthin tumour and Warthin-like mucoepidermoid carcinoma[J]. Virchows Arch, 2020, 477(3): 393-400. DOI:10.1007/s00428-020-02798-5 |
| [17] |
BISHOP JA, COWAN ML, SHUM CH, et al. MAML2 rearrangements in variant forms of mucoepidermoid carcinoma: ancillary diagnostic testing for the ciliated and warthin-like variants[J]. Am J Surg Pathol, 2018, 42(1): 130-136. DOI:10.1097/PAS.0000000000000932 |
| [18] |
ZHANG CY, GU T, HU YH, et al. Reevaluation of salivary lymphadenoma: a subgroup identified as warthin-like mucoepidermoid carcinoma following molecular investigation for MAML2 rearrangement[J]. Arch Pathol Lab Med, 2021, 145(6): 744-752. DOI:10.5858/arpa.2019-0702-OA |
| [19] |
ZHANG X, BALOCH ZW, COOPER K, et al. The significance of mucinous metaplasia in Warthin tumor: a frequent occurrence and potential pitfall[J]. Hum Pathol, 2020, 99: 13-26. DOI:10.1016/j.humpath.2020.03.008 |
| [20] |
HEATLEY N, HARRINGTON KJ, THWAY K. Warthin tumor-like mucoepidermoid carcinoma[J]. Int J Surg Pathol, 2018, 26(1): 31-33. DOI:10.1177/1066896917724889 |
| [21] |
HEGDE P, SHETTY P. Warthin-like low-grade mucoepidermoid carcinoma of the minor salivary gland: a diagnostic & therapeutic dilemma of this commingle appearance[J]. Indian J Med Res, 2020, 152(Suppl 1): S179-S180. DOI:10.4103/ijmr.IJMR_2274_19 |
| [22] |
ZHANG DW, LIAO XY, TANG YY, et al. Warthin-like mucoepidermoid carcinoma of the parotid gland: unusual morphology and diagnostic pitfalls[J]. Anticancer Res, 2019, 39(6): 3213-3217. DOI:10.21873/anticanres.13461 |
| [23] |
BASAK K, MERICOZ CA, FIRAT P. Warthin-like mucoepidermoid carcinoma: a morphological spectrum--a report of 3 cases with histological and cytological findings and review of the literature[J]. Acta Cytol, 2022, 66(3): 244-252. DOI:10.1159/000521134 |
| [24] |
LEI RX, YANG HJ. Warthin-like mucoepidermoid carcinoma of the parotid gland: a clinicopathological analysis of two cases[J]. J Int Med Res, 2022, 50(7): 3000605221101329. DOI:10.1177/03000605221101329 |
| [25] |
辛颖, 齐红, 李淑薇, 等. 涎腺恶性多形性腺瘤11例临床病理分析[J]. 临床与实验病理学杂志, 2022, 38(4): 448-451. DOI:10.13315/j.cnki.cjcep.2022.04.012 |
| [26] |
STELOW EB, WENIG BM. Update from the 4th edition of the World Health Organization classification of head and neck tumours: naso-pharynx[J]. Head Neck Pathol, 2017, 11(1): 16-22. DOI:10.1007/s12105-017-0787-0 |
| [27] |
YC G, RAMANATHAN A, GEORGE KALLARAKKAL T, et al. Oral squamous cell carcinoma and warthin tumour occurring as synchronous tumours: a report of two cases[J]. Cureus, 2022, 14(2): e22547. DOI:10.7759/cureus.22547 |
 2025, Vol. 54
2025, Vol. 54