文章信息
- 范丽, 陈莉, 杜昊
- FAN Li, CHEN Li, DU Hao
- 川陈皮素调节Shh/Gli1信号通路对子宫内膜异位症大鼠血管生成的影响
- Effect of nobiletin on angiogenesis in rats with endometriosis by regulating the Shh/Gli1 signaling pathway
- 中国医科大学学报, 2025, 54(12): 1094-1100
- Journal of China Medical University, 2025, 54(12): 1094-1100
-
文章历史
- 收稿日期:2024-10-12
- 网络出版时间:2025-12-15 13:24:21
子宫内膜异位症(endometriosis,EMT)是细胞黏附和增殖、体细胞突变、炎症、局部类固醇生成、神经发生和免疫失调等因素导致的子宫体腔以外区域存在具有活性可周期性生长的子宫内膜样组织,可能引发盆腔疼痛、不孕及终末器官损伤等[1]。川陈皮素(nobiletin,NOB)多存在于柑橘中,具有低毒性和多种药理学特性,能改善氧化应激损伤,调节机体免疫、抗炎,还具有神经保护、抗纤维化等作用[2]。既往研究[3]显示,NOB可抑制核因子κB(nuclear factor κB,NF-κB)通路激活,降低EMT小鼠炎性细胞因子水平,对炎症表现出保护潜力,还显著降低异位子宫内膜组织中增殖和血管生成相关基因的表达,激活脂质代谢相关基因,有效减小EMT小鼠病变体积,并缓解疼痛。音猬因子(sonic hedgehog,Shh)在不同器官和组织中广泛表达,能调节胚胎发育,还能激活血管生成素-1(angiopoietin-1,Ang-1)和血管内皮生长因子(vascular endothelial growth factor,VEGF)来调节成纤维细胞,促进血管生成[4]。胶质瘤相关癌基因同源物1(glioma associated oncogene homolog 1,Gli1)是Shh通路的核心介质,其在子宫内膜异位组织中阳性表达比例较高,下调其水平能减少EMT患者子宫内膜基质细胞的迁移和增殖,还可调节慢性炎症过程,可能作为阻止EMT进展的潜在靶点[5]。既往研究[6]报道,异位子宫内膜中Shh、Gli1水平上调,Shh、GLI1的异常激活能促进子宫内膜细胞在体外增殖,刺激EMT进展,可能作为预测EMT发生和病情的重要指标。然而,NOB能否通过Shh/Gli1信号通路调节EMT大鼠血管生成尚不明确。本研究探讨NOB调节Shh/Gli1信号通路对EMT大鼠血管生成的影响。
1 材料与方法 1.1 材料 1.1.1 实验动物70只6周龄,体重(200±10)g,动情期SPF级雌性健康SD大鼠购自江西中医药大学,生产许可证号:SCXK(赣)2023-0001。大鼠于动物实验室饲养,温度约25 ℃,相对湿度45%~55%,12 h/12 h光暗交替,可自由摄食饮水。本研究已获得医院动物伦理委员会审查批准(L202403-05)。
1.1.2 主要试剂与仪器NOB(CAS号478-01-3)、Shh通路激活剂嘌呤胺(PUR,CAS号483367-10-8)、Shh通路抑制剂环巴胺(CYC,CAS号4449-51-8)购自上海韵泰信息科技有限公司;谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px;货号YS07137B)试剂盒购自上海彩佑实业有限公司;HE染色试剂盒(货号XY7070)、丙二醛(malondialdehyde,MDA;货号xy-E12430)、碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF;货号xy-E12599)、白细胞介素(interleukin,IL)-6(货号XY-IL6-Ra)、VEGF(货号:XY-VEGF-Ra)、肿瘤坏死因子α(tumor necrosis factor-α,TNF-α;货号xy-E12796)、血小板衍生生长因子(platelet derived growth factor,PDGF;货号:xy-E12617)、IL-1β(货号XY-IL1β-Ra)、超氧化物歧化酶(superoxide dismutase,SOD;货号xy-E12431)试剂盒购自上海信裕生物科技有限公司。Shh、Gli1、基质金属蛋白酶2(matrix metalloproteinase-2,MMP2)、Ang-1、CD31抗体、二抗(货号ab308225、ab273018、ab92536、ab183701、ab222783、ab97080),VEGF、GAPDH(货号PA5-85171、PA1-987)购自赛默飞世尔科技(中国)有限公司。
DM2000显微镜、iMarkTM酶标仪、PowerPacT电泳仪购自上海信裕生物科技有限公司。
1.2 方法 1.2.1 EMT大鼠模型构建与分组大鼠适应性饲养7 d,随机选择10只为正常组;剩余60只大鼠造模,腹腔注射0.07 mL/kg的5%水合氯醛麻醉,消毒后切开大鼠下腹,切取右侧子宫角处子宫段(约1 cm),取内膜组织片段(5 mm×5 mm),将表面上皮对着腹壁缝合,并进行右侧子宫角断端吻合术。关腹缝合。给予青霉素避免感染。术后4周开腹观察,发现移植灶体积增大,呈透亮囊状结构,表面有血管,内部体液聚集,可见移植子宫内膜细胞生长时,即造模成功[7-8]。正常组除不进行子宫内膜与腹壁缝合外,其余操作与造模相同。
EMT大鼠随机分为EMT组、L-NOB组、H-NOB组、PUR组、CYC组,每组10只。L-NOB组、H-NOB组大鼠分别腹腔注射5、10 mg/(kg·d)NOB [3];PUR组、CYC组分别腹腔注射10 mg/(kg·d)NOB、0.69 mg/(kg·d)PUR,10 mg/(kg·d)NOB、0.69 mg/(kg·d)CYC [9];EMT组、正常组每天腹腔注射等量生理盐水,连续28 d。
1.2.2 大鼠子宫内膜组织观察和样品采集采用1.2.1中方法麻醉大鼠,处死后开腹观察病灶,并测量异位组织体积、重量和在位内膜厚度。分别抽取大鼠腹主动脉血5 mL和腹腔积液3 mL,3 000 r/min离心15 min,收集上清液待测。
1.2.3 HE染色收集正常组大鼠在位子宫内膜组织及其余组异位子宫内膜组织,分为2份,1份聚甲醛固定,制成组织切片;1份用于Western blotting实验。切片脱蜡修复,苏木素、伊红染色,封片后显微镜观察形态。
1.2.4 血清血管生成及氧化应激指标水平测定96孔板包被抗体后,按照试剂盒说明书要求加入血清及标准品,加酶标抗体孵育90 min,加显色剂避光30 min,加终止液,在特定波长用酶标仪分析血清VEGF、PDGF、bFGF、GSH-Px、SOD、MDA水平。
1.2.5 腹腔积液中IL-6、TNF-α、IL-1β水平测定采用酶联免疫吸附试验按照试剂盒说明书操作步骤检测腹腔积液中IL-6、TNF-α、IL-1β水平。
1.2.6 Western blotting检测组织中相关蛋白表达提取各组大鼠子宫内膜组织蛋白,BCA法定量。调整各组蛋白浓度,电泳转膜、封闭。加Shh(1∶1 000)、Gli1(1∶500)、VEGF(1∶500)、MMP2(1∶1 000)、Ang-1(1∶10 000)、CD31(1∶2 000)抗体4 ℃孵育,次日加二抗(1∶5 000)室温孵育1 h。加ECL液,以GAPDH(1∶1 000)为参照,分析蛋白条带灰度值计算各蛋白相对表达量。
1.3 统计学分析采用GraphPad Prism 8.0分析数据,计量资料用 x±s表示,多组间比较采用单因素方差分析,两两比较采用SNK-q检验,P < 0.05为差异有统计学意义。
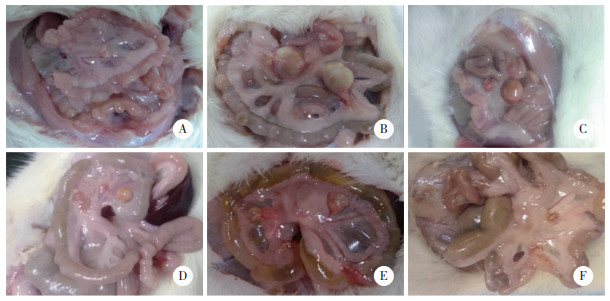
2 结果 2.1 各组大鼠异位病灶观察结果显示,正常组大鼠无异位病灶出现;EMT组、PUR组大鼠存在异位病灶,呈透亮囊状,表面有血管;L-NOB组、H-NOB组、CYC组病灶较小,表面血管生成和内部积液较少。见图 1。
|
| A, normal group; B, EMT group; C, L-NOB group; D, H-NOB group; E, PUR group; F, CYC group. 图 1 各组大鼠异位病灶观察结果 Fig.1 Observation results of ectopic lesions in each group of rats |
2.2 各组大鼠子宫内膜组织变化情况
结果显示,与正常组比较,EMT组大鼠在位内膜厚度、异位组织体积及重量增加(P < 0.05)。与EMT组比较,L-NOB组、H-NOB组在位内膜厚度、异位组织体积及重量减少(P < 0.05)。与H-NOB组比较,PUR组在位内膜厚度、异位组织体积及重量增加(P < 0.05);CYC组在位内膜厚度、异位组织体积及重量减少(P < 0.05),见表 1。
| Group | n | In situ endometrial thickness(μm) | Volume of ectopic tissues(mm3) | Weight of ectopic tissues(mg) |
| Normal | 10 | 395.26±17.65 | 0.00±0.00 | 0.00±0.00 |
| EMT | 10 | 486.28±18.731) | 93.15±8.341) | 127.52±9.061) |
| L-NOB | 10 | 457.75±17.612) | 67.21±7.792) | 87.35±8.792) |
| H-NOB | 10 | 429.18±17.542),3) | 30.52±7.812),3) | 51.28±8.652),3) |
| PUR | 10 | 470.17±18.364) | 85.39±8.264) | 114.76±8.734) |
| CYC | 10 | 400.13±17.574) | 17.68±7.934) | 28.95±8.824) |
| 1)compared with normal group,P < 0.05;2)compared with EMT group,P < 0.05;3)compared with L-NOB group,P < 0.05;4)compared with H-NOB group,P < 0.05. | ||||
2.3 各组大鼠子宫内膜组织病理学形态观察
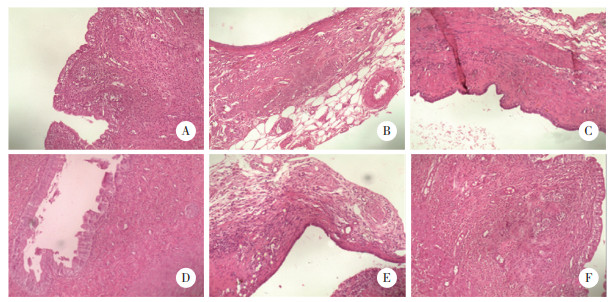
结果显示,正常组大鼠在位子宫内膜组织形态正常,细胞排列整齐均匀,界限清晰。EMT组、PUR组大鼠异位组织形态改变明显,间质细胞增多,出现大量炎症细胞浸润。L-NOB组、H-NOB组、CYC组大鼠异位病灶得到改善,炎症细胞减少。见图 2。
|
| A, normal group; B, EMT group; C, L-NOB group; D, H-NOB group; E, PUR group; F, CYC group. 图 2 各组大鼠子宫内膜组织病理学形态HE×100 Fig.2 The histological morphology of the endometrium of rats in each group HE×100 |
2.4 各组大鼠血清血管生成及氧化应激指标水平
结果显示,与正常组比较,EMT组大鼠血清VEGF、PDGF、bFGF、MDA水平升高,GSH-Px、SOD水平降低(P < 0.05)。与EMT组比较,L-NOB组、H-NOB组大鼠血清GSH-Px、SOD水平升高,VEGF、PDGF、bFGF、MDA水平降低(P < 0.05)。与H-NOB组比较,PUR组大鼠血清VEGF、PDGF、bFGF、MDA水平升高,GSH-Px、SOD水平降低(P < 0.05);CYC组大鼠血清GSH-Px、SOD水平升高,VEGF、PDGF、bFGF、MDA水平降低(P < 0.05)。见表 2。
| Group | VEGF(pg/mL) | PDGF(ng/mL) | bFGF(ng/mL) | GSH-Px(U/mg) | SOD(U/mg) | MDA(pmol/L) |
| Normal | 6.09±0.73 | 138.65±12.08 | 1.17±0.31 | 143.74±8.36 | 109.82±5.33 | 8.12±2.05 |
| EMT | 12.56±0.851) | 279.42±12.191) | 3.14±0.351) | 62.83±7.751) | 63.45±4.681) | 26.74±2.511) |
| L-NOB | 10.47±0.822) | 236.72±12.062) | 2.36±0.332) | 95.28±8.172) | 78.23±4.712) | 19.02±2.142) |
| H-NOB | 8.15±0.772),3) | 175.34±11.832),3) | 1.49±0.302),3) | 128.56±7.932),3) | 92.79±5.162),3) | 12.17±2.352),3) |
| PUR | 12.26±0.834) | 257.39±11.924) | 2.91±0.324) | 67.19±7.824) | 69.04±4.954) | 24.31±2.234) |
| CYC | 6.32±0.744) | 141.53±11.754) | 1.26±0.344) | 139.25±8.014) | 106.18±5.294) | 8.53±2.174) |
| 1)compared with normal group,P < 0.05;2)compared with EMT group,P < 0.05;3)compared with L-NOB group,P < 0.05;4)compared with H-NOB group,P < 0.05. | ||||||
2.5 各组大鼠腹腔积液中IL-6、TNF-α、IL-1β水平
结果显示,与正常组比较,EMT组大鼠腹腔积液中IL-6、TNF-α、IL-1β水平升高(P < 0.05)。与EMT组比较,L-NOB组、H-NOB组大鼠腹腔积液中IL-6、TNF-α、IL-1β水平降低(P < 0.05)。与H-NOB组比较,PUR组大鼠腹腔积液中IL-6、TNF-α、IL-1β水平升高(P < 0.05);CYC组大鼠腹腔积液中IL-6、TNF-α、IL-1β水平降低(P < 0.05),见表 3。
| Group | IL-6 | TNF-α | IL-1β |
| Normal | 141.37±15.83 | 223.65±20.15 | 93.58±9.65 |
| EMT | 353.29±16.081) | 441.34±20.031) | 177.35±10.171) |
| L-NOB | 264.17±15.862) | 352.17±19.862) | 146.92±10.032) |
| H-NOB | 176.34±16.132),3) | 275.45±20.142),3) | 108.49±10.152),3) |
| PUR | 327.56±15.924) | 335.62±19.794) | 171.26±9.734) |
| CYC | 152.03±15.894) | 242.73±19.854) | 95.03±9.814) |
| 1)compared with normal group,P < 0.05;2)compared with EMT group,P < 0.05;3)compared with L-NOB group,P < 0.05;4)compared with H-NOB group,P < 0.05. | |||
2.6 各组大鼠子宫内膜组织中各种蛋白表达
结果显示,与正常组比较,EMT组大鼠子宫内膜组织中Shh、Gli1、MMP2、VEGF、Ang-1、CD31表达增加(P < 0.05)。与EMT组比较,L-NOB组、H-NOB组大鼠子宫内膜组织中Shh、Gli1、MMP2、VEGF、Ang-1、CD31表达减少(P < 0.05)。与H-NOB组比较,PUR组大鼠子宫内膜组织中Shh、Gli1、MMP2、VEGF、Ang-1、CD31表达增加(P < 0.05);CYC组大鼠子宫内膜组织中Shh、Gli1、MMP2、VEGF、Ang-1、CD31表达减少(P < 0.05),见表 4、图 3。
| Group | Shh | Gli1 | VEGF | MMP2 | Ang-1 | CD31 |
| Normal | 0.23±0.07 | 0.31±0.10 | 0.27±0.08 | 0.45±0.09 | 0.38±0.06 | 0.40±0.10 |
| EMT | 1.56±0.101) | 2.35±0.171) | 1.15±0.101) | 1.83±0.111) | 1.20±0.081) | 1.79±0.121) |
| L-NOB | 1.04±0.082) | 1.61±0.132) | 0.82±0.092) | 1.25±0.132) | 0.93±0.072) | 1.16±0.122) |
| H-NOB | 0.51±0.072),3) | 0.83±0.122),3) | 0.49±0.092),3) | 0.67±0.102),3) | 0.56±0.072),3) | 0.54±0.082),3) |
| PUR | 1.49±0.094) | 2.07±0.154) | 1.06±0.104) | 1.74±0.114) | 1.12±0.084) | 1.63±0.114) |
| CYC | 0.37±0.074) | 0.46±0.114) | 0.33±0.084) | 0.51±0.094) | 0.44±0.064) | 0.47±0.094) |
| 1)compared with normal group,P < 0.05;2)compared with EMT group,P < 0.05;3)compared with L-NOB group,P < 0.05;4)compared with H-NOB group,P < 0.05. | ||||||

|
| 1, normal group; 2, EMT group; 3, L-NOB group; 4, H-NOB group; 5, PUR group; 6, CYC group. 图 3 各组大鼠子宫内膜组织中血管生成相关蛋白表达 Fig.3 The expression of angiogenesis-related protein in the endometrial tissues of rats in each group |
3 讨论
EMT是一种复杂的慢性疾病,在育龄妇女中的患病率很高,可能影响女性生殖功能和生活质量。EMT治疗的主要目标是减轻疼痛,改善生殖功能,并尽可能避免或延缓长期EMT相关并发症的发生。然而,目前尚未获得EMT诊断和治疗的有效策略,探究其发展的潜在机制可能对EMT的治疗十分关键[10]。
EMT的维持和发展涉及多种分子机制的复杂相互作用。血管生成是从原先存在的血管中形成新血管的一个生理过程,在卵泡成熟、功能性黄体发育和子宫内膜生长中至关重要。而血管生成失调可能有助于EMT等许多疾病的建立和发展[11]。有研究[12]指出,NOB是一种类黄酮,具有高脂质溶解和抑制氧化应激、抗炎等特性。NOB能抑制上皮间质转化和VEGF水平,以及抑制STAT3/PXN复合物的表达,从而抑制血管生成。此外,NISHIMOTO-KAKIUCHI等[13]通过研究人类EMT样本,发现EMT组织中炎性细胞因子表达上调,EMT的进展与炎症和纤维化的发展有关,而下调炎性细胞因子水平可抑制子宫内膜异位细胞的生长和侵袭,并抑制纤维化发展,从而缓解EMT。除此之外,EMT还与氧化应激产物升高、抗氧化剂减少及铁代谢失调等有关[14]。而WANG等[15]指出,NOB能改善线粒体功能和维持代谢稳态,增强抗氧化活性,清除活性氧和MDA的产生,还能抑制炎症,改善细胞自噬和凋亡,缓解衰老,可在机体内发挥多种功能。因此,推测NOB可能影响EMT的血管生成。本研究发现EMT大鼠异位组织形态明显改变,表面有血管生成,间质细胞增多,出现大量炎症细胞浸润,且大鼠在位内膜厚度,异位组织体积、重量增加;而NOB治疗后大鼠在位内膜厚度,异位组织体积、重量降低,表面血管生成和炎症细胞减少,提示NOB可能改善EMT症状。本研究通过测定大鼠腹腔积液中IL-6、TNF-α、IL-1β水平及血清MDA、GSH-Px、SOD水平来分析NOB对炎症和氧化应激的影响。结果显示,EMT大鼠IL-6、MDA、TNF-α、IL-1β水平较高,GSH-Px、SOD水平较低,而NOB治疗后上述指标均得到改善,说明NOB可能减轻了EMT的氧化应激和炎症。此外,本研究还发现,NOB治疗后EMT大鼠血清中血管生成因子VEGF、PDGF、bFGF水平及子宫内膜组织中VEGF、Ang-1、CD31、MMP2表达减少。Ang-1、CD31均能介导内皮细胞存活,促进血管生成;MMP2也与血管生成有关。这表明NOB可能减少了EMT大鼠血管生成。
本研究进一步对NOB影响EMT大鼠血管生成的作用机制进行分析,发现其可能与Shh/Gli1信号通路有关。Shh通路是多细胞胚胎发育过程中的关键调控网络,其在血管发育过程中能促进内皮细胞迁移和存活,激活血管生成细胞因子及相关通路,从而促进血管生成,对调节疾病状态十分重要[16]。Shh通路在EMT中被激活,而Shh通路阻断能减少增殖相关蛋白表达,降低子宫内膜基质细胞迁移,减少血管生成,抑制EMT的发生发展[17]。Gli1是Shh通路的下游转录因子,能在Shh激活后与微管形成复合物,激活下游基因转录,诱导M1型巨噬细胞形成,加速促炎细胞因子释放,介导炎症反应[18-19]。Gli1下调能抑制MMP2、MMP9表达,减弱子宫内膜细胞侵袭和增殖能力,减缓EMT发展[20]。有研究[21]指出,Shh、Gli1在EMT组织中表达较高,其高表达能促进EMT恶变,并引发预后不良。HEARD等[22]研究也表明,异常的Shh/Gli1信号激活有助于免疫细胞募集,导致异位组织的血管生成和黏附,从而引起子宫内膜异位病变的出现和进展。此外,还有研究[23]报道,Shh/Gli1信号通路是血管生成所必需的。在血管扩张过程中,Gli1阳性细胞数量增加,而抑制Shh/Gli1信号通路后,新生血管数量显著减少。本研究结果显示,EMT大鼠子宫内膜组织中Shh、Gli1表达增高,而NOB治疗后Shh、Gli1表达下降,提示NOB可能参与调节Shh/Gli1信号通路。进一步采用Shh通路激活剂PUR和抑制剂CYC干预,发现PUR能逆转NOB对EMT血管生成的保护作用,而CYC能进一步改善NOB对EMT血管生成的积极作用,这表明NOB可能通过调节Shh/Gli1信号通路,减轻EMT大鼠炎症、氧化应激和血管生成。
综上所述,NOB可能通过抑制Shh/Gli1信号通路抑制EMT大鼠血管生成。本研究仅是对NOB调节EMT大鼠血管生成潜在机制的初步分析,其具体作用机制还需进一步论证。
| [1] |
ALLAIRE C, BEDAIWY MA, YONG PJ. Diagnosis and management of endometriosis[J]. CMAJ, 2023, 195(10): E363-E371. DOI:10.1503/cmaj.220637 |
| [2] |
LO YH, YANG SF, CHENG CC, et al. Nobiletin alleviates ferroptosis-associated renal injury, inflammation, and fibrosis in a unilateral ureteral obstruction mouse model[J]. Biomedicines, 2022, 10(3): 595. DOI:10.3390/biomedicines10030595 |
| [3] |
WEI X, SHAO X. Nobiletin alleviates endometriosis via down-regulating NF-κB activity in endometriosis mouse model[J]. Biosci Rep, 2018, 38(3): BSR20180470. DOI:10.1042/BSR20180470 |
| [4] |
WANG JH, ZHAN HY, WANG MM, et al. Sonic hedgehog signaling promotes angiogenesis of endothelial progenitor cells to improve pressure ulcers healing by PI3K/AKT/ENOS signaling[J]. Aging, 2023, 15(19): 10540-10548. DOI:10.18632/aging.205093 |
| [5] |
NIRGIANAKIS K, SPAANDERMAN M, KRAMER BW, et al. The potential of glioma-associated oncogene homolog 1 (GLI1) as a therapeutic target in endometriosis[J]. Ann Transl Med, 2020, 8(7): 420. DOI:10.21037/atm.2020.03.36 |
| [6] |
HE YN, GUO QY, CHENG Y, et al. Abnormal activation of the sonic hedgehog signaling pathway in endometriosis and its diagnostic potency[J]. Fertil Steril, 2018, 110(1): 128-136.e2. DOI:10.1016/j.fertnstert.2018.02.138 |
| [7] |
潘敏, 王晓莉, 胡婷, 等. 原儿茶酸对子宫内膜异位症大鼠炎症反应及血管生成的作用机制研究[J]. 河北医学, 2023, 29(1): 81-85. DOI:10.3969/j.issn.1006-6233.2023.01.015 |
| [8] |
王芳, 王丽春, 商丽红, 等. 子宫内膜异位症大鼠在位及异位内膜组织中RAS与MEK的表达[J]. 海南医学, 2022, 33(4): 409-413. DOI:10.3969/j.issn.1003-6350.2022.04.001 |
| [9] |
文琳, 曾家月, 马凤雨, 等. Sonic Hedgehog信号通路在重症急性胰腺炎大鼠模型肠黏膜屏障损伤中的作用探讨[J]. 临床肝胆病杂志, 2023, 39(5): 1134-1143. DOI:10.3969/j.issn.1001-5256.2023.05.020 |
| [10] |
TASSINARI V, SMERIGLIO A, STILLITTANO V, et al. Endometriosis treatment: role of natural polyphenols as anti-inflammatory agents[J]. Nutrients, 2023, 15(13): 2967. DOI:10.3390/nu15132967 |
| [11] |
CHUNG MS, HAN SJ. Endometriosis-associated angiogenesis and anti-angiogenic therapy for endometriosis[J]. Front Glob Womens Health, 2022, 3: 856316. DOI:10.3389/fgwh.2022.856316 |
| [12] |
WU Y, CHENG CS, LI Q, et al. The application of Citrus folium in breast cancer and the mechanism of its main component nobiletin: a systematic review[J]. Evid Based Complement Alternat Med, 2021, 2021: 2847466. DOI:10.1155/2021/2847466 |
| [13] |
NISHIMOTO-KAKIUCHI A, SATO I, NAKANO K, et al. A long-acting anti-IL-8 antibody improves inflammation and fibrosis in endometriosis[J]. Sci Transl Med, 2023, 15(684): eabq5858. DOI:10.1126/scitranslmed.abq5858 |
| [14] |
CLOWER L, FLESHMAN T, GELDENHUYS WJ, et al. Targeting oxidative stress involved in endometriosis and its pain[J]. Biomolecules, 2022, 12(8): 1055. DOI:10.3390/biom12081055 |
| [15] |
WANG HH, SUN YN, QU TQ, et al. Nobiletin prevents D-galactose-induced C2C12 cell aging by improving mitochondrial function[J]. Int J Mol Sci, 2022, 23(19): 11963. DOI:10.3390/ijms231911963 |
| [16] |
MANNAN AS, DHIAMN S, GARG N, et al. Pharmacological modulation of sonic hedgehog signaling pathways in angiogenesis: a mechanistic perspective[J]. Dev Biol, 2023, 504: 58-74. DOI:10.1016/j.ydbio.2023.09.009 |
| [17] |
HE YN, WANG J, JIANG XY, et al. Effects of an inhibitor of the SHH signaling pathway on endometrial cells of patients with endometriosis[J]. BMC Mol Cell Biol, 2022, 23(1): 37. DOI:10.1186/s12860-022-00426-5 |
| [18] |
GE GR, GUO QP, ZHOU Y, et al. GLI1 facilitates collagen-induced arthritis in mice by collaborative regulation of DNA methyltransferases[J]. eLife, 2023, 12: e92142. DOI:10.7554/eLife.92142 |
| [19] |
涂仕娟, 杨红亚, 李桃, 等. 吴茱萸碱调节Shh/Gli1信号通路对膝骨关节炎大鼠软骨损伤的影响[J]. 中国医科大学学报, 2024, 53(9): 827-833. DOI:10.12007/j.issn.0258-4646.2024.09.011 |
| [20] |
LIU HW, ZHANG W, WANG LL, et al. GLI1 is increased in ovarian endometriosis and regulates migration, invasion and proliferation of human endometrial stromal cells in endometriosis[J]. Ann Transl Med, 2019, 7(22): 663. DOI:10.21037/atm.2019.10.76 |
| [21] |
赵飞, 于新平, 赵涵, 等. GLI1及Shh在卵巢型子宫内膜异位症恶变过程中的表达及其意义[J]. 中华妇产科杂志, 2022, 57(2): 125-132. DOI:10.3760/cma.j.cn112141-20211219-00736 |
| [22] |
HEARD ME, SIMMONS CD, SIMMEN FA, et al. Krüppel-like factor 9 deficiency in uterine endometrial cells promotes ectopic lesion establishment associated with activated Notch and hedgehog signaling in a mouse model of endometriosis[J]. Endocrinology, 2014, 155(4): 1532-1546. DOI:10.1210/en.2013-1947 |
| [23] |
ZHANG XL, CHEN YJ, DING PB, et al. The SHH-GLI1 pathway is required in skin expansion and angiogenesis[J]. Exp Dermatol, 2023, 32(7): 1085-1095. DOI:10.1111/exd.14815 |
 2025, Vol. 54
2025, Vol. 54