文章信息
- 廖勇杰, 杨欢, 岳嗣凤, 杨炎军, 吕淑春, 谭媛
- LIAO Yongjie, YANG Huan, YUE Sifeng, YANG Yanjun, LÜ Shuchun, TAN Yuan
- 麦冬皂苷D调控JAK2/STAT3通路对支气管肺发育不良大鼠肺组织的保护作用
- Protective effect of ophiopogonin D on lung tissue in rats with bronchopulmonary dysplasia by regulating the JAK2/STAT3 pathway
- 中国医科大学学报, 2025, 54(12): 1082-1087
- Journal of China Medical University, 2025, 54(12): 1082-1087
-
文章历史
- 收稿日期:2024-11-26
- 网络出版时间:2025-12-15 13:24:40
支气管肺发育不良(bronchopulmonary dysplasia,BPD)是早产儿常见的慢性肺部疾病,由高氧暴露等因素导致肺泡和微血管发育受损,是当前早产儿死亡和伴随长期并发症的主要原因[1]。临床治疗以营养支持、呼吸管理和抗炎等综合疗法为主,但缺乏特效药物,且氧疗本身可能加剧肺损伤[2],因此开发靶向治疗药物至关重要。麦冬皂苷D(ophiopogonin D,Oph D)是从麦冬根茎中提取的类固醇皂苷,具有显著的抗氧化、抗炎活性[3]。研究[4]表明,Oph D可通过调节丝裂原活化蛋白激酶、核因子κB及信号转导和转录激活因子3(signal transducer and activator of transcription 3,STAT3)等信号通路发挥抗炎作用。但Oph D对BPD大鼠的保护作用仍不清楚。Janus酪氨酸激酶2(Janus kinase 2,JAK2)/STAT3通路是参与氧化应激和炎症反应的关键信号通路。激活JAK磷酸化受体上的酪氨酸位点,导致受体产生STAT结合区,从而磷酸化STAT [5]。研究[6]显示,FGF21通过抑制JAK2/STAT3通路减轻脂多糖诱导的急性肺损伤。本研究通过建立BPD大鼠模型,基于JAK2/STAT3信号通路,初步探讨Oph D对BPD大鼠的保护作用。
1 材料与方法 1.1 材料 1.1.1 实验动物SPF级SD新生大鼠购自郑州大学(河南省实验动物中心),生产许可证号SCXK(豫)2022-0001。本研究获得桂林医学院附属医院动物伦理委员会批准(2021-10-0271)。
1.1.2 主要试剂Oph D购自湖北萃园生物科技有限公司;JAK2/STAT3通路激活剂Colivelin购自四川省维克奇生物科技有限公司;兔抗大鼠JAK2、STAT3抗体购自武汉菲恩生物科技有限公司;兔抗大鼠p-JAK2、p-STAT3抗体购自沈阳万类生物科技有限公司。大鼠白细胞介素(interleukin,IL)-1β、IL-6、肿瘤坏死因子α(tumor necrosis factor α,TNF-α)试剂盒购自上海信裕生物科技有限公司。大鼠过氧化氢酶(catalase,CAT)试剂盒购自上海恒斐生物科技有限公司;大鼠超氧化物歧化酶(superoxide dismutase,SOD)、丙二醛(malondialdehyde,MDA)试剂盒购自武汉佰瑞得生物技术有限公司。
1.2 建立BPD大鼠模型[7]将新生大鼠置于高氧箱中,温度25 ℃,湿度40%~70%,通高浓度O2(O2体积分数 > 90%),CO2体积分数<0.5%,每天开箱30 min,并更换饲料、水及垫料,处理7 d。随机选取1只大鼠,分离肺组织行HE染色。若肺泡数量下降,间隔厚度不均匀,则说明BPD大鼠建模成功。
1.3 实验分组取18只健康大鼠作为对照(Control)组,另将BPD大鼠模型随机分为模型(BPD)组,Oph D低、中、高剂量(Oph D-L、Oph D-M、Oph D-H)组,高剂量Oph D+JAK/STAT通路激活剂(Oph D-H+Colivelin)组,每组18只,根据参考文献[8],Oph D-L、Oph D-M、Oph D-H组分别灌胃Oph D 1.75、3.5、7.0 mg/kg,1次/d;Oph D-H+Colivelin组灌胃Oph D 7.0 mg/kg及腹腔注射Colivelin 1.0 mg/kg [9],均1次/d;Control组与BPD组灌胃等剂量生理盐水,连续给药14 d。
1.4 大鼠动脉血氧分压(arterial partial pressure of oxygen,PaO2)检测给药结束后,将大鼠麻醉取动脉血。用全自动血气分析仪检测大鼠PaO2和氧吸入浓度,分别计算呼吸指数(respiratory index,RI)、氧合指数(oxygenation index,OI)。RI为肺泡动脉血氧分压差与PaO2比值,OI为PaO2与吸入氧浓度比值。
1.5 支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)中白细胞计数、炎性细胞因子及氧化应激水平检测PaO2检测完成后,随机选取6只大鼠,切开大鼠颈胸部,将细静脉管插入气管,注入生理盐水,抽取液即为BALF,离心、分离上清并沉淀,使用全自动血液分析仪检测白细胞计数。取BALF,依据ELISA试剂盒说明书检测BALF中TNF-α、IL-6、IL-1β水平,按照说明书用试剂盒检测氧化应激指标CAT、SOD、MDA水平。
1.6 HE染色、放射状肺泡计数(radial alveolar counting,RAC)各组随机选取6只大鼠的肺组织,用甲醛固定,石蜡包埋、切片,HE染色、脱水、封片,用显微镜观察肺组织切片病理情况,检测大鼠肺组织RAC。
1.7 大鼠肺组织含水量检测每组随机选取6只大鼠,麻醉大鼠后切开胸腔,切除右肺,擦干表面,称取湿重记为W。置于80 ℃恒温干燥箱内,持续干燥48 h,称取干重记为D。以W/D比值表示肺组织含水量。
1.8 Western blotting检测蛋白表达采集BALF后,用裂解液提取大鼠肺组织蛋白并检测浓度。调整上样量,上样、电泳、转膜、封闭2 h,与p-JAK2、JAK2、p-STAT3、STAT3一抗在4℃条件下过夜孵育、洗膜,加二抗,室温孵育1 h,显色、曝光,以β-actin为内参,检测蛋白相对表达量。
1.9 统计学分析采用SPSS 25.0软件分析数据,符合正态分布的数据以x±s表示,组间比较采用单因素方差分析和SNK-q检验。P<0.05为差异有统计学意义。
2 结果 2.1 Oph D对BPD大鼠OI、RI的影响与Control组比较,BPD组大鼠OI降低,RI升高(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组OI升高,RI降低(P<0.05);与Oph D-H组比较,Oph D-H+Colivelin组OI降低,RI升高(P<0.05),见表 1。
| Group | OI(mmHg) | RI |
| Control | 431.25±44.58 | 0.22±0.02 |
| BPD | 253.69±26.151) | 0.48±0.051) |
| Oph D-L | 297.24±30.212) | 0.39±0.042) |
| Oph D-M | 346.58±35.692),3) | 0.32±0.032),3) |
| Oph D-H | 382.35±38.462),3),4) | 0.26±0.032),3),4) |
| Oph D-H+Colivelin | 328.06±33.645) | 0.35±0.045) |
| F | 56.639 | 118.481 |
| P | <0.001 | <0.001 |
| 1)P<0.05 vs. Control group;2)P<0.05 vs. BPD group;3)P<0.05 vs. Oph D-L group;4)P<0.05 vs. Oph D-M group;5)P<0.05 vs. Oph D-H group. | ||
2.2 Oph D对BPD大鼠白细胞计数的影响
与Control组[(25.83±2.63)×107/L]比较,BPD组大鼠白细胞计数[(145.78±15.69)×107/L]增加(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组白细胞计数[(114.21±12.47)×107/L、(79.35±8.03)×107/L、(60.78±6.11)×107/L]减少(P<0.05);与Oph D-H组相比,Oph D-H+Colivelin组白细胞计数[(92.36±9.42)×107/L]增加(P<0.05)。
2.3 Oph D对BPD大鼠BALF中炎性细胞因子水平的影响与Control组比较,BPD组IL-1β、TNF-α、IL-6水平升高(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组IL-1β、TNF-α、IL-6水平降低(P<0.05);与Oph D-H组比较,Oph D-H+Colivelin组IL-1β、TNF-α、IL-6水平升高(P<0.05),见表 2。
| Group | IL-1β | IL-6 | TNF-α |
| Control | 16.37±1.71 | 16.12±1.96 | 16.02±1.85 |
| BPD | 50.68±5.361) | 62.56±6.551) | 55.73±5.671) |
| Oph D-L | 42.56±4.482) | 51.67±5.482) | 46.97±4.782) |
| Oph D-M | 34.95±3.692),3) | 42.34±4.362),3) | 35.52±3.822),3) |
| Oph D-H | 25.89±2.752),3),4) | 30.07±3.242),3),4) | 27.16±2.952),3),4) |
| Oph D-H+Colivelin | 38.62±3.915) | 47.52±4.915) | 40.02±4.135) |
| F | 60.908 | 75.010 | 72.783 |
| P | <0.001 | <0.001 | <0.001 |
| 1)P<0.05 vs. Control group;2)P<0.05 vs. BPD group;3)P<0.05 vs. Oph D-L group;4)P<0.05 vs. Oph D-M group;5)P<0.05 vs. Oph D-H group. | |||
2.4 Oph D对BPD大鼠BALF中氧化应激水平的影响
与Control组比较,BPD组SOD、CAT水平降低,MDA水平升高(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组SOD、CAT水平升高,MDA水平降低(P<0.05);与Oph D-H组比较,Oph D-H+Colivelin组SOD、CAT水平降低,MDA水平升高(P<0.05),见表 3。
| Group | SOD(pg/mL) | CAT(U/mL) | MDA(ng/mL) |
| Control | 82.54±8.36 | 295.36±32.41 | 8.05±0.82 |
| BPD | 33.47±3.641) | 95.78±10.321) | 51.35±5.261) |
| Oph D-L | 43.58±4.792) | 148.75±16.782) | 40.68±4.182) |
| Oph D-M | 59.42±6.252),3) | 193.64±22.592),3) | 32.47±3.522),3) |
| Oph D-H | 70.15±7.662),3),4) | 253.22±28.442),3),4) | 23.54±2.492),3),4) |
| Oph D-H+Colivelin | 51.23±5.535) | 172.95±19.025) | 34.21±3.735) |
| F | 49.075 | 59.817 | 101.089 |
| P | <0.001 | <0.001 | <0.001 |
| 1)P<0.05 vs. Control group;2)P<0.05 vs. BPD group;3)P<0.05 vs. Oph D-L group;4)P<0.05 vs. Oph D-M group;5)P<0.05 vs. Oph D-H group. | |||
2.5 Oph D对BPD大鼠肺组织病理形态的影响
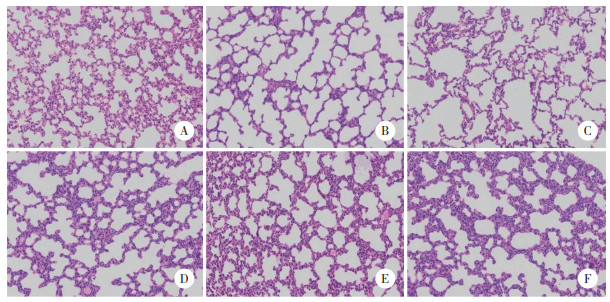
Control组大鼠肺泡和肺组织结构形态正常,未见明显损伤,BPD组大鼠肺泡变大,肺泡数量较少,出现炎症细胞浸润,肺组织损伤明显,RAC降低(4.55±0.47 vs.11.56±1.22,P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组上述肺组织损伤明显改善,RAC(5.88±0.61、7.25±0.73、8.69±0.85)升高(P<0.05);与Oph D-H组比较,Oph D-H+Colivelin组肺组织损伤加重,RAC(6.02±0.63)降低(P<0.05),见图 1。
|
| A, Control group; B, BPD group; C, Oph D-L group; D, Oph D-M group; E, Oph D-H group; F, Oph D-H + Colivelin group. 图 1 各组大鼠肺组织病理形态观察 HE染色×100 Fig.1 Morphological observation of lung tissue of rats in each group HE staining×100 |
2.6 Oph D对BPD大鼠W/D值的影响
与Control组(4.55±0.13)比较,BPD组W/D值(6.37±0.34)升高(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组W/D值(5.58±0.25、5.13±0.21、4.69±0.16)降低(P<0.05);与Oph D-H组相比,Oph D-H+Colivelin组W/D值(5.26±0.24)升高(P<0.05)。
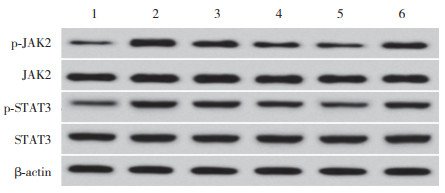
2.7 Oph D对JAK2/STAT3通路的影响与Control组比较,BPD组p-JAK2/JAK2、p-STAT3/STAT3表达上调(P<0.05);与BPD组比较,Oph D-L、Oph D-M、Oph D-H组p-JAK2/JAK2、p-STAT3/STAT3表达下调(P<0.05);与Oph D-H组相比,Oph D-H+Colivelin组p-JAK2/JAK2、p-STAT3/STAT3表达上调(P<0.05),见图 2、表 4。
|
| 1, Control group; 2, BPD group; 3, Oph D-L group; 4, Oph D-M group; 5, Oph D-H group; 6, Oph D-H+Colivelin group. 图 2 Western blotting检测JAK2/STAT3信号通路蛋白表达 Fig.2 Related-protein expression in the JAK2/STAT3 signaling pathway by Western blotting |
| Group | p-JAK2/JAK2 | p-STAT3/STAT3 |
| Control | 0.25±0.03 | 0.31±0.03 |
| BPD | 0.91±0.071) | 0.87±0.091) |
| Oph D-L | 0.76±0.082) | 0.75±0.082) |
| Oph D-M | 0.57±0.062),3) | 0.52±0.052),3) |
| Oph D-H | 0.36±0.042),3),4) | 0.37±0.042),3),4) |
| Oph D-H+Colivelin | 0.65±0.075) | 0.60±0.065) |
| F | 98.002 | 72.748 |
| P | <0.001 | <0.001 |
| 1)P<0.05 vs. Control group;2)P<0.05 vs. BPD group;3)P<0.05 vs. Oph D-L group;4)P<0.05 vs. Oph D-M group;5)P<0.05 vs. Oph D-H group. | ||
3 讨论
BPD以肺泡发育受阻为主要特征,约45%的妊娠<29周的早产儿会罹患此病,其发生与产前感染、机械通气、氧气中毒、动脉导管未闭及产后感染等多种因素相关[10]。高氧诱导的急性肺损伤在BPD发病机制中尤为关键[11],目前缺乏特效治疗BPD的药物。
麦冬作为传统中草药,其活性成分Oph D具有抗氧化、抗炎等多种药理活性[3]。研究[12]表明,Oph D通过激活AMPK和抑制NF-κB信号通路,减轻PM2.5诱导的气道炎症。本研究中BPD大鼠肺组织经HE染色后肺泡数量明显减少,炎症细胞浸润,可见明显肺组织损伤,说明BPD大鼠模型构建成功。经不同剂量Oph D处理后,BPD大鼠BALF中白细胞计数、IL-1β、IL-6、TNF-α、MDA水平降低,SOD、CAT水平升高,说明Oph D能够缓解BPD大鼠肺组织炎症和氧化应激反应。同时,OI升高,RI降低,W/D值降低,说明Oph D能改善肺功能并减轻肺水肿,且高剂量的Oph D效果更显著。还有研究[13]发现,Oph D能抑制肺组织上皮-间质转化和细胞外基质沉积,促进肺成纤维细胞凋亡,并通过阻断AKT/GSK3β通路缓解肺部炎症和肺纤维化,进一步证实其对肺组织的保护潜力。
JAK2/STAT3信号通路在氧化应激和炎症反应中被激活,参与肺损伤过程[5]。研究[14]表明,吡非尼酮通过抑制JAK2/STAT3降低矽肺病大鼠肺纤维化。还有研究[15]发现,达芙奈汀可能通过抑制JAK2/STAT3信号的激活降低了血清和肺组织中IL-6、TNF-α浓度,进而减少SAP相关的肺组织损伤。本研究结果显示,BPD大鼠经低、中、高剂量的Oph D干预后,肺组织中p-JAK2/JAK2、p-STAT3/STAT3表达水平下降,说明Oph D可能通过抑制JAK2/STAT3通路激活发挥肺组织保护作用。为了验证这一结论,本研究在Oph D处理BPD大鼠的基础上,用JAK/STAT通路激活剂Colivelin进一步处理BPD大鼠,发现Oph D的保护作用被Colivelin部分逆转,说明Oph D可通过抑制JAK2/STAT3信号通路发挥BPD大鼠肺组织的保护作用,从而缓解炎症和氧化应激,减轻肺水肿,改善肺功能。
综上所述,Oph D能够改善BPD大鼠肺功能和肺水肿,降低炎性细胞因子水平,缓解炎症和氧化应激,发挥保护肺组织的作用,其作用机制可能是通过抑制JAK2/STAT3通路实现的。然而,Oph D的生物活性较多且复杂,需进一步研究JAK2/STAT3通路上下游因子的变化,从而明确Oph D对肺组织发现保护作用的具体机制。
| [1] |
邵树铭, 张懿敏, 张晓蕊. 中国新生儿支气管肺发育不良研究现状的可视化研究[J]. 中国医科大学学报, 2021, 50(8): 719-722. DOI:10.12007/j.issn.0258-4646.2021.08.010 |
| [2] |
SHEN X, YANG ZC, WANG Q, et al. Lactobacillus plantarum L168 improves hyperoxia-induced pulmonary inflammation and hypoalveolarization in a rat model of bronchopulmonary dysplasia[J]. NPJ Biofilms Microbiomes, 2024, 10(1): 32. DOI:10.1038/s41522-024-00504-w |
| [3] |
ZHANG HY, KANG XZ, RUAN J, et al. Ophiopogonin D improves oxidative stress and mitochondrial dysfunction in pancreatic β cells induced by hydrogen peroxide through Keap1/Nrf2/ARE pathway in diabetes mellitus[J]. Chin J Physiol, 2023, 66(6): 494-502. DOI:10.4103/cjop.CJOP-D-23-00069 |
| [4] |
SHEN X, RUAN YQ, ZHAO YH, et al. Ophiopogonin D alleviates acute lung injury by regulating inflammation via the STAT3/A20/ASK1 axis[J]. Phytomedicine, 2024, 130: 155482. DOI:10.1016/j.phymed.2024.155482 |
| [5] |
FAN SL, HE J, YANG YL, et al. Intermedin reduces oxidative stress and apoptosis in ventilator-induced lung injury via JAK2/STAT3[J]. Front Pharmacol, 2022, 12: 817874. DOI:10.3389/fphar.2021.817874 |
| [6] |
CAI MS, YE HH, ZHU XY, et al. Fibroblast growth factor 21 relieves lipopolysaccharide-induced acute lung injury by suppressing JAK2/STAT3 signaling pathway[J]. Inflammation, 2024, 47(1): 209-226. DOI:10.1007/s10753-023-01905-3 |
| [7] |
吴朋, 李银华, 谭心海, 等. 桔梗总皂苷对支气管肺发育不良新生大鼠肺损伤的作用及机制研究[J]. 中国现代医学杂志, 2022, 32(5): 52-57. DOI:10.3969/j.issn.1005-8982.2022.05.009 |
| [8] |
陈婷, 包晟川, 李京涛, 等. 基于蛋白组学探讨麦冬皂苷D改善肺纤维化的作用机制[J]. 中国新药杂志, 2024, 33(4): 372-382. DOI:10.3969/j.issn.1003-3734.2024.04.008 |
| [9] |
李建军, 吴素方, 白丰玺. 基于Janus激酶/信号转导和转录激活因子信号通路的乙胺丁醇片对肺结核大鼠模型的作用机制[J]. 中国医学科学院学报, 2022, 44(4): 555-562. DOI:10.3881/j.issn.1000-503X.14923 |
| [10] |
ZHOU YH, LIU YW, XU G, et al. Human breast milk-derived exosomes through inhibiting ATⅡ cell apoptosis to prevent bron-chopulmonary dysplasia in rat lung[J]. J Cell Mol Med, 2022, 26(15): 4169-4182. DOI:10.1111/jcmm.17334 |
| [11] |
月小飞, 梅花, 宋丹, 等. 高氧诱导支气管肺发育不良模型新生大鼠肺组织中miR-21-5p的表达[J]. 中国医科大学学报, 2020, 49(7): 624-627, 635. DOI:10.12007/j.issn.0258-4646.2020.07.011 |
| [12] |
WANG Y, LI D, SONG L, et al. Ophiopogonin D attenuates PM2.5-induced inflammation via suppressing the AMPK/NF-κB pathway in mouse pulmonary epithelial cells[J]. Exp Ther Med, 2020, 20(6): 139. DOI:10.3892/etm.2020.9268 |
| [13] |
BAO SC, CHEN T, CHEN J, et al. Multi-omics analysis reveals the mechanism of action of ophiopogonin D against pulmonary fibrosis[J]. Phytomedicine, 2023, 121: 155078. DOI:10.1016/j.phymed.2023.155078 |
| [14] |
TANG Q, XING C, LI M, et al. Pirfenidone ameliorates pulmonary inflammation and fibrosis in a rat silicosis model by inhibiting macrophage polarization and JAK2/STAT3 signaling pathways[J]. Ecotoxicol Environ Saf, 2022, 244: 114066. DOI:10.1016/j.ecoenv.2022.114066 |
| [15] |
YANG SJ, SONG YD, WANG QF, et al. Daphnetin ameliorates acute lung injury in mice with severe acute pancreatitis by inhibiting the JAK2-STAT3 pathway[J]. Sci Rep, 2021, 11(1): 11491. DOI:10.1038/s41598-021-91008-6 |
 2025, Vol. 54
2025, Vol. 54