文章信息
- 李坤航, 张俊悦, 张旭东, 包义君
- LI Kunhang, ZHANG Junyue, ZHANG Xudong, BAO Yijun
- 小鼠创伤性脑损伤后损伤周边区脑血管形态变化及其对脑血流恢复的影响
- Morphological changes of blood vessel in the perilesion area and their effects on cerebral blood flow recovery after traumatic brain injury in mice
- 中国医科大学学报, 2025, 54(12): 1076-1081
- Journal of China Medical University, 2025, 54(12): 1076-1081
-
文章历史
- 收稿日期:2025-09-08
- 网络出版时间:2025-12-15 11:44:54
创伤性脑损伤(traumatic brain injury,TBI)在全球范围内已成为致死和致残的重要因素[1],在中国TBI死亡率达13/10万,显著增加慢性创伤性脑病、痴呆和抑郁风险,带来沉重的社会负担[2]。脑血管损伤是TBI的关键病理环节,急性期表现为脑结构破坏、网络稀疏和功能障碍,引发脑出血、脑梗死和脑水肿,并导致继发性损伤[3]。近期的研究[4]发现,亚急性和恢复期脑损伤周边区血管重塑仍不明确,且损伤后早期脑低灌注与预后不良密切相关。目前,仅有较少研究[5]探讨了血管形态与脑血流恢复的相关性。本研究动态监测小鼠TBI后损伤周边区脑血管的形态变化,并分析其与脑血流恢复的相关性,为通过早期调控脑血流以优化治疗效果提供理论依据。
1 材料与方法 1.1 实验动物和分组72只12周龄的成年雄性C57BL/6野生型小鼠,购自辽宁长生生物科技有限公司,体重为25~30 g。所有小鼠均饲养于12 h/12 h的光/暗环境中。将小鼠随机分为假手术组和TBI组,每组36只。在实验过程中所有小鼠存活,实验结束后对小鼠实施安乐死。本研究的动物实验方案已通过中国医科大学实验动物福利与伦理委员会的审核批准(KT2021252),全部操作遵循动物福利和伦理相关规范。
1.2 TBI模型的建立采用美国Hatteras公司的PCI3000型精确皮层撞击仪构建TBI小鼠模型[6]。该仪器具备高精度定位优势,可通过灵活调节撞击过程中的关键参数(包括撞击速度、作用深度和停留时长),精准调控脑损伤严重程度,进而构建不同损伤程度的动物模型。轻度TBI小鼠表现为神经功能轻度减退,脑组织无明显结构性改变;中度TBI小鼠可见神经功能显著下降,损伤范围局限于皮层,未累及海马;重度TBI小鼠神经功能明显受损,病变已波及海马或更深层脑组织[7]。
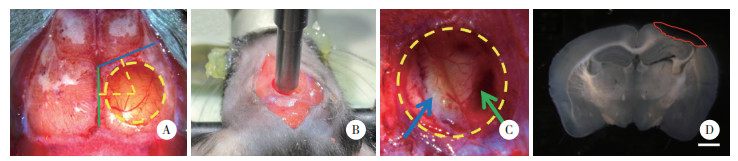
采用异氟烷吸入麻醉,麻醉后将小鼠头部固定于立体定位装置上,采用恒温加热垫维持小鼠体温处于稳定状态,避免体温波动对实验结果产生干扰。对手术操作区域进行常规消毒处理后,在小鼠头皮正中线处作一长度约10 mm的切口,随后按照组织层次依次分离皮肤和骨膜,充分暴露颅骨表面结构。在右侧顶骨区域,以矢状缝右侧、冠状缝后方5 mm的交点作为中心位置,使用颅钻缓慢钻出一个直径为4 mm的圆形骨窗,骨窗制备完成后,可清晰观察到下方硬脑膜(图 1A)。撞击操作选用直径3 mm的圆形钢制平头撞击部件,待该撞击器下端平稳接触硬脑膜表面后(图 1B),以1.5 m/s的速度垂直作用于脑皮层组织,撞击深度控制在1.0 mm,且撞击后保持该深度状态50 ms。撞击操作结束后,对小鼠头皮切口进行常规缝合,随后将小鼠置于适宜环境中,等待自然苏醒。假手术组小鼠接受与TBI组小鼠完全一致的处理,包括麻醉、头部固定、体温维持、术区消毒、头皮切口制作、骨膜剥离和骨窗制备等,但未进行皮层撞击。
|
| A, mouse brain structure (yellow dotted circle indicates craniotomy and injury site, blue solid line represents lambdoid suture, and green solid line shows sagittal suture); B, procedure of controlled cortical impact; C, TBI mice exhibiting contusion (blue arrow) and hemorrhage (green arrow); D, coronal section indicating a specific injury in the cerebral cortex, sparing the hippocampus. Scale bar = 0.5 mm. 图 1 小鼠中度TBI模型的构建 Fig.1 Establishment of a mice model of moderate TBI |
1.3 免疫荧光染色
用1%戊巴比妥钠麻醉小鼠后,经左心室进行心脏灌流。先用预冷的PBS冲洗至肝脏变白,随后换用4%多聚甲醛溶液进行灌注固定。完整取出脑组织,浸泡在4%多聚甲醛溶液中,放入4 ℃层析冷柜内过夜固定。
将固定的脑组织样本采用Leica VT1200S型振动切片机(德国Leica公司)进行连续冠状切片,切片厚度为100 μm。切片首先用含10%牛血清白蛋白和0.1% Triton X-100的PBS封闭1 h,随后在4 ℃下与CD31抗体(美国R&D Systems公司,稀释比例1∶200)孵育过夜。次日,样本与二抗(美国ThermoFisher Scientific公司,稀释比例1∶400)孵育3 h,接着在暗室环境中用DAPI(美国ThermoFisher Scientific公司,稀释比例1∶1 000)染色5 min。各步骤间均使用0.1 mol/L PBS洗涤5次,每次洗涤持续5 min。采用共聚焦显微镜(LSM 880,德国ZEISS公司)成像和观察。
1.4 激光散斑成像采用SIM BFI-HR型激光散斑血流成像系统(武汉迅微光电科技有限公司)定量测定小鼠脑血流量[6]。为动态观察TBI后脑血流变化,分别于TBI前及TBI后6 h、1 d、3 d、7 d和14 d进行成像。小鼠在恒温麻醉下维持生理状态稳定,剪开原头皮切口,暴露颅骨,清洁表面,去除残留组织和分泌物。成像过程中持续使用无菌棉保持颅骨表面清洁和干燥,避免影响成像质量。成像时,先在可见光模式下调节CCD焦距以获取清晰脑结构图像,随后切换至785 nm激光模式采集血流信号。原始数据经系统配套LSCI软件转换为可视化脑血流图像。图像以定时模式采集,间隔1 s捕获1帧,每只小鼠共采集20幅图像。采用LSCI软件进行数据分析,于小鼠大脑双侧对称位置分别选取面积为50 mm2的圆形感兴趣区,自动计算各区域平均血流指数(blood flow index,BFI)。为评估损伤区血流变化,计算相对脑血流变化值,相对脑血流变化=(损伤侧平均BFI-损伤对侧平均BFI)/损伤对侧平均BFI。
1.5 统计学分析采用GraphPad Prism 7.0软件进行数据分析。采用SPSS 21.0进行Spearman秩相关分析。计量资料用x±s表示,2组比较采用完全随机设计t检验。P<0.05为差异有统计学意义。
2 结果 2.1 构建中度TBI小鼠模型在TBI模型建立后(图 1A、1B),小鼠脑组织呈现出挫裂伤和出血等典型病理改变(图 1C)。对损伤后脑组织进行冠状切片,结果证实损伤区域仅局限于大脑皮层,未累及海马(图 1D),提示该模型符合中度TBI的制备标准。
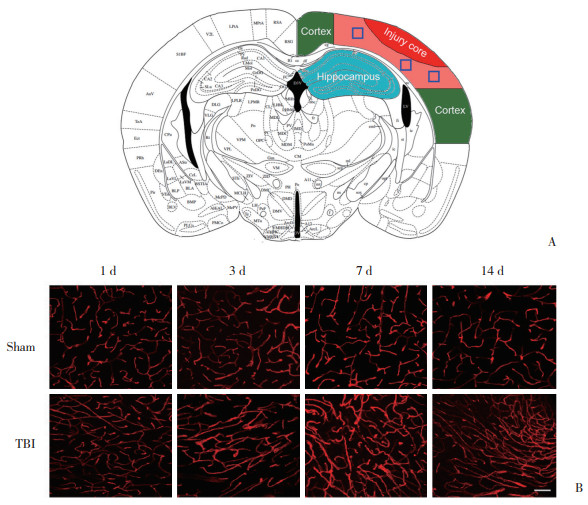
2.2 TBI后损伤周边区脑血管形态的动态变化为了定量分析TBI后损伤周边区脑血管形态的动态变化,采用免疫荧光染色结合共聚焦激光扫描成像系统,对损伤周边区脑血管微观结构实现高分辨率、可视化呈现。在损伤周边皮层区域随机划定多个独立的观察视野(图 2A),采用AngioTool图像分析软件对选定区域内的脑血管形态学指标进行定量检测和统计学分析。结果显示,各时间点TBI组损伤周边区的脑血管密度均较假手术组显著增加(P<0.05);TBI组中,TBI后3 d血管密度的增加虽较TBI后1 d有所回落,但仍较同时点的假手术组增加18.4%;TBI后14 d,与假手术组比较,TBI组血管密度增加最为显著,增加72.7%,提示该时间点损伤周边区脑血管新生和重塑进程最活跃。与血管密度的变化规律一致,各时间点TBI组的血管总长度均较假手术组明显增加(P<0.05);TBI组的血管总长度在TBI后14 d达到峰值,较同时点的假手术组增加76.9%。血管分支指数的变化呈现不同特征,在TBI后1 d和14 d,TBI组血管分支指数较假手术组均明显增加(P<0.05),尤其在TBI后14 d,较假手术组增加43.8%;而在TBI后3 d和7 d,2组比较无统计学差异(P > 0.05)。TBI后1 d,TBI组与假手术组比较,血管直径减小(P<0.05),较假手术组减少10.1%;TBI后3 d,TBI组与假手术组比较,血管直径增加(P<0.05),较假手术组增加17.6%;尽管TBI后7 d和14 d,TBI组血管直径大于假手术组,但差异无统计学意义(P > 0.05)。见图 2B、表 1。
|
| A, the area that underwent vascular analysis is delineated on the coronal brain section (blue square box); B, representative confocal micrographs of cortical cerebral microvessels at different time points after TBI. Scale bar = 0.5 mm. 图 2 TBI后脑血管修复过程中各时点的血管形态变化 Fig.2 Changes of vascular morphology at different time points during the repair phase after TBI |
| Item | n | 1 d | 3 d | 7 d | 14 d |
| Vascular density | |||||
| Sham group | 3 | 15.06±1.37 | 14.94±1.32 | 13.67±1.54 | 14.77±0.52 |
| TBI group | 3 | 24.45±1.01 | 17.69±0.51 | 23.20±1.46 | 25.51±1.41 |
| P | 0.001 | 0.028 | 0.001 | < 0.001 | |
| Total vascular length(mm) | |||||
| Sham group | 3 | 6.27±0.59 | 5.41±0.54 | 6.07±0.55 | 6.05±0.42 |
| TBI group | 3 | 9.52±1.05 | 7.08±0.51 | 9.39±0.81 | 10.70±0.92 |
| P | 0.009 | 0.018 | 0.004 | 0.001 | |
| Vascular diameter(×10-3 mm) | |||||
| Sham group | 3 | 4.58±0.12 | 4.38±0.17 | 4.37±0.07 | 4.26±0.06 |
| TBI group | 3 | 4.12±0.16 | 5.15±0.05 | 4.63±0.16 | 4.57±0.26 |
| P | 0.016 | 0.002 | 0.057 | 0.109 | |
| Vascular branching index | |||||
| Sham group | 3 | 3 591.42±253.03 | 3 608.79±449.94 | 3 657.15±263.32 | 3 776.62±376.72 |
| TBI group | 3 | 4 827.43±402.55 | 3 386.62±248.69 | 4 345.29±365.22 | 5 429.13±487.92 |
| P | 0.011 | 0.496 | 0.057 | 0.009 |
2.3 TBI后脑血流的动态变化
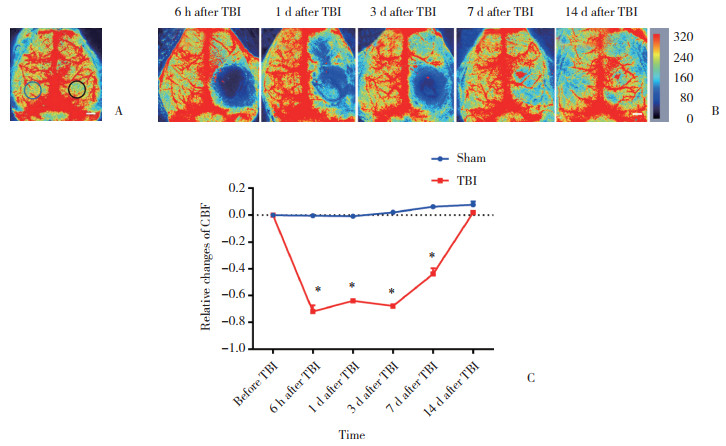
为量化小鼠TBI后局部脑血流的动态变化特征,采用激光散斑成像技术对损伤区的脑血流状态进行在体监测。于小鼠脑部左右半球对称的固定解剖位置分别设定感兴趣区,完成脑血流信号的数据采集和记录(图 3A)。结果显示,在TBI后的急性期阶段,损伤侧脑组织的血流灌注水平显著降低。在损伤后的6 h、1 d和3 d这3个时间点,损伤侧脑组织的脑血流较对侧脑血流分别减少71.9%、63.9%和67.8%。自TBI后3 d起,损伤侧脑组织的脑血流开始出现恢复迹象,到TBI后7 d时,脑血流虽有一定程度的增加,但仍较对侧脑血流减少43.9%;直至TBI后14 d,损伤侧脑组织的脑血流才基本恢复至对侧脑血流状态。见图 3B、3C。
|
| A, representative image of cerebral blood flow (CBF) detection. The regions of interest are marked with circles. The black circle denotes the site of injury, whereas the blue circle indicates the contralateral region. B, five standard laser speckle images of cortical CBF after TBI. Colored bars indicate arbitrary linear perfusion units. C, cortical CBF alterations after TBI were statistically analyzed. The results are presented as the ratio of the difference in CBF between the ipsilateral and contralateral sides to the contralateral CBF. n = 6 for each time point. Scale bar = 1 mm. * P < 0.001 vs. sham group. 图 3 TBI后脑血流的动态演变 Fig.3 Dynamic evolution of cerebral blood flow after TBI |
2.4 TBI后脑血管形态变化与脑血流动态恢复的相关性分析
为了进一步探讨小鼠TBI后损伤周边区脑血管形态与脑血流恢复间的相关性,采用Spearman秩相关分析对血管密度、血管总长度、血管直径和血管分支指数与脑血流恢复程度进行统计分析。结果表明,血管密度和血管总长度均与脑血流恢复呈显著正相关(均r = 1,P<0.01);血管分支指数与脑血流恢复虽呈正相关趋势,但无统计学意义(r = 0.8,P > 0.05);血管直径与脑血流恢复间未见相关性(r = -0.2,P > 0.05)。
3 讨论脑损伤发生后,脑血管系统的形态构造和功能状态会持续出现异常改变,这种形态层面的变化和脑功能的受损程度、后续恢复进程紧密关联[8]。在TBI早期,脑血管正常形态的破坏可能会引发脑组织血液灌注情况的改变[9],进而影响脑内正常的生理代谢活动。因此,深入、全面地认识TBI后脑血管形态的具体变化特征,对于揭示脑血流灌注异常现象的产生原因以及脑血流恢复的内在机制具有至关重要的意义。HAN等[9]采用体双光子成像技术开展研究,发现小鼠发生轻度脑损伤后的30 min~6 h内,脑动脉和毛细血管的血管直径会明显缩小,而在损伤发生1 d后,血管直径可恢复至正常水平。另有一项动物模型研究[10]表明,局灶性脑外伤会导致损伤周边区血管长度缩短、血管分叉数量减少,使该区域血管网络的复杂程度降低。既往多数研究关注损伤核心区的脑血管形态改变,针对损伤周边区血管形态的研究较少,且现有的少量相关研究仅围绕个别孤立的时间点展开分析,难以完整呈现该区域血管形态的动态变化过程。
与之前的研究不同,本研究着重对TBI发生后各阶段损伤周边区的脑血管形态学特征进行系统分析,并深入探究这些形态变化与脑血流恢复间的关联。本研究结果显示,在TBI早期阶段,尽管损伤周边区血管密度和血管总长度增长幅度存在短暂的下降趋势,但相较于正常状态仍显著增加;进入血管修复阶段后,该区域血管密度和血管总长度增长幅度逐步加大。从血管分支指数来看,其变化趋势与血管密度、血管总长度相似,在TBI早期同样出现下降趋势,而随着血管修复进程的推进逐渐增加,这一现象表明损伤周边区血管网络的复杂程度会随着修复过程不断提高。在血管直径方面,TBI后1 d轻微减小,到TBI后3 d则增至峰值,此后进入血管修复阶段,TBI后7 d和14 d,TBI组与假手术组比较,血管直径无统计学差异。上述结果表明,TBI发生后,损伤周边区的脑血管会先启动反应性增生过程,具体表现为血管密度提高、血管总长度增加、血管网络复杂程度提高和血管管径增粗。同时,该区域血管形态的变化趋势与脑血流的恢复趋势呈现一致性,这一发现提示,损伤周边区的脑血管修复可能是实现脑血流有效恢复的必要前提。
本研究发现,损伤区脑血流在TBI后6 h~3 d急剧下降,减少幅度超过60%,与临床TBI患者急性期普遍存在的脑低灌注现象一致[11]。脑血流自第3天起开始恢复,至第14天基本恢复至对侧水平,提示该模型的脑血流具备自我恢复潜力。其恢复趋势与血管密度和血管总长度的增加高度吻合,Spearman秩相关分析进一步证实二者呈显著正相关(r = 1,P<0.01),提示结构性血管重建是脑血流恢复的重要机制之一[4]。血管分支指数与脑血流恢复虽呈正相关趋势,但无统计学意义,提示微血管分支复杂性对整体血流恢复的贡献可能较小或受其他因素调节。血管直径与脑血流恢复无相关性,说明其变化更可能是一种短期适应性反应,而非长期血流恢复的主导因素。本研究结果提示,早期促进血管生成和微网络重建可能是改善TBI后脑灌注、减轻继发性损伤的有效策略[12]。如高压氧、促血管生成因子等干预手段[13],若在脑血流自然恢复的关键时间窗(如TBI后3~7 d)应用,可能协同内源性修复机制,加速血流和神经功能恢复。
本研究仍存在局限性。首先,血管形态分析基于二维图像,未来可结合三维重建技术更精确地表征血管空间结构;此外,研究未涉及血管功能指标(如血管通透性、血流速度等)的变化,后续可结合多种功能学手段进行多维度验证。
综上所述,本研究表明,TBI后损伤周边区脑血管在形态上发生显著重建,血管密度、血管总长度和血管分支指数增加与脑血流恢复密切相关,早期血管结构修复是脑血流恢复的关键环节。本研究结果为TBI后血管靶向治疗提供了理论依据和时间窗口参考。未来研究应进一步探索不同损伤程度下血管重塑的规律及其分子机制,为临床早期干预提供新思路。
| [1] |
ROOZENBEEK B, MAAS AI, MENON DK. Changing patterns in the epidemiology of traumatic brain injury[J]. Nat Rev Neurol, 2013, 9(4): 231-236. DOI:10.1038/nrneurol.2013.22 |
| [2] |
阮霄睿, 成佩霞, 胡国清. 2000-2019年我国颅脑创伤的发病率与患病率趋势分析[J]. 中华神经外科杂志, 2021, 37(12): 1223-1229. DOI:10.3760/cma.j.cn112050-20210509-00223 |
| [3] |
ZHAO ZA, YAN L, WEN J, et al. Cellular and molecular mechanisms in vascular repair after traumatic brain injury: a narrative review[J]. Burns Trauma, 2023, 11: tkad033. DOI:10.1093/burnst/tkad033 |
| [4] |
SALEHI A, ZHANG JH, OBENAUS A. Response of the cerebral vasculature following traumatic brain injury[J]. J Cereb Blood Flow Metab, 2017, 37(7): 2320-2339. DOI:10.1177/0271678X17701460 |
| [5] |
STEINMAN J, CAHILL LS, KOLETAR MM, et al. Acute and chronic stage adaptations of vascular architecture and cerebral blood flow in a mouse model of TBI[J]. Neuroimage, 2019, 202: 116101. DOI:10.1016/j.neuroimage.2019.116101 |
| [6] |
李坤航, 张旭东, 赵丹, 等. 小鼠脑外伤后脑血流的动态变化及其与行为学恢复的相关性[J]. 中国医科大学学报, 2021, 50(5): 408-412. DOI:10.12007/j.issn.0258-4646.2021.05.005 |
| [7] |
MA EL, SMITH AD, DESAI N, et al. Bidirectional brain-gut inter-actions and chronic pathological changes after traumatic brain injury in mice[J]. Brain Behav Immun, 2017, 66: 56-69. DOI:10.1016/j.bbi.2017.06.018 |
| [8] |
WRIGHT DK, MAYO JN, SUN M, et al. Contrast enhanced magnetic resonance imaging highlights neurovasculature changes following experimental traumatic brain injury in the rat[J]. Sci Rep, 2020, 10(1): 21252. DOI:10.1038/s41598-020-77975-2 |
| [9] |
HAN X, CHAI Z, PING X, et al. In vivo two-photon imaging reveals acute cerebral vascular spasm and microthrombosis after mild traumatic brain injury in mice[J]. Front Neurosci, 2020, 14: 210. DOI:10.3389/fnins.2020.00210 |
| [10] |
BENAUS A, NG M, ORANTES AM, et al. Traumatic brain injury results in acute rarefication of the vascular network[J]. Sci Rep, 2017, 7(1): 239. DOI:10.1038/s41598-017-00161-4 |
| [11] |
ROBINSON CP. Moderate and severe traumatic brain injury[J]. Continuum (Minneap Minn), 2021, 27(5): 1278-1300. |
| [12] |
MA X, AGAS A, SIDDIQUI Z, et al. Angiogenic peptide hydrogels for treatment of traumatic brain injury[J]. Bioact Mater, 2020, 5(1): 124-132. DOI:10.1016/j.bioactmat.2020.01.005 |
| [13] |
TAL S, HADANNY A, SASSON E, et al. Hyperbaric oxygen therapy can induce angiogenesis and regeneration of nerve fibers in traumatic brain injury patients[J]. Front Hum Neurosci, 2017, 11: 508. DOI:10.3389/fnhum.2017.00508 |
 2025, Vol. 54
2025, Vol. 54