文章信息
- 初高平, 林雅雯, 王子龙, 窦越, 马蕾
- CHU Gaoping, LIN Yawen, WANG Zilong, DOU Yue, MA Lei
- LY294002通过抑制Th17细胞分化减轻银屑病炎症反应
- LY294002 alleviates psoriatic inflammation by intervening with Th17 cell differentiation
- 中国医科大学学报, 2025, 54(12): 1068-1075
- Journal of China Medical University, 2025, 54(12): 1068-1075
-
文章历史
- 收稿日期:2025-04-17
- 网络出版时间:2025-12-15 13:14:33
银屑病是一种免疫介导的慢性炎症性皮肤病,以皮肤角质形成细胞过度增殖、活化的T淋巴细胞浸润以及血管生成异常为特点[1-2]。Th17细胞浸润是银屑病的重要免疫学特征。Th17细胞效应性细胞因子白细胞介素(interleukin,IL)-17A导致的免疫紊乱和炎症效应是银屑病的重要致病因素,阻断IL-17A及其受体是目前银屑病指南推荐的治疗方法之一[3]。诸多因素参与调控Th17细胞分化及功能,其中磷脂酰肌醇-3-激酶/蛋白激酶B/雷帕霉素靶蛋白C1(phosphatidylinositol 3-kinase/protein kinase B/mechanistic target of rapamycin kinase C1,PI3K/AKT/mTORC1)信号通路在Th17细胞分化过程中发挥重要作用,通过其下游信号分子多途径正向调控Th17细胞分化,包括调节低氧诱导因子1α(hypoxia inducible factor 1α,HIF-1α)表达,诱导信号转导与转录激活因子3(signal transducer and activator of transcription 3,STAT3)酪氨酸磷酸化,加速Th17细胞特异性转录因子维甲酸相关孤核受体γt(retinoic acid-related orphan receptor γt,RORγt)核转移等[4]。本研究拟探讨PI3K/AKT抑制剂LY294002通过AKT/mTORC1-STAT3/HIF-1α/RORγt信号通路抑制Th17细胞分化,从而减轻银屑病炎症反应的作用及可能机制。
1 材料与方法 1.1 实验动物雄性BALB/c小鼠(6周龄,体重18 g±2 g)购自济南朋悦实验动物繁育有限公司,饲养于滨州医学院附属医院SPF动物房,本研究获得我院动物伦理委员会批准(20190104-15)。
1.2 主要试剂和仪器5%咪喹莫特乳膏(四川明欣药业有限责任公司);LY294002(美国MedChemExpress公司);IL-17A抗体(美国R&D Systems公司、英国abcam公司);二甲基亚砜(dimethyl Sulfoxide,DMSO)、磷酸盐缓冲液(phosphate buffer saline,PBS)、细胞筛网、TRIzol(上海生工生物工程有限公司);小鼠脾脏单个核细胞(spleen mononuclear cell,SMC)分离液试剂盒(天津灏洋生物制品科技有限责任公司);胶原酶Ⅳ(美国sigma-aldrich公司);脱氧核糖核酸酶Ⅰ、苏木素-伊红(hematoxylin and eosin,HE)染色试剂盒、4%多聚甲醛、RIPA裂解液(北京索莱宝科技有限公司);CD3ε、CD28、γ干扰素(interferon-γ,IFN-γ)、IL-4、IL-2抗体(美国Bio X Cell公司);重组IL-1β、转化生长因子β1(transforming growth factor β1,TGF-β1)、IL-6、IL-23,APC-CD4、PE-IL-17A抗体(美国BioLegend公司);佛波酯、布雷非德菌素A、钙离子霉素(美国eBioscience公司);Evo M-MLV反转录预混型试剂盒、SYBR Green Pro Taq HS预混型qPCR试剂盒(湖南艾科瑞生物工程有限公司);AKT、p-AKT(Thr308)、p-AKT(Ser473)、mTORC1、p-mTOR(Ser2448)抗体(美国Cell Signaling公司);STAT3、p-STAT3(Tyr705)、β-actin抗体(武汉爱博泰克生物科技有限公司);HIF-1α抗体、DyLight 549及DyLight 488标记IgG [亚科因(武汉)生物技术有限公司];RORγt抗体(武汉三鹰生物技术有限公司);CD4抗体(美国Santa公司);CFX96 TouchTM Real-Time PCR检测系统(美国Bio-Rad公司);激光共聚焦显微镜(德国Leica公司)。
1.3 方法 1.3.1 小鼠分组及处置用5 %咪喹莫特乳膏(imiquimod,IMQ)涂抹小鼠背部皮肤制备银屑病样皮炎模型。将小鼠随机分为对照(Vehicle)组、模型(IMQ)组、25 mg/kg LY294002干预(IMQ+25 mg/kg LY)组、50 mg/kg LY294002干预(IMQ+50 mg/kg LY)组、10 mg/kg抗IL-17A抗体抑制(IMQ+Anti-IL-17A)组,每组6只。IMQ组、IMQ+25 mg/kg LY组、IMQ+50 mg/kg LY组和IMQ+Anti-IL-17A组每日涂抹62.5 mgIMQ,Vehicle组涂抹等剂量白凡士林。在涂抹IMQ后,LY294002干预组立即腹腔注射DMSO溶解的LY294002工作液25 mg/kg和50 mg/kg、IMQ+Anti-IL-17A组腹腔注射PBS溶解的抗IL-17A单克隆抗体10 mg/kg,Vehicle组及IMQ组腹腔注射等剂量DMSO与PBS混合液。以上处理均为1次/d,连续6 d。末次处理24 h后处死小鼠并留取皮肤和脾脏组织。
1.3.2 皮肤组织HE染色剪取小鼠背部约0.5 cm×0.5 cm大小皮肤组织,并将组织展平放入适量4%多聚甲醛中固定,经石蜡包埋、切片、HE染色后于显微镜下观察。
1.3.3 小鼠皮肤和SMC提取、培养及极化将皮肤样本切成0.5 cm×0.5 cm大小,用0.5%胰蛋白酶孵育2 h;分离表皮后,脱氧核糖核酸酶Ⅰ和胶原酶Ⅳ消化真皮1 h;40 μm细胞筛网过滤;3 000 r/min离心10 min;收集并重悬细胞。取小鼠新鲜脾脏,按试剂盒说明书进行操作,将细胞重悬于含10%FBS的RPMI 1640培养基中。将皮肤和SMC悬液放入已包被含5 μg/mL抗小鼠CD3ε单克隆抗体、2 µg/mL抗小鼠CD28单克隆抗体的12孔板中;每孔1×106细胞,用完全培养基调整至每孔2 mL液体;每孔依次加入终浓度为10 ng/mL重组鼠IL-1β、2 ng/mL重组鼠TGF-β1、50 ng/mL重组鼠IL-6、20 ng/mL重组鼠IL-23以及10 µg/mL抗小鼠IFN-γ、IL-4、IL-2抗体刺激Th17细胞极化。
1.3.4 小鼠SMC分组将小鼠SMC分为Control组、模型(Model)组、LY25和LY50干预组(25 mol/L和50 mol/L LY294002分别作用于模型鼠SMC)、IL-17A-antibody组(10 ng/mL抗IL-17A抗体作用于模型鼠SMC)。
1.3.5 流式细胞术检测Th17细胞比例取1.3.3和1.3.4制备的各组小鼠皮肤和SMC悬液各1 mL,分别加入12孔板,用含有10 ng/mL佛波酯、1 µg/mL钙离子霉素细胞培养基重悬细胞,37 ℃ 5% CO2培养1 h,再加入10 µg/mL布雷非德霉素A,共培养4 h。APC-CD4抗体进行表面染色,固定破膜后用PE-IL-17A抗体核内染色,上机检测Th17细胞比例(IL-17A+CD4+ T细胞/CD4+ T细胞)。
1.3.6 实时定量PCR检测HIF-1α、RORγt以及IL-17A的mRNA表达水平采用TRIzol RNA提取试剂抽提小鼠皮肤、脾脏组织、SMC中总RNA,采用Evo M-MLV反转录预混型试剂盒将RNA合成互补DNA,以β-actin为内参,使用SYBR Green Pro Taq HS预混型qPCR试剂盒在CFX96 TouchTM Real-Time PCR检测系统上进行实时定量PCR检测。
1.3.7 Western blotting检测p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、p-STAT3(Tyr705)、HIF-1α、RORγt及IL-17A蛋白表达水平RIPA裂解液提取各组皮肤组织、脾脏组织及SMC的总蛋白,SDS-PAGE电泳分离蛋白,转膜,封闭,加入AKT、p-AKT(Thr308)、p-AKT(Ser473)、mTORC1、p-mTOR(Ser2448)、STAT3、p-STAT3(Tyr705)、HIF-1α、RORγt及IL-17A(均1∶ 1 000稀释)、β-actin(1∶10 000稀释)一抗4 ℃孵育过夜;TBST洗膜;加入1∶5 000稀释的二抗室温孵育45 min,显影后采用ImageJ软件计算灰度值。
1.3.8 免疫荧光检测皮肤及SMC中Th17细胞比例将小鼠皮肤组织和SMC先后于冰上4%多聚甲醛固定、0.3%Triton X-100破膜各15 min;与10%山羊血清在室温下孵育1 h,阻断非特异性染色;抗CD4(1∶500稀释)、抗IL-17A(1∶200稀释)一抗4 ℃孵育12 h;DyLight 549、DyLight 488荧光标记二抗室温避光孵育1 h;DAPI细胞核染色后封片;激光共聚焦显微镜下观察。
1.4 统计学分析采用SPSS 19.0统计软件进行分析,计量资料以x±s表示,应用Shapiro-Wilk检验法进行正态性检验,根据Levene方差齐性检验判断方差是否齐。使用单因素方差分析比较各组间差异,Tukey检验进行多重比较。P<0.05为差异有统计学意义。
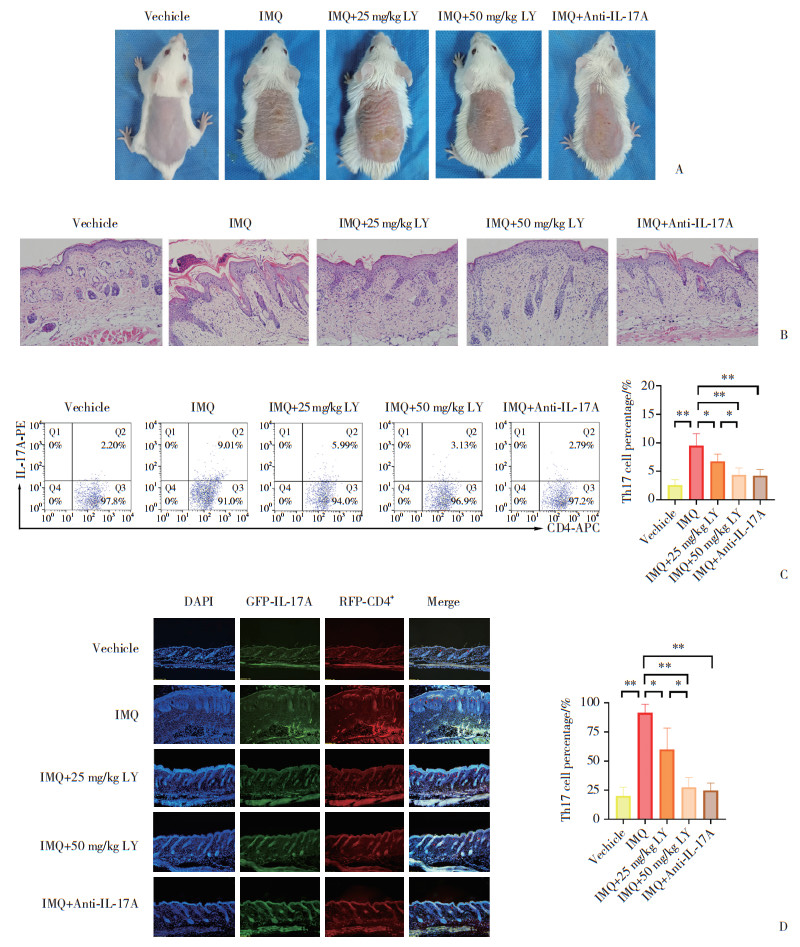
2 结果 2.1 各组小鼠皮损严重程度变化末次涂药24 h后,Vehicle组小鼠皮肤始终未出现红斑、鳞屑及浸润增厚,IMQ组小鼠呈现出明显的红斑、鳞屑及浸润增厚银屑病样皮炎改变,LY294002干预后小鼠银屑病样皮炎程度均明显减轻,且以IMQ+50 mg/kg LY组更为明显,其减轻程度与IMQ+Anti-IL-17A组相似,见图 1A。
|
| A, representative images of mouse psoriatic inflammation; B, skin pathological characteristics revealed using hematoxylin and eosin staining (×200); C, proportion (%) of Th17 cells (IL-17A+CD4+ T cells/CD4+ T cells) in skin lesions, as determined using flow cytometry analysis; D, ratio of IL-17A+CD4+ T cells/CD4+ T cells in skin lesions determined using immunofluorescence (×200). *P < 0.05, **P < 0.01. 图 1 LY294002明显减轻银屑病样皮炎严重程度、降低皮损组织中Th17细胞比例 Fig.1 LY294002 alleviates psoriatic inflammation degree and decreases Th17 cell percentage in psoriatic skin lesions |
2.2 各组小鼠皮损组织病理改变
Vehicle组小鼠表皮薄,由1~2层细胞组成;IMQ组小鼠表皮明显增生、角化过度伴表皮突向下延伸,角化不全区可见中性粒细胞聚集及Munro微脓肿形成,真皮炎症细胞大量浸润,可见血管扩张。LY294002干预后小鼠表皮增厚及真皮炎症细胞浸润程度均较IMQ组明显减轻,IMQ+50 mg/kg LY组减轻程度更为明显,IMQ+Anti-IL-17A组与IMQ+50 mg/kg LY组比较无明显差异,见图 1B。
2.3 各组小鼠皮损组织中Th17细胞比例流式细胞术检测结果显示,IMQ组小鼠皮损组织中Th17细胞比例明显高于Vehicle组(P<0.05),LY294002干预后Th17细胞比例显著降低(P均<0.05),以IMQ+50 mg/kg LY组降低更为明显(P<0.05),IMQ+Anti-IL-17A组与IMQ+50 mg/kg LY组比较无统计学差异(P > 0.05,图 1C)。免疫荧光染色检测结果显示,各组小鼠皮损切片中Th17细胞比例与其皮损组织中的Th17细胞比例变化趋势一致,见图 1D。
2.4 各组小鼠皮损组织及脾脏组织中关键节点信号分子表达水平实时定量PCR结果显示(表 1),IMQ组小鼠皮损组织与脾脏组织中HIF-1α、RORγt和IL-17A的mRNA表达水平均明显高于Vehicle组(P均<0.05),LY294002干预组表达水平均显著低于IMQ组(P均<0.05),以IMQ+50mg/kg LY组降低更为明显(P均<0.05)。IMQ+50mg/kg LY组以上关键节点信号分子mRNA水平与IMQ+Anti-IL-17A组比较无统计学差异(P均 > 0.05)。
| Group | Skin | Spleen | |||||
| HIF-1α | RORγt | IL-17A | HIF-1α | RORγt | IL-17A | ||
| Vehicle | 0.46±0.43 | 0.55±0.33 | 0.37±0.34 | 0.49±0.35 | 0.70±0.27 | 0.44±0.37 | |
| IMQ | 3.93±1.241) | 3.20±0.661) | 3.79±0.421) | 3.65±0.981) | 3.51±1.061) | 3.29±1.451) | |
| IMQ+25 mg/kg LY | 2.12±0.832) | 1.29±0.542) | 1.42±0.182) | 2.40±0.902) | 2.26±1.012) | 1.86±0.772) | |
| IMQ+50 mg/kg LY | 0.58±0.572),3) | 0.50±0.292),3) | 0.47±0.192),3) | 0.63±0.632),3) | 0.74±0.352),3) | 0.52±0.392),3) | |
| IMQ+Anti-IL-17A | 0.59±0.75 | 0.51±0.22 | 0.38±0.18 | 0.65±0.54 | 0.72±0.32 | 0.52±0.23 | |
| 1)P<0.05 vs. Vehicle group;2)P<0.05 vs. IMQ group;3)P<0.05 vs. IMQ+25 mg/kg LY group. | |||||||
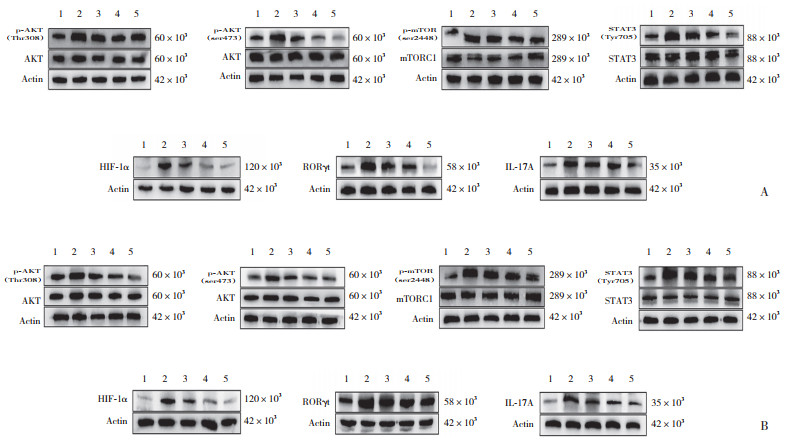
Western blotting结果显示(表 2、图 2),IMQ组小鼠皮损组织与脾脏组织中p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、p-STAT3(Tyr705)、HIF-1α、RORγt及IL-17A蛋白表达水平均显著高于Vehicle组(P均<0.05),LY294002干预组上述关键节点信号分子表达水平均明显低于IMQ组(P均<0.05),以IMQ+50mg/kg LY组降低更为明显(P均<0.05)。IMQ+50mg/kg LY组以上关键节点信号分子蛋白表达水平与IMQ+Anti-IL-17A组比较无统计学差异(P均 > 0.05)。
| Group | p-AKT (Thr308) |
p-AKT (Ser473) |
p-mTOR (Ser2448) |
p-STAT3 (Tyr705) |
HIF-1α | RORγt | IL-17A |
| Vehicle | |||||||
| Skin | 0.49±0.26 | 0.54±0.13 | 0.48±0.20 | 0.36±0.16 | 0.19±0.07 | 0.42±0.09 | 0.29±0.03 |
| Spleen | 0.57±0.14 | 0.54±0.22 | 0.59±0.11 | 0.67±0.24 | 0.57±0.10 | 0.58±0.16 | 0.50±0.17 |
| IMQ | |||||||
| Skin | 1.68±0.191) | 1.65±0.221) | 1.59±0.241) | 1.53±0.271) | 1.18±0.131) | 1.32±0.121) | 1.08±0.061) |
| Spleen | 1.29±0.261) | 1.30±0.211) | 1.21±0.161) | 1.39±0.191) | 0.99±0.101) | 1.32±0.151) | 1.04±0.231) |
| IMQ+25 mg/kg LY | |||||||
| Skin | 1.10±0.082) | 1.09±0.182) | 1.02±0.042) | 1.05±0.082) | 0.82±0.042) | 0.82±0.232) | 0.84±0.092) |
| Spleen | 0.95±0.202) | 0.91±0.182) | 0.96±0.162) | 1.07±0.162) | 0.81±0.122) | 0.97±0.192) | 0.76±0.132) |
| IMQ+50 mg/kg LY | |||||||
| Skin | 0.59±0.202),3) | 0.55±0.152),3) | 0.54±0.172),3) | 0.62±0.072),3) | 0.49±0.092),3) | 0.39±0.032),3) | 0.62±0.042),3) |
| Spleen | 0.64±0.092),3) | 0.55±0.202),3) | 0.71±0.152),3) | 0.75±0.172),3) | 0.61±0.062),3) | 0.63±0.242),3) | 0.50±0.062),3) |
| IMQ+Anti-IL-17A | |||||||
| Skin | 0.50±0.06 | 0.49±0.10 | 0.53±0.08 | 0.56±0.08 | 0.29±0.18 | 0.40±0.21 | 0.49±0.01 |
| Spleen | 0.73±0.16 | 0.58±0.21 | 0.77±0.11 | 1.03±0.15 | 0.63±0.06 | 0.61±0.16 | 0.50±0.13 |
| 1)P<0.05 vs. Vehicle group;2)P<0.05 vs. IMQ group;3)P<0.05 vs. IMQ+25 mg/kg LY group. | |||||||
|
| A, skin; B, spleen tissue. 1, Vechicle group; 2, IMQ group; 3, IMQ+25 mg/kg LY group; 4, IMQ+50 mg/kg LY group; 5, IMQ+Anti-IL-17A group. 图 2 各组小鼠皮肤及脾脏组织中p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、p-STAT3(Tyr705)、HIF-1α、RORγt和IL-17A的Western blotting结果 Fig.2 Representative Western blotting results of p-AKT (Thr308), p-AKT (Ser473), p-mTOR (Ser2448), p-STAT3 (Tyr705), HIF-1α, RORγt, and IL-17A in skin and spleen tissues of mice in each group |
2.5 各组SMC中Th17细胞比例
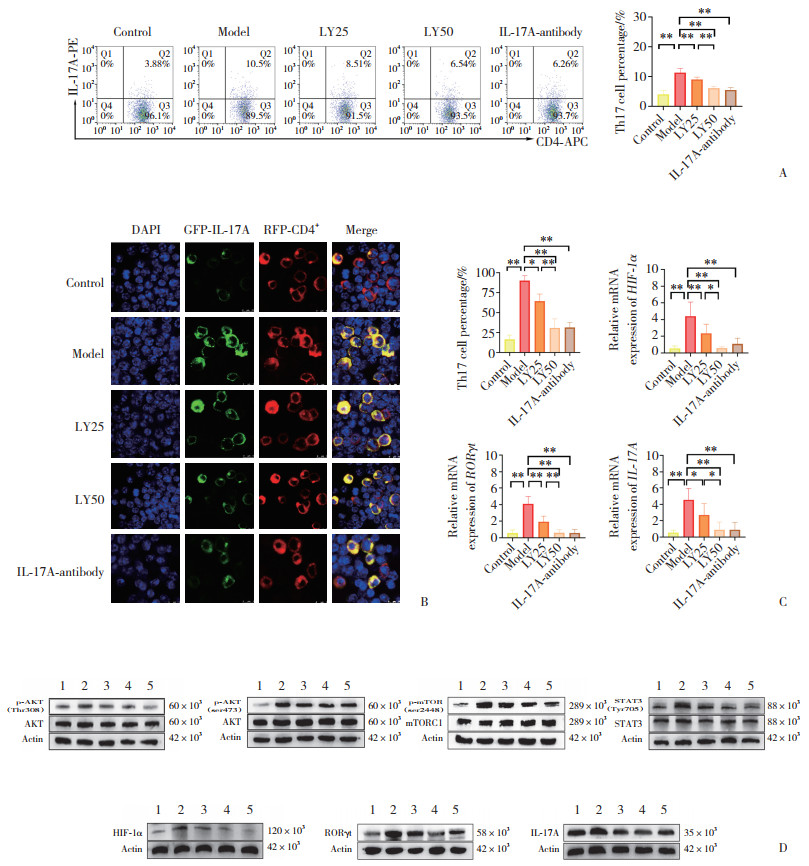
流式细胞术检测结果显示,Model组SMC中Th17细胞比例明显高于Control组(P<0.05);经LY294002干预处理后,Th17细胞比例均明显降低(P均<0.05),以LY50干预组更为明显(P<0.05),IL-17A-antibody组与LY50干预组比较无统计学差异(P > 0.05),见图 3A。免疫荧光检测各组SMC的Th17细胞比例,结果与流式细胞术检测结果变化趋势一致,见图 3B。
|
| A, flow cytometry analysis of Th17 cell percentage (IL-17A+CD4+ T cells/CD4+ T cells) in mice SMC; B, immunofluorescence detection for the ratio of IL-17A+CD4+ T cells/CD4+ T cells in mice SMC (×800); C, mRNA expression of HIF-1α, RORγt, and IL-17A in mice SMC; D, representative Western blotting results of p-AKT (Thr308), p-AKT (Ser473), p-mTOR (Ser2448), p-STAT3 (Tyr705), HIF-1α, RORγt, and IL-17A in mice SMC. 1, Control group; 2, Model group; 3, LY25 group; 4, LY50 group; 5, IL-17A-antibody group. *P < 0.05, **P < 0.01. 图 3 LY294002通过AKT/mTORC1-STAT3/HIF-1α/RORγt信号通路抑制SMC中Th17细胞分化 Fig.3 LY294002 suppresses Th17 cell differentiation through the AKT/mTORC1-STAT3/HIF-1α/RORγt signaling pathway in SMC |
2.6 各组SMC中HIF-1α、RORγt和IL-17A的mRNA表达水平
Model组SMC中HIF-1α、RORγt和IL-17A的mRNA表达水平均明显高于Control组(P均<0.05);经LY294002干预处理后,其表达水平均明显降低(P均<0.05),以LY50干预组降低更为明显(P均<0.05),IL-17A-antibody组与LY50干预组比较无统计学差异(P均 > 0.05),见图 3C。
2.7 各组SMC中p-AKT、p-mTOR、p-STAT3、HIF-1α、RORγt及IL-17A蛋白表达水平Model组SMC中p-AKT(Thr308)、p-AKT(Ser473)、p-mTOR(Ser2448)、p-STAT3(Tyr705)、HIF-1α、RORγt及IL-17A的蛋白表达水平均显著高于Control组(P均<0.05);经LY294002干预处理后,以上信号分子蛋白表达水平均明显降低(P均<0.05),以LY50干预组降低更为明显(P均<0.05),IL-17A-antibody组与LY50干预组比较,无统计学差异(P均 > 0.05),见图 3D、表 3。
| Group | p-AKT (Thr308) |
p-AKT (Ser473) |
p-mTOR (Ser2448) |
p-STAT3 (Tyr705) |
HIF-1α | RORγt | IL-17A |
| Control | 0.47±0.14 | 0.52±0.13 | 0.42±0.13 | 0.42±0.18 | 0.16±0.05 | 0.55±0.14 | 0.43±0.11 |
| Model | 1.40±0.201) | 1.58±0.241) | 1.36±0.181) | 1.19±0.251) | 0.98±0.191) | 1.23±0.211) | 0.99±0.191) |
| LY25 | 0.99±0.332) | 1.09±0.102) | 1.03±0.192) | 0.79±0.142) | 0.66±0.082) | 0.93±0.132) | 0.71±0.182) |
| LY50 | 0.60±0.232),3) | 0.76±0.132),3) | 0.70±0.202),3) | 0.41±0.192),3) | 0.32±0.172),3) | 0.57±0.092),3) | 0.44±0.142),3) |
| IL-17A-antibody | 0.60±0.18 | 0.73±0.17 | 0.67±0.22 | 0.61±0.15 | 0.43±0.12 | 0.55±0.13 | 0.44±0.11 |
| 1)P<0.05 vs. Control group;2)P<0.05 vs. Model group;3)P<0.05 vs. LY25 group. | |||||||
3 讨论
Th17细胞及其效应细胞因子IL-17A在银屑病中发挥重要作用[5]。PI3K/AKT/mTORC1信号通路是调控细胞基本功能最关键的信号通路,参与T细胞发育、活化及定向分化的全过程[6]。本研究结果显示,IMQ组小鼠皮损及脾脏组织中p-AKT(Thr308)、p-AKT(Ser473)和p-mTOR(Ser2448)表达水平显著高于Vehicle组,进一步证实PI3K/AKT/mTORC1信号通路在银屑病中发挥作用。PI3K抑制剂LY294002能减轻银屑病样皮炎小鼠皮肤损伤,并显著降低皮肤及脾脏中Th17细胞比例与IL-17A表达水平,表明LY294002可通过抑制Th17细胞分化及IL-17A分泌减轻银屑病所致的皮肤损伤及炎症反应。
本课题组前期研究[7-8]发现,PI3K/AKT/mTORC1信号通路与Notch1信号通路相互作用,IL-17信号转导的关键接头分子Act1与Notch1信号分子的胞内结构域形成复合体,构成反馈环路调控银屑病样皮炎小鼠Th17细胞分化及IL-17A表达。mTORC1主要通过调节转录因子表达或核定位促进相关基因的表达。STAT3是Th17细胞分化的关键转录因子,能够诱导RORγt的表达,促进Th17细胞极化。mTORC1通过诱导STAT3 705位酪氨酸位点磷酸化增强STAT3的活性[9]。本研究结果显示,在银屑病样皮炎小鼠皮肤及脾脏组织中p-AKT、p-mTOR表达水平升高的同时,p-STAT3和RORγt亦明显升高;给予LY294002干预时,p-STAT3和RORγt表达水平与p-AKT、p-mTOR呈现一致性降低,且高剂量LY294002的干预效应更加明显,具有作用浓度相关性,表明PI3K/AKT/mTORC1信号通路与下游转录因子STAT3构成信号轴,发挥对银屑病炎症反应的调控效应。
CD4+ T细胞的分化受代谢因素的调控,Th17细胞主要由糖酵解提供动力[10]。HIF-1α是mTORC1下游的重要转录因子,在转录水平和翻译水平促进葡萄糖转运和糖酵解过程[11]。HIF-1α被mTORC1激活后,能够上调糖酵解途径并促进RORγt表达,进而促进CD4+ T细胞向Th17细胞分化。HIF-1α缺陷型T细胞则表现出糖酵解抑制,Th17细胞分化减少[12]。STAT3是HIF-1α的原始调控分子[13],在缺氧微环境下发生自身磷酸化,p-STAT3可激活HIF-1α启动子并提高其转录及翻译活性[14]。本研究结果显示,随着LY294002作用浓度的增加,银屑病皮炎小鼠皮损、脾脏以及体外培养SMC中HIF-1α与RORγt表达水平受到明显抑制,且Th17细胞比例及IL-17A表达水平显著降低,高浓度LY294002干预效应更加明显。LY294002通过PI3K/AKT/mTORC1/HIF-1α信号通路抑制糖酵解途径,此外,STAT3与HIF-1α间存在协同效应,降低p-STAT3水平能削弱对HIF-1α转录及翻译活性的调控,二者共同抑制RORγt表达以及Th17细胞分化,从而减轻银屑病炎症反应。
综上所述,LY294002可通过抑制AKT/mTORC1-STAT3/HIF-1α/RORγt信号通路干预Th17细胞分化及IL-17A分泌,进而减轻银屑病炎症反应,为银屑病治疗提供了可能的候选靶点。
| [1] |
SUGUMARAN D, YONG ACH, STANSLAS J. Advances in psoriasis research: from pathogenesis to therapeutics[J]. Life Sci, 2024, 355: 122991. DOI:10.1016/j.lfs.2024.122991 |
| [2] |
LWIN SM, AZRIELANT S, HE J, et al. Curing psoriasis[J]. J Invest Dermatol, 2024, 144(12): 2645-2649. DOI:10.1016/j.jid.2024.09.012 |
| [3] |
中华医学会皮肤性病学分会, 中国医师协会皮肤科医师分会, 中国中西医结合学会皮肤性病专业委员会. 中国银屑病生物制剂及小分子药物治疗指南(2024版)[J]. 中华皮肤科杂志, 2024, 57(11): 976-997. DOI:10.35541/cjd.20240294 |
| [4] |
NAGAI S, KUREBAYASHI Y, KOYASU S. Role of PI3K/Akt and mTOR complexes in Th17 cell differentiation[J]. Ann N Y Acad Sci, 2013, 1280: 30-34. DOI:10.1111/nyas.12059 |
| [5] |
HU P, WANG MY, GAO H, et al. The role of helper T cells in psoriasis[J]. Front Immunol, 2021, 12: 788940. DOI:10.3389/fimmu.2021.788940 |
| [6] |
何呈燕, 李依雯, 甘玲, 等. PI3K/AKT/mTOR信号通路通过调控Th17细胞分化参与EAT小鼠甲状腺自身免疫损伤[J]. 中国医科大学学报, 2024, 53(11): 972-978. DOI:10.12007/j.issn.0258-4646.2024.11.003 |
| [7] |
LIN YW, LI XX, FU FH, et al. Notch1/Hes1-PTEN/AKT/IL-17A feedback loop regulates Th17 cell differentiation in mouse psoriasis-like skin inflammation[J]. Mol Med Rep, 2022, 26(1): 223. DOI:10.3892/mmr.2022.12739 |
| [8] |
LIN YW, ZHU XF, LI YW, et al. LY294002 ameliorates psoriatic skin inflammation in mice via blocking the Notch1/Hes1-PTEN/AKT/IL-17A feedback loop[J]. Clin Exp Immunol, 2023, 213(1): 114-124. DOI:10.1093/cei/uxad025 |
| [9] |
LEE SY, LEE AR, CHOI JW, et al. IL-17 induces autophagy dysfunction to promote inflammatory cell death and fibrosis in keloid fibroblasts via the STAT3 and HIF-1α dependent signaling pathways[J]. Front Immunol, 2022, 13: 888719. DOI:10.3389/fimmu.2022.888719 |
| [10] |
LIN YT, XUE K, LI QY, et al. Cyclin-dependent kinase 7 promotes Th17/Th1 cell differentiation in psoriasis by modulating glycolytic metabolism[J]. J Invest Dermatol, 2021, 141(11): 2656-2667.e11. DOI:10.1016/j.jid.2021.04.018 |
| [11] |
WANG P, ZHANG Q, TAN L, et al. The regulatory effects of mTOR complexes in the differentiation and function of CD4+ T cell subsets[J]. J Immunol Res, 2020, 2020: 3406032. DOI:10.1155/2020/3406032 |
| [12] |
ASO K, KONO M, KANDA M, et al. Itaconate ameliorates autoimmunity by modulating T cell imbalance via metabolic and epigenetic reprogramming[J]. Nat Commun, 2023, 14(1): 984. DOI:10.1038/s41467-023-36594-x |
| [13] |
YANG W, WEI XY, JIAO YC, et al. STAT3/HIF-1α/fascin-1 axis promotes RA FLSs migration and invasion ability under hypoxia[J]. Mol Immunol, 2022, 142: 83-94. DOI:10.1016/j.molimm.2021.12.004 |
| [14] |
MENDOZA-REINOSO V, SCHNEPP PM, BAEK DY, et al. Bone marrow macrophages induce inflammation by efferocytosis of apoptotic prostate cancer cells via HIF-1α stabilization[J]. Cells, 2022, 11(23): 3712. DOI:10.3390/cells11233712 |
 2025, Vol. 54
2025, Vol. 54