文章信息
- 樊展, 邹璟, 乐薇
- FAN Zhan, ZOU Jing, LE Wei
- 电针通过S100A9/TLR4/NF-κB通路影响星形胶质细胞活化改善神经病理性疼痛
- Electroacupuncture alleviates neuropathic pain by regulating astrocyte activation via the S100A9/TLR4/NF-κB pathway
- 中国医科大学学报, 2025, 54(12): 1062-1067
- Journal of China Medical University, 2025, 54(12): 1062-1067
-
文章历史
- 收稿日期:2025-07-21
- 网络出版时间:2025-12-15 14:29:20
神经病理性疼痛由中枢或外周神经系统损伤引起,常规镇痛药治疗效果差[1]。近年来,中医药治疗神经病理性疼痛显示出减痛优势,且安全、患者易接受[2]。研究[3]证实,电针可缓解神经病理性疼痛,但其具体机制尚不明确。S100钙结合蛋白A9(S100 calcium-binding protein A9,S100A9)在细胞损伤、感染、炎症时释放,研究[4]显示,其在带状疱疹后遗神经痛小鼠背根神经节组织中表达增加且发挥促疼痛作用。Toll样受体4(Toll-like receptor 4,TLR4)是免疫系统关键模式识别受体。研究[5]显示,儿茶素能够抑制TLR4,改善神经病理性疼痛大鼠模型的症状。核因子κB(nuclear factor κB,NF-κB)是广泛存在的转录因子复合物,激活其磷酸化可促使星形胶质细胞极化,促进神经炎症损伤[6]。研究[7]证实,S100A9通过TLR4/NF-κB通路激活星形胶质细胞向A1型转化,促进释放炎性细胞因子,引发炎症反应。但S100A9/TLR4/NF-κB通路是否参与神经病理性疼痛以及电针治疗是否通过该通路改善疼痛仍有待证实。因此,本研究构建了神经病理性疼痛大鼠模型,揭示电针改善神经病理性疼痛的机制和关键分子靶点。
1 材料与方法 1.1 主要试剂与仪器树脂毒素(resiniferatoxin,RTX),购自美国Target-Mol公司;苏木素-伊红(hematoxylin-eosin,HE)染色试剂盒、TUNEL试剂盒,购自武汉伊莱瑞特生物科技股份有限公司;S100A9抗体、TLR4抗体、p-p65抗体、p65抗体、GAPDH、胶质纤维酸性蛋白(glial fibrillary acidic protein,GFAP)抗体、山羊抗兔IgG,购自赛默飞世尔科技(中国)有限公司;S100A9通路抑制剂ABR-215757,购自美国AmBeed公司。von Frey触觉纤维丝,购自上海康朗生物科技有限公司;智能热板刺痛仪,购自安徽耀坤生物科技有限公司;多功能酶标仪,购自瑞士TECAN公司;电泳仪,购自美国Bio-Rad公司;HANS电针仪,购自南京济生医疗科技有限公司。
1.2 实验动物与分组50只8~10周龄SPF级SD雄性大鼠,体重220~250 g,由华中科技大学提供,许可证号:SCXK(鄂)20230032。大鼠在SPF级标准化环境中饲养,自由摄食和饮水,饲养7 d后用于实验。本研究经华中科技大学同济医学院实验动物伦理委员会批准(2100010305)。
将50只大鼠按随机数字表法分为正常对照组(Vehicle组)、模型组(RTX组)、假电针组(Sham-EA组)、电针组(EA组)、电针+S100A9通路抑制剂组(EA+ABR-215757组),每组10只。除Vehicle组大鼠外,其余4组大鼠麻醉后,单次腹腔注射RTX溶液(200 μg/kg,由RTX、10%乙醇、10% Tween80和80% 生理盐水混合而成),构建神经病理性疼痛大鼠模型[8]。EA组和EA+ABR-215757组大鼠在腹腔注射RTX后第8天开始使用电针刺激,主要穴位为“足三里”和“环跳穴”,治疗时间为1周[9]。大鼠吸入1.5%异氟醚进行浅麻醉后,仰卧位固定,使用无菌针垂直刺入上述2个穴位,深入4 mm,连接电针仪,接入2 Hz、1 mA电流,刺激30 min。Sham-EA组大鼠给予麻醉和针刺穴位,不通电。根据文献[10]以及药物等效剂量转化公式[11],EA+ABR-215757组大鼠在电针刺激的同时,每日口服5 mg/kg ABR-215757,持续1周。Vehicle组、RTX组、Sham-EA组、EA组大鼠口服相同体积生理盐水。行为学检测结束后,处死大鼠,进行组织检测。
1.3 行为学检测 1.3.1 机械缩足反射阈值(paw withdrawal mechanical threshold,PWMT)检测将大鼠置于玻璃罩内,适应30 min,用von Frey纤维丝(从2 g起递增)垂直刺其后足掌面5 s。观察大鼠反应,抬足或舔足为阳性,反之为阴性。若阳性,用更低强度刺激;若阴性,用更高强度刺激。记录首次阳性反应的最低刺激值为PWMT。每只大鼠连续测3次,间隔30 s,取均值[3]。
1.3.2 热缩足潜伏期(thermal withdrawal latency,TWL)检测将大鼠置于3 mm的透明玻璃板上,适应30 min,调整好辐射热刺激,使光斑对准其后足掌面。从刺激开始计时,大鼠缩足时停止,记录时间为TWL。每只大鼠测5次,间隔5 min,取均值[12]。
1.4 HE染色和TUNEL染色检测脊髓背角组织损伤和细胞凋亡 1.4.1 HE染色行为学检测后将大鼠安乐死,取出L4~6脊髓节段,经脱水、包埋,制成5 μm的石蜡切片。切片脱蜡后用乙醇复水、HE染色,再经梯度乙醇脱水,中性树胶封片,显微镜下观察脊髓背角组织病理改变。
1.4.2 TUNEL染色脊髓背角组织石蜡切片依次进行脱蜡、抗原修复等处理,经TUNEL染色、DAB显色、苏木素复染和反蓝后,脱水封片,显微镜下观察,用ImageJ软件统计凋亡细胞数,计算凋亡率。
1.5 免疫荧光染色检测GFAP阳性表达将石蜡样本制成5 μm的切片,PBS漂洗3次后,用含0.3% Triton X-100和10%山羊血清的PBS孵育1 h,加一抗GFAP,4 ℃过夜。PBS漂洗后,加二抗IgG常温避光孵育1 h,再次PBS漂洗。DAPI染细胞核后PBS冲洗,荧光封片剂封片,荧光显微镜下拍照。
1.6 实时定量PCR检测A1型(促炎)星形胶质细胞标志物C3 mRNA和A2型(抗炎)星形胶质细胞标志物Arg1 mRNA水平采用TRIzol试剂盒提取脊髓总RNA,分光光度计测量纯度/浓度。将1 μg RNA逆转录为cDNA。PCR反应条件:95 ℃ 3 min;95 ℃ 15 s,60 ℃ 1 min,40个循环。以GAPDH为内参,采用2-ΔΔCt法对C3和Arg1 mRNA的表达水平进行定量。
1.7 ELISA检测疼痛相关因子和促炎性细胞因子将采集的脊髓组织样本匀浆并离心处理,收集上清液。根据ELISA试剂盒说明书,检测疼痛相关因子P物质(substance P,SP)、降钙素基因相关肽(calcitonin gene-related peptide,CGRP)和促炎性细胞因子白细胞介素-6(interleukin-6,IL-6)、白细胞介素-1β(interleukin-1β,IL-1β)水平。
1.8 Western blotting检测S100A9/TLR4/NF-κB通路相关蛋白取脊髓背角组织,RIPA裂解,4 ℃、12 000 g离心5 min,取上清液。测定蛋白浓度、电泳、封闭后,加入S100A9、TLR4、p-p65、p65及GAPDH一抗,4 ℃孵育过夜,二抗室温孵育1 h,TBST洗3次,ECL显影,采用ImageJ软件进行灰度分析。
1.9 统计学分析采用SPSS 26.0和GraphPad Prism 9.5进行统计学分析。计量资料以x±s表示,2组间比较采用t检验,多组间比较采用单因素方差分析,进一步两两比较采用Tukey检验。P<0.05为差异有统计学意义。
2 结果 2.1 电针治疗改善RTX诱导的大鼠疼痛行为与Vehicle组比较,RTX组大鼠的PWMT、TWL显著降低(P<0.05)。Sham-EA组与RTX组比较,PWMT、TWL均无统计学差异(P > 0.05)。与RTX组比较,EA组大鼠的PWMT显著增加,TWL显著延长(P<0.05)。与EA组比较,EA+ABR-215757组大鼠PWMT显著增加,TWL显著延长(P<0.05)。见表 1。
| Group | n | PWMT(g) | TWL(s) | Apoptosis rate(%) | GFAP |
| Vehicle | 10 | 32.45±4.13 | 8.41±0.91 | 5.87±0.63 | 1.02±0.11 |
| RTX | 10 | 12.34±1.231) | 3.63±0.391) | 34.14±4.111) | 2.46±0.271) |
| Sham-EA | 10 | 13.61±1.46 | 3.72±0.40 | 32.26±3.49 | 2.38±0.25 |
| EA | 10 | 20.34±2.362) | 5.54±0.572) | 18.79±2.152) | 1.75±0.182) |
| EA+ABR-215757 | 10 | 27.65±2.973) | 7.29±0.763) | 11.37±1.283) | 1.21±0.123) |
| 1)P<0.05 vs. Vehicle group;2)P<0.05 vs. RTX group;3)P<0.05 vs. EA group. | |||||
2.2 电针治疗改善RTX诱导的大鼠脊髓背角组织细胞损伤并抑制其凋亡
Vehicle组大鼠脊髓组织结构清晰,细胞完整,排列整齐紧密。与Vehicle组比较,RTX组大鼠脊髓组织细胞核固缩,排列不整齐,炎症浸润明显,细胞凋亡率显著升高(P<0.05)。与RTX组比较,Sham-EA组大鼠脊髓组织无显著变化;EA组大鼠脊髓组织结构较为完整,炎症浸润减少,细胞凋亡率显著降低(P<0.05)。与EA组比较,EA+ABR-215757组大鼠脊髓组织结构更完善,炎症浸润减少,细胞凋亡率显著降低(P<0.05)。见图 1、表 1。
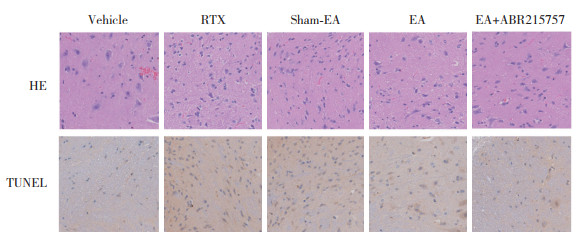
|
| 图 1 大鼠脊髓背角组织病理状态和细胞凋亡情况 ×400 Fig.1 Histopathological status and cellular apoptosis in the spinal dorsal horn tissue of rats ×400 |
2.3 电针治疗抑制RTX诱导的大鼠脊髓背角组织中星形胶质细胞激活
与Vehicle组比较,RTX组大鼠脊髓背角组织中GFAP表达水平显著升高(P<0.05)。Sham-EA组与RTX组比较,GFAP表达水平无统计学差异(P > 0.05)。EA组GFAP表达水平较RTX组显著降低(P<0.05)。与EA组比较,EA+ABR-215757组GFAP表达水平进一步降低(P<0.05)。见图 2、表 1。
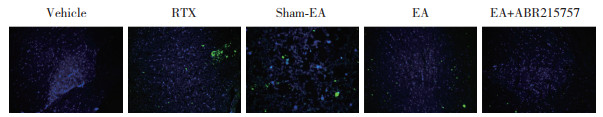
|
| 图 2 大鼠脊髓背角组织中GFAP阳性表达情况 ×400 Fig.2 Positive expression of GFAP in the spinal dorsal horn tissue of rats ×400 |
2.4 电针治疗抑制大鼠脊髓背角组织中促炎型星型胶质细胞活化
RTX组大鼠脊髓背角组织中C3 mRNA水平较Vehicle组显著升高,而Arg1 mRNA水平显著降低(P<0.05)。Sham-EA组与RTX组比较,C3 mRNA和Arg1 mRNA水平均无统计学差异(P > 0.05)。与RTX组比较,EA组C3 mRNA水平显著降低,Arg1 mRNA水平显著升高(P<0.05)。进一步比较发现,EA+ABR-215757组C3 mRNA水平较EA组显著降低,Arg1 mRNA水平显著升高(P<0.05)。表明电针治疗使A1型星形胶质细胞向A2型星形胶质细胞极化,电针与ABR-215757联合治疗的效果更显著。见表 2。
| Group | n | C3 mRNA | Arg1 mRNA | SP(pg/mL) | CGRP(pg/mL) | IL-6(pg/mL) | IL-1β(pg/mL) |
| Vehicl | 10 | 0.93±0.09 | 1.09±0.11 | 176.87±19.36 | 87.45±9.61 | 115.57±13.62 | 69.54±7.85 |
| RTX | 10 | 2.15±0.241) | 0.32±0.031) | 1 584.91±161.251) | 756.94±78.261) | 431.59±45.211) | 345.68±36.311) |
| Sham-EA | 10 | 2.08±0.21 | 0.36±0.04 | 1 564.29±157.83 | 721.37±75.69 | 408.27±42.95 | 334.27±34.63 |
| EA | 10 | 1.67±0.182) | 0.57±0.062) | 939.57±99.982) | 442.36±45.832) | 291.38±30.542) | 217.15±23.592) |
| EA+ABR-215757 | 10 | 1.16±0.123) | 0.79±0.093) | 436.24±45.523) | 243.74±25.883) | 186.73±19.783) | 132.92±15.783) |
| 1)P<0.05 vs. Vehicle group;2)P<0.05 vs. RTX group;3)P<0.05 vs. EA group. | |||||||
2.5 电针治疗抑制RTX诱导大鼠脊髓背角组织中疼痛相关因子和炎性细胞因子的释放
RTX组大鼠脊髓背角组织中SP、CGRP、IL-6和IL-1β水平较Vehicle组显著升高(P<0.05)。Sham-EA组与RTX组比较,上述指标水平均无统计学差异(P > 0.05)。与RTX组比较,EA组SP、CGRP、IL-6和IL-1β水平显著降低(P<0.05)。EA+ABR-215757组上述指标水平较EA组显著降低(P<0.05)。见表 2。
2.6 电针治疗抑制S100A9/TLR4/NF-κB信号通路的激活与Vehicle组比较,RTX组大鼠脊髓背角组织中S100A9、TLR4、p-p65和p65表达水平显著升高(P<0.05)。RTX组与Sham-EA组比较,上述蛋白表达水平均无统计学差异(P > 0.05)。与RTX组比较,EA组大鼠脊髓背角组织中S100A9、TLR4、p-p65和p65表达水平显著降低(P<0.05)。与EA组比较,EA+ABR-215757组S100A9、TLR4、p-p65和p65表达水平进一步降低(P<0.05)。这些结果表明,电针能够抑制S100A9/TLR4/NF-κB信号通路的激活。见表 3、图 3。
| Group | n | S100A9 | TLR4 | p-p65 | p65 |
| Vehicle | 10 | 0.78±0.08 | 0.34±0.04 | 0.28±0.03 | 0.52±0.04 |
| RTX | 10 | 1.64±0.171) | 1.17±0.121) | 1.14±0.121) | 0.93±0.071) |
| Sham-EA | 10 | 1.59±0.16 | 1.08±0.11 | 1.08±0.10 | 0.89±0.05 |
| EA | 10 | 0.87±0.092) | 0.76±0.082) | 0.64±0.062) | 0.67±0.062) |
| EA+ ABR-215757 | 10 | 0.61±0.063) | 0.43±0.053) | 0.39±0.043) | 0.45±0.043) |
| 1)P<0.05 vs. Vehicle group;2)P<0.05 vs. RTX group;3)P<0.05 vs. EA group. | |||||
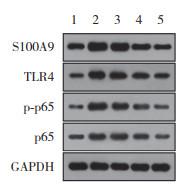
|
| 1, Vehicle group; 2, RTX group; 3, Sham-EA group; 4, EA group; 5, EA+ABR215757. 图 3 大鼠脊髓背角组织中S100A9、TLR4、p-p65、p65蛋白的表达 Fig.3 Expression of S100A9, TLR4, p-p65, and p65 proteins in the spinal dorsal horn tissue of rats |
3 讨论
针灸为中医治疗的有效手段,在缓解神经病理性疼痛方面发挥重要作用,具有见效快、安全性高、价格低廉等优点,其中电针治疗神经病理性疼痛的疗效显著[3]。星形胶质细胞参与维持中枢神经系统稳态,其介导的神经炎症是影响神经病理性疼痛的关键机制之一,可按功能分A1(促炎)和A2(抗炎)两个极化表型[13]。研究[14]证实,抑制星形胶质细胞活化是缓解神经病理性疼痛的有效途径。本研究证实,电针通过影响星形胶质细胞中S100A9/TLR4/NF-κB通路活化,进而调控神经病理性疼痛大鼠的症状。
RTX通过消融表达受体电位香草酸1的无髓鞘传入神经元,促进病理性神经发芽和重组来模拟神经病理性疼痛的症状,被广泛用于构建神经病理性疼痛模型[15]。本研究发现,电针治疗通过缓解神经病理性疼痛大鼠的痛感,并减轻脊髓背角组织的损伤,抑制细胞凋亡和星形胶质细胞活化,并使星形胶质细胞从A1型到A2型极化,减少炎性细胞因子释放,改善RTX诱导的神经病理性疼痛损伤。
S100A9作为一种典型的DAMP分子,通过与TLR4受体结合激活NF-κB通路,释放肿瘤坏死因子α、IL-6、IL-1β等炎性细胞因子,最终触发促炎级联放大,影响神经炎症和星形胶质细胞极化[7, 10]。本研究中,RTX使星形胶质细胞中的S100A9/TLR4/ NF-κB通路处于激活状态,而电针治疗能够通过抑制此通路的激活来调控神经病理性疼痛进展。此外,与EA组比较,EA+ABR-215757组大鼠的疼痛症状和脊髓损伤改善更显著,同时伴随着S100A9、TLR4、p-p65、p65蛋白水平下降。这些发现表明,抑制S100A9/TLR4/NF-κB通路的激活能够有效改善神经病理性疼痛进展。
综上所述,本研究证实,电针治疗能够通过S100A9/TLR4/NF-κB通路抑制星形胶质细胞活化,从而改善神经病理性疼痛的病理状态。S100A9/TLR4/NF-κB信号通路可能与其他通路相互作用,未来研究可以进一步探究S100A9/TLR4/NF-κB通路与其他通路间的相互作用,以更全面地了解电针改善神经病理性疼痛的机制。
| [1] |
张龙, 赵劲松, 周丽, 等. 脊髓脆性X智力低下蛋白和β-连环蛋白参与神经病理性疼痛的机制[J]. 中国医学科学院学报, 2025, 47(4): 509-518. DOI:10.3881/j.issn.1000-503X.16494 |
| [2] |
蒋庆, 衣增玮, 刘茂桐, 等. 神经病理性疼痛病人疼痛灾难化研究进展[J]. 中国疼痛医学杂志, 2025, 31(5): 366-370. DOI:10.13820/j.cnki.gdyx.2015.01.022 |
| [3] |
辛欢, 邹璟, 乐薇. 电针通过cGAS-STING通路影响小胶质细胞介导的带状疱疹后神经痛[J]. 中国医科大学学报, 2025, 54(3): 208-213. DOI:10.12007/j.issn.0258-4646.2025.03.004 |
| [4] |
JIANG D, ZHANG Z, REN F, et al. S100A8/A9 in herpes zoster neuralgia: molecular mechanisms and therapeutic perspectives[J]. Front Immunol, 2025, 16: 1615638. DOI:10.3389/fimmu.2025.1615638 |
| [5] |
JING B, ZHAO JJ, CHEN ZN, et al. (+)-Catechin alleviates CCI-induced neuropathic pain by modulating microglia M1 and M2 polarization via the TLR4/MyD88/NF-κB signaling pathway[J]. J Neuroimmune Pharmacol, 2025, 20(1): 33. DOI:10.1007/s11481-025-10202-9 |
| [6] |
YE J, ZHONG S, DENG Y, et al. HDAC7 activates IKK/NF-κB signaling to regulate astrocyte-mediated inflammation[J]. Mol Neurobiol, 2022, 59(10): 6141-6157. DOI:10.1007/s12035-022-02965-6 |
| [7] |
周鑫, 白巧, 张小印, 等. S100A9通过TLR4/NF-κB信号通路活化星形胶质细胞促进炎症反应[J]. 基因组学与应用生物学, 2022, 41(5): 1103-1111. DOI:10.13417/j.gab.041.001103 |
| [8] |
刘姣, 林采玥, 梁弘, 等. 壮医药线点灸对带状疱疹后遗神经痛模型大鼠中枢神经系统Th1/Th2/Th17细胞平衡的影响[J]. 世界科学技术-中医药现代化, 2024, 26(7): 1749-1764. DOI:10.11842/wst.20230531008 |
| [9] |
LI HP, SU W, SHU Y, et al. Electroacupuncture decreases Netrin-1-induced myelinated afferent fiber sprouting and neuropathic pain through μ-opioid receptors[J]. J Pain Res, 2019, 12: 1259-1268. DOI:10.2147/JPR.S191900 |
| [10] |
SILVA CR, MELO BMS, SILVA JR, et al. S100A9 plays a pivotal role in a mouse model of herpetic neuralgia via TLR4/TNF pathway[J]. Brain Behav Immun, 2020, 88: 353-362. DOI:10.1016/j.bbi.2020.03.033 |
| [11] |
NAIR A, MORSY MA, JACOB S. Dose translation between laboratory animals and human in preclinical and clinical phases of drug development[J]. Drug Dev Res, 2018, 79(8): 373-382. DOI:10.1002/ddr.21461 |
| [12] |
HARGREAVES K, DUBNER R, BROWN F, et al. A new and sensitive method for measuring thermal nociception in cutaneous hyperalgesia[J]. Pain, 1988, 32(1): 77-88. DOI:10.1016/0304-3959(88)90026-7 |
| [13] |
JI RR, DONNELLY CR, NEDERGAARD M. Astrocytes in chronic pain and itch[J]. Nat Rev Neurosci, 2019, 20(11): 667-685. DOI:10.1038/s41583-019-0218-1 |
| [14] |
KONG C, DU J, BU H, et al. LncRNA KCNA2-AS regulates spinal astrocyte activation through STAT3 to affect postherpetic neuralgia[J]. Mol Med, 2020, 26(1): 113. DOI:10.1186/s10020-020-00232-9 |
| [15] |
HIDAKA K, MARUTA T, KOSHIDA T, et al. Extracellular signal-regulated kinase phosphorylation enhancement and NaV1.7 sodium channel upregulation in rat dorsal root ganglia neurons contribute to resiniferatoxin-induced neuropathic pain: the efficacy and mechanism of pulsed radiofrequency therapy[J]. Mol Pain, 2022, 18: 17448069221089784. DOI:10.1177/17448069221089784 |
 2025, Vol. 54
2025, Vol. 54