文章信息
- 庞娟, 杨维, 殷俊茹, 尚粉青
- PANG Juan, YANG Wei, YIN Junru, SHANG Fenqing
- miR-92a-3p通过抑制SIRT1参与缺血性脑卒中的发生
- Effect of miR-92a-3p on the progression of ischemic stroke via SIRT1 suppression
- 中国医科大学学报, 2025, 54(11): 977-981
- Journal of China Medical University, 2025, 54(11): 977-981
-
文章历史
- 收稿日期:2025-05-22
- 网络出版时间:2025-11-21 13:04:41
2. 西北大学附属胸科医院麻醉科, 西安 710100;
3. 西北大学附属胸科医院心血管内科, 西安 710100
2. Department of Anesthesiology, Affiliated Chest Hospital of Northwest University, Xi'an 710100, China;
3. Department of Cardiovascular Medicine, Affiliated Chest Hospital of Northwest University, Xi'an 710100, China
2019年世界卫生组织全球疾病负担评估报告[1]显示,脑卒中是全球第二大死亡原因。脑卒中分为缺血性脑卒中(ischemic stroke,IS)和出血性脑卒中,其中IS约占所有脑卒中的87%[2-3]。缺血引起的神经元丢失,血管阻塞导致的活性氧过度产生,以及缺血导致的炎症是IS导致神经元损伤的主要机制[4]。及时成功的再灌注是对急性脑卒中患者最有效的治疗方法[5]。
微RNA(microRNA,miRNA)是长度约为22个碱基的非编码RNA,通过与信使RNA的3’非翻译区结合,抑制信使RNA的翻译或降解信使RNA,在转录后水平调控基因表达[6]。miRNA已经被证明参与IS的神经元凋亡、神经元兴奋毒性、神经炎症和血管新生等过程[7]。本研究拟通过公共数据库分析和实验验证探讨miR-92a-3p及其靶基因沉默信息调节因子1(silent information regulator 1,SIRT1)[8]参与IS的分子机制,以期为IS的治疗提供新的治疗靶点和思路。
1 材料与方法 1.1 材料 1.1.1 试剂DMEM完全培养基、无糖培养基(上海瑾原生物科技有限公司),SIRT1和caspase-3抗体(美国CST公司),GAPDH抗体(美国Santa Cruz公司),辣根过氧化物酶标记山羊抗兔、山羊抗鼠二抗(美国Jackson公司),PVDF膜(瑞士Roche公司),彩色预染蛋白质分子量标准品、lipofectamine 2000转染试剂(美国Thermol Fisher公司),BCA蛋白定量试剂盒、快速凝胶配制试剂盒、ECL化学发光液(上海碧云天生物技术股份有限公司),PCR引物(北京擎科生物科技股份有限公司),荧光定量PCR预混液(北京康润诚业生物科技有限公司)。
1.1.2 仪器实时定量PCR仪(西安天隆科技有限公司),酶标仪(美国BioTek公司),缺氧小室(黑龙江迈沃德工贸有限公司)。
1.1.3 细胞小鼠海马神经元细胞系HT22(上海瑾原生物科技有限公司),培养于DMEM完全培养基,置于37 ℃、5%CO2培养箱内连续培养,每1~2 d传代1次,取对数生长期细胞进行实验。将细胞随机分为对照组与氧糖剥夺组(OGD/R组)。
1.1.4 实验动物SPF级C57BL/6J小鼠12只,雄性,6~8周龄,体重20~25 g,购自西安交通大学,在室温25 ℃、自由摄食、自由饮水和12 h昼夜交替的条件下饲养。将小鼠随机分为对照组与大脑中动脉栓塞(middle cerebral artery occlusion,MCAO)组,每组6只。本研究涉及的动物实验获得西北大学附属胸科医院的动物伦理审查批准(2024PS1926K)。
1.2 方法 1.2.1 数据库数据分析在基因表达综合(Gene Expression Omnibus,GEO)数据库(https://www.ncbi.nlm.nih.gov/geo/)中,以IS和miRNA为关键词搜索miRNA表达研究,将包含正常样本、IS样本的细胞或脑组织纳入数据集,从GEO数据库中下载GSE213067和GSE215212数据集,对数据集中的目标miRNA表达进行分析。
1.2.2 miRNA靶基因预测使用miRWalk3.0(http://mirwalk.umm.uni-heidelberg.de/),输入miRNA名称和基因标识符,选择靶基因的结合区域3’非翻译区(主要调控区域)、5’非翻译区、CDS(编码区)和启动子区(需单独勾选),选择种属后查询miRNA与其靶基因的结合位点。
1.2.3 MCAO小鼠模型制作MCAO组小鼠术前禁食8 h [9]。吸入异氟烷麻醉后,将小鼠仰卧位固定于恒温手术台,沿颈中线纵向切开约0.8~1 cm,钝性分离肌肉和筋膜,在颈总动脉远心端和近心端挂线备用,用动脉夹暂时夹闭颈内动脉,近心端结扎颈外动脉和颈总动脉,在距颈总动脉4 mm处与血管呈45°角剪1个V形小切口,插入线栓,用颈总动脉远心端的手术线轻系线栓,松开颈内动脉的动脉夹,用镊子轻推线栓直至遇到阻力,大约推进9 mm即到达大脑中动脉与大脑前动脉的交叉处,系牢颈总动脉远心端的手术线,缝合皮肤[10]。
1.2.4 HT22细胞氧糖剥夺模型制作待OGD/R组HT22细胞培养至70%融合,弃完全培养基,用PBS洗涤,加入无糖培养基,置于含95%N2和5%CO2的缺氧小室中培养2、4、6、8 h后,更换无糖培养基为DMEM完全培养基,并置于含20%O2和5%CO2的培养箱中继续培养24 h后用于实验。
1.2.5 Western blotting收集HT22细胞或小鼠脑组织,提取总蛋白并进行蛋白定量,加入上样缓冲液,金属浴100 ℃变性5 min后,进行电泳分离,将分离胶上的蛋白用电泳仪转移至PVDF膜,2.5%脱脂牛奶封闭后,加入一抗(SIRT1和caspase-3抗体稀释1∶1 000,GAPDH抗体稀释1∶2 000),4 ℃孵育过夜,TBST洗膜,加入二抗(稀释1∶10 000),室温孵育2 h,洗涤后进行ECL化学发光显影。
1.2.6 实时定量PCR提取细胞或脑组织RNA进行反转录。miRNA反转录体系:10×RT缓冲液0.5 µL,RNase抑制剂0.063 µL,100 mmol/L dNTP 0.05 µL,反转录酶0.33 µL,10 µmol/L反转录引物1 µL,RNA 1.06 µL,用DEPC水补齐至5 μL。反转录程序:16 ℃ 30 min;42 ℃ 40 min;85 ℃ 5 min;4 ℃保存。miRNA扩增体系15 µL:终浓度10 µmol扩增引物0.75 µL,Promega试剂盒中Q-PCR预混物7.5 µL,cNDA 6.75 µL。mRNA反转录体系:5×预混物4 µL,RNA 1 µg,用DEPC水补齐至20 µL。反转录程序:25 ℃ 10 min;50 ℃ 30 min;85 ℃ 5 min;4 ℃ 2 h。mRNA扩增体系20 µL:终浓度1 µmol/L扩增引物5 µL,预混物10 µL,cDNA5 µL。反应条件:95 ℃ 2 min;95 ℃ 15 s,60 ℃ 30 s,40个循环。引物序列见表 1。
| Gene | Primer sequence |
| miR-92a-3p | |
| RT | 5’-CTCAACTGGTGTCGTGGAGTCGGCAATTCAGTTGAGACAGGCCG-3’ |
| Forward | 5’-ACACTCCAGCTGGGATATTGCACTTGTCCC-3’ |
| Reverse | 5’-CTGGTGTCGTGGAGTCGG-3’ |
| SIRT1 | |
| Forward | 5’-GCTGACGACTTCGACGACG-3’ |
| Reverse | 5’-TCGGTCAACAGGAGGTTGTCT-3’ |
| Caspase-3 | |
| Forward | 5’-ATGGAGAACAACAAAACCTCAGT-3’ |
| Reverse | 5’-TTGCTCCCATGTATGGTCTTTAC-3’ |
| β-actin | |
| Forward | 5’-AACAGTCCGCCTAGAAGCAC-3’ |
| Reverse | 5’-CGTTGACATCCGTAAAGACC-3’ |
1.2.7 细胞转染
将HT22细胞接种于6孔板,细胞融合度为80%时进行转染。将无血清培养基分别与lipofectamine 2000和miR-92a-3p抑制剂或miR-92a-3p抑制剂NC混合,室温静置5 min后将两者混合,混合液静置20 min后加入6孔板,6 h后更换为无糖培养基,并在缺氧小室(含氧量0)中培养4 h后,更换为含糖培养基,并于含氧量20%的培养箱中继续培养24 h后提取蛋白,进行Western blotting检测。
1.3 统计学分析采用GraphPad Prism软件进行统计学分析。计量资料用x±s表示,同一变量多组间比较采用单因素方差分析,2组间比较采用独立样本t检验,P < 0.05为差异有统计学意义。
2 结果 2.1 GEO数据库分析结果对GSE213067数据集分析发现,相比正常培养条件(13.72±0.09),氧糖剥夺12 h培养的胎鼠皮质神经元miR-92a-3p表达(14.66±0.29)升高(P < 0.001)。对GSE215212数据集分析发现,相比假手术组(137.2±37.84),永久性MCAO 3 d后小鼠脑组织miR-92a-3p表达(194.0±35.52)升高(P = 0.039 7)。
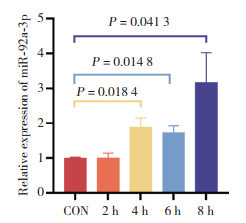
2.2 氧糖剥夺后HT22细胞miR-92a-3p表达升高用HT22细胞氧糖剥夺模拟IS,分别缺糖缺氧培养2、4、6、8 h后更换为含糖培养基,并放入正常氧含量培养箱继续培养24 h后收集细胞,实时定量PCR分析细胞中miR-92a-3p的表达,结果显示,氧糖剥夺4 h后miR-92a-3p表达开始显著升高(图 1),因此,后续实验使用4 h作为细胞IS模型时间节点。
|
| CON, control group. 图 1 HT22细胞氧糖剥夺后miR-92a-3p表达升高 Fig.1 Up-regulation of miR-92a-3p expression in HT22 cells after OGD/R |
2.3 氧糖剥夺后HT22细胞内miR-92a-3p靶基因SIRT1表达降低
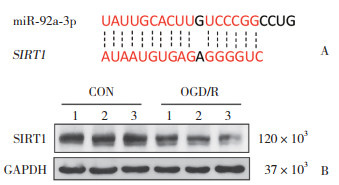
用miRWalk预测miR-92a-3p可与SIRT1的3’非翻译区区域结合(图 2),表明miR-92a-3p靶基因为SIRT1。实时定量PCR和Western blotting结果显示,OGD/R组HT22细胞SIRT1 mRNA(0.499±0.266)和蛋白(0.601±0.164)表达水平均较对照组mRNA(1.089±0.431)和蛋白(0.823±0.021)表达水平降低(P = 0.004 5,P = 0.038 4),凋亡基因caspase-3 mRNA(1.400±0.475)表达水平均较对照组(1.047±0.262)升高(P = 0.047 1)。提示HT22细胞氧糖剥夺后miR-92a-3p表达升高,促进SIRT1降解和细胞凋亡,从而促进IS的发生。
|
| A, binding site of miR-92a-3p on the 3'UTR region of SIRT1 predicted by miRWalk; B, Western blotting results. 图 2 HT22细胞氧糖剥夺后SIRT1表达降低并促进神经元凋亡 Fig.2 Reduced SIRT1 expression after OGD/R in HT22 cells promotes neuronal apoptosis |
2.4 MCAO小鼠模型脑组织中miR-92a-3p的靶基因SIRT1表达降低
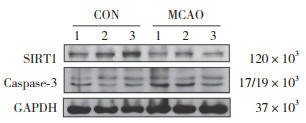
采用实时定量PCR和Western blotting检测MCAO组与对照组小鼠脑组织中miR-92a-3p靶基因SIRT1 mRNA和蛋白的表达情况,结果(图 3)显示,MCAO组小鼠脑组织中SIRT1 mRNA(0.877±0.080)和蛋白(0.315±0.074)表达水平均较对照组mRNA(1.040±0.175)和蛋白(0.644±0.191)表达水平降低(P = 0.044 8,P = 0.049 7),caspase-3 mRNA(1.830±0.180)和蛋白(0.524±0.113)表达水平均较对照组mRNA(0.853±0.103)和蛋白(0.367±0.041)表达水平升高(P < 0.000 1,P = 0.036)。提示miR-92a-3p能促进MCAO小鼠脑组织中SIRT1降解和细胞凋亡,从而参与IS的发生。
|
| 图 3 MCAO小鼠脑组织中SIRT1表达降低并促进神经元凋亡 Fig.3 Decreased SIRT1 expression promotes neuronal apoptosis in MCAO mouse |
2.5 抑制miR-92a-3p可逆转氧糖剥夺HT22细胞的凋亡
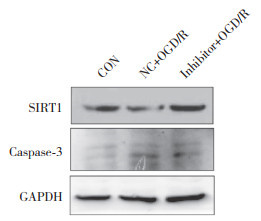
HT22细胞转染miR-92a-3p抑制剂后进行氧糖剥夺,用Western blotting检测SIRT1和caspase-3蛋白表达,结果(图 4)显示,miR-92a-3p被抑制后,SIRT1蛋白表达(0.675±0.011)较miR-92a-3p NC组(1.591±0.155)升高(P = 0.018),caspase-3蛋白表达(1.240±0.048)较miR-92a-3p NC组(0.957±0.013)降低(P = 0.011)。证明抑制miR-92a-3p后逆转了氧糖剥夺HT22细胞的凋亡。
|
| 图 4 抑制miR-92a-3p后逆转了氧糖剥夺HT22细胞的凋亡 Fig.4 Inhibition of miR-92a-3p reversed apoptosis in OGD/R-treated HT22 cells |
3 讨论
IS的发生涉及复杂的病理生理过程,而miRNA作为一类重要的基因表达调控分子,参与了IS炎症反应、神经元凋亡和神经元生成[11-12]。内皮细胞来源的外泌体miR-92a-3p可以通过调节内皮细胞和血管平滑肌细胞之间的信号转导促进动脉硬化[13],并与慢性肾脏病、阻塞性睡眠呼吸暂停、心血管疾病等多种疾病密切相关[14]。脑血管动脉硬化斑块导致的脑血管狭窄是IS的病理机制之一[15]。有文献[16]报道,作为miR-92a-3p的靶基因,SIRT1在IS中发挥保护作用。鉴于miR-92a-3p在血管疾病中的重要作用,推测miR-92a-3p可能通过调控SIRT1影响IS。本研究通过GEO数据库分析和实验验证,证明miR-92a-3p通过抑制SIRT1表达促进神经元细胞凋亡。因此,推测miR-92a-3p/SIRT1轴通过多种途径参与IS的病理过程。一方面,SIRT1的抑制可能导致细胞内氧化应激反应增强,产生过多的活性氧,损伤细胞的生物膜、蛋白质和核酸等生物大分子,最终导致神经元和神经胶质细胞的死亡[17];另一方面,SIRT1的抑制可能激活炎症信号通路,增加炎性细胞因子释放,引发过度的炎症反应,进一步加重脑损伤[18]。此外,miR-92a-3p/SIRT1轴还可能影响细胞的能量代谢,干扰细胞的正常生理功能[19]。已有研究[20]表明,天然多酚类物质白藜芦醇可以作为IS的神经保护剂,通过激活SIRT1途径发挥神经保护作用。这些作用机制相互交织,共同推动IS的发生发展。
本研究仍存在一定的局限性。首先,仅在动物模型和细胞实验中初步探讨了miR-92a-3p/SIRT1轴与IS的关系,未来需要开展大规模的临床研究,以明确miR-92-3p和SIRT1作为IS诊断标志物和治疗靶点的可行性和有效性。其次,对于miR-92a-3p/SIRT1轴下游信号通路和分子机制还需要进一步深入研究。
综上所述,本研究发现,miR-92a-3p通过抑制SIRT1表达促进神经元凋亡,参与IS的发生,为IS的发病机制提供了新的思路。进一步深入研究miR-92a-3p/SIRT1轴与其他信号通路之间的相互作用,有助于更全面地理解IS的发病机制,为开发更有效的治疗方法奠定基础。
| [1] |
FEIGIN VL, BRAININ M, NORRVING B, et al. World stroke orga-nization (WSO): global stroke fact sheet 2022[J]. Int J Stroke, 2022, 17(1): 18-29. DOI:10.1177/17474930211065917 |
| [2] |
TSAO CW, ADAY AW, ALMARZOOQ ZI, et al. Heart disease and stroke statistics-2022 update: a report from the American heart association[J]. Circulation, 2022, 145(8): e153-e639. DOI:10.1161/CIR.0000000000001052 |
| [3] |
FANG J, WANG Z, MIAO CY. Angiogenesis after ischemic stroke[J]. Acta Pharmacol Sin, 2023, 44(7): 1305-1321. DOI:10.1038/s41401-023-01061-2 |
| [4] |
ZHAO YF, ZHANG XJ, CHEN XY, et al. Neuronal injuries in cerebral infarction and ischemic stroke: from mechanisms to treatment (Review)[J]. Int J Mol Med, 2022, 49(2). DOI:10.3892/ijmm.2021.5070.DOI:10.3892/ijmm.2021.5070 |
| [5] |
RABINSTEIN AA. Update on treatment of acute ischemic stroke[J]. Continuum, 2020, 26(2): 268-286. DOI:10.1212/CON.0000000000000840 |
| [6] |
TODORAN R, FALCIONE SR, CLARKE M, et al. microRNA as a therapeutic for ischemic stroke[J]. Neurochem Int, 2023, 163: 105487. DOI:10.1016/j.neuint.2023.105487 |
| [7] |
CHEN W, SINHA B, LI Y, et al. Monogenic, polygenic, and micro-RNA markers for ischemic stroke[J]. Mol Neurobiol, 2019, 56(2): 1330-1343. DOI:10.1007/s12035-018-1055-3 |
| [8] |
AHMED FF, REZA MS, SARKER MS, et al. Identification of host transcriptome-guided repurposable drugs for SARS-CoV-1 infections and their validation with SARS-CoV-2 infections by using the integrated bioinformatics approaches[J]. PLoS One, 2022, 17(4): e0266124. DOI:10.1371/journal.pone.0266124 |
| [9] |
陈宏洋, 王泽楠, 王海璎, 等. 线栓法制备小鼠大脑中动脉闭塞再灌注模型影响因素分析[J]. 河南大学学报(自然科学版), 2022, 52(5): 552-558. DOI:10.15991/j.cnki.411100.2022.05.007 |
| [10] |
CHIANG T, MESSING RO, CHOU WH. Mouse model of middle cerebral artery occlusion[J]. J Vis Exp, 2011(48): e2761. DOI:10.3791/2761 |
| [11] |
KIM JM, BYUN JS, KIM J, et al. Analysis of microRNA signatures in ischemic stroke thrombus[J]. J Neurointerv Surg, 2022, 14(5): neurintsurg-2021-017597. DOI:10.1136/neurintsurg-2021-017597 |
| [12] |
杨利强, 关欣, 徐伟杰, 等. microRNA在缺血性脑卒中发生发展及其诊断治疗中的作用研究进展[J]. 中国老年学杂志, 2022, 42(10): 2540-2543. DOI:10.3969/j.issn.1005-9202.2022.10.061 |
| [13] |
WANG C, WU HY, XING YM, et al. Endothelial-derived extracellular microRNA-92a promotes arterial stiffness by regulating phenotype changes of vascular smooth muscle cells[J]. Sci Rep, 2022, 12(1): 344. DOI:10.1038/s41598-021-04341-1 |
| [14] |
SHANG FQ, WANG SC, HSU CY, et al. microRNA-92a mediates endothelial dysfunction in CKD[J]. J Am Soc Nephrol, 2017, 28(11): 3251-3261. DOI:10.1681/ASN.2016111215 |
| [15] |
JIA J, JIAO WJ, WANG G, et al. Drugs/agents for the treatment of ischemic stroke: advances and perspectives[J]. Med Res Rev, 2024, 44(3): 975-1012. DOI:10.1002/med.22009 |
| [16] |
舒梦琦, 戴瑶瑶, 宋丽娟, 等. 基于SIRT1/VEGFA信号通路探讨川芎嗪调节缺血性脑卒中损伤后血管内皮细胞的新生作用研究[J]. 中国中药杂志, 2024, 49(1): 162-174. DOI:10.19540/j.cnki.cjcmm.20231116.303 |
| [17] |
YAN WJ, SUN W, FAN JH, et al. Sirt1-ROS-TRAF6 signaling-induced pyroptosis contributes to early injury in ischemic mice[J]. Neurosci Bull, 2020, 36(8): 845-859. DOI:10.1007/s12264-020-00489-4 |
| [18] |
LI M, LI SC, DOU BK, et al. Cycloastragenol upregulates SIRT1 expression, attenuates apoptosis and suppresses neuroinflammation after brain ischemia[J]. Acta Pharmacol Sin, 2020, 41(8): 1025-1032. DOI:10.1038/s41401-020-0386-6 |
| [19] |
ZHU T, XIE WJ, WANG L, et al. Notoginsenoside R1 activates the NAMPT-NAD+-SIRT1 cascade to promote postischemic angiogenesis by modulating Notch signaling[J]. Biomed Pharmacother, 2021, 140: 111693. DOI:10.1016/j.biopha.2021.111693 |
| [20] |
OWJFARD M, RAHIMIAN Z, KARIMI F, et al. A comprehensive review on the neuroprotective potential of resveratrol in ischemic stroke[J]. Heliyon, 2024, 10(14): e34121. DOI:10.1016/j.heliyon.2024.e34121 |
 2025, Vol. 54
2025, Vol. 54