文章信息
- 耿建芳, 李蕾, 史雅静, 王俊耐, 肖婷伟, 奈嫚嫚
- GENG Jianfang, LI Lei, SHI Yajing, WANG Junnai, XIAO Tingwei, NAI Manman
- PLA2G2A在盆腔器官脱垂患者阴道壁中的表达及意义
- Expression of PLA2G2A and its significance in the vaginal wall of patients with pelvic organ prolapse
- 中国医科大学学报, 2025, 54(11): 1042-1047
- Journal of China Medical University, 2025, 54(11): 1042-1047
-
文章历史
- 收稿日期:2024-12-11
- 网络出版时间:2025-11-21 13:02:50
盆腔器官脱垂(pelvic organ prolapse,POP)是盆底肌肉和筋膜组织异常引起的盆底支持结构缺陷,表现为盆腔器官脱垂于阴道内或阴道外,可伴有排尿、排便和性功能障碍[1]。目前,症状性POP的患病率为3%~6%,其中50%的女性发生解剖性脱垂[2]。POP对患者的生活质量及心理健康产生严重影响[3]。
雌激素水平下降及盆底支持结构的机械损伤是POP的主要发病机制[2],研究[4]显示遗传易感基因也是POP发生的关键因素。POP患者表现出家族聚集性[5],研究[6]发现POP家族史增加了POP发生和复发的风险,JELOVSEK等[7]对POP发展进行了预测模型研究,发现POP家族史是仅次于分娩途径的重要预测因素。
已有研究[8]对POP患者和正常对照组子宫骶韧带样本进行转录组测序(RNA sequencing,RNA-seq),对差异表达基因进行功能注释分析和蛋白质-蛋白质相互作用网络构建,认为PLA2G2A基因在POP中发挥重要作用。本研究检测了POP患者阴道壁中PLA2G2A的表达情况,初步探讨了PLA2G2A在POP发生发展中的作用及意义。
1 材料与方法 1.1 材料 1.1.1 研究对象选取2023年6月至2024年10月于郑州大学第三附属医院住院并行妇科手术治疗的患者49例。其中,因POP行子宫切除术或盆底重建术的患者(POP组)26例,POP定量(Pelvic Organ Prolapse Quantification,POP-Q)评分均为Ⅲ~Ⅳ度;因非POP(子宫腺肌症、子宫肌瘤或宫颈高级别上皮内病变)行子宫切除的患者(对照组)23例,POP-Q评分均为0~Ⅰ度。2组临床资料均完整。排除标准:(1)子宫内膜异位症;(2)多囊卵巢综合征;(3)免疫疾病或结缔组织病;(4)恶性肿瘤;(5)近3个月有泌尿生殖系统感染;(6)激素替代治疗史;(7)盆底手术史。本研究获得郑州大学第三附属医院伦理委员会批准[伦审编号2023-(预)217-01],患者均签署知情同意书。
1.1.2 主要试剂PLA2G2A抗体(成都正能生物技术有限责任公司),collagen Ⅰ抗体、collagen Ⅲ抗体(武汉三鹰生物技术有限公司),β-actin抗体(武汉塞维尔生物科技有限公司),辣根过氧化物酶标记山羊抗兔IgG抗体(上海碧云天生物技术股份有限公司),DAB显色液(北京中杉金桥技术有限公司),ECL超敏better发光液(郑州源培生物科技有限公司),人原代阴道成纤维细胞(上海葵赛生物科技有限公司)。
1.2 方法 1.2.1 GEO数据集筛选差异基因在GEO数据库(http://ncbi.nlm.nih.gov/geo/)筛选出3个POP相关数据集(GSE12852、GSE28660和GSE208261),分别将数据集中POP组及非POP组分组取差异基因并下载结果,通过Microsoft Excel 2021设置筛选条件:P<0.05且|Log2FC|≥2。
1.2.2 标本选择及处理切除子宫后立即取阴道壁组织,样本标记后分为3份,一份置于10%甲醛固定液中,用于组织学分析;一份置于RNA保存液中放入4 ℃冰箱,次日转至-80 ℃冰箱保存,用于RNA提取;一份放入液氮转运至-80 ℃冰箱保存,用于组织蛋白提取。
1.2.3 HE及Masson染色将甲醛固定液中的阴道壁组织脱水、透明、浸蜡、包埋,使用切片机将其制作成5 μm的组织切片,将切片置于45 ℃恒温水箱中展平,载玻片依次捞取切片后置于60 ℃恒温烤箱中烘烤,并进行HE染色和Masson染色。镜下观察阴道壁组织学特征和胶原纤维沉积分布。
1.2.4 免疫荧光检测切片处理同HE染色,贴片后经1%PBS-Triton X浸泡后使用抗原修复液(pH9.0)进行抗原修复,5%牛血清白蛋白(bovine serum albumin,BSA)封闭非特异性抗体30 min,使用5%BSA将PLA2G2A抗体稀释100倍滴加于组织切片(1∶100),置于4 ℃冰箱过夜,次日二抗(1∶50)孵育后显色,在荧光显微镜下观察,明确PLA2G2A蛋白的定位和分布。
1.2.5 免疫组织化学检测第1天操作处理同免疫荧光,使用5%BSA将PLA2G2A抗体稀释200倍(1∶200),次日经二抗孵育后DAB显色,经过苏木素复染细胞核,分化返蓝,水化后封片。在显微镜下每个切片随机选择5个不重叠区域,PLA2G2A的阳性表达呈黄褐色。使用Image Pro plus软件图像系统分析拍照分析,计算PLA2G2A的阳性面积百分比。
1.2.6 实时PCR检测使用TRIzol法提取人阴道壁RNA,共选取阴道壁对照组6例,POP组5例,根据东洋纺(上海)生物科技有限公司提供的cDNA逆转录试剂盒(FSQ-101)建立PCR,将反转录得到的cDNA与10 μL UltraSYBR Mixture(2×),0.4 μL PLA2G2A引物在ddH2O中混合,最终体系为20 μL,反应条件为95 ℃孵育10 min预变性,循环35~40次,95 ℃ 15 s变性,60 ℃ 1 min退火延伸。以GAPDH为内参,计算每个样本目的基因和内参基因3个复孔Ct值的平均数,采用2-ΔΔCt法计算目标基因的相对表达量。引物序列如下:PLA2G2A,正向5’-GAAAGGAAGCCGAACTCAGTTAT-3’,反向5’-GCTCAGAAATTTGGTGCCACATC-3’;GAPDH,正向5-GGAGTCCACTGGCGTCTTCA-3’,反向5’-GTCATGAGTCCTTCCACGATACC-3’。
1.2.7 Western boltting检测于-80 ℃冰箱取出对照组和POP组各15例阴道壁提取蛋白,置于SDS-PAGE凝胶中电泳,将PDVF膜浸泡于甲醇中3 s以激活PDVF膜,转膜后5%脱脂牛奶封闭2 h,5%脱脂牛奶稀释一抗(β-actin为1∶500;PLA2G2A为1∶1 000),4 ℃冰箱孵育过夜。次日加入二抗孵育后曝光显影。使用Fiji软件测量各条带灰度值,结果取目的蛋白与β-actin条带灰度值比值。
1.2.8 人阴道壁原代成纤维细胞系沉默PLA2G2A后检测collagen Ⅰ和collagen Ⅲ表达脱垂患者阴道壁组织的原代成纤维细胞系经波形蛋白免疫荧光染色为阳性,培养至4~6代,使用靶向PLA2G2A的siRNA序列条带处理细胞,引物序列见表 1,以上siRNA由苏州吉玛股份有限公司化学合成,使用siRNA-Mate将对照组和含有siRNA的载体转染到成纤维细胞中,提取RNA进行实时PCR检测,提取蛋白进行Western boltting检测,一抗稀释比例PLA2G2A(1∶1 000),collagen Ⅰ(1∶2 000),collagen Ⅲ(1∶1 000),条带分析方法同1.2.7。
| siRNA | Primer sequences(5’-3’) |
| siRNA-291 | Foward:AUGAAGACCCUCCUACUGUTT |
| Reverse:ACAGUAGGAGGGUCUUCAUTT | |
| siRNA-400 | Foward:GCACUCAGUUAUGGCUUCUTT |
| Reverse:AGAAGCCAUAACUGAGUGCTT | |
| siRNA-477 | Foward:CUGUGUCACUCAUGACUGUTT |
| Reverse:ACAGUCAUGAGUGACACAGTT | |
| siRNA-657 | Foward:CCAGUACUAUUCCAAUAAATT |
| Reverse:UUUAUUGGAAUAGUACUGGTT | |
| GAPDH | Foward:UGACCUCAACUAVAUGGUUTT |
| Reverse:AACCAUGUAGUUGAGGUCATT |
1.3 统计学分析
采用SPSS 26.0软件进行数据分析,符合正态分布的数据以x±s表示,组间比较采用独立样本t检验,不符合正态分布的数据以M(P25~P75)表示,组间比较采用Mann-Whitney U检验。P<0.05为差异有统计学意义。
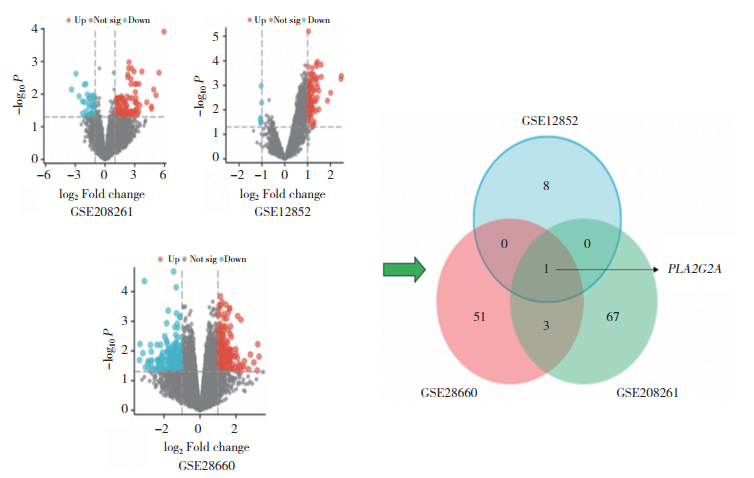
2 结果 2.1 GEO数据集筛选差异基因将数据集GSE12852、GSE28660、GSE208261中POP组及对照组取差异基因,结果显示,PLA2G2A在3个数据集的POP组中均呈显著高表达。见图 1。
|
| 图 1 差异基因火山图及韦恩图 Fig.1 Volcano plot and Venn diagram of differentially expressed genes |
2.2 2组一般资料比较
2组年龄、体重指数(body mass index,BMI)、怀孕次数、经阴道分娩次数比较,差异均无统计学意义(P>0.05),见表 2。
| Item | Control group(n = 23) | POP group(n = 26) | P |
| Age(year) | 49.65(47-53) | 52.23(44-63) | >0.05 |
| BMI(kg/m2) | 24.72±4.08 | 25.21±3.47 | >0.05 |
| Number of pregnancy | 3.61(3-5) | 3.12(2-4) | >0.05 |
| Number of vaginal deliveries | 1.57(1.0-2.0) | 1.96(1.8-2.0) | >0.05 |
2.3 2组阴道壁组织中HE和Masson染色结果比较
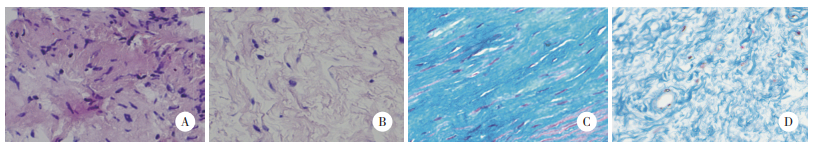
HE染色结果显示,对照组阴道壁成纤维细胞均匀分布在胶原纤维中;POP组镜下可见成纤维细胞稀疏分布,胶原纤维的排列甚至有断裂现象。Masson染色结果显示,对照组阴道壁镜下表现为成纤维排列较为规律,胶原纤维被Masson染色为条索状致密蓝色,而POP组的阴道壁镜下成纤维细胞量少且排列杂乱,胶原纤维分布稀疏紊乱,见图 2。
|
| A, HE staining of control group; B, HE staining of POP group; C, Masson staining of control group; D, Masson staining of POP group. 图 2 2组阴道壁组织学特征 ×400 Fig.2 Histological characteristics of the vaginal wall in the two groups ×400 |
2.4 阴道壁组织免疫荧光染色结果
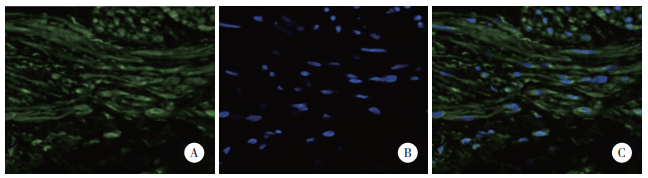
免疫荧光定位可以确定PLA2G2A主要在成纤维细胞内表达,尤其在核周部位表达更加明显,见图 3。
|
| A, collagen fibers and specific expression; B, nuclei; C, specific localization. 图 3 PLA2G2A在阴道壁组织中的定位 ×400 Fig.3 Localization of PLA2G2A in vaginal wall tissue ×400 |
2.5 2组阴道壁组织免疫组织化学检测结果
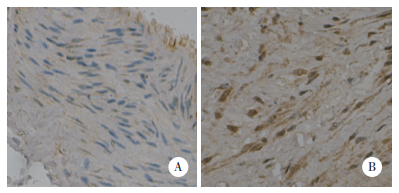
免疫组织化学检测结果显示,与对照组(6.85±2.37)相比,POP组PLA2G2A的表达水平(12.5±2.67)显著升高(P<0.001),见图 4。
|
| A, control group; B, POP group. 图 4 免疫组织化学检测2组阴道壁组织中PLA2G2A的表达 ×400 Fig.4 PLA2G2A expression in the vaginal wall tissues between two groups by immunohistochemistry ×400 |
2.6 2组阴道壁组织实时PCR和Western boltting结果
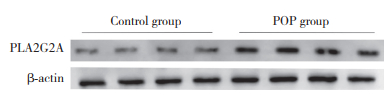
实时PCR结果显示,POP组PLA2G2A mRNA的相对表达(0.07±0.06)高于对照组(0.01±0.01,P<0.05)。Western boltting检测结果显示,POP组阴道壁中PLA2G2A的表达水平(0.84±0.22)显著均高于对照组(0.66±0.25,P<0.05)。见图 5。
|
| 图 5 2组阴道壁组织中PLA2G2A蛋白的表达 Fig.5 Expression of PLA2G2A in vaginal wall tissues between two groups |
2.7 沉默PLA2G2A后collagen Ⅰ和collagen Ⅲ的Western boltting结果
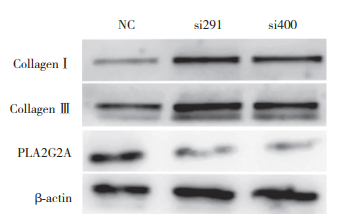
PLA2G2A转染后实时PCR检测结果显示,si291和si400的相对表达量分别为0.357 7±0.608 3,可成功沉默PLA2G2A。Western boltting结果显示,si291沉默PLA2G2A后,collagen Ⅰ和collagen Ⅲ的相对表达量显著增加(0.31±0.11 vs. 0.87±0.15,0.18±0.06 vs. 0.75±0.11),差异有统计意义(P<0.05);si400沉默PLA2G2A后, collagen Ⅰ和collagen Ⅲ的相对表达量显著增加(0.31±0.11 vs. 1.08±0.13,0.18±0.06 vs. 1.20±0.43),差异有统计意义(P<0.05)。见图 6。
|
| 图 6 人阴道壁成纤维细胞沉默PLA2G2A后collagen Ⅰ和collagen Ⅲ表达 Fig.6 Collagen Ⅰ and collagen Ⅲ expression after silencing of PLA2G2A in human vaginal wall fibroblasts |
3 讨论
女性阴道壁的支撑依赖于阴道和骨盆侧壁之间的结缔组织[9],其在支撑骨盆器官中起重要作用,纤维结缔组织的撕裂与盆腔器官脱垂的发生密切相关[10]。研究[11]认为含有细胞外基质(extracellular matrix,ECM)的结缔组织层负责支撑骨盆底,成纤维细胞分泌的胶原蛋白(主要是collagen Ⅰ和collagen Ⅲ)和弹性蛋白是形成结缔组织和增加ECM强度的2种主要成分。研究[12]表明在POP患者组织中,collagen Ⅰ、collagen Ⅲ和弹性蛋白表达减少,从而导致ECM组分失衡,这与本研究在沉默PLA2G2A后成纤维细胞collagen Ⅰ和collagen Ⅲ表达增多结果相符。
PLA2G2A是磷脂酶A2家族成员,可以水解细胞膜磷脂释放花生四烯酸(arachidonic acid,AA),AA作为重要的炎症介质,与炎症反应和组织再生有关[13]。当前对PLA2G2A基因的研究更多聚焦于参与癌症侵袭转移与发生发展[14],在POP中鲜有研究,本研究通过生信分析发现PLA2G2A基因在POP中显著高表达。阴道壁内的ECM主要由胶原蛋白和弹性蛋白构成,是阴道壁结缔组织的重要成分,其代谢活动受成纤维细胞调控[15]。在成纤维细胞中沉默PLA2G2A后胶原蛋白含量增加,其可能机制在于受到基质金属蛋白酶(matrix metalloproteinase,MMP)的调节,即PLA2G2A的高表达可能通过激活MMP,导致ECM中胶原蛋白的过度降解,进而引发组织结构的破坏和POP的发生。
在本研究中,PLA2G2A在POP患者的阴道壁中高表达,抑制PLA2G2A基因后collagen Ⅰ和collagen Ⅲ表达上调,然而PLA2G2A基因是否通过何种调节途径影响成纤维细胞的胶原分泌,PLA2G2A的转录合成是否受到其他信号级联调节还没有进一步的研究证实。GE等[14]的研究认为PLA2G2A+肿瘤相关成纤维细胞通过抑制MAPK/ERK信号通路抑制CD8+ T细胞的活化,降低CD8+ T细胞的抗肿瘤免疫功能介导胰腺癌免疫逃逸。Zhang等[16]发现巨噬细胞移动抑制因子MIF能够通过星形胶质细胞中的CD74受体结合诱导激活ERK信号通路并介导PLA2G2A表达,促进星形胶质细胞炎症反应,但ERK1/2磷酸化是否与PLA2G2A激活有关需要进一步探讨。
综上所述,PLA2G2A在POP患者阴道壁组织中高表达;其表达增加可能与POP的发生发展有关,在后续研究中会进一步探讨PLA2G2A与MEK/ERK信号通路在POP中可能存在的相互作用机制。
| [1] |
中华医学会妇产科学分会妇科盆底学组. 盆腔器官脱垂的中国诊治指南(2020年版)[J]. 中华妇产科杂志, 2020, 5(55): 300-306. DOI:10.3760/cma.j.cn112141-20200106-00016 |
| [2] |
COLLINS S, LEWICKY-GAUPP C. Pelvic organ prolapse[J]. Gastroenterol Clin N Am, 2022, 51(1): 177-193. DOI:10.1016/j.gtc.2021.10.011 |
| [3] |
DRAGE KJ, AGHERA M, MACKELLAR P, et al. The relationship between symptom severity, bother and psychological factors in women with pelvic organ prolapse: a cross-sectional observational study[J]. Neurourol Urodyn, 2022, 41(1): 423-431. DOI:10.1002/nau.24842 |
| [4] |
NORTON PA, ALLEN-BRADY K, WU J, et al. Clinical characteristics of women with familial pelvic floor disorders[J]. Int Urogynecol J, 2015, 26(3): 401-406. DOI:10.1007/s00192-014-2513-8 |
| [5] |
LINCE SL, VAN KEMPEN LC, VIERHOUT ME, et al. A systematic review of clinical studies on hereditary factors in pelvic organ prolapse[J]. Int Urogynecol J, 2012, 23(10): 1327-1336. DOI:10.1007/s00192-012-1704-4 |
| [6] |
SAMIMI P, JONES SH, GIRI A. Family history and pelvic organ prolapse: a systematic review and meta-analysis[J]. Int Urogynecol J, 2021, 32(4): 759-774. DOI:10.1007/s00192-020-04559-z |
| [7] |
ERIC JELOVSEK J, CHAGIN K, GYHAGEN M, et al. Predicting risk of pelvic floor disorders 12 and 20 years after delivery[J]. Am J Obstet Gynecol, 2018, 218(2): 222.e1-222222.e19. DOI:10.1016/j.ajog.2017.10.014 |
| [8] |
XIE RY, XU Y, FAN SX, et al. Identification of differentially expressed genes in pelvic organ prolapse by RNA-seq[J]. Med Sci Monit, 2016, 22: 4218-4225. DOI:10.12659/msm.900224 |
| [9] |
DELANCEY JOL. Anatomie aspects of vaginal eversion after hyste- rectomy[J]. Am J Obstet Gynecol, 1992, 166(6): 1717-1728. DOI:10.1016/0002-9378(92)91562-O |
| [10] |
DELANCEY JOL. What's new in the functional anatomy of pelvic organ prolapse?[J]. Curr Opin Obstet Gynecol, 2016, 28(5): 420-429. DOI:10.1097/GCO.0000000000000312 |
| [11] |
GONG RQ, XIA ZJ. Collagen changes in pelvic support tissues in women with pelvic organ prolapse[J]. Eur J Obstet Gynecol Reprod Biol, 2019, 234: 185-189. DOI:10.1016/j.ejogrb.2019.01.012 |
| [12] |
DUAN YN, CHEN YF, HE Y, et al. Expression of insulin-like growth factor binding protein 5 in the vaginal wall tissues of older women with pelvic organ prolapse[J]. Sci Rep, 2024, 14(1): 18353. DOI:10.1038/s41598-024-69098-9 |
| [13] |
LETSIOU E, HTWE YM, DUDEK SM. Secretory phospholipase A2 enzymes in acute lung injury[J]. Cell Biochem Biophys, 2021, 79(3): 609-617. DOI:10.1007/s12013-021-01003-x |
| [14] |
GE WY, YUE M, LIN RR, et al. PLA2G2A+ cancer-associated fibroblasts mediate pancreatic cancer immune escape via impeding antitumor immune response of CD8+ cytotoxic T cells[J]. Cancer Lett, 2023, 558: 216095. DOI:10.1016/j.canlet.2023.216095 |
| [15] |
林特, 夏志军. 盆腔器官脱垂患者子宫骶韧带COX2、PGE2和p16的表达及意义[J]. 中国医科大学学报, 2020, 49(1): 21-26. DOI:10.12007/j.issn.0258-4646.2020.01.005 |
| [16] |
ZHANG YX, LU SJ, FAN S, et al. Macrophage migration inhibitory factor activates the inflammatory response in joint capsule fibroblasts following post-traumatic joint contracture[J]. Aging (Albany NY), 2021, 13(4): 5804-5823. DOI:10.18632/aging.202505 |
 2025, Vol. 54
2025, Vol. 54