文章信息
- 杨延延, 方玲玉, 马雪静, 刘畅, 任丽莉, 王鹏
- YANG Yanyan, FANG Lingyu, MA Xuejing, LIU Chang, REN Lili, WANG Peng
- 基于生物信息学筛选阿尔茨海默病和慢性牙周炎的关键基因
- Screening of key genes for Alzheimer disease and chronic periodontitis based on bioinformatics
- 中国医科大学学报, 2025, 54(11): 1029-1035
- Journal of China Medical University, 2025, 54(11): 1029-1035
-
文章历史
- 收稿日期:2024-09-23
- 网络出版时间:2025-11-21 12:54:54
2. 锦州医科大学口腔医学院口腔修复科,辽宁 锦州 121000
2. Department of Prosthodontics, School of Stomatology, Jinzhou Medical University, Jinzhou 121000, China
阿尔茨海默病(Alzheimer disease,AD)是一种严重的进行性神经退行性疾病,表现为记忆丧失和认知障碍。淀粉样蛋白和tau蛋白病理是AD的核心特征,小胶质细胞反应、血管系统、血脑屏障、外周免疫系统、淋巴以及胃肠道微生物组也影响疾病的临床进展[1]。关于其致病因素和发病机制,目前尚无定论。
慢性牙周炎(chronic periodontitis,CP)是由口腔生物膜失调引起的常见的口腔炎症性疾病。当宿主免疫和炎症反应功能持续失调时,牙周炎症就会变成慢性炎症,导致破坏性炎症细胞的释放时间延长,牙周炎症持续进展并出现牙槽骨破坏和牙齿脱落,严重影响患者的日常生活[2]。研究[3-4]表明,牙周炎患者AD的发病率高于一般人群,但这2种疾病的具体联系和分子机制尚不清楚。本研究利用生物信息学方法筛选CP和AD的关键基因,为探讨CP与AD的潜在联系提供参考依据。
1 材料与方法 1.1 数据收集通过基因表达综合(Gene Expression Omnibus,GEO)数据库(https://www.ncbi.nlm.nih.gov/geo/)获取AD和CP的相关数据集,使用R软件(4.2.1)进行数据分析。AD数据集GSE63060包含104个对照样本和225个AD样本,CP数据集GSE16134包含69个健康牙龈样本和241个CP牙龈样本。
1.2 差异表达基因(differentially expressed genes,DEGs)分析采用R语言“limma”包筛选AD、CP和对照组之间的DEGs,以P<0.05,显著性阈值|log2FC |>0.5为标准。
1.3 加权基因共表达网络分析(weighted gene coexpression network analysis,WGCNA)使用R语言“WGCNA”包构建WGCNA网络,对数据集的基因表达数据进行聚类分析,确定最佳的软阈值使各基因调控关系符合无尺度分布,构建共表达网络绘制模块聚类树状图,并将表达谱相似的基因分组到不同的模块中,使用Pearson法分析基因间的相关性,获得关系矩阵,选择相关性最高的模块作为关键基因模块。
1.4 共同基因鉴定将DEGs和WGCNA获得的基因取交集,使用R语言“ggVennDiagram”包获取AD和CP的共同基因。
1.5 共同基因功能富集分析通过基因本体论(Gene Ontology,GO)和京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集分析观察AD和CP患者中DEGs的生物学功能,GO富集分析包括生物过程(biological process,BP)、细胞成分(cellular component,CC)和分子功能(molecular function,MF)。使用R语言“cluster Profiler”包对基因进行富集,P<0.05为差异有统计学意义。使用R语言“ggplot2”包展示富集分析结果。
1.6 蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络构建和关键基因筛选采用STRING数据库(http://string-db.org/)构建AD和CP之间共同基因的PPI网络,导入Cytoscape3.7.2软件进行可视化,应用插件MCODE预测出AD和CP的关键基因。
1.7 关键共同基因鉴定使用R语言“glmnet”包进行LASSO回归算法分析,进一步从共同基因中筛选关键基因。将筛选出来的关键基因与MCODE插件预测出AD和CP的关键基因取交集,得到AD和CP的关键共同基因。
1.8 基因富集分析(gene set enrichment analysis,GSEA)根据关键DEGs的中位表达水平将样本分为高表达组和低表达组,使用R语言“clusterProfiler”包进行GSEA。通过R语言“enrichment”包对结果进行可视化处理。
1.9 免疫浸润分析通过CIBERSORT算法对AD和CP样本进行免疫分析,使用CIBERSORT算法进行100次迭代,基于LM22基因标记量化了22种不同类型的免疫细胞。对患病和正常样本的免疫细胞浸润进行了比较分析。采用Spearman等级相关系数对关键共同基因表达水平与浸润免疫细胞数进行相关性分析。
1.10 统计学分析采用R Studio软件制图并进行统计学分析。绘制受试者操作特征(receiver operating characteristic,ROC)曲线,LASSO回归算法筛选关键基因,计算ROC曲线下面积(area under the curve,AUC)以评估关键基因的诊断效能。P<0.05为差异有统计学意义。
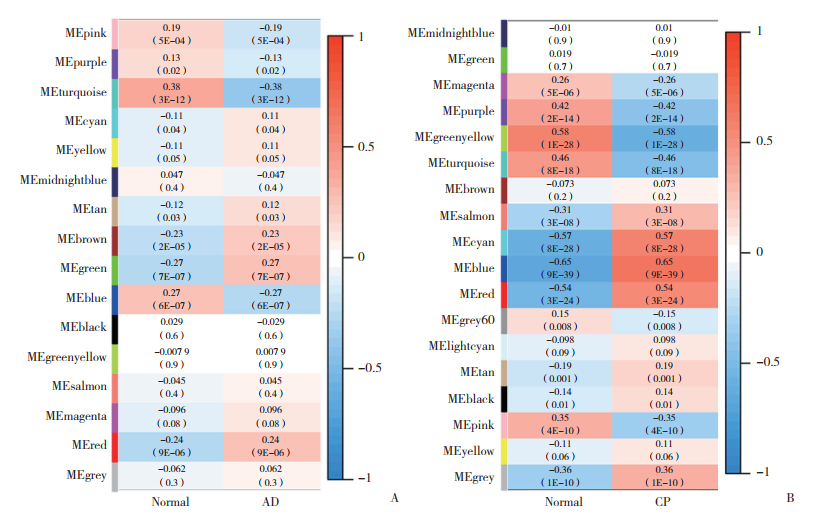
2 结果 2.1 共同基因鉴定应用R语言“limma”包识别AD和CP的DEGs,AD共检测到1 073个基因,其中上调基因466个,下调基因607个;CP共检测到1 292个DEGs,其中上调基因793个,下调基因499个。以AD和CP的样本构建共表达网络,AD共鉴定出16个共表达模块,MEturquoise模块的相关性最强(r = 0.38,P<0.000 1),该模块包含1 558个基因(图 1A)。同样,将WGCNA应用于CP,共鉴定出18个模块,其中MEgreenyellow模块表现出最强的相关性(r = 0.58,P<0.000 1),包含68个基因(图 1B)。随后对DEGs和WGCNA鉴定的基因进行了交叉分析,共鉴定出18个共同基因(TXN、KLRB1、DYNLT3、TBXAS1、ARHGAP9、GLRX、ITGB2、LY96、GZMA、SELPLG、COQ2、FAM107B、CD52、CD163、CD14、ACTA2、OGT、GZMK)。
|
| A, the interconnections between the various modules and traits in AD, the correlation coefficients and P are contained in each cell; B, associations between modules and traits in CP, correlation coefficients and P are included in each cell. 图 1 加权基因共表达网络分析 Fig.1 Weighted gene co-expression network analysis |
2.2 共同基因功能富集分析
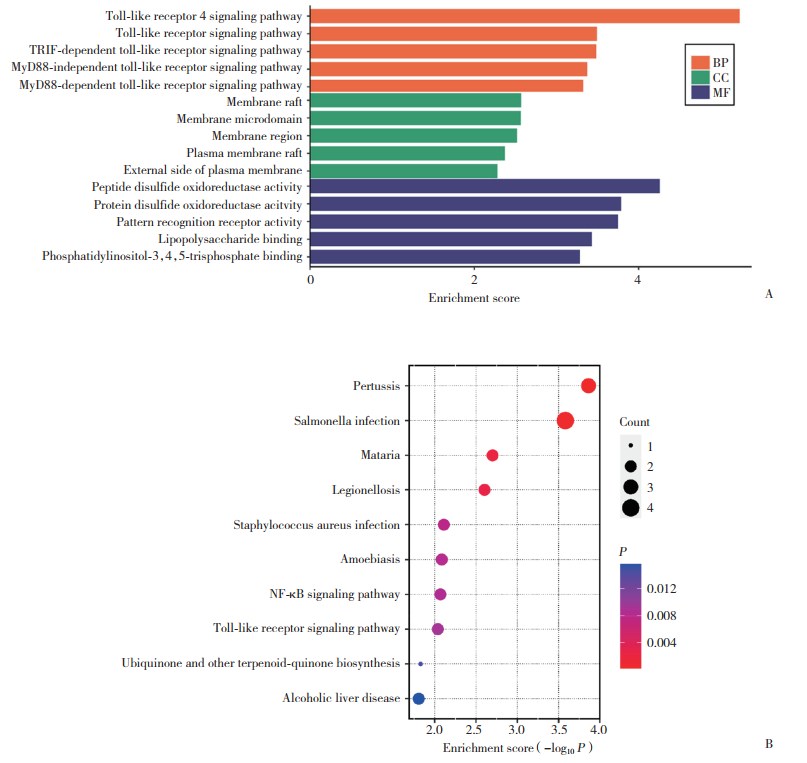
对AD和CP的共同DEGs分别进行GO和KEGG富集分析,BP结果显示,DEGs与Toll样受体信号通路、程序性坏死细胞死亡和模式识别受体信号通路密切相关;CC结果显示,DEGs主要富集于细胞膜相关过程;MF结果显示,DEGs在氧化还原酶活性、脂多糖结合和模式识别受体活性等过程中可能发挥重要作用(图 2A)。此外,KEGG富集分析结果表明,这些DEGs主要富集于菌群感染、NF-κB信号通路、Toll样受体信号通路和酒精性肝疾病通路(图 2B)。
|
| A, GO enrichment analysis; B, KEGG enrichment analysis. 图 2 共同基因功能富集分析 Fig.2 Functional enrichment analysis of common genes |
2.3 关键共同基因筛选
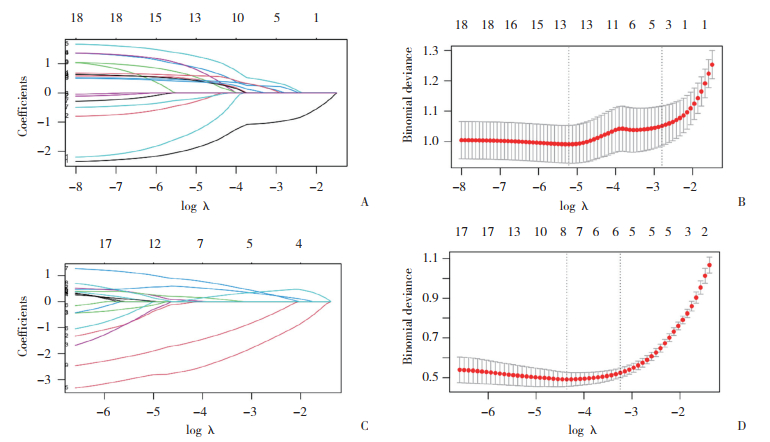
将获取到的18个共享基因导入STRING数据库获得PPI信息TSV文件,在Cytoscape 3.7.2软件中通过MCODE插件识别出由GZMK、GZMA、KLRB1、CD52、CD163组成的核心模块。LASSO回归结果显示,AD鉴定出13个候选基因(图 3A、3B),CP筛选出8个特征基因(图 3C、3D)。通过交叉验证AD、CP的LASSO结果与MCODE模块基因,确定KLRB1为最终的共同关键基因。
|
| A-B, LASSO logistic regression algorithm screened the key genes in AD; C-D, LASSO logistic regression algorithm screened key genes in CP. 图 3 LASSO回归分析 Fig.3 LASSO regression analysis |
2.4 关键共同基因的单基因GSEA
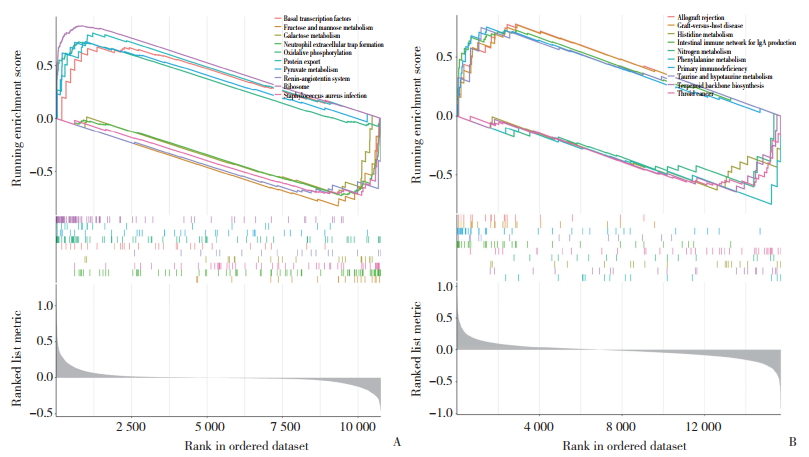
在AD中,KLRB1在代谢途径(丙酮酸代谢、肾素-血管紧张素系统、氧化磷酸化等)和免疫反应相关的途径(中性粒细胞胞外陷阱形成、趋化因子信号通路,TNF信号通路等)中发挥重要作用(图 4A)。在CP中,KLRB1与免疫反应(自然杀伤细胞介导的细胞毒性、TNF信号通路、肠道免疫网络产生IgA、原发性免疫缺陷)和代谢途径(组氨酸代谢、苯丙氨酸代谢、牛磺酸和次牛磺酸代谢、氧化磷酸化)相关(图 4B)。
|
| A, GSEA analysis of KLRB1 in AD; B, GSEA analysis of KLRB1 in CP. 图 4 单基因GSEA分析 Fig.4 Single gene GSEA analysis |
2.5 免疫浸润分析
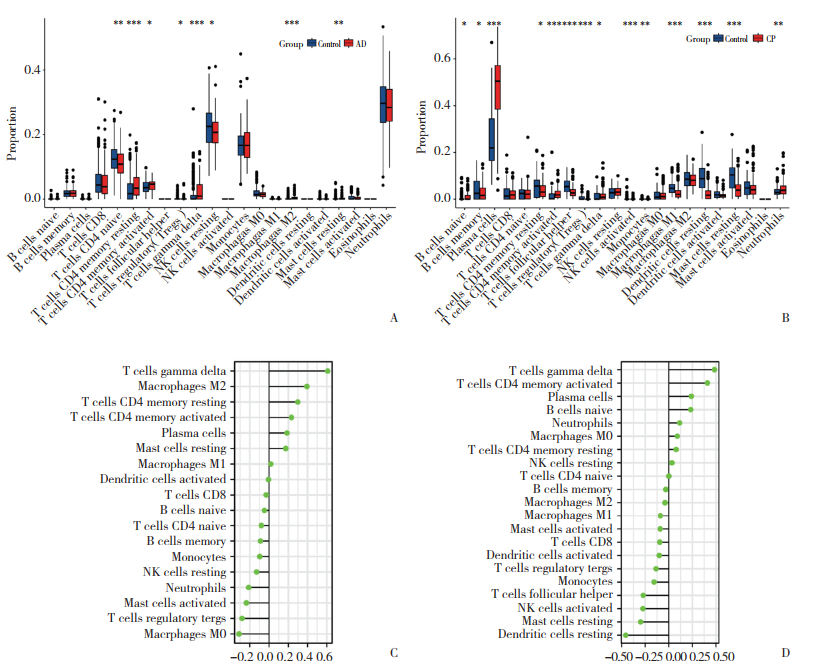
富集分析结果显示,鉴定的中心基因KLRB1与炎症和免疫过程之间存在潜在联系。使用CIBERSORT算法对不同组中免疫细胞的丰度进行分析,评估了AD和CP数据集样本中22种免疫细胞类型的比例。在AD中,观察到初始CD4+ T细胞和Treg细胞下调,静息CD4+记忆T细胞、活化CD4+记忆T细胞、γδT细胞、静息的NK细胞、M2巨噬细胞以及静息肥大细胞上调(图 5A)。CP样本(图 5B)显示幼稚B细胞、浆细胞、活化CD4+记忆T细胞、活化的NK细胞、单核细胞和中性粒细胞表达上调,而记忆B细胞、静息CD4+记忆T细胞、滤泡辅助性T细胞、Treg细胞、γδT细胞、M1巨噬细胞、静息树突细胞和静息肥大细胞下调。进一步分析AD和CP中KLRB1表达与免疫细胞比例之间的相关性(图 5C、5D)。结果显示,在AD样本中,KLRB1表达与γδT细胞、M2巨噬细胞、Treg细胞和M0巨噬细胞相关性较强。而在CP样本中,KLRB1表达与γδT细胞、活化CD4+记忆T细胞、静息肥大细胞和静息树突细胞有较强的相关性。
|
| A, box plot showed the comparison of 22 kinds of immune cells between AD group and control group; B, box plot showed the comparison of 22 kinds of immune cells between CP group and control group; C, correlation between KLRB1 expression and immune cells in AD group; D, relationship between KLRB1 expression and immune cells in CP group. *P < 0.05, **P < 0.01, ***P < 0.001. 图 5 免疫浸润分析 Fig.5 Analysis of immune infiltration |
3 讨论
近年来,AD与CP的关联性逐渐受到关注,但其共同机制尚不明确。在本研究中,DEGs和WGCNA的分析筛选出18个可能与AD和CP的共同发病机制有关的共同基因。富集分析结果显示,共同基因显著关联于Toll样受体、NF-κB信号通路、程序性坏死细胞死亡和氧化还原酶活性等过程。进一步通过MCODE模块分析和LASSO机器学习算法筛选,最终确定KLRB1为AD和CP的共同关键基因。
KLRB1编码CD161,属于c型凝集素家族,在NK细胞、T细胞亚群中表达,参与免疫调节及炎症反应[5]。研究[6-7]发现,KLRB1通过调控树突状细胞分化和NK细胞功能,与自身免疫性疾病及肿瘤预后相关。在AD与CP中,GSEA提示KLRB1与炎症及免疫通路密切相关。进一步利用CIBERSORT算法分析免疫细胞浸润模式发现,CP患者存在14种差异免疫细胞,AD患者则显示8种,提示2种疾病均存在显著的免疫失调。T/B细胞在CP中驱动牙周组织破坏[8-10],而AD中T细胞通过血脑屏障渗入脑实质加剧神经退行性变[11],此外,在AD患者的外周血中发现活化的CD4+和CD8+T细胞亚群显著增加[12]。
牙周病原体(如牙龈卟啉单胞菌)引发的慢性炎症可通过全身循环加剧AD病理,细菌毒素渗透导致系统性炎症,激活小胶质细胞并释放促炎因子,加速神经损伤[2,13-14]。KLRB1在2种疾病中均与γδ T细胞功能显著相关,该细胞亚群通过白细胞介素-17A等因子募集中性粒细胞,可能同时参与牙周骨吸收和脑缺血损伤[15]。因此,KLRB1作为免疫检查点分子,可能通过调控γδ T细胞等免疫应答,成为AD与CP共病的潜在干预靶点。
本研究基于生物信息学分析筛选关键基因,但缺乏实验验证,后续需通过基因敲除或过表达模型明确KLRB1在共病中的具体机制。此外,数据来源于公共数据库,样本异质性及混杂因素可能影响结果的可靠性。未来需结合多组学数据及纵向临床研究,进一步探索KLRB1的转化价值。
| [1] |
ZHENG QY, WANG X. Alzheimer's disease: insights into pathology, molecular mechanisms, and therapy[J]. Protein Cell, 2025, 16(2): 83-120. DOI:10.1093/procel/pwae026 |
| [2] |
ZHANG MZ, LIU YL, AFZALI H, et al. An update on periodontal inflammation and bone loss[J]. Front Immunol, 2024, 15: 1385436. DOI:10.3389/fimmu.2024.1385436 |
| [3] |
CHEN CK, WU YT, CHANG YC. Association between chronic periodontitis and the risk of Alzheimer's disease: a retrospective, population-based, matched-cohort study[J]. Alzheimers Res Ther, 2017, 9(1): 56. DOI:10.1186/s13195-017-0282-6 |
| [4] |
IWASAKI M, KIMURA Y, OGAWA H, et al. Periodontitis, periodontal inflammation, and mild cognitive impairment: a 5-year cohort study[J]. J Periodontal Res, 2019, 54(3): 233-240. DOI:10.1111/jre.12623 |
| [5] |
FANG ST, ZHOU YL. Deciphering the role of KLRB1:a novel prognostic indicator in hepatocellular carcinoma[J]. BMC Gastroenterol, 2024, 24(1): 210. DOI:10.1186/s12876-024-03299-4 |
| [6] |
ZHANG ZH, BAHABAYI A, LIU DN, et al. KLRB1 defines an activated phenotype of CD4+ T cells and shows significant upregulation in patients with primary Sjögren's syndrome[J]. Int Immunopharmacol, 2024, 133: 112072. DOI:10.1016/j.intimp.2024.112072 |
| [7] |
HE JR, LI D, ZHANG QX, et al. Inhibiting KLRB1 expression is associated with impairing cancer immunity and leading to cancer progression and poor prognosis in breast invasive carcinoma patients[J]. Aging (Albany NY), 2023, 15(22): 13265-13286. DOI:10.18632/aging.205239 |
| [8] |
KOU YY, JIANG YJ, LIU SS, et al. Regulatory T cells showed characteristics of T helper-17 (Th17) cells in mice periodontitis model[J]. Oral Dis, 2023, 29(3): 1149-1162. DOI:10.1111/odi.14072 |
| [9] |
DANIELSEN AK, DAMGAARD C, MASSARENTI L, et al. B-cell cytokine responses to porphyromonas gingivalis in patients with periodontitis and healthy controls[J]. J Periodontol, 2023, 94(8): 997-1007. DOI:10.1002/JPER.22-0438 |
| [10] |
QIAN SJ, HUANG QR, CHEN RY, et al. Single-cell RNA sequencing identifies new inflammation-promoting cell subsets in Asian patients with chronic periodontitis[J]. Front Immunol, 2021, 12: 711337. DOI:10.3389/fimmu.2021.711337 |
| [11] |
UNGER MS, LI E, SCHARNAGL L, et al. CD8+ T-cells infiltrate Alzheimer's disease brains and regulate neuronal- and synapse-related gene expression in APP-PS1 transgenic mice[J]. Brain Behav Immun, 2020, 89: 67-86. DOI:10.1016/j.bbi.2020.05.070 |
| [12] |
GATE D, SALIGRAMA N, LEVENTHAL O, et al. Clonally expanded CD8 T cells patrol the cerebrospinal fluid in Alzheimer's disease[J]. Nature, 2020, 577(7790): 399-404. DOI:10.1038/s41586-019-1895-7 |
| [13] |
ZOU J, ZENG ZJ, XIE W, et al. Immunotherapy with regulatory T and B cells in periodontitis[J]. Int Immunopharmacol, 2022, 109: 108797. DOI:10.1016/j.intimp.2022.108797 |
| [14] |
LIU SX, BUTLER CA, AYTON S, et al. Porphyromonas gingivalis and the pathogenesis of Alzheimer's disease[J]. Crit Rev Microbiol, 2024, 50(2): 127-137. DOI:10.1080/1040841X.2022.2163613 |
| [15] |
LU H, LI DJ, JIN LP. γδT cells and related diseases[J]. Am J Reprod Immunol, 2016, 75(6): 609-618. DOI:10.1111/aji.12495 |
 2025, Vol. 54
2025, Vol. 54