文章信息
- 吴珊, 郭静伟, 张莹, 田保玲, 王哲
- WU Shan, GUO Jingwei, ZHANG Ying, TIAN Baoling, WANG Zhe
- POLE突变多重分子特征的子宫内膜样腺癌临床病理特征及预后分析
- Clinicopathological characteristics and prognosis of multiple-molecular classifier endometrioid adenocarcinoma with POLE mutations
- 中国医科大学学报, 2025, 54(11): 1023-1028, 1035
- Journal of China Medical University, 2025, 54(11): 1023-1028, 1035
-
文章历史
- 收稿日期:2025-03-07
- 网络出版时间:2025-11-21 13:28:58
子宫内膜癌是常见的妇科恶性肿瘤之一,且发病率呈逐年上升趋势,其中子宫内膜样腺癌是最常见的组织学亚型[1-3]。应用传统组织学方法对子宫内膜样腺癌分级分型,诊断可重复性较差,组织学特点在各型之间常有交叠。在美国癌症基因组图谱提出的子宫内膜癌分子分型基础上[4],第5版世界卫生组织女性生殖系统肿瘤子宫内膜癌分类将子宫内膜癌分为DNA聚合酶ε催化亚基(DNA polymerase epsilon catalytic subunit,POLE)突变型、错配修复缺陷型(mismatch repair-deficient,dMMR)、p53异常型(p53 abnormal,p53abn)及无特异性分子改变型(no specific molecular profile,NSMP)4种分子分型。然而,部分患者因表现出不止1种子宫内膜癌分子分型特征导致无法明确归类,称为多重分子特征[5]。目前国内针对多重分子特征的子宫内膜癌的研究较少,POLE突变多重分子特征的子宫内膜样腺癌的临床病理特征及预后情况在辽宁地区人群中尚未明确。本研究拟探讨POLE突变多重分子特征的子宫内膜样腺癌患者的临床病理特征及预后情况,以期为丰富肿瘤的分子分型和预后相关信息提供依据。
1 材料与方法 1.1 临床资料选取2019年1月至2024年5月于中国医科大学附属盛京医院确诊子宫内膜样腺癌并进行手术治疗的病例261例。年龄35~80岁,平均(55±8.9)岁。纳入标准:经病理检查确诊子宫内膜样腺癌;术前无放疗、化疗或靶向治疗史;无其他部位原发性恶性肿瘤、感染性疾病、其他器官严重疾病和自身免疫缺陷症;有完整的病历资料及病理学报告,有相应的切片及完整的石蜡包埋标本,且石蜡标本保存期限≤2年,肿瘤细胞占比>20%;随访资料完整。所有切片由2位经验丰富的病理医师独立阅片,肿瘤分期依据子宫内膜癌国际妇产科联合会(International Federation of Gynecology and Obstetrics,FIGO)分期2023版,肿瘤浸润淋巴细胞(tumor-infiltrating lymphocyte,TIL)及肿瘤周围淋巴细胞浸润定义参考国际免疫肿瘤生物标志物工作委员会和既往研究[6-7]的评判方法。
本研究获得中国医科大学附属盛京医院医学伦理委员会批准(2024PS1926K)。
1.2 方法 1.2.1 检测p53和错配修复(mismatch repair,MMR)蛋白表达所有组织标本固定后取材,石蜡包埋,制备3 μm厚度防脱切片。针对p53及MMR蛋白行免疫组织化学(immunohistochemistry,IHC)染色,p53(DO-7)抗体购自北京中杉金桥生物技术有限公司,MLH1(M1)、PMS2(A16-4)、MSH2(G219-1129)及MSH6(SP93)抗体购自上海罗氏制药有限公司。p53判读参考以往判读标准[8],即≥80%肿瘤细胞核弥漫强阳性、核完全不着色且内对照阳性、细胞质中~强阳性同时核强弱不等阳性或染色缺失,均判读为突变型;肿瘤细胞核强弱不等着色判读为野生型;p53亚克隆性表达,即呈现1种以上染色模式。MMR蛋白在所有肿瘤细胞的细胞核均完整表达判读为表达正常[9]。
1.2.2 POLE基因检测切取蜡卷并提取DNA后,行定量PCR及酶解处理。测序PCR反应在Appliedbiosystems 7500 PCR扩增仪上进行,产物纯化后在Appliedbiosystems 3500Dx基因分析仪上分析。将结果序列文件与美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)数据库参考序列进行人工比对,序列文件与对应参考序列存在差异则视为突变,除外无义突变。根据“POLE-score”评估标准[10]评价致病性。
1.2.3 随访采用电话随访,以手术切除后第1天为随访起点,以出现复发、转移或死亡事件为随访终点,随访截止日期2024年12月31日。
1.3 统计学分析采用SPSS 26.0软件进行统计学分析。正态分布计量资料以x±s表示,组间比较用方差分析。计数资料以率(%)表示,组间比较用χ2检验或Fisher确切概率法,并对多重比较进行Bonferroni校正。使用Kaplan-Meier法进行生存分析,使用log-rank检验进行相关性分析。P<0.05为差异有统计学意义。
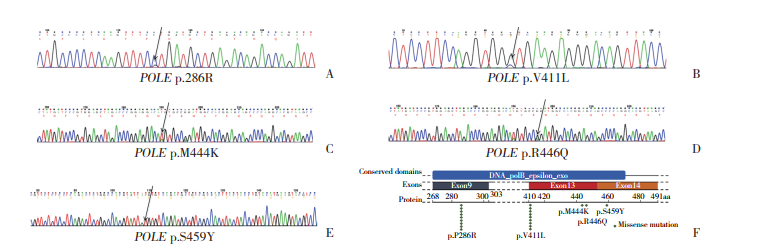
2 结果 2.1 POLE突变及p53、MMR表达检测结果在纳入病例中,共检测到21个致病性POLE突变,突变阳性率8.0%。其中POLE p.P286R突变(9/21,4.9%)和POLE p.V411L突变(9/21,4.9%)最为常见,另有POLE p.M444K突变1例,POLE p.R446Q突变1例,POLE p.S459Y突变1例。所有突变均位于POLE基因的真核DNA聚合酶ε3’-5’核酸外切酶结构域。见图 1。POLE突变子宫内膜样腺癌患者中,p53、MMR表达均正常患者12例,以POLE mut表示。多重分子特征子宫内膜样腺癌患者9例,其中6例同时存在POLE突变和p53蛋白表达异常,以POLE mut+p53abn表示;另有3例同时存在POLE突变和MMR蛋白表达缺陷,以POLE mut+dMMR表示。
|
| A, the amino acid at position 286 changes from proline to arginine; B, the amino acid at position 411 changes from valine to Leucine; C, the amino acid at position 444 changes from methionine to lysine; D, the amino acid at position 446 changes from arginine to glutarnine; E, the amino acid at position 459 changes from serine to tyrosine; F, the location distribution schematic diagram of POLE mutations. 图 1 POLE突变测序图与分布示意图 Fig.1 POLE mutations sequencing maps and distribution schematic diagram |
2.2 单一分子特征POLE mut患者临床病理特征
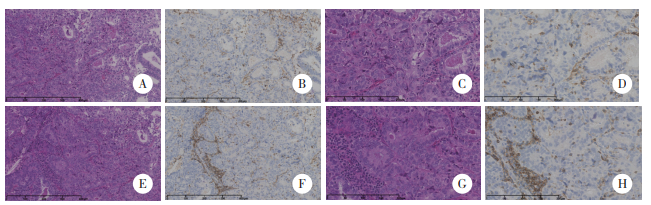
12例POLE mut患者的发病年龄为50~67岁,平均(57±6.6)岁。组织学分级G3级7例(58.33%)、FIGO分期Ⅰ~Ⅱ期12例(100%),浸润深度≤1/2子宫肌层7例(58.33%),未见宫颈间质浸润11例(91.7%),未见淋巴脉管间隙浸润(lymphovascular space invasion,LVSI)9例(75.0%),无神经侵犯(100%),无淋巴结转移(100%)。大多POLE mut患者(10/12,83.3%)HE染色可见TIL显著,IHC染色白细胞共同抗原LCA蛋白在TIL区域内呈现棕褐色阳性信号,多数(10/12,83.3%)存在肿瘤周围淋巴细胞浸润。见图 2。
|
| A, TIL HE staining (×200);B, TIL IHC staining (×200);C, TIL HE staining (×400);D, TIL IHC staining (×400);E, tumor with peritumoral lymphocytes infiltration HE staining (×200);F, tumor with peritumoral lymphocytes infiltration IHC staining (×200);G, tumor with peritumoral lymphocytes infiltration HE staining (×400);H, tumor with peritumoral lymphocytes infiltration IHC staining (×400). 图 2 TIL与肿瘤周围淋巴细胞浸润EnVision法 Fig.2 TIL and peritumoral lymphocytes infiltration EnVision method |
2.3 多重分子特征患者分子分型与临床病理特征相关性分析
POLE mut+p53abn患者与p53abn患者在TIL、是否存在肿瘤周围淋巴细胞浸润方面差异有统计学意义(P<0.05)。除此之外,尽管差异不显著,大多数POLE mut+p53abn与POLE mut患者均表现出FIGO分期Ⅰ~Ⅱ期、无淋巴结转移的特征,而p53abn患者有19例(19/41,46.3%)FIGO分期在Ⅲ~Ⅳ期,且有12例(12/41,29.3%)出现淋巴结转移。见表 1。
| Clinicopathological characteristic | POLE mut(n = 12) | p53abn(n = 41) | POLE mut+p53abn(n = 6) | POLE mut vs. p53abn vs. POLE mut+p53abn | POLE mut vs. POLE mut+p53abn | p53abn vs. POLE mut+p53abn | |||||
| F/χ2 | P | χ2 | P | χ2 | P | ||||||
| Onset age(year) | 57±6.6 | 55±8.1 | 56±2.9 | - | 0.769 | ||||||
| Histological grade [n(%)] | 2.225 | 0.329 | |||||||||
| G1 to G2 | 5(41.7) | 20(48.8) | 1(16.7) | ||||||||
| G3 | 7(58.3) | 21(51.2) | 5(83.3) | ||||||||
| FIGO stage [n(%)] | 9.782 | 0.008 | - | 0.333* | 0.867 | 0.352 | |||||
| Ⅰ to Ⅱ | 12(100) | 22(53.7) | 5(83.3) | ||||||||
| Ⅲ to Ⅳ | 0(0) | 19(46.3) | 1(16.7) | ||||||||
| Myometrium invasion [n(%)] | 2.570 | 0.277 | |||||||||
| ≤1/2 | 7(58.3) | 16(39.0) | 4(66.7) | ||||||||
| >1/2 | 5(41.7) | 25(61.0) | 2(33.3) | ||||||||
| Cervical stromal invasion [n(%)] | 3.934 | 0.140 | |||||||||
| Negative | 11(91.7) | 28(68.3) | 3(50.0) | ||||||||
| Positive | 1(8.3) | 13(31.7) | 3(50.0) | ||||||||
| Lymphovascular space invasion [n(%)] | 3.520 | 0.172 | |||||||||
| Negative | 9(75.0) | 26(63.4) | 6(100) | ||||||||
| Positive | 3(25.0) | 15(36.6) | 0(0) | ||||||||
| Nerve invasion [n(%)] | - | 0.778* | |||||||||
| Negative | 11(91.7) | 38(92.7) | 6(100) | ||||||||
| Positive | 1(8.3) | 3(7.3) | 0(0) | ||||||||
| Lymph node metastases [n(%)] | 6.613 | 0.037 | - | - | 1.070 | 0.301 | |||||
| Negative | 12(100) | 29(70.7) | 6(100) | ||||||||
| Positive | 0(0) | 12(29.3) | 0(0) | ||||||||
| Tumor infiltrating lymphocytes [n(%)] | 13.370 | 0.001 | 0.001 | 1.000 | 3.921 | 0.048 | |||||
| Low | 2(16.7) | 28(68.3) | 1(16.7) | ||||||||
| High | 10(83.3) | 13(31.7) | 5(83.3) | ||||||||
| Tumor with peritumoral lymphocyte infiltration [n(%)] | 14.731 | 0.001 | 0.001 | 1.000 | 4.492 | 0.034 | |||||
| Negative | 2(16.7) | 29(70.7) | 1(16.7) | ||||||||
| Positive | 10(83.3) | 12(29.3) | 5(83.3) | ||||||||
| * Fisher’s exact test. | |||||||||||
POLE mut、dMMR、POLE mut+dMMR患者在发病年龄、组织学分级、FIGO分期、子宫肌层浸润程度、宫颈间质浸润、LVSI、神经侵犯、淋巴结转移、TIL及是否存在肿瘤周围淋巴细胞浸润等特征方面差异无统计学意义(P>0.05)。但在本研究中,所有POLE mut+dMMR与POLE mut患者的FIGO分期均为Ⅰ~Ⅱ期,且均无淋巴结转移,而在dMMR患者中有12例(12/42,28.6%)患者FIGO分期为Ⅲ~Ⅳ期,且有9例(9/42,21.4%)患者存在淋巴结转移。见表 2。
| Clinicopathological characteristic | POLE mut(n = 12) | dMMR(n = 42) | POLE mut+ dMMR(n = 3) | POLE mut vs. dMMR vs. POLE mut+dMMR | |
| F/χ2 | P | ||||
| Onset age(year) | 57±6.6 | 56±7.7 | 40±4.2 | - | 0.068 |
| Histological grade [n(%)] | 2.148 | 0.342 | |||
| G1 to G2 | 5(41.7) | 18(42.9) | 0(0) | ||
| G3 | 7(58.3) | 24(57.1) | 3(100) | ||
| FIGO stage [n(%)] | 5.429 | 0.066 | |||
| Ⅰ to Ⅱ | 12(100) | 30(71.4) | 3(100) | ||
| Ⅲ to Ⅳ | 0(0) | 12(28.6) | 0(0) | ||
| Myometrium invasion [n(%)] | 0.674 | 0.714 | |||
| ≤1/2 | 7(58.3) | 23(54.8) | 1(33.3) | ||
| >1/2 | 5(41.7) | 19(45.2) | 2(66.7) | ||
| Cervical stromal invasion [n(%)] | 4.927 | 0.085 | |||
| Negative | 11(91.7) | 33(78.6) | 1(33.3) | ||
| Positive | 1(8.3) | 9(21.4) | 2(66.7) | ||
| Lymphovascular space invasion [n(%)] | 1.192 | 0.551 | |||
| Negative | 9(75.0) | 32(71.4) | 3(100) | ||
| Positive | 3(25.0) | 10(28.6) | 0(0) | ||
| Nerve invasion [n(%)] | 0.259 | 0.878 | |||
| Negative | 11(91.7) | 39(92.9) | 3(100) | ||
| Positive | 1(8.3) | 3(7.1) | 0(0) | ||
| Lymph node metastases [n(%)] | 3.817 | 0.148 | |||
| Negative | 12(100) | 33(78.6) | 3(100) | ||
| Positive | 0(0) | 9(21.4) | 0(0) | ||
| Tumor infiltrating lymphocytes [n(%)] | 0.987 | 0.611 | |||
| Low | 2(16.7) | 13(31.0) | 1(33.3) | ||
| High | 10(83.3) | 29(69.0) | 2(66.7) | ||
| Tumor with peritumoral lymphocyte infiltration [n(%)] | 0.594 | 0.743 | |||
| Negative | 2(16.7) | 8(19.0) | 0(0) | ||
| Positive | 10(83.3) | 34(91.0) | 3(100) | ||
2.4 生存分析
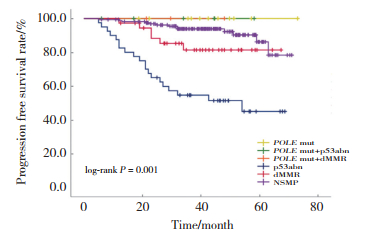
截至随访结束,41例患者出现复发、转移或死亡事件,中位随访时间47个月。不同分子分型的无进展生存期生存曲线差异有统计学意义(P<0.05)。多重分子特征POLE mut+p53abn与POLE mut+dMMR患者无进展生存率(100%)显著高于p53abn(50.0%)与dMMR患者(8.8%),差异有统计学意义(P<0.05),预后良好(图 3)。
|
| NSMP, no specific molecular profile. 图 3 不同分子分型子宫内膜样腺癌患者无进展生存期生存曲线分析 Fig.3 Progression free survival survival analysis of endometrioid adenocarcinoma patients with different molecular subtypes Progression free survival rate/% |
3 讨论
POLE基因核酸外切酶结构域内发生致病性突变后,DNA聚合酶ε的纠错能力降低,染色体DNA复制过程中的校对、修复功能丧失,基因突变率升高,发生“超突变”,诱导肿瘤发生[3]。子宫内膜样腺癌的POLE热点突变均位于第9~14号外显子,常见位点包括P286R/L、M395R、S297F/Y、F367S、D368Y、V411L、L424I/V、P436R、M444K、A456P、S459F等,涵盖所有已知POLE致病性突变的95%以上[10-11]。然而,随着全基因组和全外显子组测序的发展,逐渐有新的非热点突变被发现,具有与热点突变相当的致病性,特别是在亚洲人群中该部分突变比例较高。有研究[12]报道,POLE p.P441P突变可能是亚洲女性特征性POLE突变,针对中国女性子宫内膜癌群体的研究[13]表明,POLE p.P286C、L424V、S459Y可能是新的致病性突变。本研究中同样检测到1例POLE p.S459Y突变,携带该突变的患者临床病理特征表现为G3级低分化肿瘤,浸润深度<1/2子宫肌层,无宫颈间质浸润,无附件受累,无LVSI及淋巴结转移,该患者术后未治疗,至随访截止日期未出现复发、转移或死亡事件,预后良好,临床病理特征及预后情况符合POLE分型特点,进一步佐证了国内学者[13]的研究结论,提示POLE致病性突变的分布可能存在民族和种族差异。随着子宫内膜样腺癌的POLE基因测序进入临床实践阶段,完善POLE突变致病性评价体系标准,全面而有效地筛查出具有致病性的POLE突变并进行预后分类已迫在眉睫。
在子宫内膜癌患者中,约有0.4%~8.9%的患者同时表现出POLE突变和p53异常,约有0.5%~9.5%患者同时表现出POLE突变和dMMR[5, 14]。本研究中,具有POLE突变的多重分子特征的患者有9例,其中POLE mut+p53abn患者6例,POLE mut+dMMR患者3例,与以往研究比例基本一致。由于POLE突变和dMMR对基因组稳定性的影响[15],同时存在的p53突变通常是继发于POLE突变的非驱动性“乘客”突变,对肿瘤生物学行为和临床预后无显著影响[5]。本研究中,POLE mut+p53abn患者在子宫肌层浸润程度、淋巴结转移、TIL及是否存在肿瘤周围淋巴细胞浸润方面体现出与POLE mut患者相似的特征。而POLE mut+dMMR患者未显著体现出与POLE mut患者或dMMR患者相似的特征,究其原因可能是本研究中POLE mut+dMMR患者数量较少,也存在样本纳入或临床病理数据的统计存在主观差异等原因。研究[16]表明,当POLE突变先于dMMR获得的情况下,MMR蛋白功能缺陷并不全由POLE突变驱动,也可能是由MLH1启动子甲基化所致。少数情况下,也可能是由于MLH1启动子甲基化或Lynch综合征所致的dMMR亚克隆性改变激发了POLE的亚克隆性突变[5]。未来可通过扩大样本数量和样本收集范围,并增加MLH1甲基化检测进行深入研究。通常情况下,对POLE突变的FIGO分期为Ⅰ~Ⅱ期的肿瘤考虑降级辅助治疗[17]。对于多重分子特征病例,在本研究中,截至随访终止日期,POLE mut+p53abn与POLE mut+dMMR患者均未出现疾病的复发或死亡,预后良好。但由于子宫内膜样腺癌发病过程中多个基因的详细机制与基因间的相互作用尚未完全明确,对于多重分子特征患者的预后研究还有待进一步完善。
综上所述,本研究结果显示,多重分子特征POLE mut+p53abn与p53abn患者在TIL及是否存在肿瘤周围淋巴细胞浸润等特征上差异较大;POLE mut+p53abn与POLE mut+dMMR患者在FIGO分期、淋巴结转移的特征上与POLE mut患者相似;POLE mut+p53abn与POLE mut+dMMR患者均预后良好。但由于POLE突变率与多重分子特征发生率较低,本研究中纳入病例数较少,结果可能出现偏倚,未来将继续扩大样本量,以进一步验证本研究结果。
| [1] |
BELL DW, ELLENSON LH. Molecular genetics of endometrial carcinoma[J]. Annu Rev Pathol, 2019, 14: 339-367. DOI:10.1146/annurev-pathol-020117-043609 |
| [2] |
XIA CF, DONG XS, LI H, et al. Cancer statistics in China and Uni-ted States, 2022:profiles, trends, and determinants[J]. Chin Med J, 2022, 135(5): 584-590. DOI:10.1097/CM9.0000000000002108 |
| [3] |
杨丛语, 邓青春, 刘嘉铭. 基底膜基因在子宫内膜癌中的表达及其临床意义[J]. 中国医科大学学报, 2024, 53(5): 451-457. DOI:10.12007/j.issn.0258-4646.2024.05.011 |
| [4] |
LEVINE DA, GETZ G, GABRIEL SB, et al. Integrated genomic characterization of endometrial carcinoma[J]. Nature, 2013, 497: 67-73. DOI:10.1038/nature12113 |
| [5] |
胡阿锦, 刘岩, 刘从容. "多重分子特征"子宫内膜癌的解读[J]. 中华病理学杂志, 2024, 53(12): 1287-1291. DOI:10.3760/cma.j.cn112151-20240331-00210 |
| [6] |
SHIA JR, BLACK D, HUMMER AJ, et al. Routinely assessed morphological features correlate with microsatellite instability status in endometrial cancer[J]. Hum Pathol, 2008, 39(1): 116-125. DOI:10.1016/j.humpath.2007.05.022 |
| [7] |
LIU D, HEIJ LR, CZIGANY Z, et al. The role of tumor-infiltrating lymphocytes in cholangiocarcinoma[J]. J Exp Clin Cancer Res, 2022, 41(1): 127. DOI:10.1186/s13046-022-02340-2 |
| [8] |
SINGH N, PISKORZ AM, BOSSE T, et al. p53 immunohistochemistry is an accurate surrogate for TP53 mutational analysis in endometrial carcinoma biopsies[J]. J Pathol, 2020, 250(3): 336-345. DOI:10.1002/path.5375 |
| [9] |
刘岩, 王玉湘, 孙小婕, 等. 子宫内膜癌分子分型中错配修复和微卫星不稳定性状态的综合评估[J]. 中华妇产科杂志, 2023, 58(10): 755-765. DOI:10.3760/cma.j.cn112141-20230711-00316 |
| [10] |
LEÓN-CASTILLO A, BRITTON H, MCCONECHY MK, et al. Interpretation of somatic POLE mutations in endometrial carcinoma[J]. J Pathol, 2020, 250(3): 323-335. DOI:10.1002/path.5372 |
| [11] |
YU S, SUN Z, ZONG L, et al. Clinicopathological and molecular characterization of high-grade endometrial carcinoma with POLE mutation: a single center study[J]. J Gynecol Oncol, 2022, 33(3): e38. DOI:10.3802/jgo.2022.33.e38 |
| [12] |
MONSUR M, YAMAGUCHI M, TASHIRO H, et al. Endometrial cancer with a POLE mutation progresses frequently through the type Ⅰ pathway despite its high-grade endometrioid morphology: a cohort study at a single institution in Japan[J]. Med Mol Morphol, 2021, 54(2): 133-145. DOI:10.1007/s00795-020-00273-3 |
| [13] |
陈鑫, 王昀, 董周寰, 等. POLE突变型子宫内膜样癌临床病理及分子遗传学特征[J]. 中华病理学杂志, 2024, 53(12): 1217-1223. DOI:10.3760/cma.j.cn112151-20240409-00232 |
| [14] |
DE VITIS LA, SCHIVARDI G, CARUSO G, et al. Clinicopathological characteristics of multiple-classifier endometrial cancers: a Cohort study and systematic review[J]. Int J Gynecol Cancer, 2024, 34(2): 229-238. DOI:10.1136/ijgc-2023-004864 |
| [15] |
LEÓN-CASTILLO A, GILVAZQUEZ E, NOUT R, et al. Clinicopathological and molecular characterisation of 'multiple-classifier' endometrial carcinomas[J]. J Pathol, 2020, 250(3): 312-322. DOI:10.1002/path.5373 |
| [16] |
HARADHVALA NJ, KIM J, MARUVKA YE, et al. Distinct mutational signatures characterize concurrent loss of polymerase proofreading and mismatch repair[J]. Nat Commun, 2018, 9(1): 1746. DOI:10.1038/s41467-018-04002-4 |
| [17] |
刘俊茹, 张雅贤. 病理医师在子宫内膜癌国际妇产科联盟2023分期中的关键角色[J]. 中华病理学杂志, 2024, 53(12): 1185-1191. DOI:10.3760/cma.j.cn112151-20240529-00346 |
 2025, Vol. 54
2025, Vol. 54