文章信息
- 修银玲, 刘颖, 孙凯旋, 赵盼盼, 唐淑芳, 周静, 张伊彤, 于月新
- XIU Yinling, LIU Ying, SUN Kaixuan, ZHAO Panpan, TANG Shufang, ZHOU Jing, ZHANG Yitong, YU Yuexin
- 褪黑素改善长期低氧诱导的卵巢颗粒细胞凋亡的分子机制
- Effect of melatonin in alleviating ovarian granulosa cell apoptosis induced by chronic hypoxia
- 中国医科大学学报, 2025, 54(11): 1017-1022
- Journal of China Medical University, 2025, 54(11): 1017-1022
-
文章历史
- 收稿日期:2025-09-12
- 网络出版时间:2025-11-21 13:28:55
2. 中国人民解放军北部战区总医院急诊科,沈阳 110003
2. Emergency Department, General Hospital of Northern Theater Command, Shenyang 110003, China
卵巢功能衰退是一种严重威胁女性生殖健康的复杂内分泌疾病。研究[1-2]表明,颗粒细胞凋亡作为卵泡闭锁的关键调控机制,通过线粒体依赖性凋亡途径导致原始卵泡发育障碍,最终引发卵巢功能衰竭。卵巢功能衰退的发病机制涉及多因素交互作用,如遗传因素、自身免疫性疾病等,而氧化应激损伤是贯穿疾病进程的重要病理环节。其中,活性氧(reactive oxygen species,ROS)过量积累可通过脂质过氧化反应破坏细胞膜完整性[3],诱发DNA氧化损伤和蛋白质功能异常,进而激活p53-Bax/caspase促凋亡信号轴,同时抑制Bcl-2家族抗凋亡蛋白的表达,最终启动卵巢细胞的程序性死亡程序[4]。值得注意的是,慢性缺氧微环境会通过干扰线粒体呼吸链复合体Ⅰ和Ⅲ的电子传递效率,显著增加ROS的异常蓄积,这种恶性循环不仅加速卵泡细胞的衰老进程,更会诱发不可逆的凋亡级联反应,促进卵巢早衰的发生和发展。
目前,卵巢功能衰退的治疗仍以激素替代疗法为金标准,但其长期应用可能增加血栓形成、乳腺癌等风险,且改善生育功能的效果有限[5]。虽然新型治疗策略如脱氢表雄酮补充、抗氧化剂(维生素E/辅酶Q10)干预和间充质干细胞移植等在动物实验中显示出改善卵巢储备功能的潜力,但普遍存在临床疗效个体差异大、作用机制不明确和伦理争议等问题[6]。近年来,褪黑素作为一种具有多靶点调控特性的吲哚胺类激素,其卵巢保护作用日益受到关注[7]。研究证实,褪黑素可通过清除ROS、激活超氧化物歧化酶/谷胱甘肽过氧化物酶系统来减轻颗粒细胞氧化损伤,还可通过调控PI3K/Akt/FOXO3a信号通路提高卵巢早衰动物模型的抗米勒管激素水平[8];在炎症调控方面,褪黑素能特异性抑制核因子κB/NOD样受体热蛋白结构域相关蛋白3炎症小体活化,降低促炎性细胞因子的表达[9];褪黑素可通过MT1/MT2膜受体激活的下游cAMP-PKA-CREB通路,不仅能促进促性腺激素释放激素的脉冲式分泌以重建下丘脑-垂体-卵巢轴功能平衡,还可直接上调卵巢局部生长因子的表达[10]。然而,褪黑素在卵巢早衰模型中调控线粒体凋亡途径的具体分子机制目前尚未阐明。因此,本研究通过建立卵巢功能衰退模型,运用分子生物学、细胞生物学和形态学方法,探讨褪黑素通过调节细胞凋亡保护卵巢细胞的分子机制,为开发新型卵巢保护策略提供理论依据。
1 材料与方法 1.1 细胞培养和分组取10只21~25日龄未成熟雌性大鼠(辽宁长生生物技术股份有限公司)的卵巢组织,用75%乙醇消毒10 min后置于含10%胎牛血清和双抗(青霉素100 U/mL+链霉素100 U/mL)的预冷DMEM/F12培养基中。卵巢组织经机械剪碎后,用0.25%胰酶-EDTA消化液室温消化,经200目滤网过滤获得细胞悬液,计数后进行贴壁培养,24 h后换液,用于后续细胞实验。
将颗粒细胞分为常氧组、低氧组和褪黑素组。常氧组:颗粒细胞常氧培养(37 ℃、5%O2);低氧组:颗粒细胞低氧培养(37 ℃、1%O2);褪黑素组:颗粒细胞低氧培养(37 ℃、1%O2),并在培养基中加入1 μg/mL褪黑素(美国Sigma公司)。3组细胞均维持饱和湿度环境,每48 h更换新鲜培养基。
1.2 实验动物和分组另取24只健康雌性SD大鼠(辽宁长生生物技术股份有限公司),在SPF级环境饲养,温度(22±3)℃,湿度(45~65)%,自由摄食饮水。适应性饲养7 d后,采用随机数字表法将大鼠分为空白对照组、模型组和干预组,每组8只。模型组和干预组大鼠连续低氧(1%O2)暴露,20 h/d,持续8周,建立长期低氧致卵巢功能衰退大鼠模型。干预组大鼠在低氧暴露的同时,每天腹腔注射褪黑素(10 mg/kg)。模型组和空白对照组大鼠,每天腹腔注射等剂量芝麻油。8周后,眼眶后静脉丛采血后脱颈法处死大鼠,取大鼠卵巢组织进行乳酸分泌和蛋白检测等。动物实验经我院动物医学研究伦理委员会审查批准(第2020-08号)。
1.3 CCK-8法检测细胞活力取颗粒细胞在96孔板培养,每孔加入10 μL CCK-8试剂,37 ℃孵育4 h后,使用酶标仪测定450 nm波长处各孔光密度值。每24 h重复检测1次,持续观察5 d,最终以培养时间为横坐标、光密度值为纵坐标绘制细胞生长曲线,评估细胞的增殖能力。
1.4 乳酸分泌和缺氧诱导因子1α(hypoxia-inducible factor 1α,HIF-1α)蛋白检测各组颗粒细胞培养72 h后,收集细胞培养上清液待测。将各组大鼠卵巢组织匀浆离心后,取上清液待测。分别采用乳酸试剂盒(南京建成生物工程研究所有限公司)和HIF-1α试剂盒(上海博尔森生物科技有限公司)检测各组细胞上清液和大鼠卵巢组织上清液中乳酸和HIF-1α蛋白水平。
1.5 激素分泌检测各组颗粒细胞培养72 h后,收集细胞培养上清液。各组大鼠经麻醉后,通过眼眶后静脉丛采集全血样本,室温静置30 min,血液充分凝固后,4 ℃、1 500 r/min离心15 min分离血清。采用酶联免疫吸附试验试剂盒(上海酶联生物科技有限公司)分别检测各组细胞上清液和大鼠血清中雌二醇和孕酮水平。
1.6 细胞凋亡检测各组颗粒细胞培养72 h后,用胰酶消化,1 000 r/min离心5 min获取细胞沉淀,PBS洗涤,重悬并调整细胞密度至1×106/mL,加入5 μL Annexin V-FITC和10 μL PI染液(20 μg/mL),避光孵育15 min后立即上机检测。通过FlowJo 10.0软件分析各组颗粒细胞中活细胞、早期凋亡细胞和晚期凋亡/坏死细胞的百分比。
1.7 HE染色各组大鼠卵巢组织于组织固定液中固定72 h,取材、脱水、包埋、切片后,采用HE染色进行病理学检测。
1.8 Western blotting各组大鼠卵巢组织提取蛋白后,经SDS-PAGE电泳分离并转印至PVDF膜,5%脱脂牛奶室温封闭1 h。分别加入Bax(ab32503,英国abcam公司)和cleaved caspase-3(ab184787,英国abcam公司)一抗(1∶1 000稀释),4 ℃孵育过夜。TBST洗涤后,加入相应HRP标记二抗室温孵育1 h,ECL化学发光法显影。
1.9 统计学分析采用SPSS 22.0软件进行数据分析。计量资料以x±s表示,组间比较采用单因素方差分析。P < 0.05为差异有统计学意义。
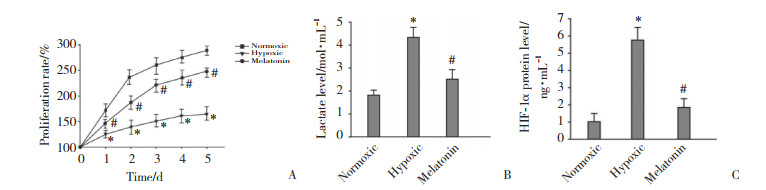
2 结果 2.1 颗粒细胞增殖率和缺氧标志物表达水平的比较CCK-8结果显示,与常氧组相比,低氧组和褪黑素组各时间点(1、2、3、4、5 d)的颗粒细胞增殖活性均明显降低(P < 0.05),且低氧组的细胞增殖活性明显低于褪黑素组(P < 0.05)。与常氧组相比,低氧组颗粒细胞乳酸和HIF-1α蛋白表达水平明显升高(P < 0.05);褪黑素能够调节上述改变,褪黑素组颗粒细胞乳酸和HIF-1α蛋白表达水平明显低于低氧组(P < 0.05)。见图 1。
|
| A, proliferation rate; B, lactate level; C, HIF-1α protein level. * P < 0.05 vs. normoxic group; # P < 0.05 vs. hypoxic group. 图 1 颗粒细胞增殖率、乳酸和HIF-1α蛋白表达水平的比较 Fig.1 Comparison of proliferation rate and levels of lactate and HIF-1α protein in granulosa cells |
2.2 大鼠卵巢组织中缺氧标志物表达水平的比较
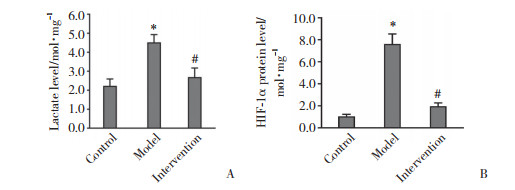
与空白对照组相比,模型组大鼠卵巢组织中乳酸和HIF-1α蛋白表达水平均明显升高(P < 0.05),且干预组乳酸和HIF-1α蛋白表达水平明显低于模型组(P < 0.05)。见图 2。
|
| A, lactate level; B, HIF-1α protein level. * P < 0.05 vs. control group; # P < 0.05 vs. model group. 图 2 大鼠卵巢组织中乳酸和HIF-1α蛋白表达水平的比较 Fig.2 Comparison of levels of lactic acid and HIF-1α protein in rat ovarian tissues |
2.3 颗粒细胞和大鼠血清中激素水平的比较
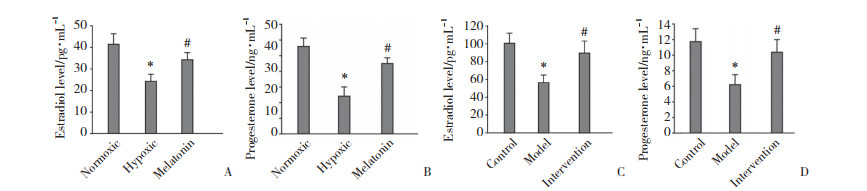
细胞实验结果显示,与常氧组相比,低氧组颗粒细胞上清液中雌二醇和孕酮水平均明显降低(P < 0.05),且低氧组雌二醇和孕酮水平明显低于褪黑素组(P < 0.05),见图 3A、3B。
|
| A, estradiol level in granulosa cells; B, progesterone level in granulosa cells; C, estradiol level in rat ovarian tissues; D, progesterone level in rat ovarian tissues. * P < 0.05 vs. normoxi or control group; # P < 0.05 vs. hypoxic or model group. 图 3 颗粒细胞和大鼠血清中激素水平的比较 Fig.3 Comparison of hormone levels in granulosa cells and rat serum |
动物实验结果显示,与空白对照组相比,模型组大鼠血清中雌二醇和孕酮水平明显降低(P < 0.05),且模型组雌二醇和孕酮水平明显低于干预组(P < 0.05),见图 3C、3D。
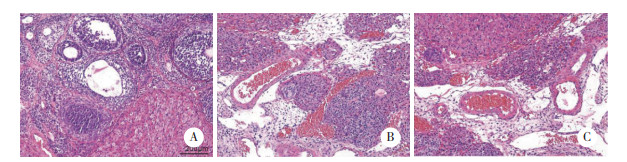
2.4 HE染色结果HE染色结果显示,与空白对照组比较,模型组大鼠原始卵泡数量减少;与模型组比较,干预组大鼠原始卵泡数量增加。见图 4。
|
| A, control group; B, model group; C, intervention group. 图 4 大鼠卵巢组织HE染色×100 Fig.4 HE staining of rat ovarian tissues ×100 |
2.5 颗粒细胞凋亡率
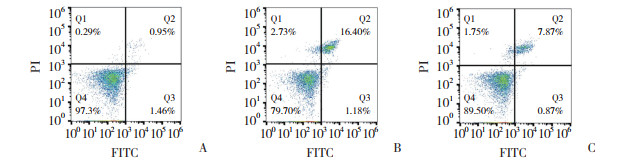
与常氧组相比,低氧组颗粒细胞的凋亡率明显升高(P < 0.05),且低氧组颗粒细胞的凋亡率明显高于褪黑素组(P < 0.05)。见图 5。
|
| A, normoxic group; B, hypoxic group; C, melatonin group. 图 5 颗粒细胞凋亡率 Fig.5 Rate of apoptosis of granulosa cells |
2.6 大鼠卵巢组织中凋亡蛋白表达水平的比较
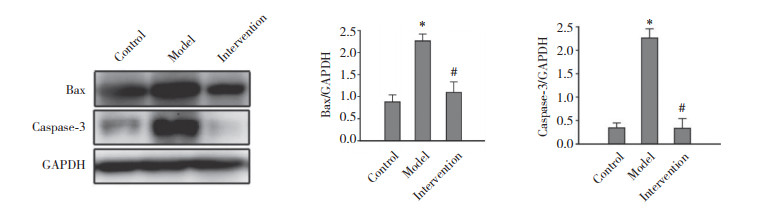
与空白对照组比较,模型组大鼠卵巢组织中促凋亡蛋白Bax和caspase-3的表达水平均明显上调(P < 0.05),且模型组Bax和caspase-3的表达水平明显高于干预组(P < 0.05)。见图 6。
|
| * P < 0.05 vs. control group; # P < 0.05 vs. model group. 图 6 大鼠卵巢组织凋亡情况 Fig.6 Apoptosis levels in rat ovarian tissues |
3 讨论
本研究通过建立长期低氧诱导的卵巢损伤模型,深入探讨了颗粒细胞凋亡在卵巢功能衰退中的作用机制,并验证了褪黑素的保护效应。本研究结果表明,低氧环境显著增加了卵巢颗粒细胞的凋亡率,表现为促凋亡蛋白Bax和效应蛋白酶caspase-3的表达上调,同时伴随卵巢内分泌功能的下降[11]。本研究结果与既往研究[12]一致,即颗粒细胞凋亡是卵泡闭锁的关键环节,过度凋亡可能导致卵巢储备功能过早衰竭。
值得注意的是,低氧诱导的氧化应激是颗粒细胞损伤的核心机制之一,ROS过量积累不仅直接破坏DNA和细胞膜结构,还可通过激活线粒体凋亡通路加速细胞死亡[13]。褪黑素通过上调Bcl-2表达并抑制Bax活化,维持线粒体膜电位的稳定性,从而减少细胞色素C的释放和caspase级联反应激活[14]。褪黑素还通过增强糖酵解和氧化磷酸化效率,改善低氧条件下的能量供应,进一步支持颗粒细胞的存活和功能维持[15]。这些发现为褪黑素在卵巢保护中的应用提供了理论依据。
本研究还发现褪黑素对HIF-1α的稳定作用,这可能与其促进低氧适应性反应有关。HIF-1α作为低氧环境下的关键转录因子,可调节多种与细胞存活相关的基因表达,从而改善组织的氧供应和代谢适应。然而,HIF-1α的长期激活也可能带来不利影响,如促进纤维化或异常血管生成,因此褪黑素对HIF-1α表达的精准调控可能具有双重意义。
从临床转化的角度来看,本研究的发现有重要的应用潜力。卵巢功能衰退的发病机制复杂,目前尚无特效治疗方法,而褪黑素作为一种天然激素,安全性高且易于获取,可能成为预防或延缓卵巢功能衰退的理想候选药物。尤其对于长期严重低氧或接受生殖毒性治疗(如化疗、放疗)的女性,褪黑素的抗氧化和抗凋亡特性可能提供额外的保护作用。本研究结果提示,颗粒细胞凋亡与卵巢内分泌功能下降密切相关,因此针对凋亡通路的干预不仅可能改善卵泡的存活率,还可能恢复正常的激素分泌,从而缓解低雌激素引发的更年期症状或生育障碍。未来研究可进一步探索褪黑素的最佳给药方案(如剂量、时机和给药途径),并评估其与其他抗氧化剂(如维生素E、辅酶Q10)的协同效应。
综上所述,本研究证实了长期低氧环境可通过细胞凋亡通路损害卵巢功能,而褪黑素有效减轻了这一损伤。本研究结果不仅深化了对卵巢生理病理过程的理解,也为开发卵巢保护策略提供了实验依据。未来研究应进一步验证褪黑素的临床疗效,并探索其与其他治疗手段联合应用的潜力,以期为卵巢功能衰退的防治提供更全面的解决方案。
| [1] |
HAMODA H, SHARMA A. Premature ovarian insufficiency, early menopause, and induced menopause[J]. Best Pract Res Clin Endocrinol Metab, 2024, 38(1): 101823. DOI:10.1016/j.beem.2023.101823 |
| [2] |
CHEN Y, ZHAO Y, MIAO C, et al. Quercetin alleviates cyclophosphamide-induced premature ovarian insufficiency in mice by reducing mitochondrial oxidative stress and pyroptosis in granulosa cells[J]. J Ovarian Res, 2022, 15(1): 138. DOI:10.1186/s13048-022-01080-3 |
| [3] |
GUO X, ZHU Y, GUO L, et al. BCAA insufficiency leads to premature ovarian insufficiency via ceramide-induced elevation of ROS[J]. EMBO Mol Med, 2023, 15(4): e17450. DOI:10.15252/emmm.202317450 |
| [4] |
XIN L, LI F, YU H, et al. Honokiol alleviates radiation-induced premature ovarian failure via enhancing Nrf2[J]. Am J Reprod Immunol, 2023, 90(4): e13769. DOI:10.1111/aji.13769 |
| [5] |
AI G, MENG M, GUO J, et al. Adipose-derived stem cells promote the repair of chemotherapy-induced premature ovarian failure by inhibiting granulosa cells apoptosis and senescence[J]. Stem Cell Res Ther, 2023, 14(1): 75. DOI:10.1186/s13287-023-03297-5 |
| [6] |
SOMAN M, HUANG LC, CAI WH, et al. Serum androgen profiles in women with premature ovarian insufficiency: a systematic review and meta-analysis[J]. Menopause, 2019, 26(1): 78-93. DOI:10.1097/GME.0000000000001161 |
| [7] |
JANG H, HONG K, CHOI Y. Melatonin and fertoprotective adjuvants: prevention against premature ovarian failure during chemotherapy[J]. Int J Mol Sci, 2017, 18(6): 1221. DOI:10.3390/ijms18061221 |
| [8] |
FLORIDO J, MARTINEZ-RUIZ L, RODRIGUEZ-SANTANA C, et al. Melatonin drives apoptosis in head and neck cancer by increasing mitochondrial ROS generated via reverse electron transport[J]. J Pineal Res, 2022, 73(3): e12824. DOI:10.1111/jpi.12824 |
| [9] |
ARIOZ BI, TASTAN B, TARAKCIOGLU E, et al. Melatonin attenuates LPS-induced acute depressive-like behaviors and microglial NLRP3 inflammasome activation through the SIRT1/Nrf2 pathway[J]. Front Immunol, 2019, 10: 1511. DOI:10.3389/fimmu.2019.01511 |
| [10] |
LI Y, PEI T, ZHU H, et al. Melatonin alleviates circadian rhythm disruption-induced enhanced luteinizing hormone pulse frequency and ovarian dysfunction[J]. J Pineal Res, 2025, 77(1): e70026. DOI:10.1111/jpi.70026 |
| [11] |
LIU J, YANG Y, HE Y, et al. Erxian decoction alleviates cisplatin- induced premature ovarian failure in rats by reducing oxidation levels in ovarian granulosa cells[J]. J Ethnopharmacol, 2023, 304: 116046. DOI:10.1016/j.jep.2022.116046 |
| [12] |
YANG ZN, DU X, WANG A, et al. Melatonin ameliorates Pb-induced mitochondrial homeostasis and ovarian damage through regulating the p38 signaling pathway[J]. Ecotoxicol Environ Saf, 2025, 292: 117937. DOI:10.1016/j.ecoenv.2025.117937 |
| [13] |
OKOYE CN, KOREN SA, WOJTOVICH AP. Mitochondrial complex ⅠROS production and redox signaling in hypoxia[J]. Redox Biol, 2023, 67: 102926. DOI:10.1016/j.redox.2023.102926 |
| [14] |
KESKIN-AKTAN A, AKBULUT KG, YAZICI-MUTLU Ç, et al. The effects of melatonin and curcumin on the expression of SIRT2, Bcl-2 and Bax in the hippocampus of adult rats[J]. Brain Res Bull, 2018, 137: 306-310. DOI:10.1016/j.brainresbull.2018.01.006 |
| [15] |
ZHU T, YAN L, DENG S, et al. Mitochondria of porcine oocytes synthesize melatonin, which improves their in vitro maturation and embryonic development[J]. Antioxidants, 2024, 13(7): 814. DOI:10.3390/antiox13070814 |
 2025, Vol. 54
2025, Vol. 54