文章信息
- 章跃, 叶里子, 罗雷茗, 王远辉, 王治, 李忠
- ZHANG Yue, YE Lizi, LUO Leiming, WANG Yuanhui, WANG Zhi, LI Zhong
- 肉苁蓉苯乙醇苷通过SIRT2-C/EBPβ-AREG轴调节成骨分化治疗骨质疏松症
- Mechanism of Cistanche phenylethanoid glycosides in treating osteoporosis by regulating osteogenic differentiation via SIRT2-C/EBPβ-AREG axis
- 中国医科大学学报, 2025, 54(11): 1011-1016, 1022
- Journal of China Medical University, 2025, 54(11): 1011-1016, 1022
-
文章历史
- 收稿日期:2024-11-07
- 网络出版时间:2025-11-21 14:30:57
2. 西南医科大学附属医院骨与关节外科,四川 泸州 646000
2. Department of Bone and Joint Surgery, Affiliated Hospital of Southwest Medical University, Luzhou 646000, China
骨质疏松症是影响中老年人健康的常见骨科疾病,近年来其发病率呈上升趋势[1]。2015年我国骨质疏松性骨折患者达269万例,预计到2035年将增至480万例以上,治疗费用高达数十亿元,将给家庭和社会带来巨大负担[2]。研究[3]表明,骨质疏松与成骨细胞分化有关。骨形成和骨吸收间的平衡是维持骨组织再生和骨质量的基础。成骨作用减少和骨吸收加速是导致骨质疏松症的病理机制。成骨细胞负责骨基质的合成、分泌和矿化,从而负责骨的形成、生长、吸收和代谢[4]。治疗骨质疏松症需要成骨细胞分化和增殖,并改善其功能。因此,探讨成骨细胞分化的机制尤为重要。目前临床主要采用药物干预治疗骨质疏松症,如抗骨吸收类药物(双膦酸盐、雌激素受体调节剂、降钙素、维生素D补充剂)和促骨形成类药物(甲状旁腺激素类似物)等。然而,长期用药可能引发剂量依赖性不良反应,常见的消化道反应包括恶心、呕吐、腹泻等。值得注意的是,尽管颌骨坏死和急性肾损伤等严重并发症的总体发生率很低,但临床上仍需密切监测其在特定人群(如肿瘤骨转移患者)中的风险[5]。
肉苁蓉具有补肾阳、益精血等功效。现代药理学研究[6]表明,肉苁蓉可通过促进成骨细胞活性、抑制破骨细胞活性来调节骨代谢,且其毒性低、不良反应少,切除卵巢的大鼠服用肉苁蓉提取物可以逆转骨质流失并预防骨质疏松症。研究[7]发现,肉苁蓉苯乙醇苷(Cistanche phenylethanoid glycosides,CPhGs)作为肉苁蓉总苷中重要的活性成分,具有独特的调节骨代谢、促进成骨细胞活性、抑制破骨细胞活性的作用,但目前尚无关于CPhGs通过调控SIRT2-C/EBPβ-AREG轴调节成骨分化的研究报道。本研究探讨了CPhGs对成骨分化的影响及其机制,旨在为CPhGs治疗骨质疏松症提供理论依据和应用基础。
1 材料与方法 1.1 材料和仪器CPhGs(松果菊苷≥40%,毛蕊花糖苷≥15%,苯乙醇苷≥80%,批号20240211),购自新疆和田帝辰医药生物有限公司。称取适量的CPhGs,溶于10 mL细胞培养基中,完全溶解后用0.22 μm微孔滤膜过滤2次,分别配制CPhGs浓度为50、100、200 μmol/L的成骨诱导培养基或破骨诱导培养基。含有CPhGs的细胞培养基均在使用前新鲜配制。
钙黄绿素AM、蛋白激酶B(protein kinase B,AKT)、磷酸化蛋白激酶B(phosphorylated protein kinase B,p-AKT)、CCAAT/增强子结合蛋白β(CCAAT/enhancer-binding protein β,C/EBPβ)、沉默调节蛋白2(Sirtuin 2,SIRT2)、骨桥蛋白(osteopontin,OPN)、Runt相关转录因子2(Runt-related transcription factor 2,RUNX2)、骨钙素(osteocalcin,OCN)抗体,购自上海碧云天生物技术股份有限公司;CO2培养箱、实时定量PCR仪,购自美国Bio-Rad公司;iMark型酶标检测仪,购自德国Eppendorf公司;lipofectamine 3000转染试剂,购自美国ThermoFisher Scientific公司;Quik Change Lightning定点突变试剂盒,购自美国Agilent公司。
1.2 实验动物和分组60只C57BL/6雌性小鼠,购自四川大学实验动物中心,所有动物实验方案获得西南医科大学实验动物伦理委员会批准(20230718-022)。
为明确CPhGs对骨质疏松的干预作用,采用经典卵巢切除法建立小鼠模型。将8周龄小鼠随机分为Sham组(仅切除卵巢周围等体积脂肪组织)、OVX组(双侧卵巢切除)和OVX+CPhGs组(双侧卵巢切除+CPhGs灌胃)。所有小鼠腹腔注射戊巴比妥钠(50 mg/kg)麻醉后,于无菌条件下行假手术或双侧卵巢切除术。术后24 h开始干预,OVX+CPhGs组小鼠CPhGs灌胃(溶于0.5%羧甲基纤维素钠溶液,300 mg·kg-1·d-1),OVX组和Sham组小鼠等体积溶剂灌胃,连续干预8周。实验期间每周监测小鼠体重变化,术后2个月通过钙黄绿素双标记法检测骨形成率,并取股骨进行micro-CT扫描(扫描参数:电压50 kV,电流200 μA,分辨率10 μm),定量分析骨体积分数(BV/TV)、骨小梁厚度(Tb.Th)和骨小梁分离度(Tb.Sp)等指标。术后第60天(总干预周期8周),对所有小鼠实施安乐死。
1.3 细胞实验和分组小鼠颅前成骨细胞系MC3T3-E1,购自广州赛库生物技术有限公司。在含10% 胎牛血清和1%青霉素-链霉素混合物的DMEM培养基中培养细胞。
为了分析CPhGs对MC3T3-E1细胞分化为成骨细胞的能力及对SIRT2-C/EBPβ-AREG轴的影响,取部分培养的MC3T3-E1细胞,随机分为对照组(NC组)和CPhGs组。NC组细胞用标准成骨诱导培养基培养,CPhGs组细胞用含50 μmol/L CPhGs的成骨诱导培养基培养。
为了验证SIRT2是否影响MC3T3-E1细胞中C/EBPβ的表达水平,取部分培养的MC3T3-E1细胞,随机分为Control组(无CPhGs处理的野生型MC3T3-E1细胞)、SIRT2 KD组(无CPhGs处理的SIRT2稳定敲低的MC3T3-E1细胞)、Control+CPhGs组(50 μmol/L CPhGs处理的野生型MC3T3-E1细胞)、SIRT2 KD+CPhGs组(50 μmol/LCPhGs处理的SIRT2稳定敲低的MC3T3-E1细胞)。SIRT2 KD组和SIRT2 KD+CPhGs组通过将小干扰RNA(small interfering RNA,siRNA)与lipofectamine 3000混合后将SIRT2敲低转染至MC3T3-E1细胞,通过实时定量PCR检测SIRT2 mRNA水平;Control组和Control+CPhGs组将NC-siRNA转染至MC3T3-E1细胞,检测SIRT2 mRNA水平。
为了证实C/EBPβ去乙酰化对促进成骨分化的影响,将剩余的MC3T3-E1细胞分为对照组(WT组)、K102R突变组、K211R突变组、CPhGs处理组(EX组)。WT组用标准成骨诱导培养基继续培养;K102R和K211R突变组根据C/EBPβ基因序列的编码区设计并合成乙酰化修饰各突变体引物序列,以野生型pc-DNA3.1-FLAG-C/EBPβ质粒为模板,利用引物序列通过Quik Change Lightning定点突变试剂盒,构建pcDNA3.1-FLAG-C/EBPβ(K102R和K211R)突变体;EX组用含50 μmol/L CPhGs的成骨诱导培养基培养。
1.4 Western blotting和免疫共沉淀检测蛋白表达将PVDF膜与一抗在4 ℃下孵育过夜,然后与辣根过氧化物酶连接的二抗(1∶5 000稀释的山羊抗兔IgG)在室温下孵育1 h。采用化学发光成像系统对蛋白印迹膜进行显影,并以β-tubulin(稀释比例1∶1 000)为内参,对目标蛋白表达水平进行相对定量分析。使用ImageJ软件进行分析。在免疫沉淀程序中,使用Pierce IP裂解缓冲液。将提取物与相应的抗体在4 ℃下孵育过夜,之后将蛋白A/G琼脂糖珠在4 ℃下孵育4 h,对蛋白A/G琼脂糖珠-抗体-抗原复合物进行共沉淀,使用SDS样品缓冲液在95 ℃下洗涤5 min。采用Western blotting检测目标蛋白的表达。
1.5 实时定量PCR检测mRNA表达水平使用TRIzol试剂提取细胞总RNA。采用超微紫外可见分光光度计测量260和280 nm波长的光密度值。根据260 nm处的光密度值计算RNA浓度,用260和280 nm处光密度的比值代表RNA的纯度。使用HiFiScript cDNA合成试剂盒(南京诺唯赞生物科技股份有限公司)合成cDNA。在实时荧光定量PCR仪上,使用ΜLtra SYBR Mixture试剂盒进行实时定量PCR。引物序列:OCN,正向5’-TCTGACCTCACAGATGCCAAG-3’,反向5’-AGGGTTAAGCTCACACTGCT-3’;OPN,正向5’-CACATGAAGAGCGGTGAGTCT-3’,反向5’-CCCTTTCCGTTGTTGTCCTG-3’;RUNX2,正向5’-GGGACTGTGGTTACCGTCAT-3’,反向5’-ATAACAGCGGAGGCATTTCG-3’;C/EBPβ,正向5’-CTTCAGCCCGTACCTGGAG-3’,反向5’-GGAGAGGAAGTCGTGGTGC-3’;GAPDH,正向5’-TGGCCTTCCGTGTTCCTAC-3’,反向5’-GAGTTGCTGTTGAAGTCGCA-3’。以GAPDH为内参基因,采用2-ΔΔCt法计算各目的基因mRNA的相对表达量。
1.6 茜素红S(alizarin red S,ARS)染色细胞培养后,用PBS清洗,4%多聚甲醛固定30 min。随后加入1% ARS溶液(pH4.2)室温染色20 min,超纯水反复洗涤至背景干净。采集图像后,使用10%氯化十六烷基吡啶溶液溶解结节并进行定量,测量562 nm波长的光密度值。
1.7 统计学分析采用SPSS 25.0软件进行统计学分析。计量资料以x±s表示,数据满足正态分布时,多组间比较采用单因素方差分析,组间两两比较使用Tukey法;数据不满足正态分布时,采用独立样本Mann-Whitney U检验进行比较。P < 0.05为差异有统计学意义。
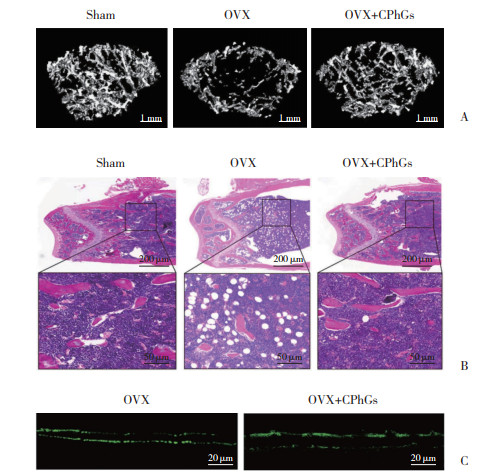
2 结果 2.1 CPhGs可减轻卵巢切除导致的小鼠骨质疏松micro-CT结果(图 1A)显示,与Sham组相比,OVX组小鼠股骨远端出现严重骨微结构破坏,表现为骨小梁稀疏断裂;OVX+CPhGs组小鼠骨小梁数量和连接性显著恢复,接近Sham组水平。结果表明,CPhGs可减轻卵巢切除引起的骨质流失。HE染色结果(图 1B)进一步证实,OVX组小鼠骨小梁数量较Sham组减少,残余小梁变细、断裂;OVX+CPhGs组小鼠骨小梁数量较OVX组增加,结构完整性明显改善。钙黄绿素双标记实验结果(图 1C)显示,OVX组荧光带模糊,间距窄,提示骨形成受到抑制;OVX+CPhGs组荧光带清晰且间距显著增宽,表明CPhGs促进骨基质矿化速率,显著增强新骨形成能力。
|
| A, representative micro-computer tomography images of the trabecular bone in the femoral metaphysis of mice; B, hematoxylin and eosin staining of the femoral sections of mice; C, calcein double-labeling images of mice in the OVX and OVX+CPhGs groups. 图 1 CPhGs可减轻卵巢切除导致的小鼠骨质疏松 Fig.1 CPhGs alleviate ovariectomy-induced osteoporosis in mice |
2.2 CPhGs对MC3T3-E1细胞成骨分化的影响
体外细胞实验结果显示,CPhGs组OCN、OPN、RUNX2蛋白和mRNA的表达水平均明显高于NC组(P < 0.05);CPhGs组第10天的碱性磷酸酶(alkaline phosphatase,ALP)活性明显高于NC组(P < 0.05)。结果表明,CPhGs可显著促进成骨细胞分化。见表 1。
| Item | NC group | CPhGs group |
| OCN protein | 0.48±0.14 | 1.24±0.181) |
| OCN mRNA | 1.00±0.11 | 1.61±0.231) |
| OPN protein | 0.51±0.15 | 1.05±0.441) |
| OPN mRNA | 1.03±0.12 | 2.11±0.241) |
| RUNX2 protein | 0.77±0.21 | 1.08±0.251) |
| RUNX2 mRNA | 1.02±0.14 | 1.58±0.171) |
| ALP activity at day 10 | 0.21±0.02 | 0.44±0.051) |
| 1)P < 0.05 vs. NC group. | ||
2.3 CPhGs对SIRT2-C/EBPβ-AREG轴的影响
细胞实验结果(表 2)显示,与NC组相比,CPhGs组MC3T3-E1细胞中C/EBPβ蛋白和mRNA表达水平、AREG mRNA表达水平明显升高(P < 0.05)。结果表明,C/EBPβ下游靶基因被激活。与NC组相比,CPhGs组SIRT2 mRNA表达水平明显升高(P < 0.05),其蛋白水平也同步升高(P < 0.05)。而CPhGs组SIRT1、SIRT3、SIRT4、SIRT5 mRNA表达水平无明显变化(P > 0.05),证实了SIRT2通路的特异性。
| Item | NC group | CPhGs group |
| C/EBPβ protein | 0.51±0.06 | 1.21±0.111) |
| C/EBPβ mRNA | 1.00±0.10 | 1.15±0.141) |
| AREG mRNA | 1.01±0.15 | 2.05±0.241) |
| SIRT1 mRNA | 1.03±0.12 | 1.01±0.11 |
| SIRT2 protein | 0.26±0.08 | 0.37±0.071) |
| SIRT2 mRNA | 0.87±0.08 | 1.88±0.211) |
| SIRT3 mRNA | 1.01±0.14 | 1.28±0.17 |
| SIRT4 mRNA | 1.21±0.12 | 1.04±0.05 |
| SIRT5 mRNA | 1.06±0.05 | 1.08±0.03 |
| 1)P < 0.05 vs. NC group. | ||
2.4 CPhGs对SIRT2和C/EBPβ的影响及作用机制
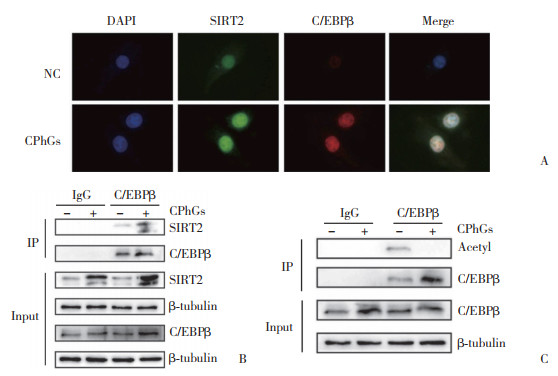
细胞免疫荧光染色结果(图 2A)表明,CPhGs组与NC组相比,SIRT2与C/EBPβ蛋白表达及核内共定位显著增强。NC组SIRT2和C/EBPβ荧光信号微弱,CPhGs组中SIRT2和C/EBPβ荧光强度均显著增强,且二者在核内形成明显共定位信号,提示相互作用增强。免疫共沉淀结果进一步证实,在C/EBPβ抗体下拉复合物中,与NC组相比,CPhGs组SIRT2蛋白量显著增加(图 2B);C/EBPβ免疫沉淀产物中,CPhGs组乙酰化赖氨酸(Acetyl)信号降低,而总C/EBPβ蛋白量不变(图 2C),表明CPhGs显著增强C/EBPβ和SIRT2间的相互作用,同时抑制MC3T3-E1细胞中内源性C/EBPβ乙酰化。
|
| A, immunofluorescence analysis of SIRT2 (red) and C/EBPβ (green) in CPhGs-treated MC3T3-E1 cells (×200);B, co-immunoprecipitation (co-IP) analysis of SIRT2-C/EBPβ interaction; C, acetylation level of C/EBPβ detected by pan-acetyllysine antibody after IP purification.Effect of CPhGs on SIRT2 and C/EBPβ and its mechanism 图 2 CPhGs对SIRT2和C/EBPβ的影响及作用机制 |
2.5 SIRT2对C/EBPβ蛋白和mRNA表达的影响
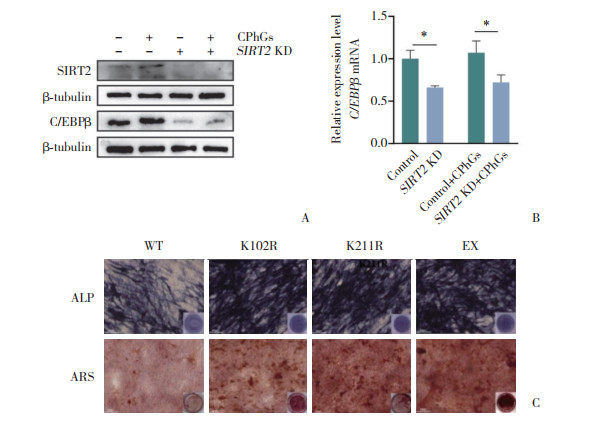
细胞实验结果表明,Control组与SIRT2 KD组相比,SIRT2敲低显著降低了MC3T3-E1细胞中C/EBPβ蛋白和mRNA表达水平;Control+CPhGs组与SIRT2 KD+CPhGs组相比,SIRT2敲低降低C/EBPβ蛋白和mRNA表达水平,且CPhGs无法逆转SIRT2敲低导致的C/EBPβ蛋白和mRNA表达水平降低(图 3A、3B)。以上结果表明,SIRT2缺失可显著降低C/EBPβ蛋白的积累和C/EBPβ mRNA的表达。
|
| A, Western blotting of C/EBPβ protein expression after SIRT2 knockdown (KD); B, quantitative real-time PCR analysis of C/EBPβ mRNA expression after SIRT2 KD; C, ALP staining on day 7 (×100) and ARS staining on day 14 (×100) in the WT, K102R, K211R, and EX groups. *P < 0.05. 图 3 C/EBPβ去乙酰化促进成骨分化 Fig.3 Deacetylation of C/EBPβ promotes osteogenic differentiation |
2.6 C/EBPβ去乙酰化对成骨分化的影响
构建C/EBPβ乙酰化位点突变体(K102R和K211R)模拟持续性去乙酰化后,分别检测各组细胞在分化早期(第7天)的ALP活性和终末期(第14天)的矿化能力。与WT组相比,K102R和K211R突变组ALP阳性面积增加,同时ARS染色结果表明,K102R和K211R突变组细胞外基质矿化增强;但EX组ALP与ARS增幅显著高于K102R和K211R突变组,表明CPhGs可通过协同调控K102和K211双位点实现全面促骨形成(图 3C)。结果表明,CPhGs的促骨形成效应与C/EBPβ去脱乙酰化介导的早期分化和终末矿化相关,为CPhGs通过SIRT2/CEBPβ/AREG轴影响成骨分化机制提供了功能学证据。
3 讨论骨质疏松症已成为全球公共卫生问题,严重影响患者的生活质量。中药如肉苁蓉、女贞子、巴戟天等,在治疗骨质疏松症中发挥重要作用,由于不良反应少、疗效稳定,越来越受到关注[8-9]。肉苁蓉及其化学成分具有调节骨形成和骨吸收的功能,在防治骨质疏松症方面具有巨大的潜力。研究[10]发现,肉苁蓉提取物能够促进骨髓间充质干细胞向成骨细胞分化,有效增加骨量,同时减少骨吸收。研究[11]发现,肉苁蓉多糖能够抑制破骨细胞生成和羟基磷灰石的吸收,其作用机制包括抑制破骨细胞标志基因(如Ctsk、MMP9和ACP5)的表达。
本研究系统探讨了CPhGs在骨质疏松治疗中的作用及其分子机制。通过体内外实验,本研究发现CPhGs通过调控SIRT2-C/EBPβ-AREG轴显著促进成骨分化,为天然产物靶向骨代谢调控提供了新的理论依据。
本研究证实,CPhGs通过激活SIRT2-C/EBPβ-AREG轴改善卵巢切除小鼠的骨丢失表型,显著增加股骨小梁数量并促进骨形成。本研究结果显示,CPhGs显著上调成骨分化标志基因(OCN、OPN、RUNX2)和ALP活性。RUNX2作为成骨分化的核心调控因子[12],其表达上调可能直接驱动骨基质矿化,而ALP活性增强则进一步支持其对成骨细胞功能成熟的促进作用。本研究首次揭示了CPhGs通过上调SIRT2表达,增强其与C/EBPβ的相互作用,并诱导C/EBPβ去乙酰化。去乙酰化的C/EBPβ不仅通过构象变化增强转录活性,还显著上调AREG mRNA表达,后者作为表皮生长因子受体配体可能激活PI3K-AKT通路,从而促进成骨分化,这一机制与ZHANG等[13]报道的肉苁蓉提取物通过PI3K/AKT通路抑制破骨细胞分化一致。通过构建C/EBPβ乙酰化位点突变体(K102R和K211R),直接证实C/EBPβ去乙酰化促进细胞外基质钙化,而SIRT2敲低实验进一步验证了该通路在CPhGs作用中的必要性,表明SIRT2介导的C/EBPβ去乙酰化是CPhGs促进骨形成的核心环节。这些发现不仅拓展了SIRT家族在骨稳态中的多样性作用,也为靶向蛋白翻译后修饰治疗骨质疏松症提供了新策略。
成骨细胞在复杂的骨重塑过程中起关键作用。骨形成与吸收间平衡的破坏主要由成骨细胞调节,是导致骨质疏松症发展的重要因素。因此,促进骨形成是骨质疏松症的基本治疗策略。有效的骨重塑依赖于成骨细胞和破骨细胞间的相互作用和协调。AREG是表皮生长因子家族的成员,在调节各种类型细胞的生长、凋亡和迁移中发挥关键作用[14]。SIRT2是一种依赖于NAD+的脱乙酰酶,主要在细胞质中表达,但也存在于线粒体和细胞核中,使其成为Sirtuin蛋白家族的一个独特成员[15]。C/EBPβ作为转录因子,在SIRT2的控制下发生脱乙酰化,并增加各种基因的转录活性。在成骨细胞分化过程中,C/EBPβ与多个基因结合,以改变其转录。本研究结果表明,CPhGs通过增强C/EBPβ蛋白表达并促进其与SIRT2的相互作用,显著抑制C/EBPβ的乙酰化修饰,进而正向调控AREG mRNA的表达,从而促进成骨分化。尽管C/EBPβ的表达水平与AREG转录呈显著正相关,但其是否直接作为AREG的转录因子仍需进一步验证。
综上所述,CPhGs通过SIRT2使C/EBPβ去乙酰化,从而促进AREG表达,促进成骨细胞分化,改善骨质疏松,CPhGs有作为骨质疏松症治疗药物的潜力。
| [1] |
AIBAR-ALMAZÁN A, VOLTES-MARTÍNEZ A, CASTELLOTE-CABALLERO Y, et al. Current status of the diagnosis and management of osteoporosis[J]. Int J Mol Sci, 2022, 23(16): 9465. DOI:10.3390/ijms23169465 |
| [2] |
SONG S, GUO Y, YANG Y, et al. Advances in pathogenesis and therapeutic strategies for osteoporosis[J]. Pharmacol Ther, 2022, 237: 108168. DOI:10.1016/j.pharmthera.2022.108168 |
| [3] |
DAKKAK M, BANERJEE M, WHITE L. Osteoporosis treatment: updated guidelines from ACOG[J]. Am Fam Physician, 2023, 108(1): 100-104. |
| [4] |
DA W, TAO L, ZHU Y. The role of osteoclast energy metabolism in the occurrence and development of osteoporosis[J]. Front Endocrinol (Lausanne), 2021, 12: 675385. DOI:10.3389/fendo.2021.675385 |
| [5] |
UKON Y, MAKINO T, KODAMA J, et al. Molecular-based treatment strategies for osteoporosis: a literature review[J]. Int J Mol Sci, 2019, 20(10): 2557. DOI:10.3390/ijms20102557 |
| [6] |
ZOU Z, LIU W, CAO L, et al. Advances in the occurrence and biotherapy of osteoporosis[J]. Biochem Soc Trans, 2020, 48(4): 1623-1636. DOI:10.1042/BST20200005 |
| [7] |
WANG C, LI F, LI Y, et al. Cistanche deserticola for regulation of bone metabolism: therapeutic potential and molecular mechanisms on postmenopausal osteoporosis[J]. Chin J Integr Med, 2023, 29(1): 74-80. DOI:10.1007/s11655-022-3518-z |
| [8] |
ZHOU S, FENG D, ZHOU Y, et al. Analysis of the active ingre- dients and health applications of Cistanche[J]. Front Nutr, 2023, 10: 1101182. DOI:10.3389/fnut.2023.1101182 |
| [9] |
ZHANG Y, LONG X, RUAN X, et al. SIRT2-mediated deacetylation and deubiquitination of C/EBPβ prevents ethanol-induced liver injury[J]. Cell Discov, 2021, 7(1): 93. DOI:10.1038/s41421-021-00326-6 |
| [10] |
LI J, ZOU Z, SU X, et al. Cistanche deserticola improves ovariectomized-induced osteoporosis mainly by regulating lipid metabolism: insights from serum metabolomics using UPLC/Q-TOF-MS[J]. J Ethnopharmacol, 2024, 322: 117570. DOI:10.1016/j.jep.2023.117570 |
| [11] |
SONG D, CAO Z, LIU Z, et al. Cistanche deserticola polysaccharide attenuates osteoclastogenesis and bone resorption via inhibiting RANKL signaling and reactive oxygen species production[J]. J Cell Physiol, 2018, 233(12): 9674-9684. DOI:10.1002/jcp.26882 |
| [12] |
IWOBI N, SPARKS NR. Endocrine disruptor-induced bone damage due to hormone dysregulation: a review[J]. Int J Mol Sci, 2023, 24(9): 8263. DOI:10.3390/ijms24098263 |
| [13] |
ZHANG B, YANG LL, DING SQ, et al. Anti-osteoporotic activity of an edible traditional Chinese medicine Cistanche deserticola on bone metabolism of ovariectomized rats through RANKL/RANK/TRAF6-mediated signaling pathways[J]. Front Pharmacol, 2019, 10: 1412. DOI:10.3389/fphar.2019.01412 |
| [14] |
NAKANISHI T, KOMA YI, MIYAKO S, et al. AREG upregulation in cancer cells via direct interaction with cancer-associated fibroblasts promotes esophageal squamous cell carcinoma progression through EGFR-Erk/p38 MAPK signaling[J]. Cells, 2024, 13(20): 1733. DOI:10.3390/cells13201733 |
| [15] |
李雨珊, 王鹏皓. 白藜芦醇介导SIRT2干预地塞米松诱导的骨髓间充质干细胞线粒体自噬[J]. 中国医科大学学报, 2024, 53(8): 731-735. DOI:10.12007/j.issn.0258-4646.2024.08.010 |
 2025, Vol. 54
2025, Vol. 54