文章信息
- 董文征, 陈平, 刘炫鑫, 高奇, 王兵
- DONG Wenzheng, CHEN Ping, LIU Xuanxin, GAO Qi, WANG Bing
- 醉茄素A通过抑制创伤性脑损伤大鼠脑组织AQP4表达减轻脑水肿
- Withaferin A alleviates cerebral edema by inhibiting AQP4 expression in the brain tissue of rats with traumatic brain injury
- 中国医科大学学报, 2025, 54(10): 931-936
- Journal of China Medical University, 2025, 54(10): 931-936
-
文章历史
- 收稿日期:2024-08-14
- 网络出版时间:2025-10-15 13:45:29
2. 南华大学衡阳医学院附属第二医院神经外科, 湖南 衡阳 421001
2. Department of Neurosurgery, The Second Affiliated Hospital, Hengyang Medical School, University of South China, Hengyang 421001, China
创伤性脑损伤(traumatic brain injury,TBI)是神经外科常见的急重症之一,主要是由外力击打头部造成的脑功能障碍和脑神经组织损伤,其继发性的脑水肿可引发颅内高压和脑疝,使TBI具有较高的致残率和致死率,而血脑屏障的破坏是导致创伤性脑水肿发生的主要原因之一[1]。水通道蛋白(aquaporin,AQP)4作为生物膜通道蛋白家族成员之一,有介导水在不同类型细胞膜间跨膜转运的作用。研究[2-3]发现,AQP4在各种颅脑疾病导致的脑水肿的形成和消散中发挥关键作用,提示调控AQP4表达可能成为治疗TBI的潜在靶点。醉茄素A是从南非醉茄中提取的一种甾体内酯,可抑制NF-κB活性,具有抗炎、抗氧化、抗血管生成、抗肿瘤等广泛的药理活性[4]。研究[5]报道,醉茄素A可改善缺血性脑卒中大鼠神经行为功能,通过提高机体抗氧化水平抑制神经元凋亡。然而,醉茄素A是否对TBI后脑水肿有改善作用目前鲜有报道。本研究拟通过建立TBI大鼠模型,探讨醉茄素A对TBI大鼠脑组织AQP4表达及脑水肿的影响。
1 材料与方法 1.1 材料ZH-ZYQ型自由落体脑损伤模型打击器(安徽正华生物仪器设备有限公司),GelDoc XR System凝胶成像系统(美国BIO-RAD公司),QS5实时荧光定量PCR仪、EVOS M5000荧光显微镜(美国Thermo Fisher Scientific公司)。
醉茄素A(纯度 > 99.0%,成都普思生物科技股份有限公司),伊文思蓝(美国Sigma公司),AQP4、Bax、Bcl-2、cleaved caspase-3及β-actin抗体(英国abcam公司),HE染色试剂盒(北京索莱宝科技有限公司),TRIzol试剂盒(美国Invitrogen公司),RIPA裂解缓冲液(武汉博士德生物工程有限公司),TUNEL细胞凋亡检测试剂盒(绿色荧光,上海碧云天生物技术股份有限公司)。
SPF级SD雄性大鼠共75只,6周龄,体重200~220 g,由重庆医科大学实验动物中心提供,实验动物生产许可证号SCXK(渝)2018-0003。实验前适应性喂养1周,自由饮水和摄食。本研究获得南华大学附属第二医院伦理委员会批准(2023032)。
1.2 方法 1.2.1 动物模型制备与分组参考文献[6],采用自由落体打击法建立TBI模型。将麻醉后大鼠固定于ZH-ZYQ型自由落体脑损伤模型打击器上,头部备皮并用乙醇擦拭消毒,于右侧颅骨作直径5 mm的圆形骨窗,用25 g砝码从40 cm高处沿导管自由坠落撞击至右侧骨窗硬膜上,止血后用骨蜡封闭骨窗并缝合创面。假手术组不进行打击损伤,仅作骨窗后由骨蜡封闭,即可缝合创面。大鼠在被撞击后出现短暂呼吸抑制则视为造模成功。将造模成功的大鼠随机分为模型组,醉茄素A低、中、高剂量组; 另设置假手术组,每组15只。醉茄素A低、中、高剂量组大鼠分别给予25、50、100 mg/kg醉茄素A腹腔注射,模型组及假手术组大鼠腹腔注射等量生理盐水,1次/d,连续7 d。
1.2.2 神经功能缺损评分(neurological severity score,NSS)药物干预结束后,参考文献[7],评估各组大鼠NSS,从运动、感觉、反射和平衡等多方面综合评价,最高分为18分,评分越高则神经功能损伤越严重。
1.2.3 脑组织含水量测定药物干预结束后,每组随机选取5只大鼠取出全脑组织,滤纸吸干后称脑湿重,于85 ℃恒温干燥箱中持续烘干24 h后称脑干重。脑组织含水量(%)=(湿重-干重)/湿重×100。
1.2.4 血脑屏障通透性测定药物干预结束后,每组随机选取5只大鼠,以5 mL/kg的剂量经静脉注射2.5%伊文思蓝,注射后立即处死大鼠取出脑组织,生理盐水洗净血液,置于10%三氯醋酸中沉淀蛋白,加入无水乙醇,匀浆机充分匀浆后离心取上清,再将上清液置于37 ℃水浴锅中水浴48 h,于酶标仪上设定波长620 nm检测光密度(optical density,OD)值,根据标准曲线计算脑组织中伊文思蓝含量。
1.2.5 HE染色取损伤侧部分大脑皮层组织,于4%多聚甲醛中固定24 h,组织脱水后石蜡包埋,作连续5 μm切片,行常规HE染色,显微镜下观察组织病理改变。
1.2.6 TUNEL染色取损伤侧部分海马组织,4%多聚甲醛室温固定2 h,用冰冻切片机按厚度14 μm切片,随后按照TUNEL细胞凋亡检测试剂盒说明书进行操作,绿色荧光标记,抗荧光淬灭封片液封片后荧光显微镜下观察。选取3个非连续切片,统计海马CA1区TUNEL染色阳性细胞数量,取均值作为海马组织细胞凋亡水平。
1.2.7 实时定量PCR取损伤侧部分大脑皮层组织,研磨后匀浆,采用TRIzol试剂盒提取总RNA,反转录后对互补的DNA链定量测定。将cDNA产物2 μL、SYBR预混液16 μL、上下游引物各1 μL,于95 ℃预变性90 s,60℃退火40 s,72 ℃延伸30 s条件下进行实时定量PCR扩增,共45个循环。以β-actin为内参,采用2-ΔΔCt法计算大脑皮层组织中AQP4 mRNA相对表达量。引物序列见表 1。
| Gene | Primer sequences |
| AQP4 | Forward,5’-TGAATCCAGCTCGATCCTTTG-3’ |
| Reverse,5’-TATCCAGTGGTTTTCCCAGTTTC-3’ | |
| β-actin | Forward,5’-CATCTCTTGCTCGAAGTCCA-3’ |
| Reverse,5’-ATCATGTTTGAGACCTTCAACA-3’ |
1.2.8 Western blotting检测
药物干预结束后,取损伤侧部分大脑皮层组织及海马组织,加入适量生理盐水将组织研磨后充分匀浆,于RIPA裂解液中分离蛋白,12 000 r/min离心10 min后取上清,对总蛋白进行定量。将20 μg总蛋白与上样缓冲液均匀混合,100 ℃水浴5 min,离心后上样,10% SDS-PAGE电泳并进行转膜,室温封闭2 h,加入AQP4(1∶1 000)、Bax(1∶1 000)、Bcl-2(1∶1 000)、cleaved caspase-3(1∶1 000)、β-actin(1∶1 000)一抗,4 ℃摇床孵育过夜; 然后加入二抗(1∶10 000),室温孵育2 h,加入ECL显色液,以β-actin为内参,计算AQP4、Bax、Bcl-2及cleaved caspase-3蛋白相对表达量。
1.3 统计学分析采用SPSS 17.0软件进行统计分析,数据用x±s表示。采用单因素方差分析对大鼠NSS、脑含水量、伊文思蓝含量及AQP4 mRNA和蛋白表达水平进行多组间比较,若方差分析结果有统计学意义,则进一步采用LSD-t法进行组间两两比较。P < 0.05为差异有统计学意义。
2 结果 2.1 各组大鼠NSS及脑组织含水量比较与假手术组比较,模型组大鼠NSS及脑组织含水量显著升高(P < 0.01); 与模型组比较,醉茄素A中、高剂量组大鼠NSS及脑组织含水量显著降低(P < 0.05),而醉茄素A低剂量组无统计学差异(P > 0.05)。见表 2。
| Group | NSS(n = 15) | Brain water content(%,n = 5) |
| Sham | 1.13±0.46 | 74.26±2.85 |
| Model | 13.07±0.611) | 83.52±3.071) |
| Withaferin A-L | 12.27±0.53 | 83.23±4.24 |
| Withaferin A-M | 7.93±0.542) | 77.36±4.052) |
| Withaferin A-H | 3.07±0.422) | 75.54±2.312) |
| 1)P < 0.05 vs. sham group;2)P < 0.05 vs. model group. | ||
2.2 各组大鼠血脑屏障通透性变化
假手术组、模型组及醉茄素A低、中、高剂量组大鼠脑组织中伊文思蓝含量分别为1.43±0.18、5.26±0.34、5.04±0.45、4.11±0.26和2.87±0.21,与假手术组比较,模型组大鼠血脑屏障通透性显著升高(P < 0.01); 与模型组比较,醉茄素A中、高剂量组大鼠血脑屏障通透性显著降低(P < 0.05),而醉茄素A低剂量组无统计学差异(P > 0.05)。
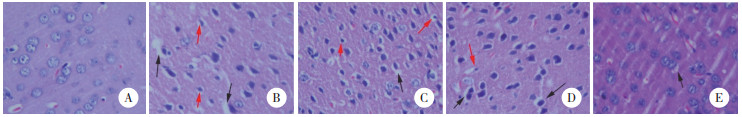
2.3 各组大鼠大脑皮层组织病理学变化假手术组大鼠大脑皮层组织结构完整,细胞核形态正常; 模型组和醉茄素A低剂量组大鼠大脑皮层组织细胞核明显固缩,可见胞质透明、轻度水肿,少量神经元变性坏死; 醉茄素A中剂量组大鼠大脑皮层组织细胞核轻度固缩,细胞水肿程度有所减轻,病理形态较模型组明显改善; 醉茄素A高剂量组大鼠大脑皮层组织细胞核形态趋于正常,无明显水肿及神经元变性坏死现象。见图 1。
|
| A, sham group; B, model group; C, withaferin A-L group; D, withaferin A-M group; E, withaferin A-H group. Red arrow, karyopyknosis; black arrow, edema. 图 1 各组大鼠脑皮质层组织HE染色× 400 Fig.1 HE staining of the cerebral cortex of the rats in each group × 400 |
2.4 各组大鼠海马组织细胞凋亡情况
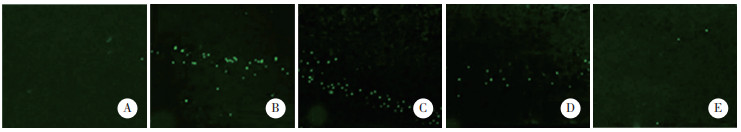
假手术组大鼠海马组织未见阳性绿色荧光,模型组和醉茄素A低剂量组大鼠海马组织可见大量绿色荧光,醉茄素A中剂量组大鼠海马组织可见少量绿色荧光,醉茄素A高剂量组大鼠海马组织隐约可见绿色荧光。假手术组、模型组、醉茄素A低、中、高剂量组大鼠海马组织细胞TUNEL染色阳性细胞数量分别为(3.03±1.25)个、(34.41±4.70)个、(33.08±4.19)个、(15.54±6.22)个和(7.96±4.87)个,与假手术组比较,模型组大鼠海马组织细胞凋亡水平显著升高(P < 0.01); 与模型组比较,醉茄素A中、高剂量组大鼠海马组织细胞凋亡水平显著降低(P < 0.05),而醉茄素A低剂量组无统计学差异(P > 0.05)。见图 2。
|
| A, sham group; B, model group; C, withaferin A-L group; D, withaferin A-M group; E, withaferin A-H group. 图 2 各组大鼠海马组织TUNEL染色×200 Fig.2 TUNEL staining of the hippocampal tissue of the rats in each group ×200 |
2.5 各组大鼠大脑皮层组织AQP4 mRNA及蛋白表达水平
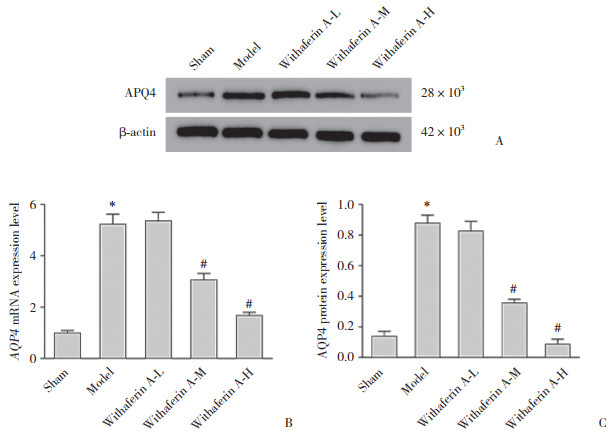
与假手术组比较,模型组大鼠大脑皮层组织中AQP4 mRNA及蛋白表达水平显著升高(P < 0.01); 与模型组比较,醉茄素A中、高剂量组大鼠大脑皮层组织中AQP4 mRNA及蛋白表达水平显著降低(P < 0.05),而醉茄素A低剂量组无统计学差异(P > 0.05)。见图 3。
|
| A, protein expression gray value; B, AQP4 mRNA expression level; C, AQP4 protein expression level. *P < 0.05 vs.sham group; #P < 0.05 vs.model group. 图 3 各组大脑皮层组织中AQP4 mRNA及蛋白表达 Fig.3 AQP4 mRNA and protein expression in the cerebral cortex tissue of each group |
2.6 各组大鼠海马组织凋亡相关蛋白表达水平
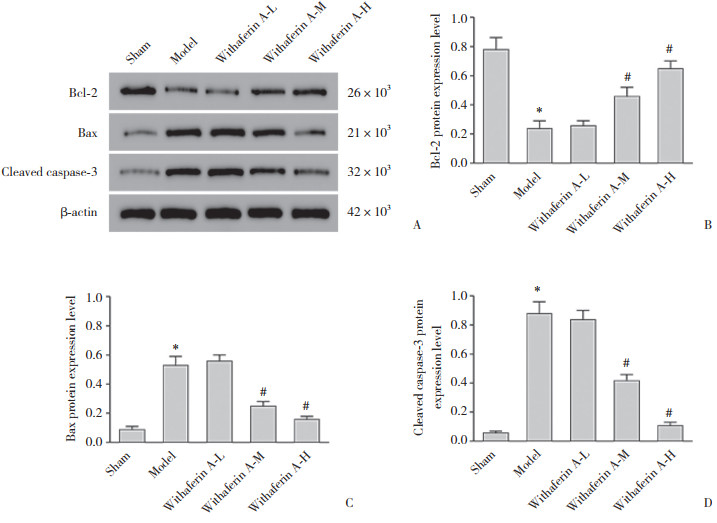
与假手术组比较,模型组大鼠海马组织中Bax、cleaved caspase-3蛋白表达水平显著升高(P < 0.01),Bcl-2蛋白表达水平显著降低(P < 0.01); 与模型组比较,醉茄素A中、高剂量组大鼠海马组织中Bax、cleaved caspase-3蛋白表达水平显著降低(P < 0.05),Bcl-2蛋白表达水平显著升高(P < 0.05),而醉茄素A低剂量组无统计学差异(P > 0.05)。见图 4。
|
| A, protein expression gray values; B, Bcl-2 protein expression levels; C, Bax protein expression levels; D, cleaved caspase-3 protein expression levels. *P < 0.05 vs.sham group; #P < 0.05 vs.model group. 图 4 Western blotting检测各组海马组织中凋亡相关蛋白表达 Fig.4 The expression of apoptosis-related proteins in the hippocampal tissues of each group as detected by Western blotting |
3 讨论
TBI分为外力直接导致的原发性损伤和后续水肿、炎症等引起的继发性损伤。研究[8]发现,醉茄素A可通过调节小胶质细胞活化和抑制内皮细胞凋亡改善脑水肿,但其在蛋白及基因层面对TBI的作用尚不明确。本研究采用自由落体Feeney法建立TBI大鼠模型,醉茄素A干预后,大鼠皮层神经元结构改善、NSS显著降低,且脑组织含水量与血脑屏障通透性降低,说明醉茄素A具有修复TBI大鼠血脑屏障,改善其脑水肿及神经功能的作用。
AQP是介导水分子跨膜转运的关键蛋白家族,其中AQP4与脑血管疾病关系密切[9]。AQP4是维持大脑水平衡、调节神经胶质细胞、脑脊液和血管间水分的关键结构基础[10]。
目前,众多学者致力于探究药物对TBI后继发性脑水肿及AQP4表达的调控作用,旨在开发有效防治继发性脑损伤的策略。熊翱等[11]研究发现,沉默AQP4表达可显著改善TBI大鼠创伤后脑水肿。同时,汪棋笙等[12]研究表明,高浓度的丙戊酸钠可通过抑制AQP4蛋白表达,减轻TBI大鼠脑水肿并改善大脑损伤。上述研究结果共同揭示了改善TBI后脑水肿与降低AQP4表达之间存在密切关联。
细胞凋亡是TBI后继发性脑损伤的重要机制。TBI后代谢应激、局部循环障碍及脑水肿加剧缺血缺氧,导致神经细胞在原发损伤基础上发生继发性凋亡[13]。海马作为边缘叶核心结构,与皮层功能高度整合,共构边缘系统。TBI中,大脑皮层以显著的脑水肿和血脑屏障损伤为特征,而海马区域则因凋亡致功能性神经元丢失,引发神经网络破坏和神经递质失衡,成为认知障碍等神经缺损的主要原因[14]。尽管AQP4非直接凋亡执行蛋白,但其水通道功能通过介导脑水肿、破坏微环境稳态及放大炎症,间接创造促凋亡微环境,在TBI继发性损伤中发挥关键促凋亡作用[15]。本研究结果显示,醉茄素A干预显著降低了TBI大鼠脑皮层组织中的AQP4 mRNA及蛋白表达水平,同时抑制海马组织细胞凋亡,并降低凋亡相关蛋白Bax和cleaved caspase-3表达水平,上调Bcl-2蛋白表达,说明醉茄素A减轻TBI大鼠脑水肿并改善其神经功能缺陷,可能与抑制AQP4表达有关。
综上所述,醉茄素A可能通过抑制AQP4表达减少细胞凋亡,修复TBI大鼠血脑屏障并减轻脑水肿,发挥神经保护作用。但因未设阳性对照组,其临床价值尚待明确,后续需在细胞水平深入探究醉茄素A调控AQP4改善TBI的具体机制。
| [1] |
赵智慧, 翟秀丽, 王晶, 等. Ghrelin介导HO-1/PGC-1α信号通路调节线粒体氧化应激改善大鼠创伤性脑损伤[J]. 中国医科大学学报, 2025, 54(4): 351-358. DOI:10.12007/j.issn.0258-4646.2025.04.012 |
| [2] |
薄文集, 石召华, 王平, 等. 七叶皂苷钠冻干粉对出血性脑水肿大鼠脑组织MMP-9及AQP4的影响[J]. 中华中医药杂志, 2018, 33(3): 1060-1062. |
| [3] |
刘佳丽, 王晔. 缺血后处理通过水通道蛋白-4对大鼠缺血再灌注损伤的脑保护作用及其机制[J]. 中风与神经疾病杂志, 2019, 36(3): 209-213. DOI:10.19845/j.cnki.zfysjjbzz.2019.03.004 |
| [4] |
王番, 宋颖, 贾艳艳, 等. 醉茄素A药理活性研究进展[J]. 中国临床药理学杂志, 2018, 34(14): 1714-1718. DOI:10.13699/j.cnki.1001-6821.2018.14.037 |
| [5] |
周弟弥, 甘露, 陈琳, 等. 醉茄素A对缺血性脑卒中大鼠的神经保护作用及其机制[J]. 吉林大学学报(医学版), 2021, 47(4): 919-925. DOI:10.13481/j.1671-587X.20210414 |
| [6] |
FEENEY DM, BOYESON MG, LINN RT, et al. Responses to cortical injury: I. Methodology and local effects of contusions in the rat[J]. Brain Res, 1981, 211(1): 67-77. DOI:10.1016/0006-8993(81)90067-6 |
| [7] |
LIU SJ, ZOU Y, BELEGU V, et al. Co-grafting of neural stem cells with olfactory en sheathing cells promotes neuronal restoration in traumatic brain injury with an anti-inflammatory mechanism[J]. J Neuroinflammation, 2014, 11: 66. DOI:10.1186/1742-2094-11-66 |
| [8] |
ZHOU ZX, XIANG WJ, JIANG YL, et al. Withaferin A alleviates traumatic brain injury induced secondary brain injury via suppres-sing apoptosis in endothelia cells and modulating activation in the microglia[J]. Eur J Pharmacol, 2020, 874: 172988. DOI:10.1016/j.ejphar.2020.172988 |
| [9] |
张海江, 樊海梅, 陈杰, 等. 急性大血管闭塞性卒中患者中omentin-1、AQP4、VILIP-1与急诊血管内治疗后血管再通的关系[J]. 中国医科大学学报, 2024, 53(2): 160-165. DOI:10.12007/j.issn.0258-4646.2024.02.012 |
| [10] |
江金文, 刘会云, 李美华. AQP4与创伤性脑水肿的研究进展[J]. 国际神经病学神经外科学杂志, 2017, 44(2): 213-217. DOI:10.16636/j.cnki.jinn.2017.02.023 |
| [11] |
熊翱, 金戈, 熊仁平, 等. 沉默水通道蛋白4对脑创伤致大鼠学习记忆功能障碍的作用研究[J]. 中华危重病急救医学, 2018(2): 170-175. DOI:10.3760/cma.j.issn.2095-4352.2018.02.015 |
| [12] |
汪棋笙, 丁华强, 廖帅, 等. 丙戊酸钠对创伤性颅脑损伤大鼠脑组织中金属基质蛋白-9及水通道蛋白4表达的影响[J]. 医学研究生学报, 2019, 32(8): 809-814. DOI:10.16571/j.cnki.1008-8199.2019.08.005 |
| [13] |
BOWMAN CE, SCAFIDI J, SCAFIDI S. Metabolic perturbations after pediatric TBI: it's not just about glucose[J]. Exp Neurol, 2019, 316: 74-84. DOI:10.1016/j.expneurol.2019.03.018 |
| [14] |
DA SILVA FIORIN F, DO ESPíRITO SANTO CC, DA SILVA JT, et al. Inflammation, brain connectivity, and neuromodulation in post-traumatic headache[J]. Brain Behav Immun Health, 2024, 35: 100723. DOI:10.1016/j.bbih.2024.100723 |
| [15] |
LI XH, XIE ZX, ZHOU Q, et al. TGN-020 alleviate inflammation and apoptosis after cerebral ischemia-reperfusion injury in mice through glymphatic and ERK1/2 signaling pathway[J]. Mol Neuro-biol, 2024, 61(2): 1175-1186. DOI:10.1007/s12035-023-03636-w |
 2025, Vol. 54
2025, Vol. 54