文章信息
- 杨超, 苏涛, 贾迪, 林岩, 程昊, 张奇, 梁晶, 张春晶
- YANG Chao, SU Tao, JIA Di, LIN Yan, CHENG Hao, ZHANG Qi, LIANG Jing, ZHANG Chunjing
- lncRNA NRON通过调节TGF-β/Smad信号通路诱导心肌梗死小鼠心肌纤维化
- lncRNA NRON induces myocardial fibrosis in mice with myocardial infarction by regulating the TGF-β/Smad signaling pathway
- 中国医科大学学报, 2025, 54(10): 926-930
- Journal of China Medical University, 2025, 54(10): 926-930
-
文章历史
- 收稿日期:2024-10-12
- 网络出版时间:2025-10-15 13:45:12
2. 齐齐哈尔医药科学研究所博士后科研工作站,黑龙江 齐齐哈尔 161006;
3. 齐齐哈尔医学院基础医学院病理生理学教研室,黑龙江 齐齐哈尔 161006;
4. 齐齐哈尔医学院医院管理处卫生所,黑龙江 齐齐哈尔 161006;
5. 齐齐哈尔医学院药学院临床药理学教研室,黑龙江 齐齐哈尔 161006;
6. 哈尔滨医科大学附属第四医院临床药学科,哈尔滨 150001
2. Postdoctoral Research Station, Qiqihar Institute of Medical and Pharmaceutical Sciences, Qiqihar 161006, China;
3. Department of Pathophysiology, School of Basic Medicine, Qiqihar Medical University, Qiqihar 161006, China;
4. Department of Clinics, Qiqihar Medical University, Qiqihar 161006, China;
5. Department of Clinical Pharmacology, School of Pharmacy, Qiqihar Medical University, Qiqihar 161006, China;
6. Department of Pharmacy, The Fourth Affiliated Hospital of Harbin Medical University, Harbin 150001, China
心肌梗死(myocardial infarction,MI)是心肌组织严重持续缺血引起的,其发病率与死亡率均较高[1-2]。心肌纤维化(myocardial fibrosis,MF)是MI后的主要病理改变,也是引起心室重塑进而诱发心力衰竭、心律失常甚至猝死的关键原因。因此,抑制MF是改善MI患者预后、治疗MI的重要手段之一[3]。研究[4]表明,多种信号通路参与MF的发生发展,其中,转化生长因子β(transforming growth factor-β,TGF-β)/Smad信号通路被认为是MF发生的关键通路。
长链非编码RNA(long non-coding RNA,lncRNA)是一类转录本长度超过200 nt的功能性RNA分子,在MI、MF等多种心血管疾病中发挥重要调控作用[5]。LUO等[6]研究发现,lncRNA SAIL在MF中表达显著降低,过表达SAIL可减少心肌胶原沉积,减少纤维化相关基因的转录,抑制MF进程。ZHANG等[7]研究发现,lncRNA CFAR作为一种新的促纤维化因子,在心脏中通过调控miR-449a-5p/LOXL3/mTOR通路发挥促纤维化作用。研究[8]发现lncRNA NRON可结合抑制活化T细胞核因子NFAT进而抑制T细胞激活。本课题组前期研究[9]证实,NRON可通过与电压依赖性阴离子通道蛋白VDAC结合并抑制其表达,影响MI后细胞凋亡的发生,但NRON在MF中的作用尚不清楚。本研究拟探讨NRON对MI诱导MF的影响及可能的作用机制,以期为临床提供参考依据。
1 材料与方法 1.1 实验动物C57BL/6J品系成年雄性小鼠32只,体重22~25 g,购自辽宁长生生物技术股份有限公司。小鼠在标准条件下饲养:室温20~25 ℃、湿度50%~60%、正常饮水饮食。本研究获得齐齐哈尔医学院实验动物伦理委员会批准。
1.2 动物分组及建模将32只小鼠随机分成假手术(Sham)组、MI组、MI+敲减NRON(MI+shNRON)组和MI+阴性对照(MI+NC)组,每组8只。Sham组仅开胸不结扎,MI组制备MI模型,MI+shNRON组先向小鼠左心室内注射100 μL敲减NRON慢病毒[1×108 TU/mL,汉恒生物科技(上海)有限公司],再进行MI造模。MI+NC组先向小鼠左心室内注射阴性对照慢病毒,再进行MI造模。所有小鼠标准饲养28 d后处死,取出心脏组织用于后续实验。小鼠MI模型制备具体方法:将小鼠麻醉后固定,剃除小鼠胸部及腋下毛发,气管插管,连入呼吸机,于第3、4肋间打开胸腔充分暴露心脏,持针器持取7-0结扎线结扎冠状动脉左前降支,阻断血流。观察心电图出现ST段抬高,则表明结扎位置正确,MI模型建立成功。完成后关闭胸腔,逐层缝合肌肉及皮肤。
1.3 HE染色检测心肌组织病理损伤小鼠心脏组织用生理盐水清洗,经4%多聚甲醛固定,石蜡包埋后,切成厚度为5 μm的切片,用HE染色试剂盒(北京索莱宝科技有限公司)进行染色。在显微镜下观察心肌细胞结构及心肌组织病理损伤变化。
1.4 Masson染色检测心肌组织纤维化程度小鼠心脏组织清洗后,浸泡在4%多聚甲醛中固定,然后经石蜡包埋,切片,脱蜡,Masson染色试剂盒(北京索莱宝科技有限公司)染色后封片,在光学显微镜下观察蓝染心肌胶原纤维的分布及数量。
1.5 免疫组织化学染色检测心肌组织Ⅰ型胶原蛋白(collagenⅠ,colⅠ)的表达小鼠心脏组织经清洗、固定、石蜡包埋、切片后,进行脱蜡水化,微波加热法进行抗原修复,山羊血清封闭后加入一抗colⅠ抗体(1∶500稀释,苏州博奥龙科技有限公司),4 ℃孵育过夜。次日加入生物素标记的二抗,37 ℃孵育20 min。滴加适量辣根酶标记链霉卵白素工作液,37 ℃孵育20 min。二氨基联苯胺显色5 min,苏木素复染3 min后,脱水,封片,置于显微镜下观察切片。
1.6 实时定量PCR检测NRON的表达水平取出小鼠心肌组织,用TRIzol法提取总RNA,用反转录试剂盒(日本TOYOBO公司)将总RNA逆转录成cDNA,并以cDNA为模板采用SYBR Green染料(瑞士Roche公司)法检测NRON的表达水平。反应条件为95 ℃ 3 min,95 ℃ 20 s,60 ℃ 30 s,72 ℃ 45 s,45个循环。引物序列:NRON,正向,5’-CAAATCCAGTTGCAAGGACC-3’,反向,5’-AGCTCAGTCCTAGGGTAGG-3’;β-actin,正向,5’-CCACTGCCGCATCCTCTT-3’,反向,5’-GGTCTTTACGGATGTCAACG-3’;以β-actin为内参,采用2-ΔΔCt法计算相对表达量。
1.7 Western blotting取小鼠心肌组织,加入RIPA裂解液(南京碧云天生物技术有限公司)后离心,取上清,用BCA试剂盒(南京碧云天生物技术有限公司)测定蛋白浓度。制备SDS-PAGE凝胶,取等质量蛋白上样,电泳、转膜,用5%脱脂奶粉室温封闭2 h,分别加入一抗TGF-β1、p-Smad2、p-Smad3(1∶1 000稀释,成都正能生物技术有限责任公司),4 ℃过夜,用PBST漂洗3次,加入二抗(1∶1 000稀释,成都正能生物技术有限责任公司),室温孵育1 h,ECL发光剂(北京索莱宝科技有限公司)显影,采用ImageJ软件分析蛋白灰度值。
1.8 统计学分析应用GraphPad Prism7.0软件对数据进行分析,计量资料以x ± s表示,2组间比较采用t检验,多组间比较采用单因素方差分析。P < 0.05为差异有统计学意义。
2 结果 2.1 各组NRON的表达水平比较实时定量PCR结果显示,与Sham组(1.00±0.38)相比,MI组NRON表达(2.16±0.46)升高,与MI组相比,MI+shNRON组NRON表达(1.38±0.33)下降,差异有统计学意义(均P < 0.05)。MI+NC组(2.08±0.32)与MI组相比,NRON表达无统计学差异(P > 0.05)。
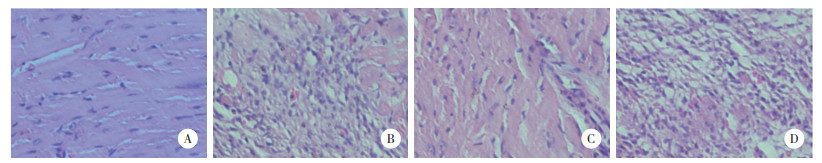
2.2 各组心肌组织病理学改变比较HE染色结果显示,Sham组心肌组织排列整齐,未见炎症浸润现象;MI组心肌细胞排列紊乱,间质增多,炎症细胞浸润明显;MI+shNRON组心肌组织有显著恢复现象,少见炎症细胞浸润;MI+NC组与MI组相比并无改善,见图 1。
|
| A, Sham group; B, MI group; C, MI+shNRON group; D, MI+NC group. 图 1 各组心肌组织病理变化 ×200 Fig.1 Pathological changes of myocardial tissue in each group ×200 |
2.3 各组心肌组织纤维化程度比较
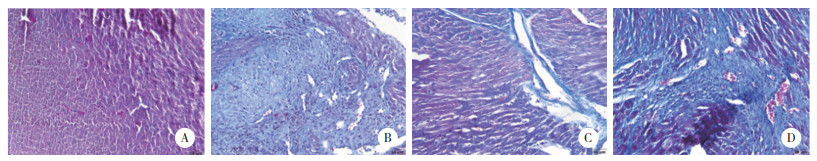
Masson染色结果显示,Sham组心肌组织几乎无纤维化现象;MI组胶原沉积明显,可见大量蓝染纤维,纤维化程度严重;MI+shNRON组纤维化程度减轻,只有少量胶原沉积现象;MI+NC组仍有严重纤维化现象,见图 2。
|
| A, Sham group; B, MI group; C, MI+shNRON group; D, MI+NC group. 图 2 各组心肌组织纤维化程度 ×200 Fig.2 The degree of myocardial fibrosis in each group ×200 |
2.4 各组心肌组织colⅠ的表达水平比较
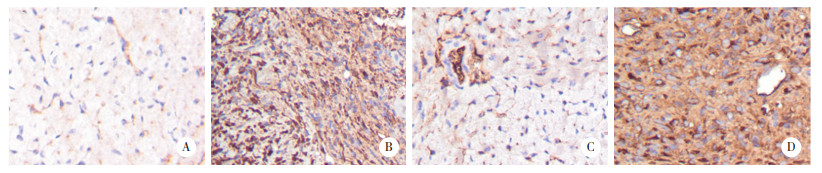
免疫组织化学检测结果显示,Sham组心肌组织colⅠ的表达极少;MI组可见大量棕黄色colⅠ的阳性染色,colⅠ表达显著升高;MI+shNRON组仅有少量colⅠ阳性染色,colⅠ表达下降;MI+NC组colⅠ表达仍较高,见图 3。
|
| A, Sham group; B, MI group; C, MI+shNRON group; D, MI+NC group. 图 3 各组心肌组织colⅠ的表达水平 ×200 Fig.3 The expression level of collagen TypeⅠ in myocardial tissue of each group ×200 |
2.5 各组心肌组织TGF-β1、p-Smad2、p-Smad3蛋白表达水平比较
Western blotting结果显示,与Sham组(1.00±0.00)相比,MI组TGF-β1(1.76±0.17)、p-Smad2(1.91±0.17)、p-Smad3(1.89±0.05)蛋白的表达显著升高(P < 0.05)。与MI组相比,MI+shNRON组TGF-β1(1.24±0.13)、p-Smad2(1.39±0.09)、p-Smad3(1.54±0.05)蛋白的表达显著下降(P < 0.05)。与MI组相比,MI+NC组TGF-β1(1.81±0.40)、p-Smad2(1.98±0.11)、p-Smad3(1.90±0.09)蛋白的表达无统计学差异(P > 0.05),见图 4。

|
| 1, Sham group; 2, MI group; 3, MI+shNRON group; 4, MI+NC group. 图 4 各组心肌组织TGF-β1、p-Smad2、p-Smad3蛋白表达水平 Fig.4 The protein expression levels of TGF-β1, p-Smad2, and p-Smad3 in myocardial tissue of each group |
3 讨论
MI具有高致死率且发病迅速,可诱发心力衰竭甚至猝死。MF是MI后胶原过度沉积的结果,MI早期胶原的沉积可形成瘢痕组织从而防止心脏破裂,但过度沉积使心肌大范围纤维化,可引起心肌僵硬度增加,心肌收缩和舒张功能障碍,最终导致心力衰竭。抑制MF并减缓心室重构是治疗MI的重要策略。
lncRNA功能失调可导致癌症、心血管等多种疾病的发生。NRON被认为是NFAT的抑制因子,可以调控NFAT的去磷酸化和核转运进程 [10]。研究[11-12]发现,NRON在多种组织和细胞中表达,包括骨骼组织、血管平滑肌细胞等,通过与不同的靶点结合发挥多种功能。本课题组前期研究[9]发现敲减NRON可显著抑制MI后细胞凋亡的发生,本研究进一步探讨了NRON对MI诱导的MF的影响,与之前的MI造模时间不同,本研究选取MI后28 d检测小鼠心肌组织中NRON的表达变化,前期研究[9]已证实NRON在MI后7 d表达上调,本研究进一步证实NRON在MI后28 d表达仍显著上调,再次提示NRON可能对MI具有重要调控作用。HE染色、Masson染色、免疫组织化学检测结果显示,敲减NRON可明显缓解由MI导致的心肌排列紊乱和炎症细胞浸润现象,减轻纤维化程度并抑制colⅠ的表达。这表明NRON可有效改善心肌损伤,抑制MF的发生,提示NRON可能是治疗MF的重要靶点。
MF的发病机制尚未完全明确,研究[13]发现TGF-β是介导纤维化发生发展的关键因子。TGF-β在体内有多种亚型,其中TGF-β1是最强有力的促纤维化因子,也是心脏中主要存在的亚型。TGF-β1下游信号通路中最为经典的是Smad依赖性TGF-β1信号传导通路,在正常情况下,TGF-β1以无活性的前体形式存在,当心肌缺血缺氧时,TGF-β1迅速活化并与受体结合,促进Smad2/3蛋白磷酸化,磷酸化的Smad2/3与Smad4蛋白结合形成Smad复合物,并转移至细胞核,诱导纤维化相关基因的表达,促进胶原蛋白沉积,发挥促纤维化的作用[14]。已有研究[15]报道,lncRNA是影响TGF-β/Smad信号转导的重要调节因子,TANG等[16]鉴定出lncRNA GAS5是一种由TGF-β诱导的成纤维细胞活化的调节因子。GAS5直接结合Smad3,并加速Smad3的去磷酸化,抑制TGF-β/Smad信号通路。本研究结果显示,特异性敲减NRON可显著逆转由MI导致的TGF-β1、p-Smad2、p-Smad3蛋白的病理性增高,提示敲减NRON可能通过影响TGF-β/Smad信号通路,发挥抑制MF的作用。
综上所述,NRON参与MI后MF的发生发展,敲低NRON可显著缓解心肌组织病理损伤,减轻纤维化程度并延缓心室重构,具体机制可能与抑制TGF-β/Smad信号通路相关。本研究为lncRNA在MF中的作用提供了新的证据。
| [1] |
SAITO Y, OYAMA K, TSUJITA K, et al. Treatment strategies of acute myocardial infarction: updates on revascularization, pharmacological therapy, and beyond[J]. J Cardiol, 2023, 81(2): 168-178. DOI:10.1016/j.jjcc.2022.07.003 |
| [2] |
DAMLUJI AA, VAN DIEPEN S, KATZ JN, et al. Mechanical complications of acute myocardial infarction: a scientific statement from the American heart association[J]. Circulation, 2021, 144(2): e16-e35. DOI:10.1161/cir.0000000000000985 |
| [3] |
TALMAN V, RUSKOAHO H. Cardiac fibrosis in myocardial infarction-from repair and remodeling to regeneration[J]. Cell Tissue Res, 2016, 365(3): 563-581. DOI:10.1007/s00441-016-2431-9 |
| [4] |
FRANGOGIANNIS NG. Cardiac fibrosis[J]. Cardiovasc Res, 2021, 117(6): 1450-1488. DOI:10.1093/cvr/cvaa324 |
| [5] |
谭冰, 方凌燕, 陈明华, 等. 长链非编码RNA FGD5-AS1调节miR-195-5p/PIM1轴对高糖诱导的心肌细胞损伤的影响[J]. 中国医科大学学报, 2024, 53(6): 487-494. DOI:10.12007/j.issn.0258-4646.2024.06.002 |
| [6] |
LUO SJ, ZHANG MY, WU H, et al. SAIL: a new conserved anti-fibrotic lncRNA in the heart[J]. Basic Res Cardiol, 2021, 116(1): 15. DOI:10.1007/s00395-021-00854-y |
| [7] |
ZHANG MY, ZHANG BW, WANG XH, et al. LncRNA CFAR promotes cardiac fibrosis via the miR-449a-5p/LOXL3/mTOR axis[J]. Sci China Life Sci, 2023, 66(4): 783-799. DOI:10.1007/s11427-021-2132-9 |
| [8] |
SHARMA S, FINDLAY GM, BANDUKWALA HS, et al. Dephosphorylation of the nuclear factor of activated T cells (NFAT) transcription factor is regulated by an RNA-protein scaffold complex[J]. Proc Natl Acad Sci USA, 2011, 108(28): 11381-11386. DOI:10.1073/pnas.1019711108 |
| [9] |
高涵, 张春晶, 李淑艳, 等. 长链非编码RNA-NRON对小鼠心肌梗死后细胞凋亡的作用机制研究[J]. 中国医科大学学报, 2024, 53(3): 218-223. DOI:10.12007/j.issn.0258-4646.2024.03.005 |
| [10] |
HOEPFNER J, LEONARDY J, LU D, et al. The long non-coding RNA NRON promotes the development of cardiac hypertrophy in the murine heart[J]. Mol Ther, 2022, 30(3): 1265-1274. DOI:10.1016/j.ymthe.2021.11.018 |
| [11] |
JIN F, LI J, ZHANG YB, et al. A functional motif of long noncoding RNA Nron against osteoporosis[J]. Nat Commun, 2021, 12(1): 3319. DOI:10.1038/s41467-021-23642-7 |
| [12] |
DU M, WANG C, YANG LY, et al. The role of long noncoding RNA Nron in atherosclerosis development and plaque stability[J]. iS-cience, 2022, 25(3): 103978. DOI:10.1016/j.isci.2022.103978 |
| [13] |
MARTELOSSI CEBINELLI GC, PAIVA TRUGILO K, BADARÓ GARCIA S, et al. TGF-β1 functional polymorphisms: a review[J]. Eur Cytokine Netw, 2016, 27(4): 81-89. DOI:10.1684/ecn.2016.0382 |
| [14] |
HU HH, CHEN DQ, WANG YN, et al. New insights into TGF-β/Smad signaling in tissue fibrosis[J]. Chem Biol Interact, 2018, 292: 76-83. DOI:10.1016/j.cbi.2018.07.008 |
| [15] |
YOUSEFI F, SHABANINEJAD Z, VAKILI S, et al. TGF-β and WNT signaling pathways in cardiac fibrosis: non-coding RNAs come into focus[J]. Cell Commun Signal, 2020, 18(1): 87. DOI:10.1186/s12964-020-00555-4 |
| [16] |
TANG R, WANG YC, MEI XH, et al. LncRNA GAS5 attenuates fibroblast activation through inhibiting Smad3 signaling[J]. Am J Physiol Cell Physiol, 2020, 319(1): C105-C115. DOI:10.1152/ajpcell.00059.2020 |
 2025, Vol. 54
2025, Vol. 54