文章信息
- 李晓明, 吴岳林, 徐振明, 富伟能, 孙媛媛
- LI Xiaoming, WU Yuelin, XU Zhenming, FU Weineng, SUN Yuanyuan
- STAT1通过调控APOL6表达促进喉癌组织中肿瘤相关巨噬细胞脂质沉积
- STAT1 promotes lipid deposition in tumor-associated macrophages in laryngeal cancer tissues by regulating APOL6 expression
- 中国医科大学学报, 2025, 54(10): 919-925
- Journal of China Medical University, 2025, 54(10): 919-925
-
文章历史
- 收稿日期:2025-06-25
- 网络出版时间:2025-10-15 13:48:31
2. 赤峰学院附属医院生殖医学科,内蒙古 赤峰 024000;
3. 沈阳市第四人民医院耳鼻喉科,沈阳 110082
2. Department of Reproductive Medicine, The Affiliated Hospital of Chifeng University, Chifeng 024000, China;
3. Department of Otolaryngology, The Fourth People's Hospital of Shenyang, Shenyang 110082, China
喉癌是常见的头颈部恶性肿瘤。我国北方地区喉癌发病率较高,且男性多发,侵袭和转移是主要致死原因[1-2]。肿瘤微环境(tumor microenvironment,TME)是肿瘤细胞产生和生存的内环境。其中,肿瘤相关巨噬细胞(tumor-associated macrophage,TAM)是TME中数量最多的免疫细胞,在肿瘤发生、侵袭、转移中发挥重要作用[3]。TAM具有极高的异质性和可塑性,在不同的环境条件下可以极化成M1型和M2型[4]。研究[5]表明,脂质沉积可调节TAM极化,进而影响肿瘤的发生发展。然而,喉癌细胞重塑TME,进而影响TAM脂质重编程相关研究鲜有报道。
本课题组前期研究[6]对喉癌组织进行了单细胞测序,并对测序结果进行了分析,结果发现,信号转导及转录激活因子1(signal transducer and activator of transcription 1,STAT1)处于基因表达调控的核心。研究[7-8]表明,STAT1具有多种生物学功能,在TAM的M2型极化和脂质代谢调节方面发挥重要作用。本研究预测分析发现,APOL6是STAT1的潜在直接下游靶基因。APOL6是载脂蛋白家族成员,能够通过与Plin1直接相互作用抑制脂肪分解,促进细胞内脂滴体积增大[9]。提示STAT1可能通过APOL6参与TAM的脂质沉积。本研究通过检测STAT1和APOL6在喉癌组织中的表达水平及对TAM脂质沉积的影响,探讨STAT1对APOL6的转录调控机制;同时探讨STAT1通过调控APOL6表达及分泌对喉癌组织中TAM脂质沉积的影响,旨在为喉癌诊治靶点的进一步研究提供线索。
1 材料与方法 1.1 细胞与试剂人喉癌细胞系TU212购自武汉尚恩生物技术有限公司,人单核细胞白血病细胞系THP-1和人正常支气管上皮细胞系BEAS-2B购自武汉普诺赛生命科技有限公司。10例喉癌患者癌组织及癌旁组织配对标本取自沈阳市第四人民医院耳鼻喉科,所有患者组织标本经病理学确诊。本研究获得中国医科大学医学伦理委员会批准,患者均知情同意并签署知情同意书。
胎牛血清购自苏州海星生物科技有限公司,RPMI 1640培养基购自武汉赛维尔科技有限公司,胰蛋白酶购自北京兰杰柯科技有限公司,jetPRIME转染试剂购自法国Polyplus公司,反转录试剂盒、PCR相关试剂购自南京诺唯赞生物科技股份有限公司,TRIzol核酸提取试剂购自日本TaKaRa公司,STAT1和β-actin抗体、山羊抗兔二抗和山羊抗鼠二抗购自美国Proteintech公司,APOL6抗体购自美国Immnuoway公司,ECL发光试剂盒购自上海天能生物技术公司,SDS-PAGE凝胶配制试剂盒购自上海碧云天生物技术公司,BCA蛋白浓度检测试剂盒、预染彩色蛋白分子量Marker购自上海铂莱生物技术公司,免疫组织化学试剂盒购自北京中杉金桥生物技术有限公司,ChIP试剂盒购自上海爱必信生物技术公司,ELISA试剂盒购自上海酶联生物技术公司,油红O试剂盒购自江苏凯基生物技术公司,PMA购自北京索莱宝科技有限公司。
1.2 实验方法 1.2.1 细胞培养使用含10%胎牛血清、1%青霉素和链霉素的RPMI 1640培养基常规培养TU212细胞、THP-1细胞和BEAS-2B细胞。
1.2.2 细胞转染按照jetPRIME转染试剂说明书步骤将STAT1过表达质粒(上海吉凯生物技术公司),siAPOL6、STAT1过表达质粒+siAPOL6和相应对照质粒或siRNA(上海生工生物工程股份有限公司)转染至喉癌细胞中,48 h后收集细胞进行后续分析。
1.2.3 条件培养收集1.2.2各转染组培养基,与正常培养基按1∶1混合,制成条件培养基,条件培养THP-1细胞24~48 h,收集细胞用于后续实验。
1.2.4 实时PCR检测收集各组细胞,应用TRIzol法提取总RNA,按照HiScript Ⅱ Q RT SuperMix for qPCR和SupRealQ Ultra Hunter SYBR qPCR Master Mix(U+)试剂盒说明书分别进行反转录和实时PCR,引物序列如下:STAT1,正向5’-GCCAGAAAACTTTTGGGAGGA-3’,反向5’-ATCCAGTTCTGTTGAGGCCG-3’;APOL6,正向5’-CCATCTACAACATCGACACCAG-3’,反向5’-CTTCCACACTATGCTCAGGTAG-3’;CD68,正向5’-GTCCACCTCGACCTGCTCT-3’,反向5’-CACTCGGGCAGGAGAAACT-3’;β-actin,正向5’-TGAGACCTTCAACACCCCAGCCATG-3’,反向5’-CGTAGATGGGCACAGTGTGGGTG-3’。以2-ΔΔCt计算目的基因相对表达量。
1.2.5 Western blotting检测:收集各组细胞,提取总蛋白,通过BCA试剂盒对蛋白浓度进行定量。加入蛋白上样缓冲液后,煮沸使蛋白变性。按照试剂盒说明书配制凝胶,每个加样孔加入30 µg蛋白进行电泳、转膜。5%脱脂牛奶室温封闭后,分别加入稀释好的抗体STAT1(1∶2 000稀释)、APOL6(1∶2 000稀释)、β-actin(1∶10 000稀释),4 ℃条件下杂交过夜。次日洗涤后,按照1∶4 000稀释相应种属二抗,室温孵育1 h,漂洗后加入ECL发光液,用化学发光成像系统进行曝光及拍照,应用ImageJ软件进行光密度分析。
1.2.6 染色质免疫共沉淀(chromatin immunoprecipitation,ChIP):收集喉癌细胞,按照试剂盒说明书进行ChIP实验。分离、纯化抗STAT1抗体沉淀的DNA,应用APOL6启动子区引物进行PCR扩增并进行检测,引物序列:正向5’-CTGCTCTTTCACCTCCTTGTT-3’;反向5’-GAGTAGGGTGGCCTTTGAAC-3’。
1.2.7 酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)收集各组细胞培养上清,按照试剂盒说明书进行APOL6水平检测。
1.2.8 油红O染色将佛波酯(phorbol 12-myristate 13-acetate,PMA)诱导后的THP-1细胞进行细胞爬片,根据试剂盒说明书进行油红O染色。
1.2.9 免疫组织化学(immunohistochemistry,IHC)检测应用4%多聚甲醛固定新鲜的喉癌组织,经石蜡包埋后切片(4 μm)。按照试剂盒说明书进行操作,分别使用抗STAT1(稀释比例1∶100)和抗APOL6(稀释比例1∶100)抗体与切片进行杂交,洗片后显微镜下观察并拍照。
1.3 统计学分析使用SPSS 26.0软件进行统计分析,计量资料以x ± s表示。2组间比较采用配对样本t检验、独立样本t检验,多间组比较采用单因素方差分析。P < 0.05为差异有统计学意义。
2 结果 2.1 喉癌组织中STAT1和APOL6的表达水平(图 1)
|
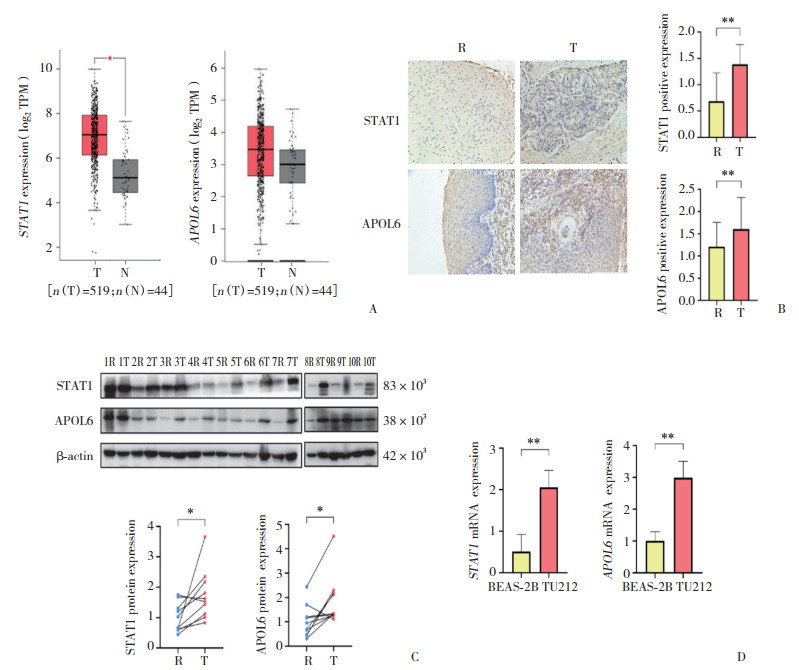
| A, expression of STAT1 and APOL6 mRNA in HNSCC from the TCGA database; B, expression of STAT1 and APOL6 proteins in laryngeal cancer tissues by immunohistochemistry (×200);C. expression of STAT1 and APOL6 proteins in laryngeal cancer tissues by Western blotting; D. expression of STAT1 and APOL6 mRNA in laryngeal cancer cells and normal respiratory epithelial cells by real-time PCR. R, paracancerous tissue; T, tumor tissue; N, normal tussue. * P < 0.05, ** P < 0.01. HNSCC, head and neck squamous cell carcinoma. 图 1 喉癌组织中STAT1和APOL6的表达 Fig.1 STAT1 and APOL6 expression in laryngeal cancer tissue |
利用癌症基因组图谱(The Cancer Genome Atlas,TCGA)数据库(https://www.cancer.gov/ccg/research/genome-sequencing/tcga)对STAT1和APOL6在头颈部鳞状细胞癌(head and neck squamous cell carcinoma,HNSCC)中mRNA表达水平进行分析,结果显示,STAT1、APOL6 mRNA在HNSCC中表达水平较对照组显著升高(P < 0.05,图 1A)。IHC检测结果显示,人喉癌组织中STAT1和APOL6蛋白表达较癌旁组织均显著升高(P < 0.01,图 1B)。Western bloting检测结果表明,喉癌组织中STAT1和APOL6蛋白表达较对照组均显著升高(P < 0.05,图 1C)。实时PCR检测结果显示,与BEAS-2B细胞相比,TU212细胞中STAT1和APOL6 mRNA表达水平均显著升高(P < 0.05,图 1D)。
2.2 喉癌细胞中STAT1对APOL6的转录调控机制(图 2)
|
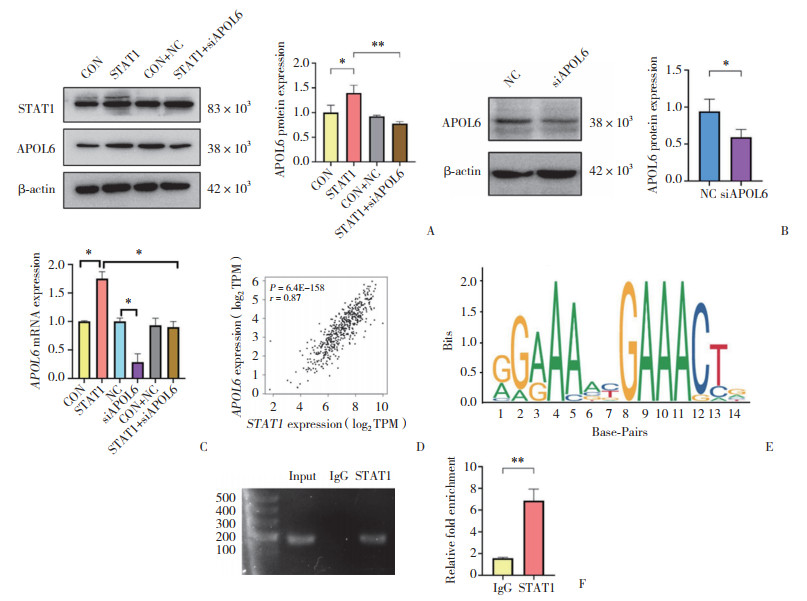
| A, STAT1 and APOL6 protein expression in TU212 cells; B, APOL6 protein expression in TU212 cells with APOL6 knockdown; C, the effect of STAT1 on APOL6 mRNA expression in TU212 cells; D, the correlation between STAT1 and APOL6 expression in HNSCC tissues from GEPIA database; E, prediction results of STAT1 binding sites in the promoter region of APOL6; F, the binding ability in vivo between STAT1 and the APOL6 promoter region in TU212 cells. *P < 0.05, ** P < 0.01. 图 2 喉癌细胞中STAT1对APOL6转录调控作用 Fig.2 The transcriptional regulatory effect of STAT1 on APOL6 in laryngeal cancer cells |
为了探讨STAT1对APOL6的调控作用,在TU212细胞中分别转染了STAT1过表达载体(STAT1组)、siAPOL6(siAPOL6组)和STAT1过表达载体+siAPOL6(STAT1+siAPLO6组)和其相应对照(CON组、NC组和CON+NC组)。Western blotting检测结果显示,转染STAT1过表达载体后APOL6蛋白表达水平较对照组显著升高(P < 0.05,图 2A);敲减APOL6后APOL6蛋白表达水平较对照组显著降低(P < 0.05,图 2B)。实时PCR检测结果显示,转染STAT1过表达载体后APOL6 mRNA表达水平较对照组也显著升高(P < 0.05,图 2C)。转染STAT1过表达载体后敲减APOL6能够显著逆转STAT1过表达对APOL6蛋白和mRNA表达的促进作用(P < 0.01,图 2A、2C)。基因表达谱交互式分析(Gene Expression Profiling Interactive Analysis,GEPIA)数据库(http://gepia.cancer-pku.cn/)结果显示,STAT1与APOL6表达呈正相关(R = 0.87,P < 0.05,图 2D)。Jaspar软件(https://jaspar.elixir.no/)预测结果显示,APOL6启动子区存在STAT1潜在的结合位点(图 2E)。ChIP实验结果显示,在体内STAT1能够与APOL6启动子区直接结合(图 2F)。
以上研究结果说明在喉癌细胞中STAT1通过与APOL6启动子区结合促进其转录,提示APOL6可能是STAT1下游新的靶基因。
2.3 喉癌细胞中STAT1通过APOL6对TAM脂质沉积的影响(图 3)
|
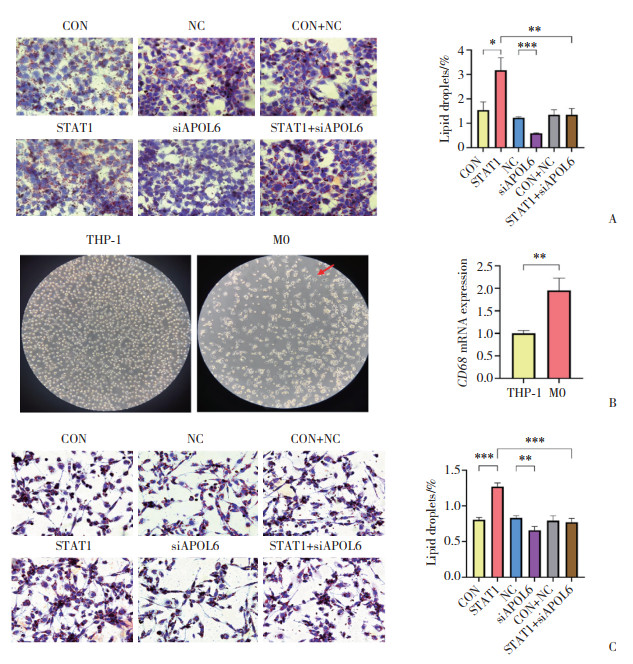
| A, lipid droplet contents in TU212 cells transfected with STAT1, siAPOL6, and STAT1+siAPOL6 (×200);B, macrophage morphology (×100, red arrows indicate pseudopodia) and CD68 mRNA expression; C, lipid droplet contents in TAM transfected with STAT1, siAPOL6, and STAT1+siAPOL6 (×200). *P < 0.05, ** P < 0.01, *** P < 0.001. 图 3 STAT1对喉癌细胞和TAM脂质沉积的影响 Fig.3 The Effect of STAT1 on lipid deposition in laryngeal cancer cells and TAM |
收集转染STAT1过表达载体和空载体的TU212细胞的上清液,并对细胞分泌APOL6的水平进行检测。ELISA结果显示,对照组、STAT1组上清液中APOL6水平分别为(70.95±1.02)、(93.77±1.34)ng/mL,STAT1组较对照组APOL6水平显著升高(P < 0.05),提示STAT1可以促进喉癌细胞分泌APOL6。油红O染色结果显示,过表达STAT1后TU212细胞中脂滴含量较对照组显著升高(P < 0.05),敲减APOL6的TU212细胞中脂滴含量较对照组显著下降(P < 0.05),siAPOL6可以显著逆转STAT1对喉癌细胞脂质沉积的影响(P < 0.05,图 3A)。显微镜下观察结果显示,PMA诱导剂诱导后的THP-1细胞出现贴壁现象并伸出伪足;同时,实时PCR结果显示,M0巨噬细胞中巨噬细胞标记基因CD68 mRNA表达水平较THP-1细胞显著升高,提示巨噬细胞诱导成功(图 3B)。收集了转染STAT1、siAPOL6、STAT1+siAPOL6和相应对照组的条件培养基培养24 h后M0巨噬细胞。油红O染色结果显示,过表达STAT1条件培养基处理的巨噬细胞中脂滴含量较对照组显著升高(P < 0.05),而敲减APOL6条件培养基处理的巨噬细胞中脂滴含量较对照组显著下降(P < 0.05),siAPOL6可以显著逆转STAT1对TAM脂质沉积的促进作用(P < 0.05,图 3C)。提示在喉癌细胞中STAT1可直接转录激活APOL6的表达和分泌,促进TAM的脂质沉积。
3 讨论肿瘤的发生发展与TME的改变密切相关。近年来,TME已成为研究肿瘤分子机制的切入点和新靶点。肿瘤细胞与免疫细胞、肿瘤相关成纤维细胞、血液、淋巴管以及细胞外基质和信号分子一起构成了TME[10]。TME对包括喉癌在内的头颈部鳞癌的发生发展和临床复发耐药起着重要作用[11]。研究[12]表明,肿瘤细胞与周围微环境细胞之间通过交流对话相互促进,进而不断影响肿瘤细胞的增殖和转移。因此,针对TME寻找肿瘤诊治分子靶标是一种有效途径。
STAT1具有多种生物学功能,在不同肿瘤中发挥不同的作用。有研究[13]报道,过表达STAT1可抑制紫杉醇耐药性卵巢癌细胞的干性,然而,在一些人类肿瘤(如乳腺癌和HNSCC)中,STAT1呈现异常激活状态,且其表达水平与患者预后差有关[14-15]。最近,STAT1引起的肿瘤代谢异常受到越来越多的关注。有学者[16]发现,STAT1直接或间接调节肿瘤细胞中的各种代谢相关过程。本研究结果显示,STAT1促进TU212细胞和TAM中脂质沉积,提示STAT1参与喉癌细胞及TAM的脂质代谢重塑。
APOL6是一种广泛表达的脂质结合蛋白[9],属于载脂蛋白L家族,该家族成员之间具有高度相似性,通常情况下认为它们具有与APOL1相似的功能。有研究[17]表明,APOL1在肝癌细胞中合成及分泌。本研究发现APOL6是STAT1的下游靶基因,二者在HNSCC中均高表达。进一步研究发现,STAT1能够通过与APOL6启动子区直接结合,转录激活APOL6表达和分泌,参与喉癌细胞及TAM的脂质代谢重塑。然而,APOL6分泌方式和跨膜转运机制仍不清楚,有待进一步探讨。此外,细胞微环境中APOL6如何促进TAM脂质摄取和沉积仍不清楚。有学者[13]发现,TAM倾向于通过其表面CD36受体从TME摄取更多的脂质,以维持其肿瘤促进能力。HE等[18]发现,口腔鳞癌中TAM高表达PLIN2促进脂质沉积。WANG等[9]发现,APOL6通过Plin1直接相互作用,抑制脂肪分解作用促进细胞内脂滴体积增大,甘油三酯含量升高。APOL6是否通过与脂类摄取相关分子结合,协调促进TAM脂质摄取和累积有待进一步研究。
综上所述,本研究通过ChIP实验明确了STAT1与APOL6启动子区直接结合;喉癌中STAT1通过转录激活APOL6进而促进喉癌细胞和TAM中脂质沉积。这些发现将为深入了解喉癌发生发展的分子机制,寻找喉癌早期诊治的潜在分子靶标提供新思路。然而,脂质代谢重塑对TAM的影响是复杂多向的,不仅表现在其M1/M2极化状态变化,还会影响其分化产生特异性细胞亚群调控肿瘤免疫,因此需进一步研究论证。
| [1] |
YI XH, CHEN W, LI C, et al. Circular RNA circ_0004507 contributes to laryngeal cancer progression and cisplatin resistance by sponging miR-873 to upregulate multidrug resistance 1 and multidrug resistance protein 1[J]. Head Neck, 2021, 43(3): 928-941. DOI:10.1002/hed.26549 |
| [2] |
孙倩, 刘盛力, 马钰, 等. 长链非编码RNA SLC25A25-AS1对喉癌细胞侵袭和迁移的影响及其机制[J]. 中国医科大学学报, 2022, 51(4): 324-328. DOI:10.12007/j.issn.0258-4646.2022.04.007 |
| [3] |
TIWARI A, TRIVEDI R, LIN SY. Tumor microenvironment: barrier or opportunity towards effective cancer therapy[J]. J Biomed Sci, 2022, 29(1): 83. DOI:10.1186/s12929-022-00866-3 |
| [4] |
QIU X, ZHAO TJ, LUO R, et al. Tumor-associated macrophages: key players in triple-negative breast cancer[J]. Front Oncol, 2022, 12: 772615. DOI:10.3389/fonc.2022.772615 |
| [5] |
SU P, WANG Q, BI EG, et al. Enhanced lipid accumulation and metabolism are required for the differentiation and activation of tumor-associated macrophages[J]. Cancer Res, 2020, 80(7): 1438-1450. DOI:10.1158/0008-5472.CAN-19-2994 |
| [6] |
SUN YY, CHEN S, LU YP, et al. Single-cell transcriptomic analyses of tumor microenvironment and molecular reprograming landscape of metastatic laryngeal squamous cell carcinoma[J]. Commun Biol, 2024, 7(1): 63. DOI:10.1038/s42003-024-05765-x |
| [7] |
HSU CH, PAN YJ, ZHENG YT, et al. Ultrasound reduces inflammation by modulating M1/M2 polarization of microglia through STAT1/STAT6/PPARγ signaling pathways[J]. CNS Neurosci Ther, 2023, 29(12): 4113-4123. DOI:10.1111/cns.14333 |
| [8] |
YOU WJ, LIU SQ, LI J, et al. GADD45A regulates subcutaneous fat deposition and lipid metabolism by interacting with Stat1[J]. BMC Biol, 2023, 21(1): 212. DOI:10.1186/s12915-023-01713-z |
| [9] |
WANG YH, NGUYEN HP, XUE PY, et al. ApoL6 associates with lipid droplets and disrupts Perilipin1-HSL interaction to inhibit lipolysis[J]. Nat Commun, 2024, 15(1): 186. DOI:10.1038/s41467-023-44559-3 |
| [10] |
DE VISSER KE, JOYCE JA. The evolving tumor microenvironment: from cancer initiation to metastatic outgrowth[J]. Cancer Cell, 2023, 41(3): 374-403. DOI:10.1016/j.ccell.2023.02.016 |
| [11] |
VAN DEN BOSSCHE V, ZARYOUH H, VARA-MESSLER M, et al. Microenvironment-driven intratumoral heterogeneity in head and neck cancers: clinical challenges and opportunities for precision medicine[J]. Drug Resist Updat, 2022, 60: 100806. DOI:10.1016/j.drup.2022.100806 |
| [12] |
ELMUSRATI A, WANG J, WANG CY. Tumor microenvironment and immune evasion in head and neck squamous cell carcinoma[J]. Int J Oral Sci, 2021, 13(1): 24. DOI:10.1038/s41368-021-00131-7 |
| [13] |
WANG FC, ZHANG LY, LIU J, et al. Highly expressed STAT1 contributes to the suppression of stemness properties in human paclitaxel-resistant ovarian cancer cells[J]. Aging, 2020, 12(11): 11042-11060. DOI:10.18632/aging.103317 |
| [14] |
HUANG PP, LIAO RC, CHEN XY, et al. Nuclear translocation of PLSCR1 activates STAT1 signaling in basal-like breast cancer[J]. Theranostics, 2020, 10(10): 4644-4658. DOI:10.7150/thno.43150 |
| [15] |
ANDERSON K, RYAN N, NEDUNGADI D, et al. STAT1 is regulated by TRIM24 and promotes immunosuppression in head and neck squamous carcinoma cells, but enhances T cell antitumour immunity in the tumour microenvironment[J]. Br J Cancer, 2022, 127(4): 624-636. DOI:10.1038/s41416-022-01853-z |
| [16] |
WU RY, KONG PF, XIA LP, et al. Regorafenib promotes antitumor immunity via inhibiting PD-L1 and IDO1 expression in melanoma[J]. Clin Cancer Res, 2019, 25(14): 4530-4541. DOI:10.1158/1078-0432.ccr-18-2840 |
| [17] |
CHENG DM, WECKERLE A, YU Y, et al. Biogenesis and cytotoxicity of APOL1 renal risk variant proteins in hepatocytes and hepatoma cells[J]. J Lipid Res, 2015, 56(8): 1583-1593. DOI:10.1194/jlr.M059733 |
| [18] |
HE YJ, DONG YX, ZHANG XW, et al. Lipid droplet-related PLIN2 in CD68+ tumor-associated macrophage of oral squamous cell carcinoma: implications for cancer prognosis and immunotherapy[J]. Front Oncol, 2022, 12: 824235. DOI:10.3389/fonc.2022.824235 |
 2025, Vol. 54
2025, Vol. 54