文章信息
- 于芳婧, 付欣雨, 张斌, 董岩, 李俣君, 崔晓楠
- YU Fangjing, FU Xinyu, ZHANG Bin, DONG Yan, LI Yujun, CUI Xiaonan
- 蟾毒灵对肝细胞癌小鼠肿瘤微环境中乳酸脱氢酶A和调节性T细胞的影响
- Effect of bufalin on lactate dehydrogenase A and regulatory T cells in the tumor microenvironment of hepatocellular carcinoma in mice
- 中国医科大学学报, 2025, 54(10): 876-882
- Journal of China Medical University, 2025, 54(10): 876-882
-
文章历史
- 收稿日期:2024-11-08
- 网络出版时间:2025-10-15 13:44:37
2. 大连医科大学第一临床学院,辽宁 大连 116011;
3. 大连医科大学附属第一医院中西医结合实验室,辽宁 大连 116011
2. The First Clinical College of Dalian Medical University, Dalian 116011, China;
3. Integrated Traditional Chinese and Western Medicine Laboratory, The First Affiliated Hospital of Dalian Medical University, Dalian 116011, China
肝细胞癌(hepatocellular carcinoma,HCC)在全球癌症相关死亡原因中居第3位[1],其发生、发展与肿瘤微环境密不可分[2]。研究[3]显示,HCC肿瘤微环境中存在大量调节性T细胞(regulatory T cell,Treg),FoxP3+ CD4+ Treg细胞是一个功能成熟且独特的CD4+ T细胞亚群,具有很强的免疫抑制功能,能够促进肿瘤细胞免疫逃逸。FoxP3是Treg细胞关键转录因子,对Treg细胞的发育和功能起重要作用。Treg细胞缺失的荷瘤动物可以出现强烈的抗肿瘤免疫反应[4]。研究[5]发现,Treg细胞可以通过摄取乳酸,增强自身功能。肿瘤微环境中的乳酸主要由肿瘤细胞通过有氧糖酵解产生,乳酸脱氢酶A(lactate dehydrogenase A,LDHA)是这一过程的关键酶。因此,靶向调控LDHA的活性和功能,能够调控乳酸代谢途径,改善肿瘤微环境,可以作为一种抑制肿瘤发生和发展的方法。
目前,华蟾素在临床上表现出良好的抗肿瘤效果,蟾毒灵是华蟾素中主要的抗肿瘤活性成分。研究[6-7]发现,蟾毒灵不仅可以抑制肿瘤细胞增殖,还可以改善肿瘤微环境。本研究通过检测LDHA、FoxP3、CD4在HCC中的表达,探讨蟾毒灵对HCC小鼠肿瘤微环境中LDHA和Treg细胞分化及功能的影响,从而为华蟾素的临床应用提供更多的理论依据,为HCC免疫治疗提供新的方向。
1 材料与方法 1.1 材料 1.1.1 细胞株鼠源肝癌细胞系Hep1-6,购自武汉尚恩生物技术有限公司。
1.1.2 主要试剂蟾毒灵,购自美国APExBIO公司。丙酮酸,购自美国Selleck公司。草氨酸盐,购自美国Glpbio公司。CD4山羊抗兔单克隆抗体、CD4山羊抗鼠单克隆抗体、FoxP3山羊抗兔单克隆抗体、FoxP3山羊抗鼠单克隆抗体,购自英国abcam公司。LDHA抗体,购自美国ABclonal公司。胎牛血清,购自澳大利亚AusGeneX公司。DMEM培养基、0.25% EDTA-胰蛋白酶,购自美国Gibco公司。0.9%氯化钠溶液,购自四川科伦药业股份有限公司。转化生长因子β(transforming growth factor β,TGF-β)、白细胞介素-10(interleukin-10,IL-10)酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)试剂盒,购自上海爱萌优宁生物技术有限公司。
1.1.3 临床标本收集2019年1月1日至2020年12月30日间在大连医科大学附属第一医院行肝癌切除术、术后病理诊断为HCC的91例患者的癌组织和癌旁组织样本。
1.1.4 实验动物SPF级C57BL/6小鼠20只,4周龄,体重18~20 g,购自辽宁长生生物技术股份有限公司。
1.2 细胞培养鼠源Hep1-6细胞在37 ℃、5% CO2、饱和湿度条件下,在含10%胎牛血清的DMEM培养基中常规培养。当细胞生长融合度达到90%以上时,用0.25% EDTA-胰蛋白酶消化后传代,取对数生长期的细胞用于后续实验。
1.3 Hep1-6皮下荷瘤小鼠模型的建立和分组收集对数生长期的Hep1-6细胞,制成4×106/mL单细胞悬液。所有小鼠右腋皮下注射100 μL单细胞悬液,建立肝癌模型。计算肿瘤体积,体积(cm3)=长×宽2/2。
将建立的小鼠模型随机分为对照组、蟾毒灵联合丙酮酸组、草氨酸盐组、蟾毒灵组,每组5只。成瘤后第1天,对照组小鼠给予0.9%氯化钠溶液(0.1 mL/20 g);蟾毒灵联合丙酮酸组小鼠给予蟾毒灵(1 mg/kg)+丙酮酸(4 mmol/L);草氨酸盐组小鼠给予草氨酸盐(400 mg/kg);蟾毒灵组小鼠给予蟾毒灵(1 mg/kg)。均腹腔注射给药,1次/d。其中,丙酮酸具有刺激乳酸脱氢酶(lactate dehydrogenase,LDH)表达的作用[8],草氨酸盐具有抑制LDHA表达的作用。研究终点为给药后第15天。本研究经大连医科大学附属第一医院医学伦理委员会审批通过(AEE24007)。
1.4 免疫组织化学染色采用免疫组织化学方法检测HCC患者临床标本和各组小鼠肿瘤中LDHA和Treg细胞特异性分子标识FoxP3、CD4的表达。给药15 d后,眼框后静脉丛采血后,处死小鼠,取瘤。石蜡标本切片、烤片。切片放入二甲苯Ⅰ、Ⅱ、Ⅲ溶液中脱蜡,依次置于不同浓度(100%、85%和75%)乙醇中脱水。切片浸泡于抗原修复液中,微波炉加热后冷却至室温。3%过氧化氢溶液滴于切片上,灭活内源酶活性。切片滴加封闭血清后,依次孵育一抗、二抗溶液。DAB显色为黄色时,终止染色。苏木素复染细胞核。应用75%、85%和100%乙醇使切片脱水,二甲苯Ⅰ、Ⅱ、Ⅲ溶液使切片透明,中性树胶封片,凝固后显微镜下观察和拍照。
1.5 ELISA检测采用ELISA检测各组小鼠血清中IL-10和TGF-β水平,评估Treg细胞的免疫功能。按照ELISA试剂盒说明书进行操作。采用分光光度仪测量450 nm波长下的吸光度。依据标准曲线,计算TGF-β和IL-10浓度。
1.6 统计学分析应用SPSS 27.0软件进行统计分析。计量资料用x±s表示,人肝癌组织和癌旁组织中各指标的比较采用Wilcoxon秩和检验;小鼠实验中组间比较采用Mann-Whitney U检验。采用Spearman秩相关分析人肝癌组织和癌旁组织中LDHA与FoxP3、CD4表达的相关性。P < 0.05为差异有统计学意义。
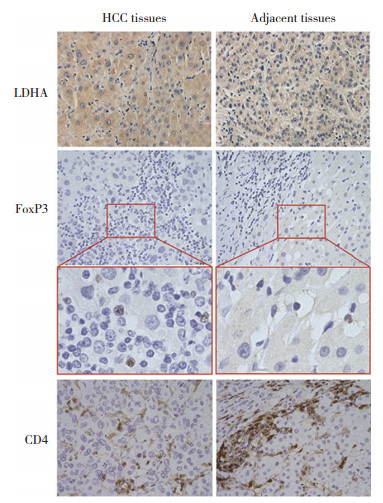
2 结果 2.1 LDHA、FoxP3、CD4在人肝癌组织和癌旁组织中的表达及其相关性CD4分布于Treg细胞的细胞膜表面,阳性细胞呈不规则小灶性分布;FoxP3表达于Treg细胞的细胞核内,阳性细胞呈弥散分布;LDHA表达于所有细胞的细胞质,阳性细胞呈弥散分布。见图 1。
|
| 图 1 人HCC组织免疫组织化学染色×40 Fig.1 Immunohistochemical staining of human HCC tissues ×40 |
免疫组织化学染色结果显示,肝癌组织和癌旁组织中LDHA表达水平分别为0.235±0.056和0.142±0.055,肝癌组织中LDHA呈高表达,LDHA表达水平明显高于癌旁组织(P < 0.001);肝癌组织和癌旁组织中FoxP3+细胞百分比分别为(3.108±2.635)%和(0.825±0.665)%,CD4+细胞百分比分别为(11.800±9.389)%和(18.900±8.962)%,肝癌组织中FoxP3+细胞百分比明显高于癌旁组织(P < 0.001),CD4+细胞百分比明显低于癌旁组织(P < 0.001)。FoxP3+与CD4+细胞百分比反映Treg细胞占CD4+T细胞比值,肝癌组织和癌旁组织分别为(0.330 2±0.244 5)%和(0.050 31±0.043 96)%,提示癌组织中Treg细胞明显多于癌旁组织(P < 0.001)。
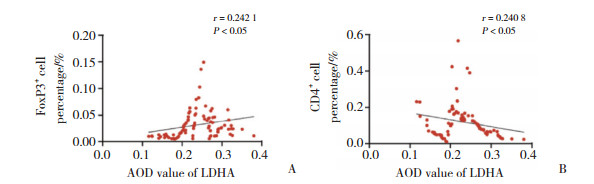
相关性分析结果显示,LDHA与FoxP3表达呈正相关(r = 0.242 1,P < 0.05,图 2A);LDHA与CD4表达呈负相关(r = -0.240 8,P < 0.05,图 2B)。
|
| A, correlation between LDHA and FoxP3 expression; B, correlation between LDHA and CD4 expression. 图 2 人HCC组织中LDHA与FoxP3、LDHA表达的相关性 Fig.2 Correlation of LDHA expression with FoxP3 and LDHA expression in human HCC tissues |
2.2 4组小鼠生长情况以及肿瘤质量和体积的比较
Hep1-6皮下荷瘤小鼠模型和皮下肿瘤见图 3。4组小鼠体重稳定增长,给药第1、9、15天时4组小鼠比较,体重均无统计学差异(P > 0.05),提示药物安全性较好。所有小鼠于给药后第15天处死,测量和比较第15天时的肿瘤质量以及第1、9、15天时的肿瘤体积。结果显示,第15天时,蟾毒灵组和草氨酸盐组小鼠肿瘤质量和体积明显小于蟾毒灵联合丙酮酸组(P < 0.001);蟾毒灵组小鼠肿瘤体积明显小于草氨酸盐组(P < 0.05)。说明草氨酸盐和蟾毒灵均可阻止肿瘤的发生和发展,且蟾毒灵效果更好。见表 1。

|
| A, subcutaneous tumor-bearing mice; B, subcutaneous tumor. 图 3 Hep1-6皮下荷瘤小鼠模型和皮下肿瘤 Fig.3 Hep1-6 subcutaneous tumor-bearing mice model and subcutaneous tumor |
| Group | Body weight(mg) | Tumor mass(g) | Tumor volume(mm3) | ||||
| Day 1 | Day 9 | Day 15 | Day 1 | Day 9 | Day 15 | ||
| Control | 18.31±0.71 | 20.18±0.80 | 21.20±0.52 | 0.60±0.05 | 109.62±9.82 | 323.44±11.95 | 589.91±36.41 |
| Bufalin+pyruvic acid | 18.27±0.65 | 20.06±0.89 | 21.15±0.74 | 0.43±0.051) | 100.56±7.17 | 224.32±19.541) | 398.73±23.441) |
| Oxalate | 17.73±0.46 | 19.54±0.51 | 20.59±0.55 | 0.24±0.021),2) | 105.64±8.33 | 174.67±7.631),2) | 221.16±14.491),2) |
| Bufalin | 18.49±0.90 | 20.30±0.77 | 21.37±0.79 | 0.17±0.011),2) | 101.30±3.85 | 127.58±7.131),2),3) | 176.41±9.901),2),3) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. bufalin+pyruvic acid group;3)P < 0.05 vs. oxalate group. | |||||||
2.3 4组小鼠血清TGF-β和IL-10水平的比较
ELISA结果显示,草氨酸盐组和蟾毒灵组TGF-β和IL-10水平明显低于蟾毒灵联合丙酮酸组(P < 0.05);蟾毒灵组TGF-β和IL-10水平明显低于草氨酸盐组(P < 0.01)。结果提示,蟾毒灵能抑制Treg细胞分泌TGF-β和IL-10。见表 2。
| Group | TGF-β | IL-10 |
| Control | 36 975.87±108.67 | 88.53±1.73 |
| Bufalin+pyruvic acid | 36 331.89±114.441) | 85.19±2.681) |
| Oxalate | 34 600.96±76.991),2) | 80.01±1.531),2) |
| Bufalin | 33 048.56±78.551),2),3) | 77.26±2.271),2),3) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. bufalin+pyruvic acid group;3)P < 0.05 vs. oxalate group. | ||
2.4 4组小鼠LDHA、FoxP3、CD4表达水平的比较及其相关性
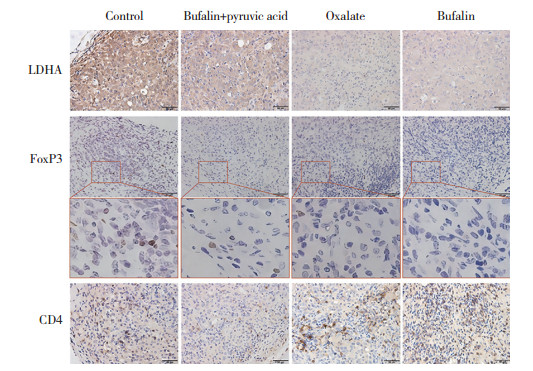
免疫组织化学染色结果(表 3、图 4)显示,蟾毒灵组和草氨酸盐组LDHA表达水平、FoxP3+细胞百分比均明显低于对照组(P < 0.001)、蟾毒灵联合丙酮酸组(P < 0.01);蟾毒灵组与草氨酸盐组比较,LDHA表达水平、FoxP3+细胞百分比的差异均无统计学意义(P > 0.05)。结果提示,蟾毒灵能够抑制肿瘤组织LDHA表达,其效果与草氨酸盐相似,且蟾毒灵或草氨酸盐均可有效减少肿瘤组织中Treg细胞数量。蟾毒灵组CD4+细胞百分比明显高于对照组、蟾毒灵联合丙酮酸组(P < 0.05);草氨酸盐组CD4+细胞百分比略高于对照组,但差异无统计学意义(P > 0.05)。FoxP3+细胞占CD4+细胞百分比反映Treg细胞占CD4+ T细胞的比值。蟾毒灵组FoxP3+细胞占CD4+细胞百分比明显低于对照组、蟾毒灵联合丙酮酸组(P < 0.001)。结果提示,蟾毒灵不仅可以减少肿瘤组织中Treg细胞数量,还可以增加CD4+ T细胞数量,从而使Treg细胞占CD4+T细胞比值降低。
| Group | Average optical density value of LDHA | FoxP3+ cell percentage(%) | CD4+ cell percentage(%) | Ratio of FoxP3+ cells to CD4+ cells |
| Control | 0.301±0.058 | 6.483±1.209 | 15.860±9.439 | 50.24±19.86 |
| Bufalin+pyruvic acid | 0.222±0.030 | 4.700±0.101 | 18.030±5.530 | 28.39±10.01 |
| Oxalate | 0.138±0.0121),2) | 2.090±0.3051),2) | 21.040±4.796 | 10.42±2.811),2) |
| Bufalin | 0.148±0.0101),2) | 0.705±0.3241),2) | 32.680±10.8601),2) | 2.37±1.591),2) |
| 1)P < 0.05 vs. control group;2)P < 0.05 vs. bufalin+pyruvic acid group. | ||||
|
| 图 4 小鼠肿瘤组织免疫组织化学染色结果×40 Fig.4 Immunohistochemical staining of the tumor tissues of mice ×40 |
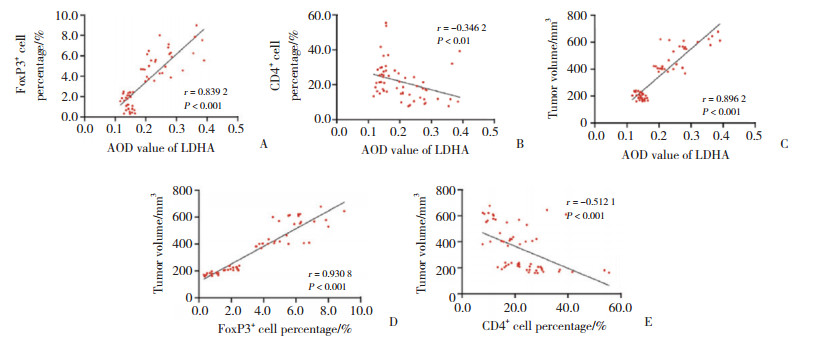
相关性分析结果(图 5)显示,LDHA与FoxP3表达呈正相关(P < 0.001),与CD4表达呈负相关(P < 0.01),与人肝癌组织检测结果相同。肿瘤体积与肿瘤组织中LDHA水平和FoxP3+细胞百分比呈正相关(P < 0.001),与CD4+细胞百分比呈负相关(P < 0.001)。结果提示,蟾毒灵可以减少肿瘤组织中Treg细胞数量,从而达到抑制肿瘤发生和发展的作用。
|
| A, correlation between LDHA expression and FoxP3+ cell percentage; B, correlation between LDHA expression and CD4+ cell percentage; C, correlation between LDHA expression and tumor volume; D, correlation between FoxP3+ cell percentage and tumor volume; E, correlation between CD4+ cell percentage and tumor volume. 图 5 肿瘤组织中LDHA、FoxP3、CD4表达与肿瘤体积的相关性 Fig.5 Correlation between the expression of LDHA, FoxP3, and CD4 in tumor tissues and tumor volume |
3 讨论
本研究通过对HCC患者手术标本进行分析,证实了肝癌组织中LDHA表达水平显著升高,这与Treg细胞富集呈显著正相关。本研究结果与肿瘤微环境有氧糖酵解特征相吻合,并支持“酸性肿瘤微环境是Treg细胞分化、增殖和功能维持的理想场所”这一理论[9]。本研究结果进一步提示,LDHA表达及其产生乳酸不仅影响Treg细胞数量,还可能通过改变局部代谢环境,影响CD4+ T细胞亚群的整体平衡,促使免疫反应向抑制状态倾斜。
基于上述发现,本研究采用皮下荷瘤小鼠模型进一步探究传统中药活性成分蟾毒灵的抗肿瘤机制。结果显示,蟾毒灵和草氨酸盐能显著下调肿瘤组织中LDHA表达,而应用丙酮酸重新激活LDHA表达则部分逆转了蟾毒灵的抑瘤效果。结果证明,抑制LDHA介导的糖酵解途径是蟾毒灵发挥抗肿瘤作用机制之一。
鉴于乳酸已被广泛证实是促进Treg细胞生成和功能的关键因子[10],本研究发现,蟾毒灵可抑制LDHA表达,从而减少乳酸生成。本研究进一步评估了蟾毒灵对Treg细胞的影响,结果显示,蟾毒灵组和草氨酸盐组小鼠肿瘤内Treg细胞数量显著减少,且Treg细胞占比与LDHA表达呈显著正相关。证明了蟾毒灵通过靶向抑制LDHA,有效削弱肿瘤微环境中Treg细胞数量。这一机制在血清学层面也得到了印证:蟾毒灵显著降低了Treg细胞功能活化相关的免疫抑制因子IL-10和TGF-β表达。进一步证实了蟾毒灵不仅减少了Treg细胞数量,也抑制了其免疫抑制功能。
本研究将蟾毒灵的作用机制与HCC肿瘤微环境的关键调控轴LDHA-乳酸-Treg细胞紧密联系起来。近期研究[9]揭示,当Treg细胞环境乳酸水平降低时,其免疫抑制能力被削弱,为免疫治疗创造有利条件。本研究表明,蟾毒灵作为中药复方华蟾素的核心活性成分之一,能够有效干预LDHA-乳酸-Treg细胞轴,不仅直接抑制肿瘤生长,更能重塑免疫微环境,削弱Treg细胞介导的免疫逃逸。这为华蟾素在肝癌治疗中的临床应用,尤其是作为免疫治疗的潜在增敏剂,提供了坚实的理论基础和实验依据。
| [1] |
BRAY F, LAVERSANNE M, SUNG H, et al. Global cancer statistics 2022:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2024, 74(3): 229-263. DOI:10.3322/caac.21834 |
| [2] |
蒋磊, 李玉强, 李男, 等. 缺氧肝细胞癌细胞来源外泌体miR-432-5p通过SOCS3/STAT3促进M2型巨噬细胞极化[J]. 中国医科大学学报, 2023, 52(7): 601-607. DOI:10.12007/j.issn.0258-4646.2023.07.005 |
| [3] |
LI C, JIANG P, WEI S, et al. Regulatory T cells in tumor microenvironment: new mechanisms, potential therapeutic strategies and future prospects[J]. Mol Cancer, 2020, 19(1): 116. DOI:10.1186/s12943-020-01234-1 |
| [4] |
LIU X, ZHANG W, HAN Y, et al. FOXP3+regulatory T cell perturbation mediated by the IFNγ-STAT1-IFITM3 feedback loop is essential for anti-tumor immunity[J]. Nat Commun, 2024, 15(1): 122. DOI:10.1038/s41467-023-44391-9 |
| [5] |
WARBURG O. Iron, the oxygen-carrier of respiration-ferment[J]. Science, 1925, 61(1588): 575-582. DOI:10.1126/science.61.1588.575 |
| [6] |
YU Z, LI YY, LI Y, et al. Bufalin stimulates antitumor immune response by driving tumor-infiltrating macrophage toward M1 phenotype in hepatocellular carcinoma[J]. J Immunother Cancer, 2022, 10(5): e004297. DOI:10.1136/jitc-2021-004297 |
| [7] |
FU R, YU F, WU W, et al. Bufalin enhances the killing efficacy of NK cells against hepatocellular carcinoma by inhibiting MICA shedding[J]. Int Immunopharmacol, 2021, 101(Pt B): 108195. DOI:10.1016/j.intimp.2021.108195 |
| [8] |
ZHANG Q, LYU W, YU M, et al. Investigating the inotropic effect of pyruvic acid on the isolated rat heart and its underlying mechanism[J]. Environ Toxicol Pharmacol, 2019, 71: 103206. DOI:10.1016/j.etap.2019.103206 |
| [9] |
WATSON MJ, VIGNALI PDA, MULLETT SJ, et al. Metabolic support of tumour-infiltrating regulatory T cells by lactic acid[J]. Nature, 2021, 591(7851): 645-651. DOI:10.1038/s41586-020-03045-2 |
| [10] |
GU J, ZHOU J, CHEN Q, et al. Tumor metabolite lactate promotes tumorigenesis by modulating MOESIN lactylation and enhancing TGF-β signaling in regulatory T cells[J]. Cell Rep, 2022, 39(12): 110986. DOI:10.1016/j.celrep.2022.110986 |
 2025, Vol. 54
2025, Vol. 54