文章信息
- 宋芷琪, 宋囡, 刘玉, 刘竞男, 王群, 贾连群, 闵冬雨
- SONG Zhiqi, SONG Nan, LIU Yu, LIU Jingnan, WANG Qun, JIA Lianqun, MIN Dongyu
- 丹蒌片通过调控氧化应激改善HepG2细胞脂质沉积
- Danlou tablet ameliorates lipid deposition in HepG2 cells by regulating oxidative stress
- 中国医科大学学报, 2025, 54(10): 865-868, 882
- Journal of China Medical University, 2025, 54(10): 865-868, 882
-
文章历史
- 收稿日期:2025-04-10
- 网络出版时间:2025-10-15 13:48:06
2. 辽宁中医药大学中医脏象理论及应用教育部重点实验室,沈阳 110847;
3. 辽宁中医药大学医学检验学院实训室,沈阳 110847;
4. 辽宁中医药大学附属医院中医药实验中心,沈阳 110032
2. Key Laboratory of Ministry of Education for Traditional Chinese Medicine Viscera-State Theory and Applications, Liaoning University of Traditional Chinese Medicine, Shenyang 110847, China;
3. Training Laboratory, Medical Laboratory College, Shenyang 110847, China;
4. TCM Experimental Center, Affiliated Hospital of Liaoning University of Traditional Chinese Medicine, Shenyang 110032, China
临床多种常见代谢疾病(如动脉粥样硬化、脂肪肝、糖尿病等)均与脂质代谢障碍关系密切,因此通过调控脂质代谢障碍防治代谢疾病尤为重要[1]。脂质代谢有多种途径,最主要的分解途径是通过线粒体β氧化将脂肪酸彻底水解。当摄入过多油脂时,体内脂质含量异常增加,分解、消化、吸收、转运出现异常,血液和组织器官中脂质含量失衡,从而影响身体机能,脂质堆积体内,而脂质代谢异常可进一步发展为动脉粥样硬化等疾病[2]。
中医认为,脂质沉积本质是脏腑功能失调,导致阴阳气血失衡,痰湿、淤血等病理产物堆积,阻滞经络气血运行。《黄帝内经》中记载:“肥者令人内热,甘者令人中满,故其气上溢,转为消渴”[3],“嗜食肥甘厚味”导致脾家伤,脾家伤则运化失司,痰饮水湿郁于中焦则出现脘腹胀满等症状,郁而化久则生热。治则上以疏肝健脾为主,疏肝以促进脂质代谢,健脾以祛除湿浊,同时兼顾活血化瘀以通络。《中华人民共和国药典》中记载,丹蒌片由瓜蒌皮、薤白、川芎等十味中药组成,具有化痰散结、活血化瘀的功效,此方是目前临床用于治疗痰瘀互结导致胸痹的常见药。现代研究[4]表明,丹蒌片可以降低总胆固醇、甘油三酯(triglyceride,TG)水平,抑制动脉粥样硬化斑块形成,并通过调控炎症小体抑制炎症反应和氧化应激反应等。但丹蒌片改善脂质代谢的机制并未阐明。本课题组前期研究[5]发现,丹蒌片可能通过干预氧化应激反应调控脂质代谢。本研究采用油酸诱导HepG2细胞建立脂质沉积模型,探究丹蒌片改善脂质沉积的作用机制,为临床治疗脂质沉积提供依据。
1 材料与方法 1.1 细胞系、主要试剂和仪器HepG2细胞,购自中国科学院典型培养物保藏委员会细胞库。p53激动剂,购自美国MedChemExpress公司;丹蒌片,购自吉林康乃尔药业有限公司;TG、非酯化脂肪酸(non-esterified fatty acid,NEFA)、过氧化氢酶(catalase,CAT)试剂盒,购自南京建成生物工程研究所有限公司;总超氧化物歧化酶比色法测试盒、氧化应激指标丙二醛(malondialdehyde,MDA)比色法测试盒、活性氧(reative oxygen species,ROS)荧光法测试盒,购自武汉伊莱瑞特生物科技股份有限公司;环氧化酶-2(cyclooxygenase-2,COX-2)测定试剂盒,购自上海酶联生物科技有限公司。酶标仪,购自上海普迈生物科技有限公司;高速冷冻离心机,购自美国ThermoFisher Scientific公司;荧光细胞成像仪,购自美国Bio-Rad公司。
1.2 方法 1.2.1 确定含丹蒌片血清最佳给药浓度和时间大鼠适应性喂养1周,随机分为空白对照组和丹蒌片组,每组6只。按照表面积换算法计算给药量,丹蒌片组用丹蒌片水溶液(680 mg/kg)灌胃,40.3 mg/次,空白对照组等体积生理盐水灌胃,2次/d,连续灌胃7 d。末次给药2 h后,腹主动脉采血,室温静置1 h,3 000 r/min离心10 min。收集血清,进行过滤灭活处理,于-20 ℃冰箱保存。将含丹蒌片血清用培养基稀释,配制成含丹蒌片血清体积分数分别为5%、10%、15%、20%的培养液。用0%(空白对照)、5%、10%、15%、20%含丹蒌片血清培养液分别培养HepG2细胞12、24和48 h。采用CCK-8试剂盒计算细胞活性,筛选出丹蒌片最佳给药浓度和给药时间。
1.2.2 不同浓度油酸对HepG2细胞活性影响:取对数期HepG2细胞,接种于96孔板中,待细胞培养贴壁后,用含0(空白对照)、100、200、400、800、1 000 μmol/L油酸的新鲜培养液继续培养细胞,再加入CCK-8溶液继续培养2 h,通过酶标仪检测各孔光密度(optical density,OD)值,计算细胞活性,确定最佳油酸浓度,构建脂质沉积模型[6]。
1.2.3 细胞处理和分组将HepG2细胞分为空白对照组(不做处理)、模型组(给予油酸)、丹蒌片组(给予油酸+含丹蒌片血清),用于后续实验。分组处理所用的含丹蒌片血清和油酸的浓度,为1.2.1和1.2.2中确定的最佳浓度。
1.2.4 酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)检测细胞上清液NEFA和TG的含量取各组细胞上清液,按照试剂盒说明书进行检测,于酶标仪上读取各孔OD值,计算各组细胞中NEFA和TG含量。
1.2.5 油红O染色观察脂滴分布情况取对数期细胞,接种于6孔板,每孔2 mL,待细胞贴壁后培养24 h,按照说明书操作,封片后,光学显微镜下观察脂滴分布情况。
1.2.6 细胞内SOD、MDA、CAT及COX-2含量测定吸取各组细胞培养液,4 000 r/min离心5 min,取上清液待测。按照ELISA试剂盒说明书操作,于酶标仪上读取各孔OD值,计算各组细胞中SOD、MDA、CAT和COX-2含量。
1.2.7 DCFH-DA荧光探针测定ROS表达取对数期细胞,接种于6孔板,培养好的细胞用PBS洗涤3次,加入DMEM培养基,根据说明书配置工作液,加入DCFH-DA探针,室温下避光孵育30 min,PBS再次洗涤3次,去除探针,荧光显微镜下观察细胞并拍照。
1.3 统计学分析采用GraphPad Prism 8.0进行统计分析。数据用x±s表示,2组间比较采用独立样本t检验,多组间比较采用单因素方差分析。P < 0.05为差异有统计学意义。
2 结果 2.1 不同浓度丹蒌片及不同给药时间对HepG2细胞活性的影响与对照组相比,15%和20%丹蒌片组在12、24、48 h时细胞活性明显降低(均P < 0.01),10%丹蒌片组在48 h时细胞活性明显降低(P < 0.01),在12和24 h时细胞活性无统计学差异(均P > 0.05)。见表 1。因此,本研究确定的丹蒌片最佳给药浓度是10%,给药时间是24 h。
| Group | n | 12 h | 24 h | 48 h |
| Control | 6 | 100.00±4.58 | 100.00±3.88 | 100.00±12.57 |
| 5% Danlou tablet | 6 | 92.12±3.081) | 93.59±8.65 | 79.49±3.412) |
| 10% Danlou tablet | 6 | 94.09±5.97 | 91.25±5.89 | 71.36±5.722) |
| 15% Danlou tablet | 6 | 73.71±3.292) | 66.85±4.802) | 59.99±5.452) |
| 20% Danlou tablet | 6 | 67.83±2.802) | 57.86±5.242) | 48.13±4.172) |
| 1)P < 0.05 vs. control group;2)P < 0.01 vs. control group. | ||||
2.2 不同浓度油酸对HepG2细胞活性的影响
对照组以及100、200、400、800、1 000 μmol/L油酸组细胞活性分别为(100.00±4.49)%、(97.68±6.96)%、(93.12±5.89)%、(85.66±8.81)%、(85.88±7.01)%、(49.77±7.78)%。与对照组相比,100和200 μmol/L油酸组细胞活性无明显变化(均P > 0.05),400、800和1 000 μmol/L油酸组细胞活性明显降低(分别为P < 0.05,P < 0.05,P < 0.01)。因此,本研究确定的最佳油酸浓度为800 μmol/L。
2.3 丹蒌片调控HepG2细胞中NEFA和TG水平空白对照组、模型组、丹蒌片组HepG2细胞中NEFA水平分别为(0.009±0.003)、(0.285±0.025)、(0.213±0.014)mmol/L,TG水平分别为(0.081±0.031)、(0.398±0.046)、(0.171±0.017)mmol/L。与空白对照组相比,模型组HepG2细胞中NEFA和TG水平明显升高(P < 0.01);与模型组相比,丹蒌片组NEFA和TG水平明显降低(P < 0.01)。
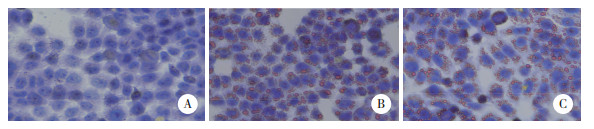
2.4 丹蒌片调控HepG2细胞脂质水平与空白对照组相比,模型组HepG2细胞中红染明显,脂滴数量较多;与模型组相比,丹蒌片组HepG2细胞中脂质红染情况改善,脂滴体积明显缩小。见图 1。
|
| A, control group; B, model group; C, Danlou tablet group. 图 1 油红O染色检测细胞内脂滴累积×400 Fig.1 Intracellular lipid droplet accumulation detected by oil red O staining × 400 |
2.5 丹蒌片对HepG2细胞氧化应激的影响
与空白对照组相比,模型组MDA和COX-2水平明显升高,CAT和SOD水平明显降低(P < 0.05);与模型组相比,丹蒌片组MDA和COX-2水平明显降低,CAT和SOD水平明显升高(P < 0.05)。见表 2。
| Group | n | MDA(μmol/L) | CAT(U/mg protein) | SOD(U/mL) | COX-2(ng/mL) | Fluorescence intensity of ROS |
| Control | 6 | 1.42±0.04 | 2.49±0.04 | 73.23±0.33 | 67.29±6.20 | 28.52±1.72 |
| Model | 6 | 2.38±0.361) | 2.07±0.071) | 60.42±1.821) | 143.69±1.901) | 47.93±1.821) |
| Danlou tablet | 6 | 1.67±0.032) | 2.38±0.033) | 69.43±0.233) | 108.10±3.983) | 35.67±2.933) |
| 1)P < 0.01 vs. control group;2)P < 0.05 vs. model group;3)P < 0.01 vs. model group. | ||||||
2.6 丹蒌片对ROS表达的影响
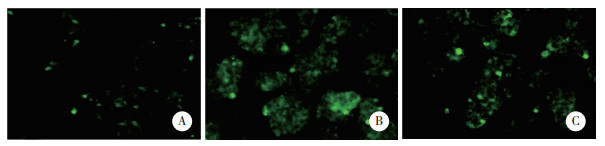
与空白对照组相比,模型组ROS荧光强度明显增强(P < 0.01);与模型组相比,丹蒌片组ROS荧光强度明显减弱(P < 0.01)。见图 2、表 2。
|
| A, control group; B, model group; C, Danlou tablet group. 图 2 DCFH-DA荧光探针检测细胞内ROS水平×200 Fig.2 Intracellular reactive oxygen species levels detected by DCFH-DA fluorescent probe ×200 |
3 讨论
流行病学调查显示,全球约30%的成年人存在脂质沉积,且脂质沉积有年轻化的趋势[7]。脂质沉积的核心机制是肝脏脂质代谢失衡,胰岛素抵抗促使外周脂肪组织分解增加,释放过量NEFA进入肝脏,同时肝细胞自身合成TG增多,而极低密度脂蛋白分泌不足,导致脂质在肝细胞内堆积[8]。此外,ROS过度生成引发氧化应激,促使肝细胞脂质过氧化,激活炎症通路,导致肝细胞损伤和脂肪变性,从而进一步加重脂质沉积[9]。油酸作为重要的游离脂肪酸,能够通过直接诱导脂质沉积、引发氧化应激及调控脂质代谢相关基因表达,扰乱脂质代谢平衡,从而建立脂质沉积模型[6]。因此,本研究采用油酸刺激HepG2细胞,建立脂质沉积细胞模型。
本研究发现,当油酸浓度达到400和800 μmol/L时,细胞活性下降,但细胞存活率仍在80%以上;但当油酸浓度达到1 000 μmol/L时,细胞活性显著降低,细胞死亡率超50%。因此,本研究后续实验选用800 μmol/L油酸作为最佳造模浓度。ELISA和油红O染色结果证明,模型组NEFA和TG含量明显高于空白对照组,提示油酸诱导脂质沉积细胞模型成功建立。
中医治疗脂质沉积以健脾化痰祛瘀法为主。《中华人民共和国药典》中记载,丹蒌片用于治疗痰瘀互结型冠状动脉粥样硬化性心脏病,方中诸药配伍通过“化痰-祛瘀-补气-调气机”的立体配伍,实现标本兼治。根据中医“未病先防”的观念,本课题组前期做了多项相关实验,探究丹蒌片在治疗脂质代谢方面的功效及其机制。本课题组前期研究发现,丹蒌片可以减轻非酒精性脂肪性肝病小鼠模型肝脏氧化损伤[10-11];可以影响TG合成,改善ApoE-/-AS小鼠肝脏脂质沉积[12];亦可介导线粒体损伤,改善高脂喂养的ApoE-/-小鼠脂质代谢水平[5, 13]。本研究通过CCK-8法检测不同浓度含丹蒌片血清对细胞活性的影响,发现丹蒌片给药浓度为15%时,细胞活性明显降低,因此选取10%含丹蒌片血清用于后续实验。本研究结果表明,丹蒌片可明显降低油酸导致的NEFA和TG水平升高,且油红O染色结果显示,与模型组相比,丹蒌片组脂滴体积缩小且脂滴数量减少,提示丹蒌片可以有效改善脂质沉积情况。
氧化应激与脂质沉积是一个双向恶性循环,脂质沉积可导致线粒体膜脂质过氧化,破坏电子传递链功能,引发“电子泄漏”,释放大量ROS,同时肝脏脂滴沉积会抑制线粒体脂肪酸氧化能力,迫使细胞依赖效率较低的过氧化物酶体β氧化途径,进一步加剧ROS[14-15]。而大量ROS可攻击细胞膜中的多不饱和脂肪酸,引发脂质过氧化反应,生成MDA等毒性产物,破坏线粒体功能,抑制脂肪酸β氧化,导致NEFA和TG在体内异常堆积。本研究结果表明,模型组MDA和COX-2水平明显升高,抗氧化酶SOD和CAT水平明显降低,丹蒌片干预后抗氧化酶呈高表达,而MDA和COX-2表达水平降低。本研究中,DCFH-DA荧光探针法检测结果表明,模型组ROS呈高表达,丹蒌片组ROS含量明显降低,证实丹蒌片可能通过影响氧化应激反应调控脂质代谢。
综上所述,丹蒌片通过抑制氧化应激反应,促进脂质代谢,从而改善油酸诱导的HepG2高脂细胞模型脂质沉积情况。
| [1] |
LAVIE CJ, MCAULEY PA, CHURCH TS, et al. Obesity and cardiovascular diseases: implications regarding fitness, fatness, and severity in the obesity paradox[J]. J Am Coll Cardiol, 2014, 63(14): 1345-1354. DOI:10.1016/j.jacc.2014.01.022 |
| [2] |
MORIGNY P, BOUCHER J, ARNER P, et al. Lipid and glucose metabolism in white adipocytes: pathways, dysfunction and therapeutics[J]. Nat Rev Endocrinol, 2021, 17(5): 276-295. DOI:10.1038/s41574-021-00471-8 |
| [3] |
梁瑛楠, 陈振杰, 杜怡然, 等. 基于《黄帝内经》"阳结"理论探析糖尿病肾病病机及治法[J]. 北京中医药, 2025, 44(6): 782-786. DOI:10.16025/j.1674-1307.2025.06.024 |
| [4] |
李崇钗, 张明雪. 丹蒌片临床应用研究进展[J]. 辽宁中医杂志, 2023, 50(4): 199-203. DOI:10.13192/j.issn.1000-1719.2023.04.052 |
| [5] |
宋芷琪, 宋囡, 朱敬轩, 等.丹蒌片通过影响线粒体损伤改善高脂喂饲ApoE-/-小鼠肝脏脂质沉积的机制研究[J/OL].辽宁中医杂志, https://link.cnki.net/urlid/21.1128.r.20241216.1005.112.
|
| [6] |
林晓宇, 朱月永, 江家骥. 油酸诱导HepG2细胞脂肪变性模型的建立[J]. 数理医药学杂志, 2015, 28(1): 6-8. DOI:10.3969/j.issn.1004-4337.2015.01.002 |
| [7] |
RUBINO F, CUMMINGS DE, ECKEL RH, et al. Definition and diag-nostic criteria of clinical obesity[J]. Lancet Diabetes Endocrinol, 2025, 13(3): 221-262. DOI:10.1016/S2213-8587(24)00316-4 |
| [8] |
VESKOVIĆ M, ŠUTULOVIĆ N, HRNČIĆ D, et al. The interconnection between hepatic insulin resistance and metabolic dysfunction- associated steatotic liver disease-the transition from an adipocentric to liver-centric approach[J]. Curr Issues Mol Biol, 2023, 45(11): 9084-9102. DOI:10.3390/cimb45110570 |
| [9] |
CLARE K, DILLON JF, BRENNAN PN. Reactive oxygen species and oxidative stress in the pathogenesis of MAFLD[J]. J Clin Transl Hepatol, 2022, 10(5): 939-946. DOI:10.14218/JCTH.2022.00067 |
| [10] |
张新, 陈文娜, 宋囡, 等. 丹蒌片通过铁死亡途径减轻非酒精性脂肪性肝病模型小鼠肝脏氧化损伤[J]. 中国病理生理杂志, 2021, 37(12): 2180-2188. DOI:10.3969/j.issn.1000-4718.2021.12.009 |
| [11] |
张新, 陈文娜, 宋囡, 等. 基于分子互作网络探讨丹蒌片干预PI3K/AKT/NF-κB/TNF通路防治非酒精性脂肪肝病的机制[J]. 中国免疫学杂志, 2022, 38(11): 1324-1332. DOI:10.3969/j.issn.1000-484X.2022.11.008 |
| [12] |
张美菱, 朱敬轩, 王杰, 等. 丹蒌片通过PTP1B/PP2A/SP1途径影响甘油三酯合成改善ApoE-/-AS小鼠肝脏脂质沉积的机制研究[J]. 时珍国医国药, 2024, 35(3): 571-575. DOI:10.3969/j.issn.1008-0805.2024.03.14 |
| [13] |
朱敬轩, 陈文娜, 宋囡, 等. 丹蒌片对ApoE-/-小鼠肝脏脂质沉积自噬及脂质代谢的调节作用[J]. 时珍国医国药, 2023, 34(2): 269-272. DOI:10.3969/j.issn.1008-0805.2023.02.04 |
| [14] |
杨冰清, 尹静亚, 王琦. 肝线粒体功能障碍在非酒精性脂肪性肝病发病中的作用机制[J]. 临床肝胆病杂志, 2024, 40(1): 147-150. DOI:10.12449/JCH240124 |
| [15] |
张艺萍, 丁璟, 张祎, 等. 鸢尾素在糖脂代谢及肥胖中的作用[J]. 中国医科大学学报, 2024, 53(7): 646-650. DOI:10.12007/j.issn.0258-4646.2024.07.012 |
 2025, Vol. 54
2025, Vol. 54