文章信息
- 栾云, 孙菲, 滕浩
- LUAN Yun, SUN Fei, TENG Hao
- 丙戊酸钠致高氨血症脑病2例报道并文献复习
- Valproate-induced hyperammonemic encephalopathy: report of two cases and literature review
- 中国医科大学学报, 2025, 54(1): 90-93
- Journal of China Medical University, 2025, 54(1): 90-93
-
文章历史
- 收稿日期:2024-02-05
- 网络出版时间:2025-01-09 16:15:44
丙戊酸钠是一种常见的抗癫痫药物,应用于全身性或局灶性癫痫发作[1]。此外,丙戊酸钠还是一种情绪稳定剂,可用于治疗多种精神疾病(躁狂抑郁性精神病、重度抑郁症和创伤后应激障碍等)[2]。丙戊酸钠通常耐受性良好,临床应用越来越广泛,其不良反应也受到关注。丙戊酸钠致高氨血症脑病(valproate-induced hyperammonemic encephalopathy,VHE)是较为严重的不良反应[3],其临床表现主要包括急性发作性意识障碍、局灶性神经症状以及癫痫发作频率增加等[4]。VHE临床表现无特异性,极易漏诊、误诊甚至导致死亡。本文报道了我院神经外科收治的2例VHE患者的诊疗经过,并结合文献进行分析,旨在为VHE患者的诊断和治疗提供参考。
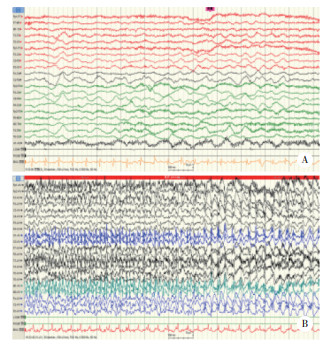
1 临床资料病例1,女,26岁,以“间断抽搐5年再发作8 h”为主诉于2022年7月14日入院。患者5年前产后开始出现抽搐,每年发作2~3次,每次发作时间数十秒至2 min,具体发作形式不详,未系统诊治。8 h前患者自觉头痛,于当地医院就诊,完善检查过程中出现抽搐,给予静脉镇静,具体药物不详,抗癫痫药物丙戊酸钠缓释片口服(0.25 g/次,2次/d),控制效果不佳。症状加重后转至我院急诊。患者否认高血压、糖尿病史,急诊化验肝肾功能均正常。查体结果:患者头面部向左侧偏转,双眼向左凝视,发作时瞳孔散大,呼之不应,无肢体强直震挛,无舌咬伤,无二便失禁,持续1 min左右,凝视及头部偏转症状缓解,期间意识未完全恢复。临时给予1次苯巴比妥(0.1 g)肌肉注射,丙戊酸钠缓释片(0.25 g/次,2次/d)口服。10 min后再次发作,呈癫痫持续状态,遂转入神经外科继续治疗。入院后给予丙戊酸钠[1 mg/(kg·h)]静脉泵入,口服左乙拉西坦片(0.25 g/次,2次/d)控制癫痫。2 d后完善视频脑电图,结果显示,清醒状态下,弥漫性低波幅混合慢波活动。发作期间监测发现患者均为意识丧失,持续约1 min,肢体异常活动不明显,发作期全导δ波活动夹杂少量棘波,见图 1。脑电图监测期间患者出现精神状态萎靡,拒绝进食,夜间出现大喊大叫、四肢乱动等情况,完善血氨检查,结果为183.1 μmol/L。根据临床表现考虑患者可能为VHE,遂停用丙戊酸钠,继续口服左乙拉西坦片(0.25 g,2次/d),并口服奥卡西平(0.3 g/次,2次/d)控制癫痫。同时口服乳果糖(20 g/次,1次/d)降血氨治疗。患者症状逐渐好转,1 d后神志转清,精神症状完全消失,反应灵敏,四肢肌力Ⅴ级,复查血氨下降至59.9 μmol/L,无癫痫及再发精神症状。患者顺利出院,出院后随访1年,再无上述症状发作。
|
| A,清醒状态;B,发作期. 图 1 视频脑电图结果 |
病例2,男,46岁,以“外伤后脑出血7 d”为主诉于2023年6月7日入院,患者7 d前无明显诱因出现肢体活动不便伴头晕后摔倒,伤及头部,于当地医院行CT检查提示右侧顶枕叶脑出血。遂行脑出血钻孔引流术,术后对症给予降颅内压等治疗后症状缓解,1 d前患者复查头CT见出血范围较前明显增加,遂转入我科继续治疗。患者否认高血压、糖尿病及冠状动脉粥样硬化性心脏病史,入院化验肝肾功能均正常。查体结果:患者神清语明,双瞳孔等大正圆,直径3.0 mm,对光反射灵敏,眼球向各方向活动自如,眼位居中,无眼震,左侧肢体活动较差,肌力Ⅳ级,右侧肢体活动自如,肌力Ⅴ级。入院后急诊全身麻醉下行右侧脑内血肿清除术,术后给予丙戊酸钠[1 mg/(kg·h)]静脉泵入预防癫痫发作等治疗,术后3 d患者突然出现发热,意识不清,大声喊叫,肌张力增高等异常表现,血氨139.8 μmol/L,根据临床症状分析可能是VHE,遂停用丙戊酸钠,改用盐酸右美托咪定[0.4 μg/(kg·h)]静脉注射,联合奥卡西平口服(0.3 g/次,2次/d)。门冬氨酸鸟氨酸静脉滴注(5 g/次,1次/d);乳果糖口服(20 g/次,1次/d)降氨治疗,症状逐渐好转。1 d后精神症状完全消失,反应灵敏,左侧肢体活动较差,肌力Ⅳ级,右侧肢体肌力Ⅴ级,3 d后复查血氨下降至54.0 μmol/L,无癫痫及再发精神症状。患者顺利出院,出院后随访6个月,再无上述症状发作。
2例患者均知情同意并签署知情同意书。
2 讨论 2.1 发病机制丙戊酸钠引起脑病的主要原因是高氨血症。星形胶质细胞中谷氨酰胺水平增加导致渗透压升高,从而导致脑水肿。此外,高氨血症可引起星形胶质细胞对谷氨酸摄取的抑制,导致细胞兴奋性增加[5]。另外增多的氨与α-酮戊二酸结合生成谷氨酸会导致脑内ATP合成减少,进而引起脑功能障碍、昏迷等症状。这是由于过多的氨会干扰三羧酸循环的代谢过程,从而导致ATP合成受到抑制[6]。丙戊酸钠引起的脑病患者大多有高氨血症。已有研究[7]发现,所有出现脑病症状的患者血氨水平都升高。另有1项对107例接受丙戊酸钠治疗的情绪障碍和癫痫患者进行的前瞻性研究[8]发现,55.3%患者血氨水平升高。这表明高氨血症可能是丙戊酸钠诱导脑病的重要原因。丙戊酸钠导致血氨升高的原因主要包括以下几点:(1)丙戊酸钠可增强谷氨酰胺的摄取和肾氨的释放,导致血氨水平升高。当血氨水平升高时,谷氨酰胺合成酶将谷氨酸和氨转化为谷氨酰胺。(2)大多数丙戊酸钠引起的脑病患者表现为低肉毒碱血症[9]。肉毒碱是将脂肪酸转运到线粒体中进行氧化的载体,是线粒体能量代谢的重要辅助因子。丙戊酸钠可与肉毒碱相互作用,增加其肾脏排泄。此外,丙戊酸钠、肉毒碱和辅酶A可以形成复合物,降低血清肉毒碱水平,从而影响游离脂肪酸的代谢和乙酰辅酶A的产生,进一步导致N-乙酰谷氨酸缺乏,血氨水平升高和脑病发生。因此,肉毒碱是氨排泄和丙戊酸钠代谢的重要辅助因子,其缺乏可促进丙戊酸钠诱导的脑病发生。此外,研究[7]显示口服L-肉毒碱可逆转或抑制丙戊酸钠诱导的脑病进展。(3)尿素循环障碍患者的高氨血症脑病可能是由于丙戊酸钠抑制尿素循环限速酶CPS-I的活性所致。尿素循环障碍可使氨排泄减少,进而导致血清氨水平升高[10]。VERBIEST等[8]对1例丙戊酸钠诱导昏迷的成人患者的肝活检结果显示,CPS-I活性降低。表明尿素循环障碍可能是丙戊酸钠诱导脑病的原因之一。
2.2 危险因素研究[11]统计显示,丙戊酸钠治疗后高氨血症发生率为27.8%,其中VHE的发生率为5.1%。但也有研究[12]显示,VHE的严重程度与丙戊酸钠的血药浓度和治疗时间以及血氨浓度无明显关系。即使患者在接受丙戊酸钠治疗之前未出现任何并发症,也无法表明以后治疗中不会发生VHE。研究[13]显示,肉毒碱或尿素循环酶缺乏、高代谢状态、素食等营养不良(减少游离肉毒碱)、年龄 < 2岁(肝功能不成熟)以及精神发育迟滞和甲状腺相关疾病均可能是诱发VHE的高危因素。同时,丙戊酸钠与其他抗癫痫药的相互作用,也可能增加发生VHE的风险,尤其是丙戊酸钠与托吡酯、苯巴比妥、苯妥英、卡马西平等抗癫痫药物同时使用时,高氨血症发生率高于单纯丙戊酸钠治疗[8, 14-15]。另外,有研究[4]指出,遗传因素也可能影响个体对VHE的易感性,某些基因突变可能与VHE的发生风险有关。然而,目前这方面的研究有限,仍需进一步论证。
2.3 临床表现VHE可分为急性和亚急性2种,其临床表现多样。急性VHE的临床表现主要包括:(1)意识障碍,患者常表现为嗜睡、昏睡或昏迷状态[8, 16]。(2)癫痫持续状态,部分患者可能出现全身性癫痫发作伴随谵妄和注意力不集中。根据脑电图出现的广泛性癫痫放电,患者可被诊断为非惊厥性癫痫持续状态[7]。(3)精神和行为异常,大多数患者出现不同程度的精神和行为障碍,包括人格改变和易怒等[17]。亚急性VHE的临床表现主要包括:(1)认知功能障碍,部分患者可能出现认知功能障碍,如反应时间延长等。(2)帕金森病,表现为可逆性帕金森病,包括运动迟缓、僵硬、姿势不稳和静止性震颤等症状。(3)其他临床表现,可能包括孤独症谱系障碍和夜间遗尿等[18]。
2.4 治疗丙戊酸钠诱发的无症状高氨血症不需要治疗,而VHE治疗有多种方式,最重要的是当出现高氨血症脑病时需停用丙戊酸钠,症状一般在停药1 d至数天内消失,但也有症状较长时间才消失,甚至导致患者死亡的报道[16, 19]。由于抗癫痫药不能突然停药,需逐渐减量,所以在停用丙戊酸钠的同时需换用其他能快速起效且不经肝脏代谢的抗癫痫药物[7]。左乙拉西坦一般与丙戊酸钠联用不会增加高氨血症脑病的风险,且左乙拉西坦起效迅速,将将其加量可稳定因丙戊酸钠减量导致的血药浓度波动[20]。与此同时,降血氨治疗也是十分必要的,口服乳果糖,加用精氨酸、谷氨酸、左卡尼汀等均可降低血氨水平。
综上所述,本文报道了2例VHE患者的诊治经过,2例患者的临床表现不同,但均存在高氨血症。对于应用丙戊酸钠期间出现精神神经症状的患者,应警惕高氨血症脑病的可能,并要尽快检测血氨水平以明确诊断。治疗方面应尽早停用丙戊酸钠,并根据病情给予适当的镇静、降氨和抗癫痫治疗。另外,临床医生应提高对VHE的认识,做到早发现早治疗,以改善患者预后。
| [1] |
VILORIA ALEBESQUE A, MONTES CASTRO N, ARCOS SÁNCHEZ C, et al. Non-convulsive status epilepticus secondary to valproate-induced hyperammonaemic encephalopathy[J]. Neurologia, 2020, 35(8): 603-606. DOI:10.1016/j.nrl.2019.05.010 |
| [2] |
SHETTY SS, ANNAJIGOWDA HH, DAHALE AB. Valproate-induced hyperammonemia, neuroleptic sensitivity, and cerebellar atrophy-a clinical conundrum in the management of bipolar disorder[J]. Bipolar Disord, 2024, 26(2): 200-203. DOI:10.1111/bdi.13403 |
| [3] |
陈晶贞, 朱仁敬, 林晓芳, 等. 丙戊酸致高氨血症脑病二例并文献复习[J]. 实用药物与临床, 2019, 22(7): 730-733. DOI:10.14053/j.cnki.ppcr.201907015 |
| [4] |
WU JH, LI JY, JING W, et al. Valproic acid-induced encephalopathy: a review of clinical features, risk factors, diagnosis, and treatment[J]. Epilepsy Behav, 2021, 120: 107967. DOI:10.1016/j.yebeh.2021.107967 |
| [5] |
VAIDYANATHAN S, CHATORIKAR S, PRAHARAJ SK, et al. Valproate-associated hyperammonemic encephalopathy: clinical correlates and management strategies in a tertiary care center[J]. J Clin Psychopharmacol, 2023, 43(2): 145-148. DOI:10.1097/JCP.0000000000001659 |
| [6] |
孙振晓, 于相芬. 丙戊酸钠导致高氨血症及脑病的研究进展[J]. 中华临床医师杂志(电子版), 2012, 6(8): 2163-2164. DOI:10.3877/cma.j.issn.1674-0785.2012.08.044 |
| [7] |
AMANAT S, SHAHBAZ N, HASSAN Y. Valproic acid induced hyperammonaemic encephalopathy[J]. J Pak Med Assoc, 2013, 63(1): 72-75. |
| [8] |
VERBIEST HB, STRAVER JS, COLOMBO JP, et al. Carbamyl phosphate synthetase-1 deficiency discovered after valproic acid-induced coma[J]. Acta Neurol Scand, 1992, 86(3): 275-279. DOI:10.1111/j.1600-0404.1992.tb05085.x |
| [9] |
DAWSON LP, LEE SJ, HOLLANDER YS. Valproate-induced hypera-mmonemic encephalopathy associated with urinary tract infection and urinary retention in the psychiatric setting[J]. Aust N Z J Psychiatry, 2016, 50(11): 1110. DOI:10.1177/0004867416640906 |
| [10] |
KANKANANARACHCHI I, JASINGE E, HEWAWITHARANA G. A case of carbamazepine-induced aggravation of self-limited epilepsy with centrotemporal spikes epilepsy and valproate-induced hyperammonemic encephalopathy in a child with heterozygous gene variant of carbomoyl phosphatase synthetase deficiency[J]. Case Rep Neurol Med, 2021, 2021: 2362679. DOI:10.1155/2021/2362679 |
| [11] |
LEWIS C, TESAR GE, DALE R. Valproate-induced hyperammonemic encephalopathy in general hospital patients with one or more psychiatric disorders[J]. Psychosomatics, 2017, 58(4): 415-420. DOI:10.1016/j.psym.2017.02.003 |
| [12] |
WOO PYM, WOO AWY, LAM SW, et al. Incidence, presentation, and risk factors for sodium valproate-associated hyperammonemia in neurosurgical patients: a prospective, observational study[J]. World Neurosurg, 2020, 144: e597-e604. DOI:10.1016/j.wneu.2020.09.027 |
| [13] |
GLATSTEIN M, BONIFACIO RINO P, DE PINHO S, et al. Levocarnitine for the treatment of valproic acid-induced hyperammonemic encephalopathy in children: the experience of a large, tertiary care pediatric hospital and a poison center[J]. Am J Ther, 2019, 26(3): e344-e349. DOI:10.1097/MJT.0000000000000706 |
| [14] |
CHOPRA A, KOLLA BP, MANSUKHANI MP, et al. Valproate-induced hyperammonemic encephalopathy: an update on risk factors, clinical correlates and management[J]. Gen Hosp Psychiatry, 2012, 34(3): 290-298. DOI:10.1016/j.genhosppsych.2011.12.009 |
| [15] |
WESSELMAN K, CAVALIERE V, GOYAL R, et al. Valproate, risperidone, and paliperidone: a case of valproate-induced hyperammonemic encephalopathy[J]. Ment Health Clin, 2024, 14(1): 28-32. DOI:10.9740/mhc.2024.02.028 |
| [16] |
NZWALO H, CARRAPATOSO L, FERREIRA F, et al. Valproic acid-induced hyperammonaemic coma and unrecognised portosystemic shunt[J]. Epileptic Disord, 2013, 15(2): 207-210. DOI:10.1684/epd.2013.0575 |
| [17] |
VAKRINOU A, MURPHY E, SISODIYA SM, et al. Risk factors and outcome of hyperammonaemia in people with epilepsy[J]. J Neurol, 2022, 269(12): 6395-6405. DOI:10.1007/s00415-022-11304-7 |
| [18] |
ZHU X, LI XL, ZHANG T, et al. Risk factors for valproic acid-induced hyperammonaemia in Chinese paediatric patients with epilepsy[J]. Basic Clin Pharmacol Toxicol, 2018, 123(5): 628-634. DOI:10.1111/bcpt.13049 |
| [19] |
LEE S, CHEONG J, KIM C, et al. Valproic acid-induced hyperammonemic encephalopathy as a cause of neurologic deterioration after unruptured aneurysm surgery[J]. J Korean Neurosurg Soc, 2015, 58(2): 159-162. DOI:10.3340/jkns.2015.58.2.159 |
| [20] |
SAMMAR A, TAWFIK M, FATIMA F, et al. Valproate-induced hyperammonemic encephalopathy causing new-onset seizures[J]. Cureus, 2023, 15(10): e47288. DOI:10.7759/cureus.47288 |
 2025, Vol. 54
2025, Vol. 54