文章信息
- 高质涵, 高铭泽, 陈培剑, 付高洁, 刘洁婷, 肖阳
- GAO Zhihan, GAO Mingze, CHEN Peijian, FU Gaojie, LIU Jieting, XIAO Yang
- 新型生物可降解锌合金植入材料在大鼠骨修复模型中的应用
- Application of a new type of biodegradable zinc alloy implant material in a rat model of bone repair
- 中国医科大学学报, 2025, 54(1): 69-74, 81
- Journal of China Medical University, 2025, 54(1): 69-74, 81
-
文章历史
- 收稿日期:2024-06-16
- 网络出版时间:2025-01-09 14:59:56
2. 牡丹江医科大学医学影像学院电工电子教研室, 黑龙江 牡丹江 157000;
3. 牡丹江医科大学附属第二医院普外科, 黑龙江 牡丹江 157000
2. Department of Electrical Engineering and Electronics, School of Medical Imaging, Mudanjiang Medical University, Mudanjiang 157000, China;
3. Department of General Surgery, The Second Affiliated Hospital, Mudanjiang Medical University, Mudanjiang 157000, China
生物可降解金属材料是一类可以在人体内自动降解的金属植入材料,材料降解产物的生物毒性对材料的安全性至关重要。生物可降解金属材料可以帮助患者避免进行移除植入物的二次手术,从而减轻患者的痛苦和经济负担[1-2]。目前,人们对生物可降解金属材料进行了广泛研究,希望其在未来能够替代一些传统的永久性植入材料并用于临床治疗。其中镁(Mg)、铁(Fe)和锌(Zn)合金材料是目前研究的主要热点。在生理环境中Mg合金的降解率低于0.23 mm/年,Zn合金的降解率为0.02~0.10 mm/年,Fe合金的降解率为0.001~0.090 mm/年。在骨科领域,植入物需要在植入体内的一段时间内提供足够的力学支撑,植入物的降解率需要与植入物周围组织的生长速率相匹配。Zn合金的降解率介于Mg合金和Fe合金之间,从材料的降解率方面考虑,Zn合金的降解率最符合临床需求[3]。Zn是人体必需的微量元素和第二丰富的过渡金属元素,在人体生理环境中起到非常重要的作用。Zn不仅在酶和调节蛋白中发挥辅助因子的重要作用[4],还具有一定的广谱抗菌活性。同时,Zn还可以促进成骨细胞活性,加速骨形成,促进骨折愈合,干扰血管内皮细胞代谢,延缓动脉粥样硬化形成。因此,从生理学角度看,Zn合金作为新一代生物可降解医用植入物,在骨折内固定、血管支架等领域具有良好的应用前景[5-7]。
目前,Zn合金材料仍然存在一些缺陷,限制了其在临床的应用,如铸态纯Zn的强度、硬度和延伸率较低,无法满足植入材料的力学要求。为了解决这些问题,国内外学者将合金化与热机械加工2种方法结合,可以在保证材料力学性的基础上最大限度地提高材料的生物相容性[7-9]。其中,合金化常见的元素有Mg、铜(Cu)、锰和锶(Sr)等。有研究[10]对铸态和挤压条件下Zn-3Cu-xMg(x=0、0.1、0.5和1.0 wt.%)合金的机械性能、腐蚀行为和体外细胞相容性进行了系统研究,发现Cu和Mg的添加显著提高了合金的拉伸屈服强度、生物相容性和降解率。还有研究[11-12]分析了Zn-1Mg-xSr(x=0.1和0.5 wt.%)合金的机械性能、体外降解行为和生物相容性,结果发现,添加Mg和Sr可显著提高拉伸屈服强度、极限强度,并且可以降低腐蚀率和生物相容性。
Cu和Sr都是人体的必需营养素。Cu在体内参与调节葡萄糖和胆固醇代谢、心脏电生理、神经行为以及免疫系统等。Sr可以通过增强前成骨细胞的复制和降低破骨细胞的活性,减少骨吸收并加速骨重塑过程。鉴于Cu和Sr的生理学作用以及之前的研究[10-12]结果,本课题组开发了一种新型Zn-2Cu-xSr(x=0、0.5、1 wt.%)合金体系,通过测算体外降解率以及分析体外生物相容性、体内促成骨能力和体内生物相容性,评估三元Zn-2Cu-xSr合金作为新型生物可降解植入材料的应用潜力。
1 材料与方法 1.1 材料纯Zn、Zn合金材料和商业级纯度钛(Ti),由哈尔滨理工大学金属研究所提供。Zn-2Cu、Zn-2Cu-0.5Sr、Zn-2Cu-1Sr合金的标称成分和实际成分分别为Zn 98 wt.%,Cu 2 wt.%,Sr 0 wt.%;Zn 97.5 wt.%,Cu 2 wt.%,Sr 0.5 wt.%;Zn 97 wt.%,Cu 2 wt.%,Sr:1 wt.%。
1.2 合金材料制备通过感应熔化法熔化高纯度的纯Zn(99.95%)、纯Cu(99.9%)和纯Sr(99.9%),制备Zn-2Cu、Zn-2Cu-0.5Sr、Zn-2Cu-1Sr合金铸锭。将纯Zn、纯Cu和纯Sr储存在阴凉、干燥和密封的环境中。将材料在700 ℃的石墨坩埚中熔化,采用钢模铸造,铸锭尺寸为长150 mm、高55 mm、厚30 mm。将纯Zn、Zn-2Cu合金、Zn-2Cu-0.5Sr合金、Zn-2Cu-1Sr合金和纯Ti锭分别加工成圆片(直径15 mm,厚度3 mm)和棒(直径1 mm,长3 mm),用于浸没实验、体外细胞实验以及动物实验。测试前,使用去离子水作为润滑剂,用砂纸对加工后的样品进行机械研磨,直至表面颗粒度达到2 000,然后分别在丙酮、乙醇(96%)和去离子水中超声清洗5 min,风干,备用。将准备好的合金样品放置在真空干燥器中,避免污染和氧化。
1.3 方法 1.3.1 材料体外降解率计算及pH检测通过人体液模拟培养基中pH的变化和降解率的改变,评估所有金属材料的体外降解行为。将人体液模拟培养基加入24孔培养板中,每孔中加入纯Zn、Zn-2Cu、Zn-2Cu-0.5Sr、Zn-2Cu-1Sr和纯Ti样品,在37 ℃、95%湿度、5%CO2和pH 7.4的生理条件下,在加湿培养箱中分别培养24和72 h。使用pH计(SevenExcellence S470,澳大利亚METTLER TOLERO公司)监测pH值。在培养箱中培养24和72 h后,从人体液模拟培养基中取出金属样本,用流动的去离子水冲洗,然后用含200 g/L铬酸、10 g/L硝酸钡和10 g/L银的混合物清洗。根据样本制备清洁处理和评估的操作标准(ASTM G1-03),在室温下用硝酸盐处理1 min,以去除表面的降解产物。将样品放置在实验台中室温干燥过夜。将清洁后的样品在电子天平上称重,精度为0.1 mg。估算培养基中样本的体外降解率(C),C =(M0-Mx)/ρAt。其中,M0为金属试样的初始质量,Mx为指定时间点浸泡清洗后的质量,ρ为材料密度,A为样品表面积,t为浸泡时间。实验重复进行3次。
1.3.2 材料浸提液制备根据ISO 10993标准,制备纯Zn、Zn-2Cu、Zn-2Cu-0.5Sr和Zn-2Cu-1Sr合金浸提液。将纯Zn、Zn-2Cu、Zn-2Cu-0.5Sr和Zn-2Cu-1Sr合金样品按1.25 mL/cm2的培养基与材料表面积比例,浸泡在DMEM(美国ThermoFisher Scientific公司)细胞培养基中,并在37 ℃、5%CO2细胞培养箱中共培养。24 h后收集合金浸提液,使用无菌过滤器过滤。将制备好的材料浸提液放置在4 ℃冰箱中保存,保存时间不超过72 h。
1.3.3 体外细胞相容性检测采用人骨髓间充质干细胞(上海泽叶生物科技有限公司)进行体外细胞毒性评价。在DMEM培养基中加入15%胎牛血清(美国ThermoFisher Scientific公司)和1%双抗与细胞共培养24 h,用胰酶将贴壁的人骨髓间充质干细胞从培养液中分离出来,使用细胞计数板计数。将密度为1×104/孔的人骨髓间充质干细胞接种于24孔培养板中,加入培养基,在37 ℃细胞培养箱中培养24 h,使细胞获得最佳黏附状态。24 h后用移液器吸取培养板中的培养基,更换为制备好的纯Zn、Zn-2Cu、Zn-2Cu-0.5Sr和Zn-2Cu-1Sr合金浸提液培养基(3孔/组),空白对照组更换为正常培养基,将更换完培养基的培养板置于37 ℃细胞培养箱中共培养72 h。细胞增殖情况可间接反映细胞的生物相容性,采用CCK-8细胞增殖试剂盒(上海碧云天生物技术股份有限公司)检测共培养72 h时各组细胞的增殖情况。使用鬼笔环肽(美国ThermoFisher Scientific公司)和DAPI(美国ThermoFisher Scientific公司)荧光染料对细胞骨架进行染色,并在激光共聚焦显微镜(FV4000,日本OLYMPUS公司)下观察细胞形态。
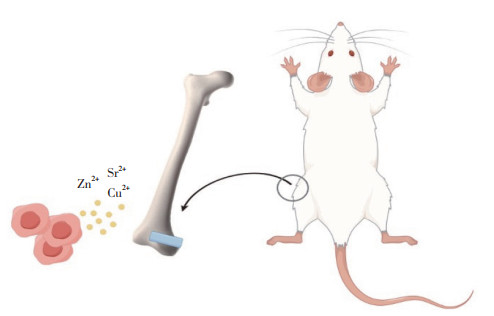
1.3.4 大鼠骨缺损模型建立24只SPF级SD大鼠(牡丹江医科大学动物实验中心提供),3月龄,体重202~228 g,平均体重(215±13)g。随机分成4组,分别为Zn组、Zn-2Cu组、Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组,每组6只。聚维酮碘消毒后,腹腔注射4%水合氯醛(0.9 mL/100 g)麻醉,确定穿刺点,在股骨内上髁最高点位置克氏针钻孔定位,沿水平方向钻直径1 mm的小孔,钻透双层皮质,将制备好的纯Zn、Zn-2Cu合金、Zn-2Cu-0.5Sr合金、Zn-2Cu-1Sr合金材料插入开大的骨髓腔(图 1)。骨蜡封闭伤口,无菌生理盐水冲洗,逐层缝合(未给予抗生素),术后在无菌、通风的房间饲养大鼠。本研究的动物实验经牡丹江医科大学实验动物福利与伦理委员会批准(20210828-16)。
|
| 图 1 动物实验示意图 Fig.1 Schematic diagram of animal experiment |
1.3.5 micro-CT检测骨小梁
植入材料5周后,使用CO2法处死大鼠。将大鼠置于可透视的密闭盒子中,以6.5 L/min的速度灌注CO2于盒子内,待大鼠不动、不呼吸、瞳孔放大,关闭CO2,观察2~3 min,确定大鼠死亡。取出股骨标本,评价材料促成骨能力。固定,进行mirco-CT扫描,检测骨小梁,评价材料促成骨能力。
1.3.6 体内生物相容性检测根据micro-CT的骨小梁检测结果,选取成骨效果最显著的Zn-2Cu-1Sr合金进行后续体内生物相容性实验。设立Zn-2Cu-1Sr组和空白对照组,每组3只大鼠。根据1.3.4的方法建立骨缺损大鼠模型,Zn-2Cu-1Sr组植入Zn-2Cu-1Sr合金材料,空白对照组不植入材料。手术8周后,采用1.3.5的方法处死大鼠,取出心、肝、肺、肾,组织固定和切片后进行HE染色。通过与空白对照组对比,判断Zn-2Cu-1Sr合金的体内生物相容性。
1.4 统计学分析采用SPSS 21.0软件进行统计分析,计量资料以x±s表示,3组间比较采用单因素方差分析,2组间比较采用t检验。计数资料用率(%)表示,采用χ2检验进行比较。P < 0.05为差异有统计学意义。
2 结果 2.1 体外降解率和pH检测结果培养24 h和72 h后,Zn组、Zn-2Cu组、Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组与Ti组比较,pH值均无统计学差异(P > 0.05);各组内24 h与72 h比较,pH值也无统计学差异(P > 0.05)。见表 1。
| Time point | Zn group | Zn-2Cu group | Zn-2Cu-0.5Sr group | Zn-2Cu-1Sr group | Ti group |
| 24 h | 6.87±0.02 | 6.94±0.02 | 6.91±0.02 | 6.95±0.02 | 6.90±0.05 |
| 72 h | 6.77±0.11 | 6.91±0.03 | 6.93±0.07 | 6.93±0.02 | 6.94±0.03 |
记录Zn合金材料在人体液模拟培养基中浸泡24和72 h的质量损失,得出材料降解率。24 h时,Zn-2Cu-0.5Sr组降解率显著低于Zn-2Cu组和Zn-2Cu-1Sr组(P < 0.01),Zn-2Cu组显著低于Zn-2Cu-1Sr组(P < 0.05)。72 h时,Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组降解率显著低于Zn-2Cu组(P < 0.01),而Zn-2Cu-0.5Sr组与Zn-2Cu-1Sr组比较,降解率无统计学差异(P > 0.05)。随着培养时间的增加,Zn-2Cu组、Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组中72 h与24 h相比,降解率均显著升高(P < 0.01)。见表 2。
| Time point | Zn-2Cu group | Zn-2Cu-0.5Sr group | Zn-2Cu-1Sr group |
| 24 h | 0.009 0±0.000 1 | 0.007 2±0.000 51) | 0.009 4±0.000 21),2) |
| 72 h | 0.016 8±0.000 73) | 0.012 1±0.001 11),3) | 0.012 9±0.000 81),3) |
| 1)P < 0.05 vs. Zn-2Cu group at the same time point;2)P < 0.05 vs. Zn-2Cu-0.5Sr group at the same time point;3)P < 0.05 vs. 24 h within group. | |||
2.2 体外细胞相容性
采用CCK-8实验测定各组材料浸提液在72 h的细胞增殖率。Zn组、Zn-2Cu组、Zn-2Cu-0.5Sr组、Zn-2Cu-1Sr组、空白对照组材料与细胞共培养72 h后,细胞增殖率分别为0.63±0.03、0.89±0.01、1.71±0.09、1.51±0.14和1.13±0.05。Zn-2Cu组、Zn-2Cu-0.5Sr组、Zn-2Cu-1Sr组和空白对照组细胞增殖率显著高于Zn组(P < 0.01),空白对照组细胞增殖率显著低于Zn-2Cu-0.5Sr组(P < 0.01)和Zn-2Cu-1Sr组(P < 0.05)。
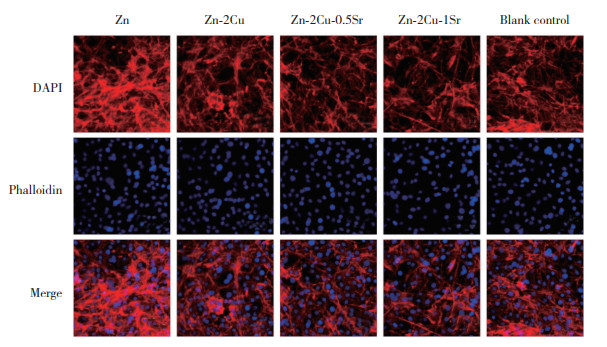
与CCK-8实验结果类似,细胞骨架荧光染色结果(图 2)显示,Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组细胞扩张形态良好,密度高于空白对照组。Zn-2Cu-0.5Sr组的延展状态最佳,说明在Zn-2Cu中加入Sr可以增加Zn合金的生物相容性。
|
| 图 2 细胞骨架荧光染色结果 ×200 Fig.2 Fluorescence staining of cytoskeleton ×200 |
2.3 材料促成骨能力
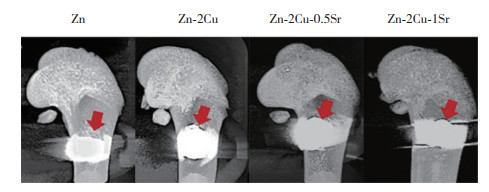
图 3为3D重建后的大鼠股骨及其中的材料,红色箭头为植入的Zn合金位置。Zn组、Zn-2Cu组、Zn-2Cu-0.5Sr组、Zn-2Cu-1Sr组骨矿物质密度分别为(1 225.33±34.70)、(2 551.33±134.79)、(2 833.67±46.14)和(3 104.00±19.97)mgHA/ccm。Zn-2Cu组、Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组骨矿物质密度显著高于Zn组(P < 0.05),Zn-2Cu-0.5Sr组骨矿物质密度显著高于Zn-2Cu组(P < 0.05),Zn-2Cu-1Sr组显著高于Zn-2Cu组和Zn-2Cu-0.5Sr组(P < 0.01)。
|
| 图 3 micro-CT三维重建观察Zn、Zn-2Cu、Zn-2Cu-0.5Sr和Zn-2Cu-1Sr在大鼠股骨内的植入情况 Fig.3 Implantation of Zn, Zn-2Cu, Zn-2Cu-0.5Sr, and Zn-2Cu-1Sr in rat femur observed by micro-CT three-dimensional reconstruction |
2.4 体内生物相容性
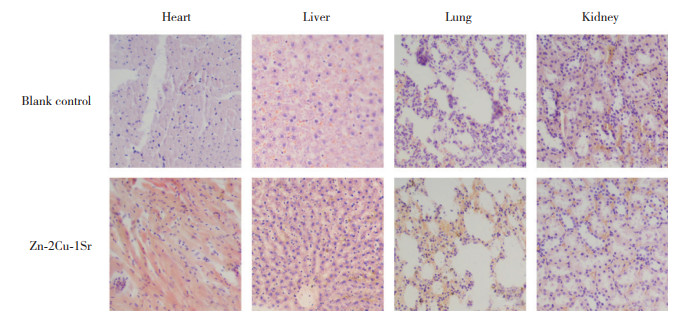
与空白组对照组相比,Zn-2Cu-1Sr组大鼠心脏、肝脏、肺和肾组织的HE染色结果(图 4)未见异常或病理形态,说明Zn-2Cu-1Sr合金具有较好的体内生物安全性。
|
| 图 4 空白对照组和Zn-2Cu-1Sr组大鼠重要脏器的HE染色结果 ×200 Fig.4 HE staining of the organs of the blank control and Zn-2Cu-1Sr group rats ×200 |
3 讨论
内固定术是最常见的骨折治疗方法之一。目前,临床上使用的内固定材料以Ti和镍钴合金为主,这类材料因为强度过大、容易形成应力遮挡从而导致骨折不愈合,限制了其在临床中的应用[11-12]。同时,Ti和镍钴合金材料不可降解,需要二次手术取出,增加了患者身体和经济的负担。众所周知,人体中水占体重的65%,液态环境可能会加重生物可降解材料周围的腐蚀环境,从而导致材料的降解率不可控制。Zn具有适中的电极电位,因此Zn合金材料具有优于Mg和Fe合金材料的基础降解率[2-5]。而且Mg、Fe合金材料在降解时会产生有毒产物,会使植入物周围的pH发生波动,从而影响周围骨细胞的生长[13]。
本研究发现,纯Zn及Zn合金在人体环境中具有很好的pH稳定性,这可能与Zn在降解时不会产生氢气有关。有研究[14]检测了一种超纯Zn微型管的降解率,发现超纯Zn材料的降解率为0.028~0.037 mm/年。有研究[14]报道Zn-1Mg、Zn-1Ca和Zn-1Sr合金在Hank’s液中的腐蚀情况,结果显示,Zn-1Mg、Zn-1Ca和Zn-1Sr合金在Hank’s液中的降解率为0.08~0.12 mm/年。本研究发现,在Zn-2Cu中加入微量的Sr,可以进一步调控降解率,随着Sr的加入,降解率呈先降低后增高的趋势。这种现象可能是由于Sr与Zn形成了SrZn13相,并在合金中弥散均匀分布,由于其腐蚀电位低于η-Zn相,在腐蚀过程中作为腐蚀阳极优先腐蚀,阻碍了η-Zn基体的腐蚀。因此,当Sr含量为0.5 wt.%时,SrZn13相的数量可能分布最均匀,这使得Zn-2Cu-0.5Sr合金降解率最低。当Sr含量增加至1 wt.%时,降解率又有所提高。这主要是随着Sr含量的增加,SrZn13相与基体相形成更多的微电池,加速了Zn合金的腐蚀。因此,在Zn-2Cu体系中加入适量的Sr,可以起到降低材料降解率的作用。
生物相容性是骨修复用内固定金属材料需要具备的重要特性,探索Zn及其合金的生物相容性对其最终植入人体具有重要意义。细胞增殖实验结果能在一定程度上反映材料的生物安全性。本研究发现,与Ti组相比,纯Zn组和Zn-2Cu组细胞增殖率受到一定程度的抑制,相反,Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组细胞增殖率远高于Ti组。与细胞增殖率实验结果相似,细胞骨架荧光染色结果显示,Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组细胞扩张形态良好,并且密度高于Ti组、纯Zn组和Zn-2Cu组。Zn-2Cu-0.5Sr组和Zn-2Cu-1Sr组展示出良好的生物相容性,主要是因为其降解率远低于Zn-2Cu,使得培养基中Zn离子和Cu离子浓度更适于细胞增殖。本课题组的前期研究[15]发现,微量的Sr有助于人骨髓间充质干细胞增殖。目前,尚未明确定义Cu离子在体外生物相容性中的作用,Cu离子可能促进成细胞生长,但这一机制还不明确。
体内模型是一种成本高昂但直接、有效的实验方法,可用于评估生物系统与植入材料间的相互作用,并为临床试验提供足够的依据。通过SD大鼠模型对材料进行体内评价,结果发现,在Zn材料中添加少量的Cu离子和Sr离子,有助于骨组织恢复。根据micro-CT测算骨矿物质密度,结果显示,Zn-2Cu-xSr(x=0、0.5、1 wt.%)组骨矿物质密度远高于纯Zn组,其中加入了Sr的材料组骨矿物质密度的增加较纯Zn组更明显,并且骨矿物质密度增加也随Sr含量的增加而增加,这与既往研究[12, 15]报道一致。对Zn-2Cu-1Sr组大鼠的重要脏器进行免疫组织化学染色,结果发现,植入物对体内重要脏器无毒性作用,与体外细胞相容性实验结果类似。
综上所述,本研究发现,通过合金化的方式将少量的Cu和Sr加入到Zn材料中,可以减缓Zn合金的降解率,同时加入了Cu和Sr的Zn合金材料其生物相容性有效提高,并且达到了促进骨骼修复的作用。Cu、Sr以及Zn材料在机体中的作用机制尚未完全了解,还需要进一步的研究探索。Zn材料作为未来新一代医用生物可降解材料,其应用前景极其广阔。
| [1] |
ZHANG Z, JIA B, YANG H, et al. Biodegradable ZnLiCa ternary alloys for critical-sized bone defect regeneration at load-bearing sites: in vitro and in vivo studies[J]. Bioact Mater, 2021, 6(11): 3999-4013. DOI:10.1016/j.bioactmat.2021.03.045 |
| [2] |
YUAN W, XIA D, WU S, et al. A review on current research status of the surface modification of Zn-based biodegradable metals[J]. Bioact Mater, 2021, 7: 192-216. DOI:10.1016/j.bioactmat.2021.05.018 |
| [3] |
YANG H, JIA B, ZHANG Z, et al. Alloying design of biodegradable zinc as promising bone implants for load-bearing applications[J]. Nat Commun, 2020, 11(1): 401. DOI:10.1038/s41467-019-14153-7 |
| [4] |
马小雯, 范明伟, 杜江. 锌指蛋白502在肺腺癌中的表达及作用机制[J]. 中国医科大学学报, 2023, 52(9): 798-804. DOI:10.12007/j.issn.0258-4646.2023.09.005 |
| [5] |
SHUAI C, XUE L, GAO C, et al. Rod-like eutectic structure in biodegradable Zn-Al-Sn alloy exhibiting enhanced mechanical strength[J]. ACS Biomater Sci Eng, 2020, 6(7): 3821-3831. DOI:10.1021/acsbiomaterials.0c00290 |
| [6] |
SHI ZZ, YU J, LIU XF, et al. Effects of Ag, Cu or Ca addition on microstructure and comprehensive properties of biodegradable Zn-0.8Mn alloy[J]. Mater Sci Eng C Mater Biol Appl, 2019, 99: 969-978. DOI:10.1016/j.msec.2019.02.044 |
| [7] |
QIAO W, PAN D, ZHENG Y, et al. Divalent metal cations stimulate skeleton interoception for new bone formation in mouse injury models[J]. Nat Commun, 2022, 13(1): 535. DOI:10.1038/s41467-022-28203-0 |
| [8] |
OKAZAKI Y, KATSUDA SI. Biological safety evaluation and surface modification of biocompatible Ti-15Zr-4Nb alloy[J]. Materials, 2021, 14(4): 731. DOI:10.3390/ma14040731 |
| [9] |
MOSTAED E, SIKORA-JASINSKA M, ARDAKANI MS, et al. Towards revealing key factors in mechanical instability of bioabsorbable Zn-based alloys for intended vascular stenting[J]. Acta Biomater, 2020, 105: 319-335. DOI:10.1016/j.actbio.2020.01.028 |
| [10] |
TANG ZB, HUANG H, NIU JL, et al. Design and characterizations of novel biodegradable Zn-Cu-Mg alloys for potential biodegradable implants[J]. Mater Des, 2017, 117: 84-94. DOI:10.1016/j.matdes.2016.12.075 |
| [11] |
LIN J, TONG X, SUN Q, et al. Biodegradable ternary Zn-3Ge-0.5X (X=Cu, Mg, and Fe) alloys for orthopedic applications[J]. Acta Biomater, 2020, 115: 432-446. DOI:10.1016/j.actbio.2020.08.033 |
| [12] |
HASIAK M, SOBIESZCZAŃSKA B, ŁASZCZ A, et al. Production, mechanical properties and biomedical characterization of ZrTi-based bulk metallic glasses in comparison with 316L stainless steel and Ti6Al4V alloy[J]. Materials, 2021, 15(1): 252. DOI:10.3390/ma15010252 |
| [13] |
WANG JL, XU JK, HOPKINS C, et al. Biodegradable magnesiumbased implants in orthopedics-a general review and perspectives[J]. Adv Sci, 2020, 7(8): 1902443. DOI:10.1002/advs.201902443 |
| [14] |
LIU Y, DU T, QIAO A, et al. Zinc-based biodegradable materials for orthopaedic internal fixation[J]. J Funct Biomater, 2022, 13(4): 164. DOI:10.3390/jfb13040164 |
| [15] |
GAO Z, SONG M, LIU RL, et al. Improving in vitro and in vivo antibacterial functionality of Mg alloys through micro-alloying with Sr and Ga[J]. Mater Sci Eng C Mater Biol Appl, 2019, 104: 109926. DOI:10.1016/j.msec.2019.109926 |
 2025, Vol. 54
2025, Vol. 54