文章信息
- 张久严, 时娟娟, 张丹
- ZHANG Jiuyan, SHI Juanjuan, ZHANG Dan
- 生化散瘕汤调控Fas/FasL信号通路对人工流产后大鼠子宫内膜损伤的影响
- Effect of Shenghua Sanjia decoction on endometrial damage after induced abortion in rats by regulating Fas/FasL signaling pathway
- 中国医科大学学报, 2025, 54(1): 30-37, 43
- Journal of China Medical University, 2025, 54(1): 30-37, 43
-
文章历史
- 收稿日期:2023-12-16
- 网络出版时间:2025-01-09 15:09:08
2. 滕州市中心人民医院妇一科, 山东 滕州 277599
2. Department of Gynecology, Tengzhou Central People's Hospital, Tengzhou 277599, China
近年来人工流产发生率呈现上升趋势[1]。临床上人工流产手段包括手术流产和药物流产2种。其中,药物流产相比于手术流产更容易获得且侵入性更小,可被绝大多数患者接受[2]。然而研究[3]显示,药物流产的安全性和有效性虽然有较大的保障,但依然可能出现不完全流产,导致出血时间延长、感染以及子宫变薄等并发症,从而严重损害子宫内膜,引发宫内粘连,甚至闭经和不孕。因此,有效修复损伤的子宫内膜是人工流产后医疗保健中的重要问题之一。目前,雌激素(estrogen,E2)治疗仍是临床上治疗子宫内膜损伤的最常用方法,但并不是对所有患者有效,且一些患者存在严重不良反应。因此,开发新的有效治疗人工流产后子宫内膜损伤的策略仍然很有必要[4]。
已有研究[5]表明,传统中医为促进人工流产后子宫内膜修复的治疗方法提供了新见解。生化散瘕汤由当归、熟地黄、川芎、益母草等12种中药材组成,与低剂量米非司酮联合使用能够促进药物流产后宫腔残留物排出,减少阴道流血时间,加快月经复潮,且不增加药物不良反应。另有报道[6]显示,生化散瘕汤中的主要药物组成当归、熟地黄和川芎是治疗子宫内膜损伤的中药复方中使用频次最多的3种中药,益母草、川牛膝使用频次也较高。目前,生化散瘕汤在人工流产后子宫内膜损伤修复中的作用及其机制尚不清楚。Fas/Fas配体(Fas ligand,FasL) 信号通路作为细胞凋亡途径之一,在子宫内膜细胞凋亡过程中起重要作用,并参与子宫内膜异位症的进展[7]。此外,抑制Fas/FasL信号通路激活能够降低氧化应激诱导的子宫内膜细胞凋亡,从而缓解氧化应激对子宫内膜细胞造成的不利影响[8]。本研究通过药物流产构建人工流产模型大鼠,并采用机械损伤法建立人工流产后子宫内膜损伤模型,探讨生化散瘕汤对大鼠人工流产后子宫内膜损伤以及Fas/FasL信号通路的影响,以期为生化散瘕汤应用于人工流产后子宫内膜损伤修复提供实验依据。
1 材料与方法 1.1 实验动物8周龄SPF级SD大鼠(雌60只,雄30只),体重(210±20) g,购自山东大学实验动物中心,实验动物生产许可证号为SCXK (鲁) 2019-0001。所有大鼠统一饲养于温度(23±1) ℃、相对湿度40%~50%、12 h光照/12 h黑暗的恒定环境下,自由进食与饮水。本研究获得滕州市中心人民医院伦理委员会批准(202212031)。
1.2 药物、试剂与仪器生化散瘕汤由当归24 g、益母草15 g、川芎9 g、鸡血藤15 g、炒桃仁6 g、蒲黄9 g、川牛膝9 g、炙黄芪15 g、熟地黄15 g、党参15 g、炮姜3 g、炙甘草3 g组成;所有中药材均购自滕州市中心人民医院。上述药材加500 mL蒸馏水浸泡40 min,先武火后文火煎煮30 min后滤出药液,药渣再加400 mL蒸馏水煎煮20 min,合并2次药液并浓缩至1.26 g/mL,于4 ℃冰箱中保存。米非司酮片、米索前列醇片(北京紫竹药业有限公司),地屈孕酮片(荷兰AbbottBiologicalsB.V.公司)。E2、孕激素(progesterone,P)、催乳素(prolactin,PRL) 酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA) 试剂盒(南京森贝伽生物科技有限公司),HE染色液(上海源叶生物科技有限公司),Masson三色染色试剂盒(北京索莱宝科技有限公司),原位末端转移酶标记法(TdT-mediated dUTP nick-end labeling,TUNEL) 凋亡检测试剂盒(美国Sigma-Aldrich公司),Trizol试剂(美国Invitrogen公司),反转录试剂盒、QuantiNova SYBR Green PCR试剂盒(德国QIAGEN公司),兔抗大鼠FasL抗体(上海雅吉生物科技有限公司),兔抗大鼠转化生长因子-β (transforming growth factor-β,TGF-β)、基质金属蛋白酶-9 (matrix metalloproteinase-9,MMP-9)、Fas、GAPDH抗体以及HRP标记羊抗兔IgG (英国abcam公司)。iMark酶标仪[伯乐生命医学产品(上海) 有限
公司],Nikon Eclipse Ci生物显微镜(日本Nikon公司),LightCycler 480实时定量PCR仪(瑞士Roche公司),WD-9413C凝胶成像分析系统(北京六一生物科技有限公司)。
1.3 动物造模、分组及给药所有大鼠适应性饲养7 d后,于下午5时按雌雄比2∶1合笼交配,次日上午8时对雌鼠进行阴道涂片检查,发现阴栓或大量精子表示受孕,记为妊娠第1天。将妊娠成功的50只大鼠随机分为正常对照组,模型组,低、高剂量生化散瘕汤组和地屈孕酮组,每组10只。
除正常对照组外,其余各组大鼠于妊娠第7天上午8时米非司酮(16.6 mg/kg) 灌胃,于下午6时米索前列醇(100 μg/kg) 灌胃,构建大鼠人工流产模型;在孕鼠阴道内置入1个消毒棉球,次日清晨收集阴道棉球,棉球上若见血迹表示人工流产大鼠模型造模成功[9]。第8天进行子宫内手术,用2.5%戊巴比妥钠腹腔注射麻醉大鼠,切开腹部,在子宫远端(靠近卵巢侧) 做1个小切口(长约0.2 cm),将内膜刮刀放入子宫内,沿子宫内壁反复刮擦内膜,直到子宫内膜变得粗糙,停止刮擦,缝合切口、关腹,建立人工流产后子宫内膜损伤大鼠模型[10]。造模成功次日,低、高剂量生化散瘕汤组分别灌胃给予生化散瘕汤(12.6 g/kg、25.2 g/kg;根据人和大鼠间等效剂量系数折算大鼠给药剂量,体重70 kg人的有效临床剂量约为2 g/kg,故大鼠等效剂量为2 g/kg×6.3=12.6 g/kg);地屈孕酮组灌胃给予地屈孕酮(3 mg/kg) [11];正常对
照组、模型组灌胃给予蒸馏水,灌胃体积均为20 mL/kg,1次/d,连续10 d。
1.4 样本采集给药结束后24 h内,腹腔注射1%戊巴比妥钠麻醉大鼠,腹主动脉取血,血液静置2 h后3 000 r/min离心15 min,分离血清,放入-20 ℃冰箱中保存。取血后处死大鼠,小心剥离子宫内膜,一部分组织放入4%多聚甲醛固定,剩余组织放入-80 ℃冰箱中保存。
1.5 检测方法 1.5.1 ELISA检测血清中E2、P、PRL含量取出冰箱中保存的血清,参照ELISA试剂盒说明书,使用酶标仪检测各孔标准品和血清吸光度(optical density,OD) 值,根据标准曲线计算血清中E2、P、PRL含量。
1.5.2 HE染色检测子宫内膜组织病理学改变子宫内膜组织于4%多聚甲醛固定24 h后进行石蜡包埋,并切成4 µm厚的切片。将切片脱蜡、水合后,于苏木素染液中染色5 min,1%氨水返蓝后0.5%伊红染液染色1 min,脱水、透明、封片后在显微镜下观察子宫内膜组织病理学改变并拍照。
1.5.3 Masson染色检测子宫内膜组织纤维化将子宫内膜组织石蜡切片脱蜡至水,依次进行Weigert铁苏木素染色8 min、Masson蓝化液返蓝4 min、丽春红品红染色8 min、苯胺蓝染色2 min、1%醋酸分化1 min等步骤,脱水、透明、封片后在显微镜下观察子宫内膜组织纤维化情况(胶原纤维呈蓝色) 并拍照。
1.5.4 TUNEL检测子宫内膜组织中细胞凋亡将子宫内膜组织石蜡切片脱蜡至水,依次添加蛋白酶K、3%H2O2进行孵育,随后TUNEL反应液37 ℃避光孵育1 h,Streptavidin-HRP工作液孵育20 min,DAB显色液显色,苏木素染核,脱水、透明、封片后在显微镜下观察染色细胞(凋亡细胞呈棕褐色) 并拍照,随机选取5个视野计数凋亡细胞,计算凋亡率。凋亡率(%) =凋亡细胞数/总细胞数×100。
1.5.5 实时定量PCR检测子宫内膜组织中雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)、催乳素受体(prolactin receptor,PRLR)、血管内皮生长因子(vascular endothelial growth factor,VEGF)、Fas、FasL mRNA表达取出冰箱中保存的部分子宫内膜组织,Trizol试剂提取组织中总RNA,参照反转录试剂盒说明将RNA反转录为cDNA,随后以cDNA为模板,并参照QuantiNova SYBR Green PCR试剂盒说明书配制实时定量PCR反应体系,置于实时定量PCR仪中进行扩增,获取循环阈值(Ct值)。引物由山东沃恩生物科技有限公司设计并合成,引物序列见表 1。以β-actin为内参基因,采用2-ΔΔCt法计算目的基因mRNA表达水平。
| Gene | Forward (5’-3’) | Reverse (5’-3’) |
| ER | TCTGGAGTGTGCCTGGTTGGA | GCGGAATCGACTTGACGTAGCC |
| PR | GACAACACAAAGCCCGACAC | CGGAAACCTGGCAGAGACTT |
| PRLR | TTACACGGGGCTCAGGAAAC | TTCAGGTTGGCCCCTTCTTC |
| VEGF | GCACTGGACCCTGGCTTTACT | ACTTCACCACTTCATGGGCTTTCTG |
| Fas | TGTCAACCGTGTCAGCTG | GTGCAAGGCTCAAGGAGT |
| FasL | AATGCCTGCATCATGAGCCA | AGTCTCAGCTTATCCATGA |
| β-actin | CCCGCGAGTACAACCTTCTTG | GTCATCCATGGCGAACTGGTG |
1.5.6 Western blotting检测子宫内膜组织中TGF-β、MMP-9、Fas、FasL蛋白表达
取出冰箱中保存的剩余部分子宫内膜组织,使用RIPA裂解液充分裂解后获取总蛋白,采用BCA法定量蛋白浓度并将蛋白煮沸变性,每泳道上样20 µg蛋白(20 µL) 进行SDS-PAGE电泳,通过电转移将切胶分离的蛋白转至PVDF膜,使用5%脱脂奶粉室温封闭膜1.5 h,添加一抗(TGF-β、MMP-9、Fas、FasL、GAPDH抗体,1∶1 000稀释) 4 ℃孵育过夜,PBST洗涤后添加二抗(HRP标记羊抗兔IgG,1∶5 000稀释),再次洗涤后添加化学发光试剂显色。ImageJ软件分析各蛋白条带灰度值,以GAPDH为内参蛋白计算目的蛋白的相对表达量。
1.6 统计学分析采用SPSS 25.0统计软件分析数据,结果以x±s表示,多组间比较采用单因素方差分析,组间比较采用SNK-q检验。P < 0.05为差异有统计学意义。
2 结果 2.1 生化散瘕汤对人工流产大鼠血清中E2、P、PRL含量的影响与正常对照组比较,模型组大鼠血清中E2、P、PRL含量降低(均P < 0.05)。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠血清中E2、P、PRL含量升高(均P < 0.05)。见表 2。
| Group | n | E2 (ng/L) | P (µg/L) | PRL (µg/L) |
| Normal control | 10 | 93.54±4.69 | 2.63±0.38 | 3.57±0.42 |
| Model | 10 | 49.89±3.871) | 1.27±0.191) | 1.94±0.261) |
| Low-dose Shenghua Sanjia decoction | 10 | 64.37±4.052) | 1.88±0.242) | 2.69±0.292) |
| High-dose Shenghua Sanjia decoction | 10 | 76.95±4.382) | 2.34±0.282) | 3.32±0.342) |
| Dydrogesterone | 10 | 78.62±4.162) | 2.41±0.312) | 3.38±0.402) |
| 1) P < 0.01 vs. normal control group;2) P < 0.01 vs. model group. | ||||
2.2 生化散瘕汤对人工流产大鼠子宫内膜组织病理学损伤的影响
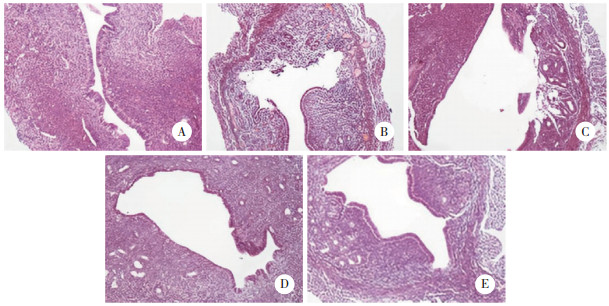
正常对照组大鼠子宫内膜组织结构完整,上皮细胞排列整齐,血管、腺体清晰。与正常对照组比较,模型组大鼠子宫内膜变薄,血管、腺体数量减少。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜厚度以及血管、腺体数量均有不同程度增加。另外,高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜组织病理学损伤改善程度较低剂量生化散瘕汤组更为明显。见图 1。
|
| A,normal control group;B,model group;C,low-dose Shenghua Sanjia decoction group;D,high-dose Shenghua Sanjia decoction group;E,dydrogesterone group. 图 1 生化散瘕汤对人工流产大鼠子宫内膜组织病理学损伤的影响HE×200 Fig.1 Effect of Shenghua Sanjia decoction on the histopathological damage of the endometrium in rats subjected to induced abortion HE×200 |
2.3 生化散瘕汤对人工流产大鼠子宫内膜组织纤维化的影响
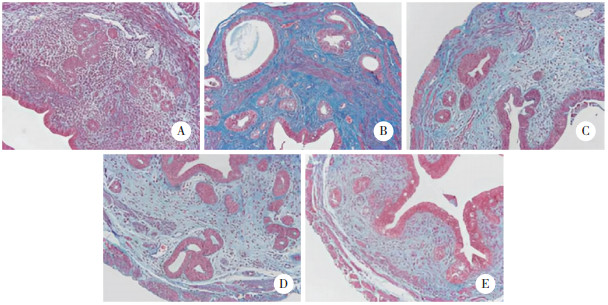
正常对照组大鼠子宫内膜形态、结构正常,呈蓝色染色的胶原纤维排列整齐。与正常对照组比较,模型组大鼠子宫内膜中胶原纤维增多。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜中胶原纤维均不同程度减少。
另外,高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜中胶原纤维较低剂量生化散瘕汤组减少。见图 2。
|
| A,normal control group;B,model group;C,low-dose Shenghua Sanjia decoction group;D,high-dose Shenghua Sanjia decoction group;E,dydrogesterone group. 图 2 生化散瘕汤对人工流产大鼠子宫内膜组织纤维化的影响Masson×200 Fig.2 Effect of Shenghua Sanjia decoction on endometrial tissue fibrosis in rats subjected to induced abortion Masson ×200 |
2.4 生化散瘕汤对人工流产大鼠子宫内膜组织中细胞凋亡的影响
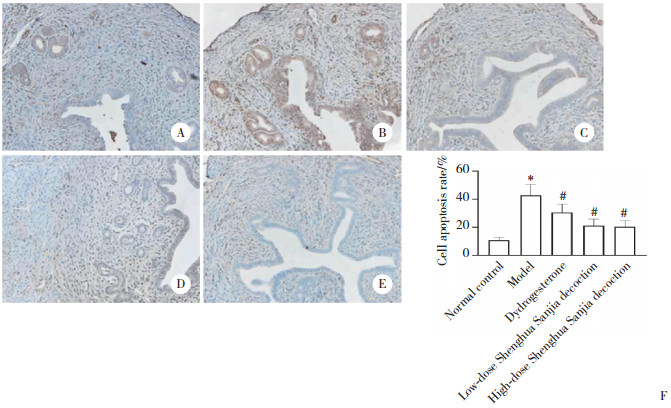
TUNEL检测结果显示,与正常对照组比较,模型组大鼠子宫内膜组织中细胞凋亡率升高(P < 0.05)。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜组织中细胞凋亡率降低(均P < 0.05)。见图 3。
|
| A,normal control group (×200);B,model group (×200);C,low-dose Shenghua Sanjia decoction group (×200);D,high-dose Shenghua Sanjia decoction group (×200);E,dydrogesterone group (×200);F,statistical results of cell apoptosis. *P < 0.01 vs. normal control group;#P < 0.01 vs. model group. 图 3 生化散瘕汤对人工流产大鼠子宫内膜组织中细胞凋亡的影响 Fig.3 Effect of Shenghua Sanjia decoction on endometrial tissue apoptosis in rats subjected to induced abortion |
2.5 生化散瘕汤对人工流产大鼠子宫内膜组织中ER、PR、PRLR、VEGF mRNA表达的影响
与正常对照组比较,模型组大鼠子宫内膜组织中ER、PR、PRLR、VEGF mRNA表达水平降低(均P < 0.05)。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜组织中ER、PR、PRLR、VEGF mRNA表达水平升高(均P < 0.05)。见表 3。
| Group | n | ER mRNA | PR mRNA | PRLR mRNA | VEGF mRNA |
| Normal control | 10 | 1.01±0.08 | 1.03±0.09 | 1.00±0.07 | 0.98±0.08 |
| Model | 10 | 0.64±0.061) | 0.68±0.081) | 0.52±0.061) | 0.61±0.071) |
| Low-dose Shenghua Sanjia decoction | 10 | 0.78±0.072) | 0.81±0.072) | 0.69±0.062) | 0.77±0.082) |
| High-dose Shenghua Sanjia decoction | 10 | 0.89±0.082) | 0.92±0.082) | 0.83±0.072) | 0.90±0.092) |
| Dydrogesterone | 10 | 0.93±0.072) | 0.94±0.092) | 0.85±0.072) | 0.91±0.082) |
| 1) P < 0.01 vs. normal control group;2) P < 0.01 vs. model group. | |||||
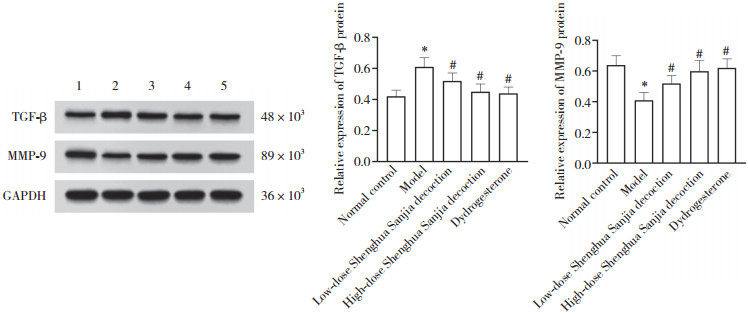
2.6 生化散瘕汤对人工流产大鼠子宫内膜组织中TGF-β、MMP-9蛋白表达的影响
与正常对照组比较,模型组大鼠子宫内膜组织中TGF-β蛋白表达水平升高,MMP-9蛋白表达水平降低(均P < 0.05)。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜组织中TGF-β蛋白表达水平降低,MMP-9蛋白表达水平升高(均P < 0.05)。见图 4。
|
| 1,normal control group;2,model group;3,low-dose Shenghua Sanjia decoction group;4,high-dose Shenghua Sanjia decoction group;5,dydrogesterone group. *P < 0.01 vs. normal control group;#P < 0.01 vs. model group. 图 4 生化散瘕汤对人工流产大鼠子宫内膜组织中TGF-β、MMP-9蛋白表达的影响 Fig.4 Effect of Shenghua Sanjia decoction on the protein expression of TGF-β and MMP-9 in the endometrial tissue of rats subjected to induced abortion |
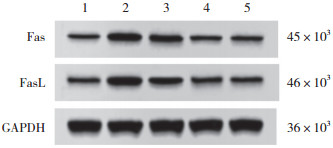
2.7生化散瘕汤对人工流产大鼠子宫内膜组织中Fas、FasL mRNA及蛋白表达的影响
与正常对照组比较,模型组大鼠子宫内膜组织中Fas、FasL mRNA及蛋白表达水平升高(均P < 0.05)。与模型组比较,低、高剂量生化散瘕汤组和地屈孕酮组大鼠子宫内膜组织中Fas、FasL mRNA及蛋白表达水平降低(均P < 0.05)。见表 4、图 5。
| Group | n | Fas | FasL | |||
| mRNA | Protein | mRNA | Protein | |||
| Normal control | 10 | 1.02±0.07 | 0.21±0.03 | 0.99±0.08 | 0.25±0.04 | |
| Model | 10 | 2.16±0.111) | 0.57±0.051) | 2.58±0.131) | 0.68±0.061) | |
| Low-dose Shenghua Sanjia decoction | 10 | 1.63±0.092) | 0.42±0.052) | 1.89±0.112) | 0.47±0.052) | |
| High-dose Shenghua Sanjia decoction | 10 | 1.21±0.082) | 0.30±0.042) | 1.32±0.122) | 0.32±0.052) | |
| Dydrogesterone | 10 | 1.15±0.092) | 0.26±0.032) | 1.25±0.112) | 0.29±0.042) | |
| 1) P < 0.01 vs. normal control group;2) P < 0.01 vs. model group. | ||||||
|
| 1,normal control group;2,model group;3,low-dose Shenghua Sanjia decoction group;4,high-dose Shenghua Sanjia decoction group;5,dydrogesterone group. 图 5 生化散瘕汤对人工流产大鼠子宫内膜组织中Fas、FasL蛋白表达的影响 Fig.5 Effect of Shenghua Sanjia decoction on the protein expression of Fas and FasL in the endometrial tissue of rats subjected to induced abortion |
3 讨论
药物流产(尤其米非司酮联合米索前列醇) 具有安全、简便、有效且不良反应少等优点,已成为早期妊娠终止的主要方式[12]。但同时药物流产也存在一些弊端与不足,如出血多、宫腔残留等,甚至可能损害生育能力;而且药物流产后引发的子宫内膜损伤仍是目前亟待解决的重要问题[13]。已有研究[14]表明,基于干细胞的治疗已经成为修复子宫内膜损伤的一种有利的替代方法,但至今仍未应用于人类,还需要进一步的临床试验,另外,干细胞治疗的安全性也是具有争议的话题。因此,积极寻找新的有效缓解人工流产后子宫内膜损伤的方法至关重要。
研究[10]证实,传统中医药在促进人工流产后子宫内膜修复中显示出一定优越性,其中人参、熟地黄、党参等15种中药材组成的滋肾育胎丸能够加速大鼠人工流产后子宫内膜的修复,并恢复生育能力。此外,已有临床研究[5]证实,相比于低剂量米非司酮单独治疗,生化散瘕汤与其联合可加快药物流产后宫腔残留包块吸收,临床效果好,患者满意度高。E2、P、PRL是维持女性正常内分泌的关键激素,可分别与靶细胞上对应的受体ER、PR、PRLR结合发挥作用,一旦其分泌异常可引发子宫内膜的一系列病理变化,且其水平增加有助于子宫内膜的恢复;VEGF是由血管内皮细胞产生的一种促血管生成因子,其高表达有利于加速子宫内膜再生[15-16]。本研究结果显示,模型大鼠血清中E2、P、PRL含量以及子宫内膜组织中ER、PR、PRLR、VEGF mRNA表达水平均降低,且HE染色可见子宫内膜变薄,且血管、腺体数量减少等病理改变。提示本研究构建的人工流产模型大鼠子宫内膜严重受损。经低、高剂量生化散瘕汤治疗后,人工流产大鼠血清中E2、P、PRL含量以及子宫内膜组织中ER、PR、PRLR、VEGF mRNA表达水平均升高,且子宫内膜组织病理学损伤均有所改善,表明生化散瘕汤可能通过调节性激素水平以及促进血管新生修复受损的子宫内膜,并与地屈孕酮作用效果一致。此外,时娟娟等[5]研究显示生化散瘕汤联合米非司酮治疗能够降低血VEGF水平,降低宫腔残留蜕膜或绒毛膜组织的生长及血管生成,促进残留物的脱落,与本研究结果不一致,分析原因可能是其研究纳入的患者为药物流产后宫腔残留患者,与本研究所构建人工流产模型大鼠的子宫内膜损伤所处阶段或严重程度不同。
人工流产后引起的子宫内膜损伤亦可导致子宫内膜纤维化,故阻断子宫内膜纤维化有利于子宫内膜修复。研究[17]显示,TGF-β高表达可导致子宫内膜纤维化,而MMP-9有助于减少纤维化,并参与子宫内膜组织重塑过程[18]。本研究结果显示,人工流产模型大鼠子宫内膜组织中胶原纤维增多,且MMP-9蛋白表达水平降低,TGF-β蛋白表达水平升高;而生化散瘕汤和地屈孕酮均能够减少人工流产大鼠子宫内膜组织中胶原纤维,促进MMP-9表达并抑制TGF-β表达。这表明人工流产大鼠子宫内膜组织存在纤维化,而生化散瘕汤可能通过调控MMP-9、TGF-β表达减轻大鼠人工流产后子宫内膜纤维化。LI等[10]研究也显示,滋肾育胎丸可降低大鼠流产后子宫内膜纤维化的严重程度。
细胞过度凋亡也是子宫内膜受损的重要表现之一。Fas/FasL信号通路是与子宫细胞凋亡密切相关的信号转导途径[19],且FasL上调可促进子宫内膜纤维化[20]。本研究结果显示,人工流产模型大鼠子宫内膜组织中细胞凋亡率以及Fas、FasL mRNA和蛋白表达水平均升高,提示人工流产大鼠子宫内膜组织中细胞凋亡严重,且Fas/FasL信号通路参与调控此细胞凋亡过程。进一步分析显示,生化散瘕汤和地屈孕酮均能够降低人工流产大鼠子宫内膜组织中细胞凋亡率,并抑制Fas、FasL mRNA和蛋白表达。表明生化散瘕汤可能通过抑制Fas/FasL信号通路激活,减轻大鼠人工流产后子宫内膜细胞凋亡和纤维化,促进子宫内膜修复。
综上所述,生化散瘕汤能够减轻大鼠人工流产后子宫内膜纤维化和细胞凋亡,促进子宫内膜修复,其机制可能与抑制Fas/FasL信号通路激活有关。本研究为生化散瘕汤在人工流产后子宫内膜修复中的应用提供了可能。在未来的研究中将对Fas/FasL信号通路进行干预来进一步验证生化散瘕汤在人工流产后子宫内膜修复中的作用机制。
| [1] |
WANG T, JIANG QB. Recent trend and correlates of induced abortion in China: evidence from the 2017 China Fertility Survey[J]. BMC Womens Health, 2022, 22(1): 469. DOI:10.1186/s12905-022-02074-5 |
| [2] |
MAZZA D, BURTON G, WILSON S, et al. Medical abortion[J]. Aust J Gen Pract, 2020, 49(6): 324-330. DOI:10.31128/ajgp-02-20-5223 |
| [3] |
DICKENS BM. Post-abortion care: ethical and legal duties[J]. Int J Gynaecol Obstet, 2019, 147(2): 273-278. DOI:10.1002/ijgo.12951 |
| [4] |
SHAO XW, AI GH, WANG L, et al. Adipose-derived stem cells transplantation improves endometrial injury repair[J]. Zygote, 2019, 27(6): 367-374. DOI:10.1017/S096719941900042X |
| [5] |
时娟娟, 张丹, 张久严, 等. 生化散瘕汤联合米非司酮治疗药物流产术后宫腔残留的临床疗效研究[J]. 国际医药卫生导报, 2022, 28(13): 1825-1829. DOI:10.3760/cma.j.issn.1007-1245.2022.13.010 |
| [6] |
张云, 艾浩, 薛晓鸥, 等. 基于现代文献探析治疗子宫内膜损伤的中药复方用药规律分析[J]. 中医药信息, 2017, 34(5): 84-87. DOI:10.3969/j.issn.1002-2406.2017.05.024 |
| [7] |
AKHAVAN SALES Z, TAHOORI MT, SHEIKHHA MH, et al. Identification of a FAS/FASL haplotype associated with endometriosis in Iranian patients[J]. Gynecol Endocrinol, 2020, 36(3): 261-264. DOI:10.1080/09513590.2019.1655729 |
| [8] |
靳青, 张相伦, 魏晨, 等. 氧化应激通过Fas/FasL信号通路调控奶牛子宫内膜细胞凋亡[J]. 畜牧兽医学报, 2022, 53(6): 1819-1828. DOI:10.11843/j.issn.0366-6964.2022.06.015 |
| [9] |
马静静, 刘宇, 梁艳, 等. 益母草总生物碱对药物流产大鼠蜕膜绒毛组织排出的促进作用及其机制[J]. 吉林大学学报(医学版), 2021, 47(6): 1476-1484. DOI:10.13481/j.1671-587X.20210618 |
| [10] |
LI MM, NING N, LIU Y, et al. The potential of Zishen Yutai pills to facilitate endometrial recovery and restore fertility after induced abortion in rats[J]. Pharm Biol, 2021, 59(1): 1505-1516. DOI:10.1080/13880209.2021.1993272 |
| [11] |
WU HW, FENG YH, WANG DY, et al. Effect of total flavones from Cuscuta chinensis on anti-abortion via the MAPK signaling pathway[J]. Evid Based Complement Alternat Med, 2018, 2018: 6356190. DOI:10.1155/2018/6356190 |
| [12] |
KAPP N, ECKERSBERER E, LAVELANET A, et al. Medical abortion in the late first trimester: a systematic review[J]. Contraception, 2019, 99(2): 77-86. DOI:10.1016/j.contraception.2018.11.002 |
| [13] |
KAPP N, LOHR PA. Modern methods to induce abortion: safety, efficacy and choice[J]. Best Pract Res Clin Obstet Gynaecol, 2020, 63: 37-44. DOI:10.1016/j.bpobgyn.2019.11.008 |
| [14] |
LU XY, CUI JJ, CUI LL, et al. The effects of human umbilical cord-derived mesenchymal stem cell transplantation on endometrial receptivity are associated with Th1/Th2 balance change and uNK cell expression of uterine in autoimmune premature ovarian failure mice[J]. Stem Cell Res Ther, 2019, 10(1): 214. DOI:10.1186/s13287-019-1313-y |
| [15] |
LI YQ, LI WL, YU XH, et al. Mechanisms of traditional Chinese medicine Bushenantai granules in promoting angiogenesis at the maternal-fetal interface of recurrent spontaneous abortion mice[J]. J Tradit Chin Med, 2021, 41(4): 556-563. DOI:10.19852/j.cnki.jtcm.20210319.001 |
| [16] |
YAMAGUCHI M, ERDENEBAATAR C, SAITO F, et al. Prolactin enhances the proliferation of proliferative endometrial glandular cells and endometrial cancer cells[J]. J Endocr Soc, 2019, 4(2): bvz029. DOI:10.1210/jendso/bvz029 |
| [17] |
ZHANG ZH, LI S, DENG J, et al. Aspirin inhibits endometrial fibrosis by suppressing the TGF-β1-Smad2/Smad3 pathway in intrauterine adhesions[J]. Int J Mol Med, 2020, 45(5): 1351-1360. DOI:10.3892/ijmm.2020.4506 |
| [18] |
LI CQ, WANG WY, SUN SY, et al. Expression and potential role of MMP-9 in intrauterine adhesion[J]. Mediators Inflamm, 2021, 2021: 6676510. DOI:10.1155/2021/6676510 |
| [19] |
ZHANG Y, ZHANG LC, BAO JL, et al. Perfluorooctanoic acid exposure in early pregnancy induces oxidative stress in mice uterus and liver[J]. Environ Sci Pollut Res Int, 2021, 28(46): 66355-66365. DOI:10.1007/s11356-021-15453-6 |
| [20] |
AI Y, CHEN MQ, LIU J, et al. lncRNA TUG1 promotes endometrial fibrosis and inflammation by sponging miR-590-5p to regulate Fasl in intrauterine adhesions[J]. Int Immunopharmacol, 2020, 86: 106703. DOI:10.1016/j.intimp.2020.106703 |
 2025, Vol. 54
2025, Vol. 54