文章信息
- 满超, 王岩松
- MAN Chao, WANG Yansong
- 淫羊藿苷对糖尿病大鼠骨质疏松症的作用及其机制
- Effects and mechanism on icariin for osteoporosis in diabetic rats
- 中国医科大学学报, 2025, 54(1): 12-17, 23
- Journal of China Medical University, 2025, 54(1): 12-17, 23
-
文章历史
- 收稿日期:2023-12-06
- 网络出版时间:2025-01-09 15:02:26
2. 锦州医科大学附属第一医院骨外科, 辽宁 锦州 121001
2. Department of Orthopedics, The First Affiliated Hospital of Jinzhou Medical University, Jinzhou 121001, China
研究[1-3]显示,糖尿病(diabetes mellitus,DM) 发病率逐年增高,糖尿病性骨质疏松症(diabetic osteoporosis,DOP) 是DM的并发症之一。DM患者由于受损的骨量和骨外因素导致骨折风险增加[4-5],而具体作用机制尚未明确。目前DOP尚无有效的治疗方法。雌激素受体(estrogen receptor,ER) 属于核内受体,和其他的类固醇激素受体相似,有雌激素结合域、DNA结合域及转录激活域,属于转录因子核受体超家族成员[6]。研究[7]显示,基因多态性与绝经后骨质疏松症有关,但ER1在DOP中的作用机制尚不清楚。
淫羊藿苷是从淫羊藿属植物中分离出的活性成分。淫羊藿苷已被用于骨折和骨质疏松症的防治研究[8]。研究[9]表明,体内淫羊藿苷处理显著降低了链脲佐菌素(streptozotocin,STZ) 诱导Wistar大鼠的骨吸收;在体外以剂量依赖方式抑制高糖诱导的大鼠破骨细胞生成。淫羊藿苷能够促进MC3T3-E1细胞的分化和矿化,激活Runx2启动子和Wnt/β-catenin通路对成骨细胞分化[10]。然而,淫羊藿苷对DOP的保护作用尚不清楚。本研究探讨淫羊藿苷对DOP的作用及其机制,旨在为DOP的防治提供新思路。
1 材料与方法 1.1 实验动物50只SPF级6周龄雄性SD大鼠,体重(220±20) g,购自锦州医科大学实验动物中心,许可证编号为SYXK [辽] 2019-0007。将大鼠置于22~24 ℃、湿度55%~60%环境中饲养,12 h光/12 h暗循环,自由取食、饮水,适应性培养1周后进行实验。本研究获得锦州医科大学实验动物伦理委员会批准(20220622198)。
1.2 主要试剂和仪器STZ购自美国Sigma公司,淫羊藿苷购自中国Selleck公司,ER1、PDE5A和β-cantenin抗体购自英国abcam公司,Wnt抗体购自中国Proteintech公司,HE试剂盒和Western blotting二抗购自中国Solarbio公司,RIPA裂解液、BCA试剂盒购自中国Beyotime公司,ELISA试剂盒购自中国MLBIO公司。倒置显微镜购自日本Olympus公司,水平电泳仪购自美国BIO-RAD公司。
1.3 方法 1.3.1 DM大鼠骨质疏松症模型的建立及分组大鼠饲养1周后,禁食水2 h,采用单次腹腔注射STZ (50 mg/kg) 制备DM模型。72 h后血糖≥16.7 mmol/L为DM模型建立成功。
大鼠随机分为5组:对照组(Control组,无任何处理)、STZ组(构建DM大鼠模型)、低剂量淫羊藿苷组[DM模型大鼠构建成功4周后,50 mg/ (kg·d) 淫羊藿苷灌胃,连续8周]、高剂量淫羊藿苷组[DM大鼠模型构建成功4周后,100 mg/ (kg·d) 淫羊藿苷灌胃,连续8周[4]]、高剂量淫羊藿苷+ER1-siRNA组[DM大鼠模型构建成功4周后,100 mg/ (kg·d) 淫羊藿苷灌胃,连续8周;10 μL ER1-siRNA尾静脉注射,1次/4周,共2次],每组10只。给药8周后取材用于后续实验。
1.3.2 siRNA设计及构建利用美国Invitrogen公司siRNA软件设计大鼠ER1 mRNA的siRNA,靶向特异性干扰片段ER1-siRNA和si-RNA阴性对照(si-NC) 干扰片段由上海吉凯基因化学技术有限公司完成。ER1-siRNA引物序列见表 1。
| Gene | Primer sequence |
| ER1-siRNA | 5’-GAGGGAGAAUGUUGAAACATT-3’ |
| 5’-UGUUUCAACAUUCUCCCUCTT-3’ | |
| ER1-siRNA-NC | 5’-GGCUACGUCCAGGAGCGCACC-3’ |
| 5’-UGCGCUCCUGGACGUAGCCUU-3’ |
1.3.3 股骨组织病理形态学检测
各组大鼠股骨组织石蜡切片脱水后PBS清洗3遍,苏木素染色5 min。分化30 s后伊红染色2 min,然后清洗5 min。乙醇和二甲苯溶液脱水透明,中性树胶封片。
1.3.4 酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA) 检测血清碱性磷酸酶(alkaline phosphatase,ALP)、抗酒石酸酸性磷酸酶(tartrate resistant acid phosphatase,TRAP) 水平和血钙浓度各组大鼠心脏取血,于4 ℃、12 000 r/min离心20 min,取上层清澈血清,按照ELISA试剂盒说明书操作,10 μL标准品、阴性对照、阳性对照和待测样本加入孔板,加液后37 ℃水浴60 min。A液B液混匀后反应15 min,然后加终止液检测吸光度(optical density,OD)值。
1.3.5 淫羊藿苷蛋白质-蛋白质相互作用(protein-protein interaction,PPI) 网络分析及核心靶点预测利用STITCH数据库(http://stitch.embl.de/ ),以“Homo sapiens”为物种划分,筛选出淫羊藿苷可能的作用靶点,分析核心靶点的相互作用关系。
1.3.6 分子对接验证淫羊藿苷三维结构来源于PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/),结合PDB数据库(https://www.rcsb.org/) 中核心靶点的蛋白质结构,利用Autodock Vina对淫羊藿苷与核心靶点进行分子对接验证;同时验证淫羊藿苷对相关蛋白表达的影响。
1.3.7 免疫组织化学检测大鼠股骨组织中ER1表达石蜡切片脱蜡至水后,高压修复2 min。恢复室温后3% H2O2避光反应10 min,PBS清洗,封闭30 min,一抗4 ℃孵育过夜。次日二抗孵育1 h,PBS清洗,DAB显色并苏木素复染,梯度乙醇和二甲苯脱水透明,中性树胶封片,晾干后在倒置荧光显微镜下观察。
1.3.8 Western blotting检测大鼠股骨组织中ER1、PDE5A、Wnt和β-cantenin蛋白表达各组取新鲜股骨组织加入裂解液,超声破碎仪打碎后收集上清,于4 ℃、12 000 r/min离心25 min,提取上清液。使用BCA试剂盒检测蛋白含量,根据蛋白含量配置分离胶、浓缩胶,制备SDS-PAGE凝胶。加样后80 V 30 min电泳,然后改为120 V 60 min电泳,电泳结束后按照0.25 A 90 min进行转膜。转膜结束后用TBST配制5%脱脂牛奶封闭2 h。按照抗ER1抗体(1∶1 000)、抗PDE5A抗体(1∶2 000)、抗Wnt抗体(1∶1 000)、抗β-cantenin抗体(1∶4 000) 和内参GAPDH (1∶4 000) 稀释一抗,并将PVDF膜按照目标分子量裁切后分别放入对应抗体中,4 ℃孵育过夜。二抗(1∶4 000) 室温孵育2 h,ECL显影,然后利用ImageJ软件进行分析。
1.4 统计学分析利用SPSS 20.0软件进行统计分析,符合正态分布的计量资料采用x±s表示,组间比较采用单因素方差分析;方差齐时采用SNK-q检验,方差不齐时采用Games-Howell法进行两两比较,P < 0.05为差异有统计学意义。
2 结果 2.1 各组大鼠血糖和体重比较结果显示,与Control组比较,STZ组大鼠血糖升高,体重降低(均P < 0.01)。与STZ组比较,低剂量、高剂量淫羊藿苷组大鼠血糖降低(P < 0.01),但体重比较差异无统计学意义(P > 0.05),见表 2。
| Group | n | Blood glucose (mmol/L) | Body weight (g) | |||
| Before STZ administration | 12 weeks after STZ administration | Before STZ administration | 12 weeks after STZ administration | |||
| Control group | 5 | 4.67±0.30 | 4.75±0.39 | 212.00±12.85 | 364.80±9.05 | |
| STZ group | 5 | 4.58±0.39 | 26.16±2.381) | 200.20±13.70 | 304.40±21.531) | |
| Low-dose icariin group | 5 | 4.53±0.37 | 23.38±1.942) | 216.60±8.14 | 291.80±13.00 | |
| High-dose icariin group | 5 | 4.72±0.34 | 20.73±2.182) | 206.50±18.88 | 295.50±25.01 | |
| 1) P < 0.01 vs. control group;2) P < 0.01 vs. STZ group. | ||||||
2.2 各组大鼠股骨组织HE染色结果比较
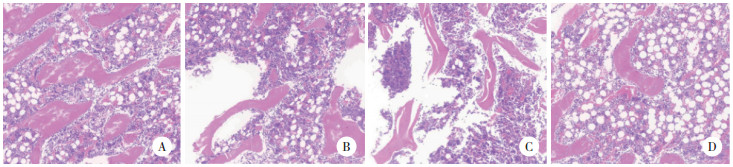
结果显示,Control组大鼠骨膜下及股骨组织表面分布扁平成骨细胞,软骨下区骨小梁稍厚、交织成网,成骨细胞分布均匀。与Control组比较,STZ组大鼠股骨表面成骨细胞显著减少,骨细胞扁平,软骨下区骨细胞核固缩,空骨陷窝明显增多。与STZ组比较,低剂量、高剂量淫羊藿苷组骨小梁增厚、部分交织成网,成骨细胞分布较均匀,见图 1。
|
| A,Control group;B,STZ group;C,low-dose icariin group;D,high-dose icariin group. 图 1 各组大鼠股骨组织病理形态学改变HE×200 Fig.1 The pathological morphology of femoral tissue of rats in each group HE×200 |
2.3 各组大鼠血清ALP、TRAP水平和血钙浓度比较
与Control组比较,STZ组大鼠ALP水平和血钙浓度下降,TRAP水平升高(均P < 0.01)。与STZ组比较,低剂量、高剂量淫羊藿苷组大鼠ALP水平和血钙浓度升高,TRAP水平降低(均P < 0.01),见表 3。
| Group | n | Serum ALP | Serum TRAP | Blood calcium concentration |
| Control group | 5 | 2 952.75±22.45 | 53.73±1.94 | 1.22±0.07 |
| STZ group | 5 | 2 458.49±15.661) | 74.21±1.381) | 0.85±0.011) |
| Low-dose icariin group | 5 | 2 647.49±9.952) | 67.07±1.012) | 0.93±0.022) |
| High-dose icariin group | 5 | 2 864.31±7.082) | 57.64±0.802) | 1.04±0.022) |
| 1) P < 0.01 vs. Control group;2) P < 0.01 vs. STZ group. | ||||
2.4 淫羊藿苷治疗DOP核心靶点的筛选及分子对接验证
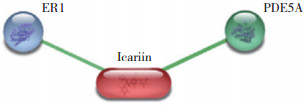
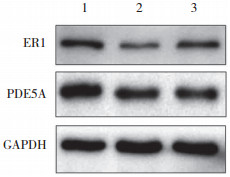
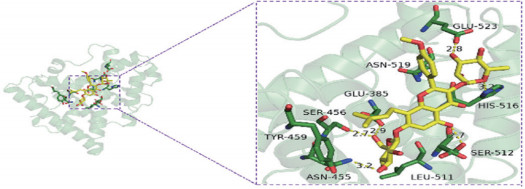
PPI网络分析筛选出淫羊藿苷相关的2个核心靶点:ER1和PDE5A,见图 2。Western blotting检测验证淫羊藿苷对ER1和PDE5A表达的影响。结果显示,与对照组比较,STZ组ER1和PDE5A表达降低(P < 0.01);与STZ组比较,高剂量淫羊藿苷组ER1表达上调(P < 0.01),而PDE5A表达的差异无统计学意义(P > 0.05),见图 3、表 4。分子对接验证结果显示,淫羊藿苷可以通过GLU-523、ASN-519、GLU-385、SER-456、HIS-516、TYR-459、SER-512、ASN-455和LEU-511氨基酸残基稳定结合到ER1蛋白结构上,表明ER1可能是淫羊藿苷在DOP中的潜在靶点,见图 4。
|
| 图 2 淫羊藿苷的PPI网络分析 Fig.2 PPI network analysis of icariin |
|
| 1,control group;2,STZ group;3,high-dose icariin group. 图 3 各组大鼠ER1和PDE5A蛋白表达 Fig.3 Protein expression of ER1 and PDE5A in rats in each group |
| Group | n | ER1 protein | PDE5A protein |
| Control group | 3 | 83.14±1.66 | 114.22±3.46 |
| STZ group | 3 | 44.82±2.131) | 75.35±1.361) |
| High-dose icariin group | 3 | 63.83±1.062) | 73.57±0.82 |
| 1) P < 0.01 vs. Control group;2) P < 0.01 vs. STZ group. | |||
|
| 图 4 淫羊藿苷与ER1的分子对接 Fig.4 Molecular docking between icariin and ER1 |
2.5 各组大鼠ER1表达比较
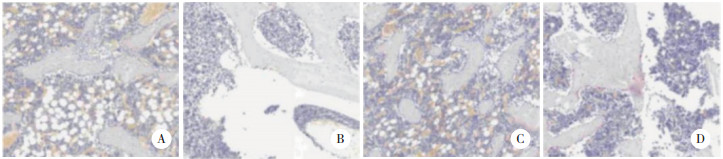
免疫组织化学结果显示,与Control组,STZ组股骨组织中ER1表达减少;与STZ组比较,高剂量淫羊藿苷组ER1表达明显增多;与高剂量淫羊藿苷组比较,高剂量淫羊藿苷+ER1-siRNA组ER1表达减少,见图 5。
|
| A,Control group;B,STZ group;C,high-dose icariin group;D,high-dose icariin+ER1-siRNA group. 图 5 免疫组织化学检测各组大鼠股骨组织ER1表达 ×200 Fig.5 ER1 expression in bone tissue of rats in each group by immunohistochemistry ×200 |
2.6 Western blotting检测各组大鼠ER1、Wnt和β-cantenin蛋白表达
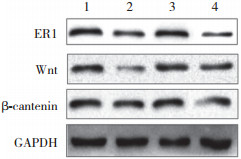
结果显示,与Control组比较,STZ组大鼠ER1、Wnt和β-cantenin表达降低(均P < 0.01)。与STZ组比较,高剂量淫羊藿苷组大鼠ER1、Wnt和β-cantenin表达升高(均P < 0.01)。与高剂量淫羊藿苷组比较,高剂量淫羊藿苷+ER1-siRNA组大鼠ER1、Wnt和β-cantenin表达降低,说明淫羊藿苷的保护作用被逆转,见图 6、表 5。
|
| 1,Control group;2,STZ group;3,high-dose icariin group;4,high-dose icariin+ER1-siRNA group. 图 6 各组大鼠ER1、Wnt和β-cantenin蛋白表达 Fig.6 Protein expression of ER1, Wnt and β-cantenin in rats in each group |
| Group | n | ER1 protein | Wnt protein | β-cantenin protein |
| Control group | 3 | 83.62±1.34 | 72.59±1.08 | 83.12±2.06 |
| STZ group | 3 | 45.28±1.091) | 28.74±0.861) | 51.82±1.781) |
| High-dose icarrin group | 3 | 65.01±0.822) | 65.68±0.742) | 74.11±1.372) |
| High-dose icarrin+ER1-siRNA group | 3 | 42.08±0.943) | 39.72±0.713) | 45.03±1.243) |
| 1) P < 0.01 vs. control group;2) P < 0.01 vs. STZ group;3) P < 0.01 vs. high-dose icarrin group. | ||||
3 讨论
DOP导致骨脆性和骨折风险增加[11-12]。DM患者的高血糖状态可以影响人体正常的骨转换和骨完整性,DM患者的骨质流失及骨转换速度都较正常人增加[13-14]。研究[15]显示,淫羊藿苷对去卵巢大鼠有骨保护作用。本研究结果显示,与Control组比较,STZ组大鼠血糖升高,体重减轻,股骨表面成骨细胞软骨下区骨细胞核固缩,ALP和血钙浓度降低,TRAP升高,表明DOP大鼠模型构建成功。淫羊藿苷治疗后,上述指标均显著改善,说明淫羊藿苷对DOP大鼠具有保护作用。持续高血糖可抑制成骨细胞增殖,促进破骨细胞分化,目前,已有研究[16]认为骨髓中葡萄糖可引起破骨细胞分化增加,这可能是DOP的发病机制之一。本研究结果显示,给药8周后与STZ组比较,高剂量淫羊藿苷组血糖显著降低,表明淫羊藿苷的降糖作用可能是减轻DM所致骨质损伤的重要机制之一。
淫羊藿苷是一种传统中药,可用于减轻炎症和恢复成骨的形成[17]。既往研究[18]表明淫羊藿苷是治疗骨代谢相关疾病的有效药物。淫羊藿苷还能刺激骨髓间充质干细胞或长骨源性细胞的成骨分化,促进骨愈合,预防骨质疏松症,改善股骨头坏死。淫羊藿苷通过抑制骨吸收、提高峰值骨密度和骨质量促进骨形成,对预防不同原因引起的骨质疏松及骨折具有重要意义[9]。
本研究结果显示,与Control组比较,STZ组大鼠股骨表面成骨细胞减少,空骨陷窝明显增多,ALP和血钙浓度水平下降,TRAP水平升高(均P < 0.01)。与STZ组比较,低、高剂量淫羊藿苷组空骨陷窝减少,ALP和血钙浓度水平升高,TRAP水平降低(均P < 0.01),表明淫羊藿苷能有效改善DOP的病理改变。
已有研究[19]显示ER1基因多态性与骨质疏松症风险相关。本研究核心靶点筛选和分子对接结果发现,淫羊藿苷可以通过GLU-523、ASN-519、GLU-385、SER-456、HIS-516、TYR-459、SER-512、ASN-455和LEU-511氨基酸残基稳定地结合到ER1蛋白结构上。Western blotting检测结果显示,STZ组ER1、Wnt和β-cantenin表达水平较Control组降低,淫羊藿苷治疗后ER1、Wnt和β-cantenin表达上调。而在淫羊藿苷治疗基础上给予ER1-siRNA干扰后,ER1、Wnt和β-cantenin表达减少,淫羊藿苷的保护作用被逆转,表明淫羊藿苷可能通过ER1调节Wnt/β-cantenin信号通路减轻DOP。
综上所述,淫羊藿苷可以降低DM大鼠血糖、提高血清ALP水平和血钙浓度、降低TRAP水平,对DM大鼠骨质疏松症具有保护作用;其机制可能与激活ER1介导的Wnt/β-cantenin信号通路有关。淫羊藿苷可能是治疗DOP的潜在药物。本研究不足之处在于缺少体外实验,今后将进一步探究淫羊藿苷对DOP大鼠的保护机制。
| [1] |
SRIVASTAVA RK, SAPRA L, BHARDWAJ A, et al. Unravelling the immunobiology of innate lymphoid cells (ILCs): implications in health and disease[J]. Cytokine Growth Factor Rev, 2023, 74: 56-75. DOI:10.1016/j.cytogfr.2023.09.002 |
| [2] |
KALRA S, JOSHI A, KAPOOR N. Osteoporosis and diabetes: the dual pandemics[J]. J Pak Med Assoc, 2022, 72(8): 1663-1664. DOI:10.47391/JPMA.22-86 |
| [3] |
ZHANG Y, JIA SY, WEN GC, et al. Zoledronate promotes peri- implant osteogenesis in diabetic osteoporosis by the AMPK pathway[J]. Calcif Tissue Int, 2023, 113(3): 329-343. DOI:10.1007/s00223-023-01112-0 |
| [4] |
QI SS, HE J, ZHENG HX, et al. Icariin prevents diabetes-induced bone loss in rats by reducing blood glucose and suppressing bone turnover[J]. Molecules, 2019, 24(10): 1871. DOI:10.3390/molecules24101871 |
| [5] |
侯甜, 秦雅芝, 张妍, 等. 唑来膦酸盐通过p38 MAPK信号通路调控高糖微环境下成骨细胞分化[J]. 天津医药, 2022, 50(12): 1239-1245. DOI:10.11958/20220368 |
| [6] |
ZHANG JF, GAI JL, MA HQ, et al. Understanding the molecular mechanism of Ginkgo Folium-Forsythiae Fructus for cerebral athe- rosclerosis treatment using network pharmacology and molecular docking[J]. Medicine, 2023, 102(7): e32823. DOI:10.1097/MD.0000000000032823 |
| [7] |
陈娟, 郭凯, 李惠莉, 等. 雌激素受体基因多态性与雷洛昔芬对绝经后女性骨质疏松症疗效的关系[J]. 中国现代医生, 2019, 57(23): 8-10, 14. |
| [8] |
CHANG H, LV SJ, YUAN TT, et al. Identification and analysis of chemical constituents and rat serum metabolites in gushuling using UPLC-Q-TOF/MS coupled with novel informatics UNIFI platform[J]. Evid Based Complement Alternat Med, 2021, 2021: 2894306. DOI:10.1155/2021/2894306 |
| [9] |
CHU SF, LIU DL, ZHAO HX, et al. Effects and mechanism of Zishen Jiangtang pill on diabetic osteoporosis rats based on proteomic analysis[J]. Evid Based Complementary Altern Med, 2021, 2021: 7383062. DOI:10.1155/2021/7383062 |
| [10] |
LIU YJ, HUANG LL, HAO BH, et al. Use of an osteoblast overload damage model to probe the effect of icarrin on the proliferation, differentiation and mineralization of MC3T3-E1 cells through the Wnt/β-catenin signalling pathway[J]. Cell Physiol Biochem, 2017, 41(4): 1605-1615. DOI:10.1159/000470896 |
| [11] |
MOHSIN S, BANIYAS MM, ALDARMAKI RS, et al. An update on therapies for the treatment of diabetes-induced osteoporosis[J]. Expert Opin Biol Ther, 2019, 19(9): 937-948. DOI:10.1080/14712598.2019.1618266 |
| [12] |
天津市医学会骨质疏松和骨矿盐疾病分会, 天津市口腔医学会口腔颌面外科专业委员会. 天津市抗骨质疏松治疗与药物相关性颌骨坏死问题的专家共识[J]. 天津医药, 2023, 51(9): 897-903. DOI:10.11958/20230147 |
| [13] |
ZHANG ZW, JI CH, WANG YN, et al. Maresin1 suppresses high-glucose-induced ferroptosis in osteoblasts via NRF2 activation in type 2 diabetic osteoporosis[J]. Cells, 2022, 11(16): 2560. DOI:10.3390/cells11162560 |
| [14] |
ZHANG D, DU J, YU M, et al. Urine-derived stem cells-extracellular vesicles ameliorate diabetic osteoporosis through HDAC4/HIF-1α/VEGFA axis by delivering microRNA-26a-5p[J]. Cell Biol Toxicol, 2023, 39(5): 2243-2257. DOI:10.1007/s10565-022-09713-5 |
| [15] |
陈茹, 苏莹, 柳江. 淫羊藿苷通过Wnt/β-catenin信号通路对卵巢癌细胞CAOV3增殖的影响[J]. 医学研究杂志, 2019, 48(3): 44-49. DOI:10.11969/j.issn.1673-548X.2019.03.011 |
| [16] |
BAO KR, JIAO YH, XING L, et al. The role of Wnt signaling in diabetes-induced osteoporosis[J]. Diabetol Metab Syndr, 2023, 15(1): 84. DOI:10.1186/s13098-023-01067-0 |
| [17] |
LI X, WANG YX, SHI P, et al. Icariin treatment reduces blood glucose levels in type 2 diabetic rats and protects pancreatic function[J]. Exp Ther Med, 2020, 19(4): 2690-2696. DOI:10.3892/etm.2020.8490 |
| [18] |
ZHANG XY, LI HN, CHEN F, et al. Icariin regulates iR-23a-3p- mediated osteogenic differentiation of BMSCs via BMP-2/Smad5/ Runx2 and WNT/β-catenin pathways in osteonecrosis of the femoral head[J]. Saudi Pharm J, 2021, 29(12): 1405-1415. DOI:10.1016/j.jsps.2021.10.009 |
| [19] |
刘敏. E2靶向ER1通过ERK信号通路调控软骨细胞增殖的实验研究[D]. 重庆: 重庆医科大学, 2019.
|
 2025, Vol. 54
2025, Vol. 54