文章信息
- 王红梅, 王祥卉, 张文竹, 何蕊, 廖天佐, 高青华, 郝丽英
- WANG Hongmei, WANG Xianghui, ZHANG Wenzhu, HE Rui, LIAO Tianzuo, GAO Qinghua, HAO Liying
- 钙/钙调蛋白依赖性蛋白激酶Ⅱ质粒的构建和表达及其与CaV1.2通道结合的鉴定
- Construction and expression of Ca2+/calmodulin-dependent protein kinase Ⅱ plasmid and identification of CaV1.2 channel binding
- 中国医科大学学报, 2025, 54(1): 1-4, 11
- Journal of China Medical University, 2025, 54(1): 1-4, 11
-
文章历史
- 收稿日期:2024-06-13
- 网络出版时间:2025-01-09 15:39:21
2. 赤峰市医院药剂科, 内蒙古 赤峰 024000;
3. 中国医科大学继续教育学院综合办公室, 沈阳 110001;
4. 中国医科大学生命科学学院发育细胞生物学教研室, 沈阳 110122
2. Pharmacy Department, Chifeng Municipal Hospital, Chifeng 024000, China;
3. General Office, Continuing Education College, China Medical University, Shenyang 110001, China;
4. Department of Developmental Cell Biology, School of Life Sciences, China Medical University, Shenyang 110122, China
钙/钙调蛋白依赖性蛋白激酶Ⅱ (Ca2+/calmodulin-dependent kinase Ⅱ,CaMKⅡ) 是一种丝氨酸/苏氨酸蛋白激酶,能够将底物磷酸化,并修饰苏氨酸/丝氨酸等重要氨基酸,从而调节心脏的各种生理和病理过程[1]。CaMKⅡ的靶蛋白种类多样,因而具有广泛的调控作用。CaMKⅡ作用的多样性与其组织分布和亚细胞定位有关。在哺乳动物中,CaMKⅡ由4种不同的亚型(α、β、γ、δ) 组成,具有多种剪接体,虽然高度同源,但因组织分布不同,具有不同的生理功能。CaMKⅡδ主要表达在心肌[2],CaMKⅡα和CaMKⅡβ主要表达在中枢神经系统,CaMKⅡγ在多种组织和细胞中均有表达[3-4]。CaMKⅡ的活性可被直接或间接调节,多样化的CaMKⅡ信号通路有助于广泛调节多种生物活动。CaMKⅡ最初因其在学习记忆中的作用被广泛关注[4],后来研究发现其过度激活在心脏疾病的发生中具有核心作用。因此,CaMKⅡ有望成为治疗心血管疾病的关键靶点。
本课题组前期采用膜片钳单通道inside-out技术,发现CaMKⅡ可以消除CaM对L型钙通道run-down现象调节的时间依赖性,用CaMKⅡ处理CaV1.2通道的C末端片段(CT1) 后,CaM与CT1的结合能力增加,说明CaMKⅡ磷酸化可提高CaM与CaV1.2通道的结合能力,进而调节L型钙通道功能。目前研究表明,CaMKⅡ在心肌肥厚[5]、心律失常[6]、心力衰竭[7]、缺血性心脏病和扩张性心肌病等的发生和发展中都具有重要作用。提取高纯度的CaMKⅡ在相关心血管疾病研究中具有重要意义,但应用常规技术手段提取CaMKⅡ蛋白的效果一直不佳。
本研究通过改进酶切温度和时间,成功构建长片段CaMKⅡ重组质粒并制备纯化长片段CaMKⅡ蛋白,采用SDS-PAGE鉴定纯化后GST-CaMKⅡ和CaMKⅡ蛋白分子量和相对纯度;采用pull-down结合Western blotting检测长片段CaMKⅡ与CaV1.2通道的结合能力,为研究CaMKⅡ与钙通道CaV1.2的相互作用及其分子机制奠定了重要的生物学基础,为进一步研究CaMKⅡ在心血管疾病中的作用提供理论依据。
1 材料与方法 1.1 材料原核表达载体pGEX-6P-1、BL-21感受态细胞,由武汉金开瑞生物工程有限公司合成和提供;DL-二硫苏糖醇(DL-dithiothreitol,DTT)、异丙基-β-D-硫代半乳糖苷( isopropyl-β-D-thiogalactoside,IPTG)、氨苄西林(ampicillin,Amp)、溶菌酶(lysozyme,LYS)、膜再生液,购自北京索莱宝科技有限公司;三色预染蛋白marker,购自上海雅酶生物医药科技有限公司。CaMKⅡ抗体,购自英国abcam公司;CaV1.2抗体,购自美国Omnimabs公司;山羊抗兔IgG (H+L) 二抗,购自武汉伊莱瑞特生物科技股份有限公司。
1.2 长片段CaMKⅡ重组质粒的提取和鉴定将pGEX-6p-1/CaMKⅡ重组质粒TOP10 (60 μL) 细菌接种在含50 μg/mL Amp的1×LB液体培养基中,摇床培养箱中培养12 h。10 000 g离心1 min,收集菌液。参照SanPrep柱式质粒试剂盒说明书提取质粒,测定质粒DNA浓度,将质粒DNA送至生工生物工程(上海) 股份有限公司测序,应用PubMed网站的BLAST软件比对重组质粒同源性。
1.3 BL21感受态细胞的转化将pGEX-6P-1/CaMKⅡ质粒转入100 μL大肠杆菌BL21中,冰上静置30 min。42 ℃水浴45 s,快速放回冰上,静置2 min。搅拌混匀,在37 ℃、摇床转速为200 r/min下复苏60 min。5 000 r/min离心1 min,取菌液50 μL均匀涂于含50 μg/mL Amp的1×LB固体培养基上。在37 ℃细菌培养箱中培养12~16 h[8]。
1.4 重组质粒pGEX-6P-1/CaMKⅡ的诱导和表达将重组质粒pGEX-6P-1/CaMKⅡ成功转入大肠杆菌BL21后,加入200 mL无菌1×LB培养液,同时加入200 μL Amp (50 mg/mL),在37 ℃、摇床转速为110 r/min下振荡过夜。测定菌液光密度,待600 nm波长处光密度值为0.6~1.0时,加入IPTG进行诱导,在37 ℃、摇床转速为130 r/min下振荡4 h。
1.5 CaMKⅡ蛋白的提取重组蛋白诱导表达4 h后,将200 mL菌液分装到50 mL无菌离心管中,配平,4 000 r/min离心10 min后弃掉上清,留取沉淀。将沉淀用PBS重悬,加入100 μL LYS (0.1 mg/mL) 和100 μL DTT (1 mol/L),充分混匀后冰上静置30 min,7 ℃~8 ℃超声处理20 min。16 000 g离心10 min,将上清与PBS洗过2遍的300 μL GS-4B在4 ℃孵育,摇晃过夜[9]。次日早晨,1 000 r/min离心,弃上清,GS-4B用5 mL Tris缓冲液1 000 r/min离心4次,转移至2 mL EP管中,加入295 μL Tris缓冲液和4 μL PreScission蛋白酶,室温旋转8 h,800 r/min离心3 min后取上清,得到长片段CaMKⅡ蛋白。
采用相同技术,从膜蛋白CaV1.2中提取出GST-CT1融合蛋白。在重悬液中加入LYS和DTT,冰上静置30 min,超声处理后,加入15% N-月桂酰肌氨酸,再次冰上静置30 min,但不进行PreScission蛋白酶酶切步骤,用于后续鉴定与CaMKⅡ的结合。
1.6 纯化后蛋白纯度和浓度的测定 1.6.1 CaMKⅡ纯度的测定取制备的GST-CaMKⅡ与酶切后CaMKⅡ蛋白各10 μL,加入5 μL 1×上样缓冲液,100 ℃金属浴5 min后,15% SDS-PAGE电泳80 V 30 min、110 V 90 min后,考马斯亮蓝染色1 h,根据蛋白条带位置,比对蛋白marker条带位置,评估目的蛋白纯度。
1.6.2 CaMKⅡ蛋白浓度的测定以牛血清白蛋白作为标准蛋白,绘制标准曲线,计算CaMKⅡ蛋白浓度。
1.7 CaMKⅡ蛋白活性的鉴定采用pull-down结合Western blotting检测CaMKⅡ生物学活性。GS-4B连接的GST-CT1 (40 μL) 加入0.7 μmol/L CaMKⅡ,加入CaCl2至终浓度为2 mmol/L,同时加入Tris缓冲液补齐至300 μL体系中,于旋转培养器4 ℃结合4 h;反应后用含2 mmol/L Ca2+的Tris缓冲液1 000 r/ min离心GS-4B 3遍。再向其中加入10 μL1×上样缓冲液,金属浴100 ℃、5 min后,经SDS-PAGE电泳后电转至PVDF膜上,5%脱脂奶粉室温封闭2 h,TBST洗膜5 min×3次后,CaV1.2抗体(1∶1 000) 4 ℃孵育过夜,次日TBST洗膜7 min×3次后,二抗(1∶50 000) 室温孵育1 h,TBST洗膜7 min×3次,ECL显影。用膜再生液孵育20 min后,用新鲜配制的5%脱脂奶粉室温封闭1 h,TBST洗膜5 min×3次后,CaMKⅡ抗体(1∶2 000) 4 ℃孵育过夜,次日TBST洗膜5 min×3次后,二抗(1∶50 000) 室温孵育1 h,TBST洗膜5 min×3次,ECL显影。
2 结果 2.1 重组质粒DNA测序结果DNA测序结果显示,CaMKⅡ重组质粒含有1 614 bp DNA片段。通过BLAST软件比对,同源性为100%,读码框架一致,且插入方向一致,表明重组质粒构建成功。见图 1。

|
| 图 1 重组质粒DNA序列鉴定 Fig.1 DNA sequence identification of recombinant plasmid |
2.2 纯化后CaMKⅡ蛋白分子量和纯度
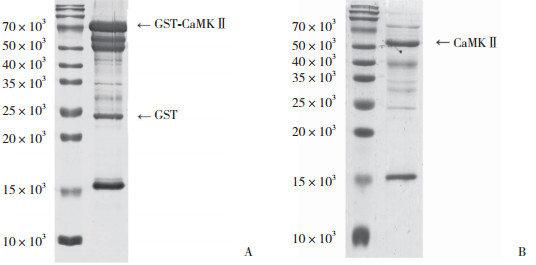
CaMKⅡ蛋白表观分子量约为54×103。在表观分子量约为80×103 (GST-CaMKⅡ) 和54×103 (CaMKⅡ) 处出现明显条带,与预期结果相符,表明已经成功获得纯度较高的CaMKⅡ蛋白。见图 2。
|
| A,purified GST-CaMKⅡ;B,purified CaMKⅡ after PreScission GST treatment. 图 2 SDS-PAGE电泳鉴定GST-CaMKⅡ和CaMKⅡ蛋白 Fig.2 GST-CaMKⅡ and CaMKⅡ proteins identified using SDS-PAGE |
2.3 纯化后蛋白浓度测定
采用牛血清白蛋白作为标准蛋白,绘制标准曲线,计算CaMKⅡ蛋白浓度为0.59 mg/mL。
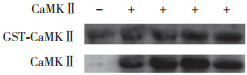
2.4 CaMKⅡ蛋白活性将纯化后的CaMKⅡ蛋白与CaV1.2通道蛋白上GST-CT1蛋白片段相互作用,电化学发光在表观分子量约54×103处出现明显条带,见图 3。说明纯化后的CaMKⅡ蛋白与钙通道蛋白CT1结合能力强,提示具有生物学活性。
|
| 图 3 Western blotting检测CaMKⅡ与GST-CT1结合 Fig.3 Binding of CaMKⅡ to GST-CT1 detected using Western blotting |
3 讨论
CaMKⅡ是一类由Ca2+调控的蛋白激酶,当细胞内Ca2+增加时,Ca2+结合型钙调蛋白(Ca2+/CaM) 与CaMKⅡ结合,将假底物从催化结构域中移出,使CaMKⅡ能够接触底物和ATP,进而发挥其活性。CaMKⅡ的瞬时激活是可逆的:当细胞内Ca2+浓度降低时,CaM脱钙并与CaMKⅡ解离;当细胞内Ca2+浓度持续升高时,CaMKⅡ持续激活,这一过程常发生在心动过速或心肌动作电位延长期间。此时CaMKⅡ第287位的苏氨酸(T287,CaMKⅡα中为T286) 发生自身磷酸化,T287自身磷酸化通过2种机制使CaMKⅡ可以不受Ca2+浓度的调节:(1) 由于CaMKⅡ与CaM的亲和力增加了数千倍,从而增加了与CaM的持续结合;(2) CaMKⅡ也通过降低假底物与催化结构域的亲和力,促进自身磷酸化。此外,CaMKⅡ也可由氧化应激、亚硝化应激以及高血糖等刺激而激活[10]。CaMKⅡ通过磷酸化下游多种靶点[11] (如兰尼定受体、肌浆网钙ATP酶、受磷蛋白等) 参与心肌细胞兴奋收缩偶联。因此,CaMKⅡ被认为是心律失常、心肌肥厚和心力衰竭的核心靶蛋白。
心脏中CaMKⅡ的亚型主要为CaMKⅡδ[12]。目前已经确定,CaMKⅡδ经过选择性剪接后有11个剪接变体(CaMKⅡδ1~ CaMKⅡδ11),其中CaMKⅡδ2/C、CaMKⅡδ3/B和CaMKⅡδ9的研究最多。本研究提取的CaMKⅡ蛋白不仅在54×103处有明显条带,在40×103和15×103处也有明显条带,推测这与CaMKⅡ的剪接体存在形式有关。
CaMKⅡ是细胞内的重要调节因子,与多种心血管疾病及其他系统疾病密切相关。本研究成功构建了CaMKⅡ质粒,该质粒能够很好地在大肠杆菌中表达,经过GS-4B beads纯化后,具有较高的纯度、浓度以及生物活性。纯化后的CaMKⅡ可用于后续Ca2+/CaM/CaMKⅡ调节机制的研究,为进一步阐明CaMKⅡ相关疾病的发病机制和提供精准的治疗策略奠定了生物学基础。
| [1] |
BHATTACHARYYA M, KARANDUR D, KURIYAN J. Structural insights into the regulation of Ca2+/calmodulin-dependent protein kinase Ⅱ (CaMKⅡ)[J]. Cold Spring Harb Perspect Biol, 2020, 12(6): a035147. DOI:10.1101/cshperspect.a035147 |
| [2] |
ZHANG J, LIANG R, WANG K, et al. Novel CaMKⅡ-δ inhibitor hesperadin exerts dual functions to ameliorate cardiac ischemia/ reperfusion injury and inhibit tumor growth[J]. Circulation, 2022, 145(15): 1154-1168. DOI:10.1161/CIRCULATIONAHA.121.055920 |
| [3] |
RHEIN C, MÜHLE C, LENZ B, et al. Association of a CAMK2A genetic variant with logical memory performance and hippocampal volume in the elderly[J]. Brain Res Bull, 2020, 161: 13-20. DOI:10.1016/j.brainresbull.2020.05.001 |
| [4] |
TAO W, LEE J, CHEN X, et al. Synaptic memory requires CaMKⅡ[J]. Elife, 2021, 10: e60360. DOI:10.7554/eLife.60360 |
| [5] |
MARTINEZ-CANTON M, GALLEGO-SELLES A, GELABERT-REBATO M, et al. Role of CaMKⅡ and sarcolipin in muscle adaptations to strength training with different levels of fatigue in the set[J]. Scand J Med Sci Sports, 2021, 31(1): 91-103. DOI:10.1111/sms.13828 |
| [6] |
LEBEK S, PICHLER K, REUTHNER K, et al. Enhanced CaMKⅡ- dependent late INa induces atrial proarrhythmic activity in patients with sleep-disordered breathing[J]. Circ Res, 2020, 126(5): 603-615. DOI:10.1161/circresaha.119.315755 |
| [7] |
BOYLE AJ, SCHULTZ C, SELVANAYAGAM JB, et al. Calcium/calmodulin-dependent protein kinaseⅡ delta inhibition and ventricular remodeling after myocardial infarction: a randomized clinical trial[J]. JAMA Cardiol, 2021, 6(7): 762-768. DOI:10.1001/jamacardio.2021.0676 |
| [8] |
DURAN J, NICKEL L, ESTRADA M, et al. CaMKⅡδ splice variants in the healthy and diseased heart[J]. Front Cell Dev Biol, 2021, 9: 644630. DOI:10.3389/fcell.2021.644630 |
| [9] |
齐爽, 孙旋旋, 王绮萱, 等. β淀粉样蛋白1-42质粒的构建及其与钙调蛋白的结合作用[J]. 中国医科大学学报, 2024, 53(6): 495-500. DOI:10.12007/j.issn.0258-4646.2024.06.003 |
| [10] |
BACKS J. CaMKⅡ transforms glucose into reactive oxygen species[J]. Circ Res, 2020, 126(10): 1327-1329. DOI:10.1161/CIRCRESAHA.120.316982 |
| [11] |
HEIJMAN J, MUNA AP, VELEVA T, et al. Atrial myocyte NLRP3/CaMKⅡ nexus forms a substrate for postoperative atrial fibrillation[J]. Circ Res, 2020, 127(8): 1036-1055. DOI:10.1161/CIRCRESAHA.120.316710 |
| [12] |
SONG Z, SONG H, LIU D, et al. Overexpression of MFN2 alleviates sorafenib-induced cardiomyocyte necroptosis via the MAM-CaMK Ⅱδ pathway in vitro and in vivo[J]. Theranostics, 2022, 12(3): 1267-1285. DOI:10.7150/thno.65716 |
 2025, Vol. 54
2025, Vol. 54