文章信息
- 李蕙彤, 任鲁宁, 王菲, 杨冬梅, 杜红阳
- LI Huitong, REN Luning, WANG Fei, YANG Dongmei, DU Hongyang
- IL-18、IL-18BP、IL-18R在特应性皮炎患者外周血B淋巴细胞及单核细胞中的表达
- Expression of IL-18, IL-18BP, and IL-18R in peripheral blood B lymphocytes and monocytes of patients with atopic dermatitis
- 中国医科大学学报, 2024, 53(9): 782-787
- Journal of China Medical University, 2024, 53(9): 782-787
-
文章历史
- 收稿日期:2023-11-15
- 网络出版时间:2024-09-10 15:46:01
特应性皮炎(atopic dermatitis,AD)是一种较为常见的慢性炎症性皮肤病,以皮肤瘙痒、反复发作的湿疹样皮损为主要临床特征[1]。其发病与遗传、环境、自身免疫等因素密切相关,其中外源性AD的加重与屏障功能障碍和外来过敏原渗透侵入有关,皮肤屏障破坏使患者的皮肤对环境过敏原(尘螨、动物皮屑、草花粉等)高度易感[2]。
白细胞介素(interlukin,IL)-18是IL-1家族细胞因子[3],在许多过敏性疾病表达增加,能引起严重的过敏性炎症反应[4]。IL-18与IL-18受体(interleukin-18 receptor,IL-18R)结合能促进Th1细胞相关因子的释放,导致Th1/Th2失衡。IL-18结合蛋白(interleukin-18 binding protein,IL-18BP)是一种糖蛋白,能抑制IL-18诱导Th1细胞产生γ干扰素(interferon-γ,INF-γ),是IL-18的天然拮抗剂,与IL-18协调作用参与细胞免疫反应[5],二者在多种炎症性皮肤病和自身免疫性疾病中表达增加[4, 6]。体内多种免疫细胞(如单核细胞、巨噬细胞、T细胞、B细胞、NK细胞和中性粒细胞)及肥大细胞和嗜碱性粒细胞可表达IL-18[7]。但是,关于过敏原对AD患者血液单核细胞和B淋巴细胞中IL-18、IL-18BP和IL-18R的表达情况却知之甚少。因此,本研究拟探讨AD患者外周血B淋巴细胞和单核细胞中IL-18、IL-18BP和IL-18R的表达情况,以及过敏原对其表达的影响。
1 材料与方法 1.1 材料主要试剂:Zombie GreenTM Fixable Viability Kit、Human TruStain FcXTM、PE/Cy7-CD14、APC/Cy7-CD19、BV510驴抗兔IgG抗体、红细胞裂解液、布雷非德菌素A(Brefeldin A,BFA),购自美国Biolegend公司;APC-IL-18Rα、APC-IL-18Rα同型、PE-IL-18、PE-IL-18同型,购自美国R & D Systems公司;兔抗人IL-18BP抗体、兔IgG同型对照抗体,购自美国NOVUS公司;大籽蒿过敏原提取物(Artemisia sieversiana wild allergen extract,ASWE)、尘螨过敏原提取物(house dust mite allergen extract,HDME)、梧桐花粉过敏原提取物(Platanus pollen allergen extract,PPE),购自北京新华联协和药业有限责任公司(中国);Cytofix /CytopermTM固定/透膜试剂盒购自美国BD Biosciences Pharmigen公司。主要仪器:低温高速离心机购自美国Thermo Scientific公司,FACSVerse流式细胞仪购自美国BD Biosciences公司。
1.2 方法 1.2.1 研究对象和样本采集选取2021年11月至2022年12月就诊于锦州医科大学附属第一医院皮肤科的AD患者28例(AD组),其中,女17例,男11例,年龄17(1~64)岁;ASWE阳性25例,HDME阳性25例,PPE阳性25例。选取同期我院健康体检志愿者21例作为健康对照组,其中,女11例,男10例,年龄33(29~41)岁。AD诊断符合AD Williams诊断标准,入组患者要求停止服用抗过敏药物≥2周。本研究获得锦州医科大学附属第一医院医学伦理委员会批准(审批号202397),所有研究对象知情同意。采集所有研究对象的外周静脉血于含有EDTA抗凝剂的采血管中,用于流式细胞检测。
1.2.2 流式细胞术检测外周静脉血B淋巴细胞和单核细胞IL-18、IL-18BP和IL-18R的表达取100 μL外周静脉血标本,置入2 mL EP管中;分别加入1.0 μg/mL的ASWE、HDME、PPE 3 μL,并加入2 μL BFA,37 ℃孵育1 h;每管加入FITC去死细胞染料和人Fc受体阻断剂,室温避光孵育15 min;依次加入表面抗体PE/Cy7-CD14、APC/Cy7-CD19和APC-IL-18Rα,荧光减一(fluorescence minus one,FMO)对照管加入相应的表面同型抗体,室温避光孵育15 min;裂解红细胞后用固定/透膜液固定细胞,加入PE-IL-18和抗人IL-18BP一抗,FMO对照管加入相应的胞内同型抗体,4 ℃避光孵育30 min;透膜洗液清洗,加入BV510 Secondary Ab驴抗兔抗体,4 ℃避光孵育30 min;透膜洗液清洗,PBS重悬细胞,流式上机检测。使用FlowJo_v10.6.2软件进行数据分析。
1.3 统计学分析采用GraphPad Prism 5.0软件和SPSS 17.0软件进行统计分析。用非参数Mann-Whitney检验评估静息状态和不同过敏原刺激后健康对照组和AD组指标的差异,P < 0.05为差异有统计学意义。
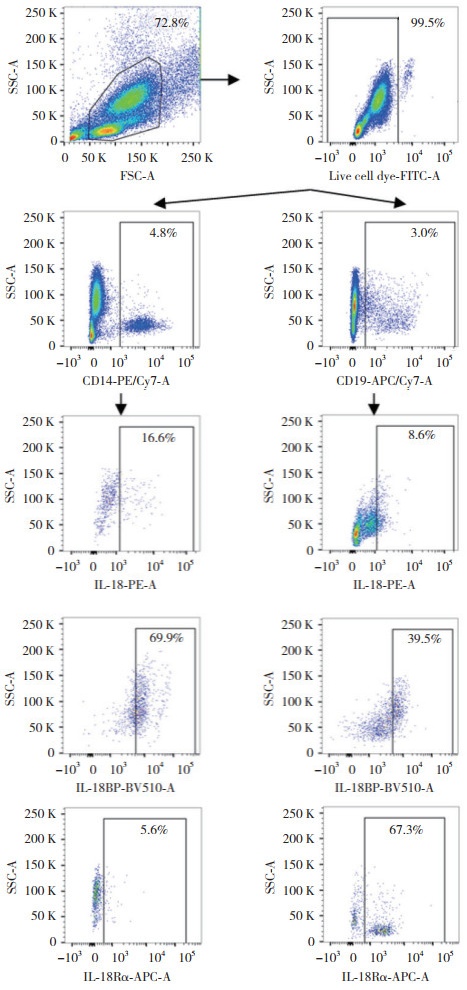
2 结果流式细胞术分别检测B淋巴细胞和单核细胞IL-18、IL-18BP和IL-18R的表达,设门方法见图 1。
|
| 图 1 门控策略图 Fig.1 Gating strategies |
2.1 B淋巴细胞富集群中IL-18、IL-18BP和IL-18R的表达
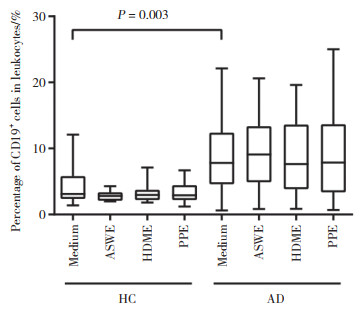
与健康对照组比较,AD组静息状态下血液中CD19+B淋巴细胞比例增加,差异有统计学意义(P = 0.003),3种过敏原对B淋巴细胞比例的影响不显著(图 2)。
|
| HC, health control group; AD, atopic dermatitis group. 图 2 CD19+细胞占白细胞百分比 Fig.2 Percentage of CD19+ cells in leukocytes |
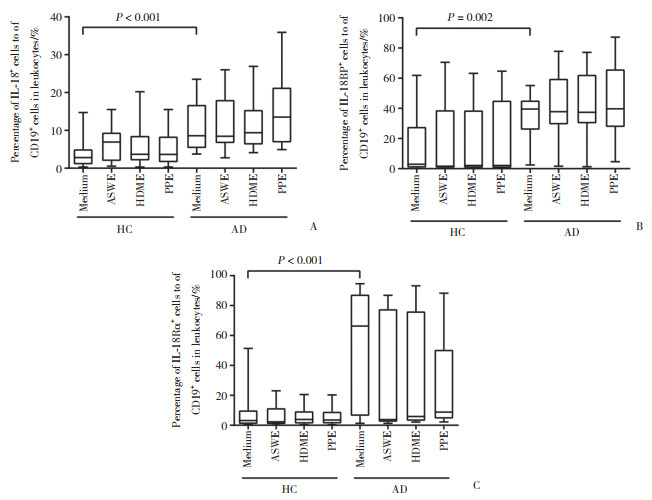
与健康对照组比较,AD患者静息状态下B淋巴细胞群中IL-18+细胞比例升高2.01倍(图 3A),IL-18BP+细胞比例升高10.35倍(图 3B),IL-18R+细胞比例升高20.85倍(图 3C),过敏原ASWE、HDME和PPE对B淋巴细胞上的IL-18、IL-18BP和IL-18R表达影响不显著。
|
| A, IL-18+; B, IL-18BP+; C, IL-18Rα+. 图 3 IL-18+、IL-18BP+、IL-18Rα+细胞占白细胞中CD19+细胞百分比 Fig.3 Percentage of IL-18+, IL-18BP+, and IL-18Rα+ cells to CD19+ cells in leukocytes |
2.2 单核细胞富集群中IL-18、IL-18BP和IL-18R的表达
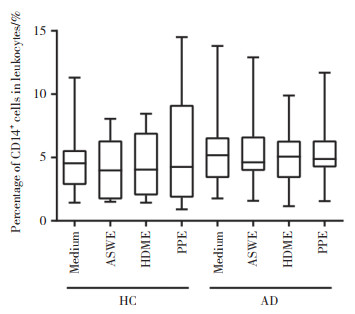
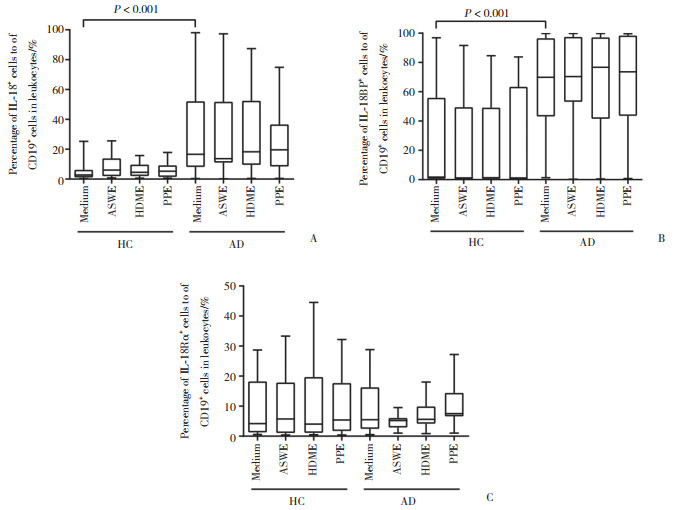
静息状态下健康对照组和AD组CD14+单核细胞比例无统计学差异(P > 0.05),3种过敏原对单核细胞比例的影响不显著(图 4)。与健康对照组比较,AD组静息状态下单核细胞群中IL-18+细胞比例升高5.51倍(图 5A),IL-18BP+细胞比例升高41.88倍(图 5B),而IL-18R+细胞比例无明显变化(图 5C),过敏原ASWE、HDME和PPE对单核细胞IL-18、IL-18BP和IL-18R表达影响不显著。
|
| 图 4 CD14+细胞占白细胞百分比 Fig.4 Percentage of CD14+ cells in leukocytes |
|
| A, IL-18+; B, IL-18BP+; C, IL-18Rα+. 图 5 IL-18+、IL-18BP+、IL-18Rα+细胞占白细胞中CD14+细胞百分比 Fig.5 Percentage of IL-18+, IL-18BP+, and IL-18Rα+ cells to CD14+ cells in leukocytes |
3 讨论
AD也称为特应性湿疹、遗传过敏性湿疹等,曾称为异位性皮炎。其特征为本人或其家族中具有明显的“特应性”特点,是最常见的皮肤科疾病之一[8]。AD患者血清中IL-18水平升高,本研究结果显示,AD患者血液中B淋巴细胞和单核细胞IL-18+细胞的比例明显升高,提示炎症性皮肤疾病患者血液IL-18水平的升高可能与B淋巴细胞和单核细胞有关[6]。IL-18是一种多效促炎性细胞因子,在炎症过程中起双相调节作用,可以调控Th1和Th2型免疫应答,调节IgE的合成,主要由活化的单核巨噬细胞产生[9]。
AD患者外周血中单核细胞可产生大量前列腺素E2(prostaglandin E2,PGE2),后者又可直接刺激B淋巴细胞产生IgE [10]。研究[11]发现,AD的发病机制部分由Th2介导,Th2促进IL-4和IL-13的产生并诱导IgE,而IL-18能够增强Th2应答。IgE和肥大细胞可以促进多种炎症介质的产生,故IL-18有助于评估AD发生发展,抑制IL-18可能是AD潜在的治疗靶点。
IL-18成熟活化后,通过IL-18R参与多种生物学功能。IL-18R由异源二聚体组成,即α链(IL-18Rα)和β链(IL-18Rβ)[12]。IL-18Rα在大多数细胞中表达,而IL-18Rβ链只有少数细胞如T细胞、树突状细胞和肥大细胞表达[13]。IL-18通过与细胞表面的IL-18Rα相互作用,在机体防御及致病过程中发挥其生物学功能。有研究[14]发现,儿童过敏性哮喘患者肺组织中嗜酸性粒细胞增多,并伴有IL-18R+表达增加。也有研究[15]显示,过敏性鼻炎合并哮喘患者血液中嗜酸性粒细胞IL-18R+细胞的比例与正常对照组比较无统计学差异。本研究结果显示,AD患者血液单核细胞中IL-18R+细胞的比例与健康对照组相比无统计学差异,而B细胞中IL-18R+细胞的比例明显升高。提示B细胞表面的IL-18R可能在AD中起重要作用,但其机制需进一步研究。
IL-18BP是一种受体样可溶性蛋白,是IL-18的内源性拮抗剂,通过抑制IL-18与IL-18R的结合,减少IFN-γ的产生,从而抑制Th1免疫应答[16]。而IL-18/IL-18BP平衡的失调可能有助于Th1慢性炎症的发生[6]。研究[17]发现,IL-18BP在炎症和自身免疫性疾病患者中表达增加,通常与IL-18水平升高同时发生。本研究结果表明,AD患者血液中B淋巴细胞和单核细胞中IL-18+细胞和IL-18BP+细胞的比例均明显升高,提示IL-18与IL-18BP的失衡可能诱导AD的发生,为AD的治疗提供了新思路。
综上所述,本研究发现,B淋巴细胞及单核细胞中IL-18、IL-18BP和IL-18R可能在AD中起重要作用,这3种IL可能是治疗AD的潜在靶点。
| [1] |
YU L, LI LF. Potential biomarkers of atopic dermatitis[J]. Front Med, 2022, 9: 1028694. DOI:10.3389/fmed.2022.1028694 |
| [2] |
周杰, 陈曙光, 宋志强. 特异性免疫疗法治疗特应性皮炎[J]. 中华临床免疫和变态反应杂志, 2021, 15(1): 76-81. DOI:10.3969/j.issn.1673-8705.2021.01.014 |
| [3] |
VECCHIÉ A, BONAVENTURA A, TOLDO S, et al. IL-18 and infections: is there a role for targeted therapies?[J]. J Cell Physiol, 2021, 236(3): 1638-1657. DOI:10.1002/jcp.30008 |
| [4] |
IHIM SA, ABUBAKAR SD, ZIAN Z, et al. Interleukin-18 cytokine in immunity, inflammation, and autoimmunity: biological role in induction, regulation, and treatment[J]. Front Immunol, 2022, 13: 919973. DOI:10.3389/fimmu.2022.919973 |
| [5] |
YASUDA K, NAKANISHI K, TSUTSUI H. Interleukin-18 in health and disease[J]. Int J Mol Sci, 2019, 20(3): 649. DOI:10.3390/ijms20030649 |
| [6] |
WANG XY, WANG L, WEN X, et al. Interleukin-18 and IL-18BP in inflammatory dermatological diseases[J]. Front Immunol, 2023, 14: 955369. DOI:10.3389/fimmu.2023.955369 |
| [7] |
王君灵, 何韶衡. IL-18在过敏性气道疾病中的作用研究进展[J]. 西安交通大学学报(医学版), 2023, 44(4): 654-659. DOI:10.7652/jdyxb202304024 |
| [8] |
赵辩. 中国临床皮肤病学[M]. 南京: 江苏凤凰科学技术出版社, 2019: 765-774.
|
| [9] |
崔夫波, 柴文戍, 张慧云, 等. 过敏性鼻炎患者外周血嗜酸性粒细胞富集群中IL-18、IL-18BP和IL-18R的表达[J]. 郑州大学学报(医学版), 2018, 53(1): 125-128. DOI:10.13705/j.issn.1671-6825.2016.12.010 |
| [10] |
CHEN JL, NIU XL, GAO YL, et al. IL-18 knockout alleviates ato-pic dermatitis-like skin lesions induced by MC903 in a mouse model[J]. Int J Mol Med, 2020, 46(2): 880-888. DOI:10.3892/ijmm.2020.4630 |
| [11] |
VOSS GT, DE OLIVEIRA RL, DAVIES MJ, et al. Suppressive effect of 1, 4-anhydro-4-seleno-D-talitol (SeTal) on atopic dermatitis-like skin lesions in mice through regulation of inflammatory mediators[J]. J Trace Elem Med Biol, 2021, 67: 126795. DOI:10.1016/j.jtemb.2021.126795 |
| [12] |
ZHOU T, DAMSKY W, WEIZMAN OE, et al. IL-18BP is a secreted immune checkpoint and barrier to IL-18 immunotherapy[J]. Nature, 2020, 583(7817): 609-614. DOI:10.1038/s41586-020-2422-6 |
| [13] |
SHIMIZU M, TAKEI S, MORI M, et al. Pathogenic roles and diagnostic utility of interleukin-18 in autoinflammatory diseases[J]. Front Immunol, 2022, 13: 951535. DOI:10.3389/fimmu.2022.951535 |
| [14] |
WANG JL, ZHANG HY, ZHENG WJ, et al. Correlation of IL-18 with tryptase in atopic asthma and induction of mast cell accumulation by IL-18[J]. Mediators Inflamm, 2016, 2016: 4743176. DOI:10.1155/2016/4743176 |
| [15] |
王玲, 胡雅琳, 杨蕊铭, 等. 过敏性鼻炎合并哮喘患者血液嗜酸性粒细胞富集群中IL-18、IL-18BP及IL-18R的表达[J]. 郑州大学学报(医学版), 2017, 52(5): 598-602. DOI:10.13705/j.issn.1671-6825.2017.05.020 |
| [16] |
ITALIANI P, MANCA ML, ANGELOTTI F, et al. IL-1 family cytokines and soluble receptors in systemic lupus erythematosus[J]. Arthritis Res Ther, 2018, 20(1): 27. DOI:10.1186/s13075-018-1525-z |
| [17] |
GABAY C, FAUTREL B, RECH J, et al. Open-label, multicentre, dose-escalating phase Ⅱ clinical trial on the safety and efficacy of tadekinig Alfa (IL-18BP) in adult-onset Still's disease[J]. Ann Rheum Dis, 2018, 77(6): 840-847. DOI:10.1136/annrheumdis-2017-212608 |
 2024, Vol. 53
2024, Vol. 53